节律性听觉刺激对卒中后步行功能的影响
葛亚丽 曹磊 宋为群
我国成人群体卒中发病率、死亡率和致残率均高,70%~80%的卒中患者伴有不同程度的功能障碍[1]。 一半以上的卒中患者表现出步速降低、步态不对称[2]等步行功能障碍,且在住院康复期间并无明显改善[3],造成这种现象的原因可能为缺乏特异性的步态训练[4]。有证据表明,卒中后患者的步态不对称以及步行速度等步行功能可能会逐步恶化[5]。因此,改善步行功能很重要,需针对卒中后的步行功能开发新的干预措施。节律性听觉刺激(rhythmic auditory stimulation,RAS)[6]是将听觉节奏提示作为一种外部指示信号来调整运动功能,是改善卒中后步行功能障碍的一种新的治疗方法。本研究旨在探究听觉节律的干预对卒中后步行功能障碍的影响及将RAS纳入步行训练的临床可行性。
1 对象与方法
1.1 对象
采用前瞻性研究,连续纳入2021年1月至12月于首都医科大学宣武医院康复医学科就诊的40例卒中患者,其中男18例,女22例;年龄24~78岁,平均(58±11)岁;左侧偏瘫19例,右侧偏瘫21例。根据随机数字表法将40例患者分为对照组和试验组各20例,两组患者一般资料差异均无统计学意义(均P>0.05)。
纳入标准:符合2015年中国脑血管疾病分类中的卒中诊断标准[7];经头部CT或头部MRI确诊;初次发病,生命体征平稳,意识清醒,可配合康复评估和治疗;满足步行训练条件(站位平衡≥2级,患侧负重≥75%)[8]且未行步行训练;Brunnstrom分期[9]≥Ⅳ期,改良Ashworth分级[10]≤2级。
排除标准:存在严重的认知功能障碍,蒙特利尔认知评估量表(Montreal cognitive assessment,MoCA)≤22分[11];有严重的言语功能障碍;存在中重度听力损失[12];其他影响步态的损伤或疾病(如帕金森病)。
所有入组患者签署诊疗知情同意书。本研究方案经首都医科大学宣武医院医学伦理委员会审核批准(伦理号:临研审[2020]046号)。
1.2 方法
两组患者均接受常规康复治疗[13],试验组在对照组的基础上增加RAS。
1.2.1常规康复治疗:(1)偏瘫肢体综合训练,包括肌力训练、转移训练、平衡训练、患侧负重训练、重心转移训练、步态训练等,每次治疗时间30 min,2次/d,5 d/周。(2)下肢康复踏车训练,20 min/次,2次/d,5 d/周。
1.2.2RAS训练:(1)训练前测出患者的基础步频(即患者在自由行走中每分钟迈出的步数)[14],重复测量3次并取平均值。(2)以超出平均值10%作为节拍器软件的节拍设置参数,将步频输入节拍器中。(3)告知患者可以使用任何必要的策略来帮助其找到节拍,如原地踏步或用手拍腿。(4)一旦他们找到节拍,患者就开始在训练时尽可能与其动作相匹配,要求患者在进行运动训练包括仰卧位训练、屈髋、屈膝、踝背屈以及站位重心转移等动作训练时,在治疗师引导下使动作频率与节拍器保持一致,康复踏车训练时将踏车速度调至与节拍器节拍保持一致。告知患者,如果失去了节拍,应该在两次节拍之间暂停,重新获得节拍后再继续下一个动作。如果患者多次尝试后动作依然不能与节拍相匹配,将节拍器参数调整为超出平均值5%作为节拍器软件的节拍设置参数。待患者适应该频率时,可逐步增加节拍器的频率至超出平均值10%作为节拍参数,每次治疗时间30 min,2次/d,5 d/周。
1.3 评定标准
1.3.1Fugl-Meyer下肢运动功能评估(Fugl-Meyer assessment:lower extremity,FMA-LE)量表:评定患者治疗前后的运动功能,总分34分,分数越高表明下肢功能越好[15]。
1.3.2盖力步(Gaitboter)步态分析系统:运用中国科学院计算技术研究所研制的盖力步步态分析系统中的可穿戴采集设备进行数据收集,同时应用相应的步态分析软件进行步态分析。选取步速(m/s)、步幅时间(s)和步频(步/min)评定患者治疗前后的步行能力,步速(m/s)、步幅时间(s)和步频(步/min)增大越多,表明患者步行的节奏和稳定性越好,反之越差。选取步长时间差(∣健侧步长(s)-患侧步长(s)∣)、着地冲击力差(∣健侧冲击力(g)-患侧冲击力(g)∣)作为患者治疗前后步态对称性的评定数据,差值越小表明患者步态越对称,反之越不对称[16]。
1.3.310 m行走时间测试(10 meter walk test,10-MWT):让患者以能够自行控制的速度进行直线行走10 m,记录行走消耗的时间,患者步行能力越好,所需时间越短[17]。
1.4 统计学分析

2 结果
2.1 基本资料比较
两组患者性别、年龄、身高、患侧差异均无统计学意义(均P>0.05)。见表1。
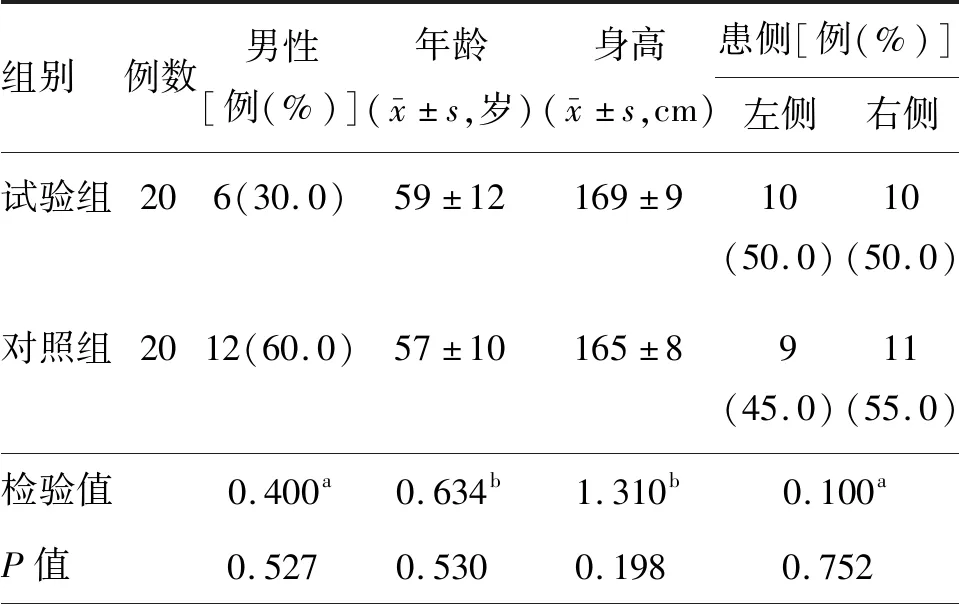
表1 两组卒中后偏瘫患者的基本资料比较
2.2 FMA-LE量表评分比较
治疗前,2组患者FMA-LE量表评分差异无统计学意义(P>0.05)。治疗2周后,两组FMA-LE量表评分较治疗前均明显提高(均P<0.01),且试验组FMA-LE量表评分改善明显优于对照组(P<0.01)。见表2。
2.3 步行参数比较
治疗前两组患者步速、步幅时间、步频、步长时间差、着地冲击力差组间差异均无统计学意义(均P>0.05),治疗2周后,两组患者的步速、步幅及步频较治疗前均有提高,步长时间差、着地冲击力差较治疗前均减小(均P<0.05),且试验组步速、步幅及步频、步长时间差、着地冲击力差改善均明显优于对照组,差异均有统计学意义(均P<0.05)。见表3~表7。
2.4 10-MWT比较
治疗前2组患者10-MWT比较差异无统计学意义(P>0.05),治疗2周后,两组10-MWT较治疗前均有显著缩短,差异均有统计学意义(均P<0.01),且试验组治疗前与治疗后的10-MWT差值多于对照组(P<0.05)。见表8。

表2 两组卒中后偏瘫患者康复治疗前后Fugl-Meyer下肢运动功能量表评分比较[M(P25,P75),分]
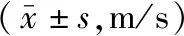
表3 两组卒中后偏瘫患者康复治疗前后步速比较
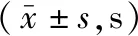
表4 两组卒中后偏瘫患者康复治疗前后步幅时间比较

表5 两组卒中后偏瘫患者康复治疗前后步频比较步/min)

表6 两组卒中后偏瘫患者康复治疗前后步长时间差比较[M(P25,P75),s]
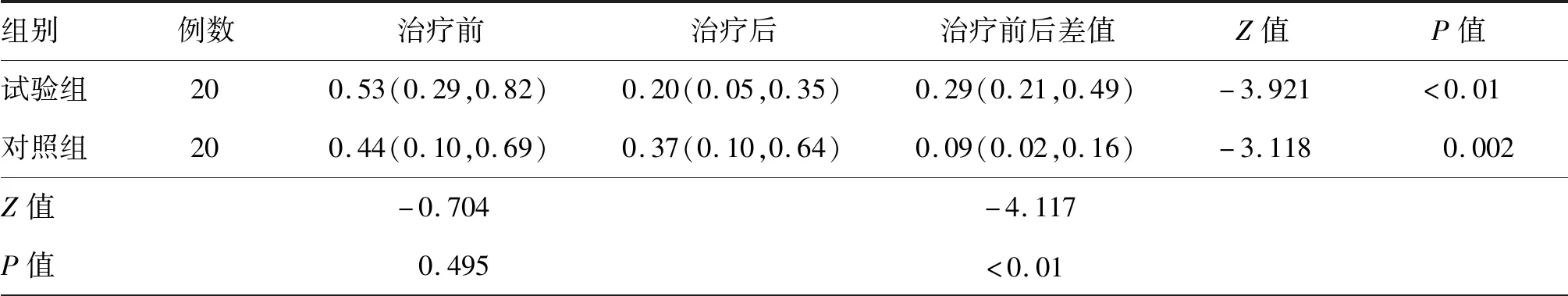
表7 两组卒中后偏瘫患者康复治疗前后着地冲击力差比较[M(P25,P75),g]
3 讨论
行走障碍是卒中后偏瘫遗留的最严重的残疾之一,行走能力通常在卒中后 12 周恢复。然而,步行功能的恢复往往是不完全的,一些特定的步态问题仍然存在[18]。75%的患者在出院后仍然步行困难,步行速度和距离难以达到社区安全步行的要求,主要原因是偏瘫患者步态适应性下降,面对复杂环境无法及时做出相应的步态调整[19],主要表现为步速减慢,步长缩短,步幅降低,步宽增大,步态周期延长[20]。Park和Kim[21]研究结果表明,步速和步长的改善可以提高卒中患者卒中后的生存质量。因此,步行功能的恢复被列为卒中康复的首要目标[22]。步态训练中的早期物理治疗干预被认为对于增强卒中后患者的步行功能很有价值。偏瘫患者的物理治疗通常在卒中后数周内进行,但是偏瘫患者的步行训练通常受到时间(1次/d或2次/d,每次几分钟)、空间(在医院范围内)和成本效益的限制[23]。为了克服这些缺点,RAS作为一种新兴的步行训练方法,是促进卒中后步行功能恢复的一种容易适用且安全的方法。
RAS对步行表现的积极影响是由一个耦合过程引起的,在这个耦合过程中,除了节奏模式和步行运动程序之外,听觉信号通过位于小脑白质中部的小脑运动区向腹内侧髓质网络投射,激活脊髓神经间网络,导致重复的有节奏的步态周期[24]。此外,所有运动的步骤规划可能与听觉反馈密切相关,听觉反馈通过影响运动时机、优化运动表现,在减少反应时间和降低疲劳感的同时提供反馈信息来发挥作用[25]。步行时肢体按一定顺序,以相对恒定的节奏进行重复运动。以适当节奏呈现的听觉节律可以增强患者的行走能力,因为患者可以使他们的运动与节奏相互协调[26]。有节奏的听觉刺激可以通过网状脊髓通路增加脊髓运动的兴奋性神经元,从而改善肌肉活动[23]。目前关于RAS改善运动的脑区仍不明确。Sherman等[27]研究表明,中脑背侧网状结构的运动区域可能参与调节个体的步态周期。Ozen等[28]认为,小脑也参与了节律的调节,当内源性节律的频率与刺激的频率相匹配,带动了包括小脑在内的运动神经网络的节律性活动,导致了人类自然步行节律的调节。
盖力步步态分析系统是中国科学院计算技术研究所研制的可穿戴步态分析设备,是通过标记在位于患者双侧的大腿外侧中部、小腿外侧中部以及腰椎第二椎体的5个蓝牙感应器采集患者步行时的各种参数值。评定时让患者静止站在水平地面5 s以上采集静态数据后,嘱患者在自然地面上按日常步态形式直线行走。盖力步步态分析系统具有穿戴便捷、对检查场地无特殊要求以及可实时获得步态参数等优点,并且自然地上行走能更加准确地评估步态节奏的调节。本研究使用盖力步步态分析系统对卒中后步态参数进行数据收集,并利用相应的步态分析软件对步速、步幅时间、步频、步长时间差、着地冲击力差进行数字化评估分析。步速、步幅和步频是步行的主要参数,步速和步幅代表患者的步行能力,步频代表步行的稳定性和下肢控制能力,步长时间差、着地冲击力差是评价步态对称性的重要参数。

表8 两组卒中后偏瘫患者康复治疗前后10 m行走时间测试比较
本研究结果显示,治疗2周后,2组患者的步速、步频、步幅、FMA-LE量表评分较治疗前均有提高,且试验组改善优于对照组;治疗后,步长时间差、着地冲击力差和10-MWT相比治疗前均有减少,且试验组改善优于对照组。本研究结果与Thaut等[29]和Hamacher等[30]的研究结果一致,表明RAS可以提高卒中后患者的步行速度、步频和步幅,缩短步长差和着地冲击力差,改善卒中后步态的不对称,提高卒中后患者的步行能力。
综上所述,RAS可有效改善卒中后患者的下肢运动功能,提高患者步态的步行速度,改善患者的步态对称性,并且简便易行,不受训练场地和康复器械的限制,不额外增加患者的训练时间和费用,值得临床应用推广。本研究有一些局限性,如样本量小,未长期随访,不能确定RAS是否有长期效果。因此,进一步的对照研究需要更大样本量和更长时间的干预以确定RAS作为一种行走训练方式的临床益处。另外盖力步步态分析系统可获取髋膝踝的角度以及足偏角等步行空间参数和步行时足底压力的数据,由于目前仍无信度比较[31],本研究未对空间参数和压力参数进行比对分析,未来可对这些数据进行评估分析,为偏瘫步态训练提供更精准的康复训练。

