纳米TiO2/SiC复合材料的光致发光性能*
文程程,王冬华,杨 乐
(渭南师范学院 化学与材料学院,陕西 渭南714099)
作为重要的纳米半导体材料,TiO2和SiC广泛应用于传感器、电子器件、光电转换、光催化剂、发光材料等领域。材料的表面结构特性是在这些领域应用的重要影响因素[1-2]。由于纳米半导体材料的光致发光和光催化特性都是在适当能量光作用下的一种特性,均与光生载流子的产生、分离与复合动力学过程有很大关系,因此可以利用光致发光光谱从不同的角度揭示纳米半导体材料的表面氧空位和缺陷等结构特性、表面态及光生载流子的分离与复合等信息,为开发和制备高性能的半导体功能材料提供有力的理论依据[3]。
TiO2纳米材料因为具有抗腐蚀性较强、物理、化学性质稳定等特点受到关注,逐渐成为研究最多且应用最广泛的半导体材料之一[4]。杨金鑫等[5]通过微乳液静电纺丝法制备了多孔结构的TiO2纳米纤维,并具有优异的光催化性能;宋艳等[6]通过分步沉淀法制备了CdS/TiO2复合材料,对含重金属的废水有良好的处理效果。但是TiO2的带隙较宽(3.2 eV),且常规制备TiO2的方法需要进行高温煅烧,制成的TiO2易发生团聚,粒径增大,会降低TiO2的比表面积,影响光生电子和空穴的复合程度[7]。
SiC纳米材料由于带隙较窄(2.4 eV)、无毒无害、具有优良的光催化性能和极其稳定的化学性质,近年来逐渐成为光催化领域重要的研究方向[8]。郝建英等[9]通过碳热还原法制备蠕虫状纳米SiC,具有较好的光催化活性;成旭敏等[10]通过溶胶-凝胶法和碳热还原法制备SiC纳米线,对于甲基橙分解反应具有一定的光催化效果。单一的纳米SiC作为光催化剂仍存在以下问题。(1)纳米SiC与其他的单一半导体光催化剂一样,光生电子和电子空穴容易复合,从而降低了光生电子的浓度,影响光催化的效率;(2)SiC作为一种疏水性的材料,不易与液态体系反应物接触,影响其光催化反应的进行[11]。因此,通过光致发光光谱研究对SiC改性以增强其光催化性能的方法具有重要意义。
将TiO2与SiC进行复合,两者特性互相补充,降低光生电子与空穴的复合程度,改善材料的光催化特性。作者通过碳热还原法和溶胶-凝胶法合成了TiO2/SiC复合材料,并研究了不同w(TiO2)对TiO2/SiC复合材料光致发光性能的影响。
1 实验部分
1.1 原料、试剂与仪器
石墨粉:邯郸市启明碳素有限公司。
钛酸丁酯:化学纯,天津市福晨化学试剂厂;硝酸镍:西安化学试剂厂;正硅酸乙酯、六次甲基四胺:天津市天力化学试剂有限公司;草酸:天津市百世化工公司化学试剂厂;无水乙醇:利安隆博华(天津)医药化学有限公司;浓硝酸:北京化工厂;氢氟酸:四川西陇科学有限公司;以上试剂均为分析纯;去离子水:自制。
X射线衍射仪(XRD):XRD-6100,岛津企业管理(中国)有限公司;场发射扫描电子显微镜(FESEM):Sigma 500,卡尔·蔡司公司;X射线能谱仪(EDS):X-MAX-20,牛津仪器科技有限公司;荧光分光光度计(PL):F-7000,Hitachi(日立)公司;箱式高温烧结炉:KSL-1700XA2,合肥科晶材料技术有限公司;高温管式炉:SGL-1600,中国科学院上海光学精密机械研究所;分析天平:ME103E,METTLER TOLEDO公司;鼓风干燥箱:DHG-9005A,上海和呈仪器制造有限公司;真空干燥箱:DZF-6021,上海一恒科学仪器有限公司;磁力搅拌器:RCT Basic,艾卡(广州)仪器设备有限公司;循环水多用真空泵:SHB-D(Ⅲ),河南省泰斯特仪器有限公司。
1.2 纳米SiC的制备
(1)3 g硝酸镍溶解于100 mL无水乙醇中,加入50 mL正硅酸乙酯,滴加10 mLw(草酸)=3.4%溶液,持续搅拌并用保鲜膜密封,30 min后加入12 g棉花和100 mL无水乙醇,盖上保鲜膜后继续搅拌24 h后,逐滴加入10 mLw(六次甲基四胺)=35.8%溶液,继续搅拌直至形成凝胶。
(2)将凝胶烘干后研磨,并放入氩气保护的高温管式炉中,10 ℃/min升温至1000 ℃,2 ℃/min升温至1350 ℃,保温5h后随炉降至25 ℃。
(3)将高温管式炉中的样品取出后放入箱式高温炉中,800 ℃煅烧2 h,冷却后取出进行酸洗[V(氢氟酸)∶V(浓盐酸)=3∶1],并浸泡24 h,抽滤,然后用去离子水反复清洗至滤液呈中性。
(4)将得到的样品重复(3)操作,最终烘干样品得到浅绿色的SiC粉末。
1.3 纳米TiO2的制备
取10 mL钛酸丁酯,将其溶入40 mL无水乙醇中,搅拌20 min,滴加5~6滴浓硝酸,得到溶液A;取6 mL去离子水和6 mL无水乙醇,均匀混合后得到溶液B,将溶液B缓慢滴加到溶液A中,形成淡黄色且透明的凝胶,将凝胶捣碎,放入鼓风干燥箱中100 ℃烘干3 h,取出研磨后得到浅黄色粉末,放入箱式高温烧结炉中煅烧,5 ℃/min升温至300 ℃,1 ℃/min升温至500 ℃保温3 h,得到白色的TiO2粉末[12]。
1.4 TiO2/SiC复合材料的制备
在4只100 mL烧杯中分别加入20 mL无水乙醇和0.2 g SiC,再量取0.1、0.2、0.3、0.4 mL钛酸丁酯置于其中,搅拌均匀,加入2~3滴浓硝酸,分别滴加0.2、0.4、0.6、0.8 mLV(无水乙醇)∶V(去离子水)=1∶1溶液,搅拌30 min,放入烘箱烘干,高温烧结炉5 ℃/min升温至300 ℃,1 ℃/min升温至500 ℃,保温3h,得到浅绿色的TiO2/SiC复合材料。复合材料中的w(TiO2)=10%、20%、30%、40%,分别记为10%TiO2/SiC、20%TiO2/SiC、30%TiO2/SiC、40%TiO2/SiC。
1.5 材料性能表征
采用XRD对样品的结晶性和纯度进行分析,测试条件为铜靶,扫描速度5°/min,扫描范围10°~80°,步长0.02°;采用FESEM对样品进行微观形貌分析;采用EDS对样品进行化学成分分析;采用PL对样品的光致发光性能进行分析,测试参数为荧光发射波长330 nm,扫描范围200~700 nm,扫描速度2 400 nm/min。
2 结果与讨论
2.1 SiC和TiO2及其复合材料的XRD图谱分析
2.1.1 纳米SiC的XRD分析
对实验制得的绿色粉末进行XRD物相分析,结果见图1。
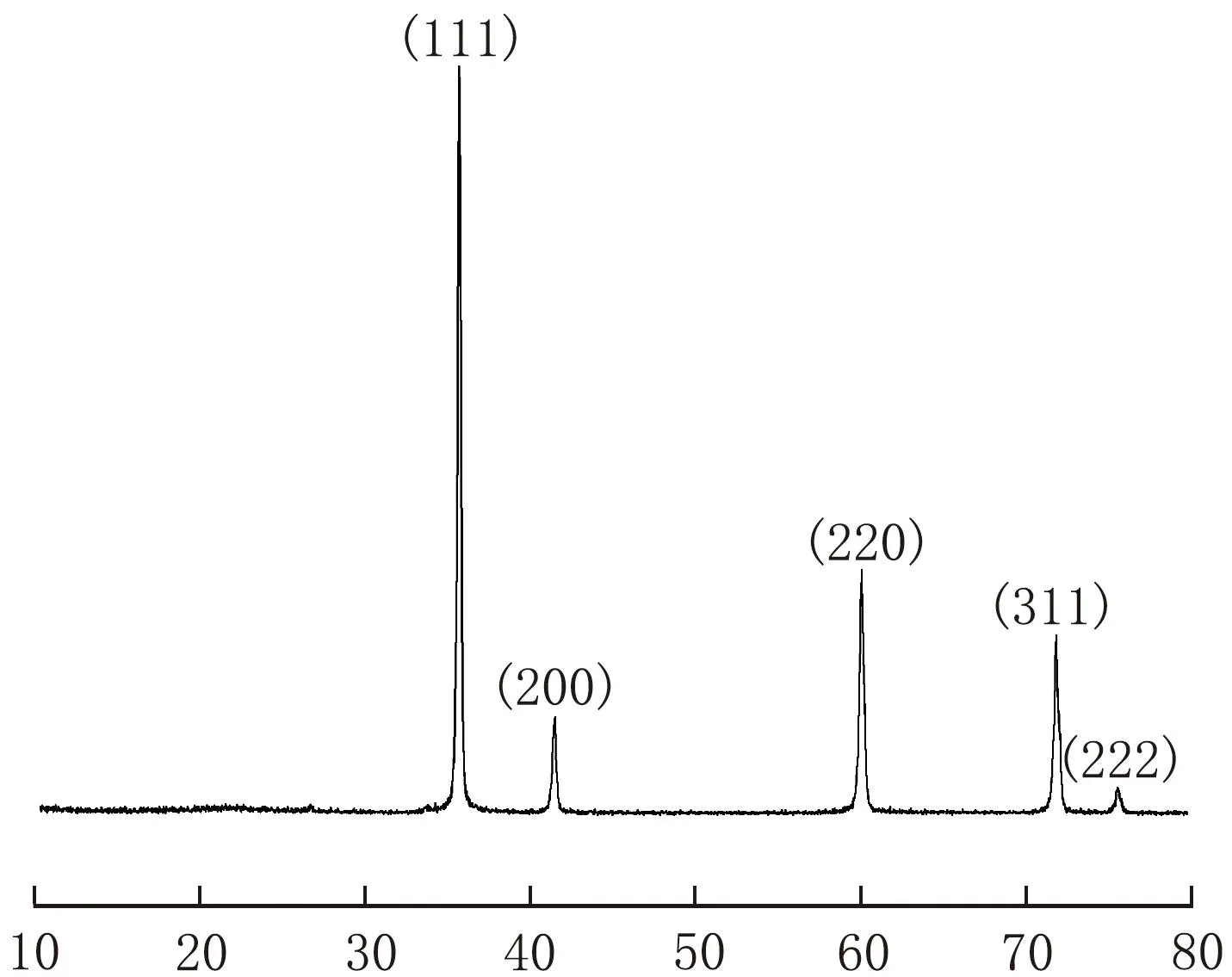
2θ/(°)图1 SiC样品的XRD谱图
由图1可知,2θ=35.62°、41.38°、59.98°、71.74°、75.36°出现了衍射峰,各峰位置与β-SiC的(111)、(200)、(220)、(311)和(222)衍射面相对应,与SiC标准图谱的衍射峰位置相匹配,即该样品为β-SiC。样品的XRD谱图中无其他杂峰,表明SiC的纯度较高,并且谱图中的衍射峰强而尖锐,说明样品的结晶性较好。
2.1.2 纳米TiO2的XRD分析
对制备的白色粉末样品进行XRD分析,结果见图2。
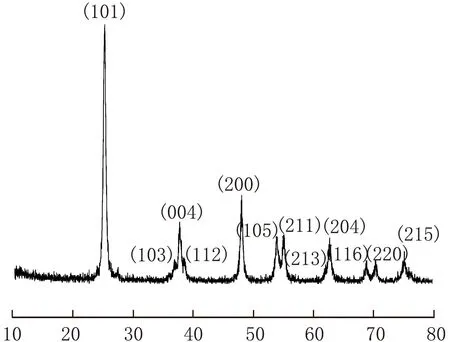
2θ/(°)图2 TiO2样品的XRD谱图
由图2可知,2θ=25.18°、37.64°、37.78°、37.88°、47.98°、54.02°、55.16°、62.16°、62.74°、68.68°、70.40°、75.02°出现衍射峰,峰的位置与锐钛矿TiO2的(101)、(103)、(004)、(112)、(200)、(105)、(211)、(213)、(204)、(116)、(220)、(215)衍射面相对应,且与标准图谱的衍射峰相对应,证明样品为锐钛矿TiO2,此外谱图中无其他杂峰,表明TiO2的纯度较高,并且谱图中的衍射峰强而尖锐,说明样品的结晶性较好[13]。
2.1.3 TiO2/SiC复合材料的XRD分析
对实验所制得的不同w(TiO2)复合材料进行XRD分析,结果见图3。
由图3可知,谱图中出现的衍射峰,均有TiO2或SiC中的衍射峰与之对应,证明样品为两者形成的复合材料,无TiO2和SiC的衍射峰之外的其他杂峰,说明样品无杂质。此外,随着复合材料中w(TiO2)的增大,SiC衍射峰的相对强度随之变小,TiO2衍射峰的强度随之增大,表明得到的样品为TiO2/SiC复合材料。
2.2 SiC和TiO2及其复合材料的FESEM、EDS分析
2.2.1 SiC和TiO2的FESEM分析
不同放大倍数SiC样品的微观形貌图见图4。

a 放大20 000倍
由图4可知,SiC样品主要由短棒组成;SiC纳米棒的直径为50~200 nm。纳米棒表面不光滑,有大量堆积缺陷。
不同放大倍数TiO2的微观形貌图见图5。

a 放大10 000倍
由图5可知,制备的TiO2呈较大块状,由小颗粒组成,直径为20~50 nm,分布比较均匀。
2.2.2 不同w(TiO2)复合材料的FESEM及EDS分析
不同w(TiO2)复合材料的FESEM及EDS分析结果见图6。
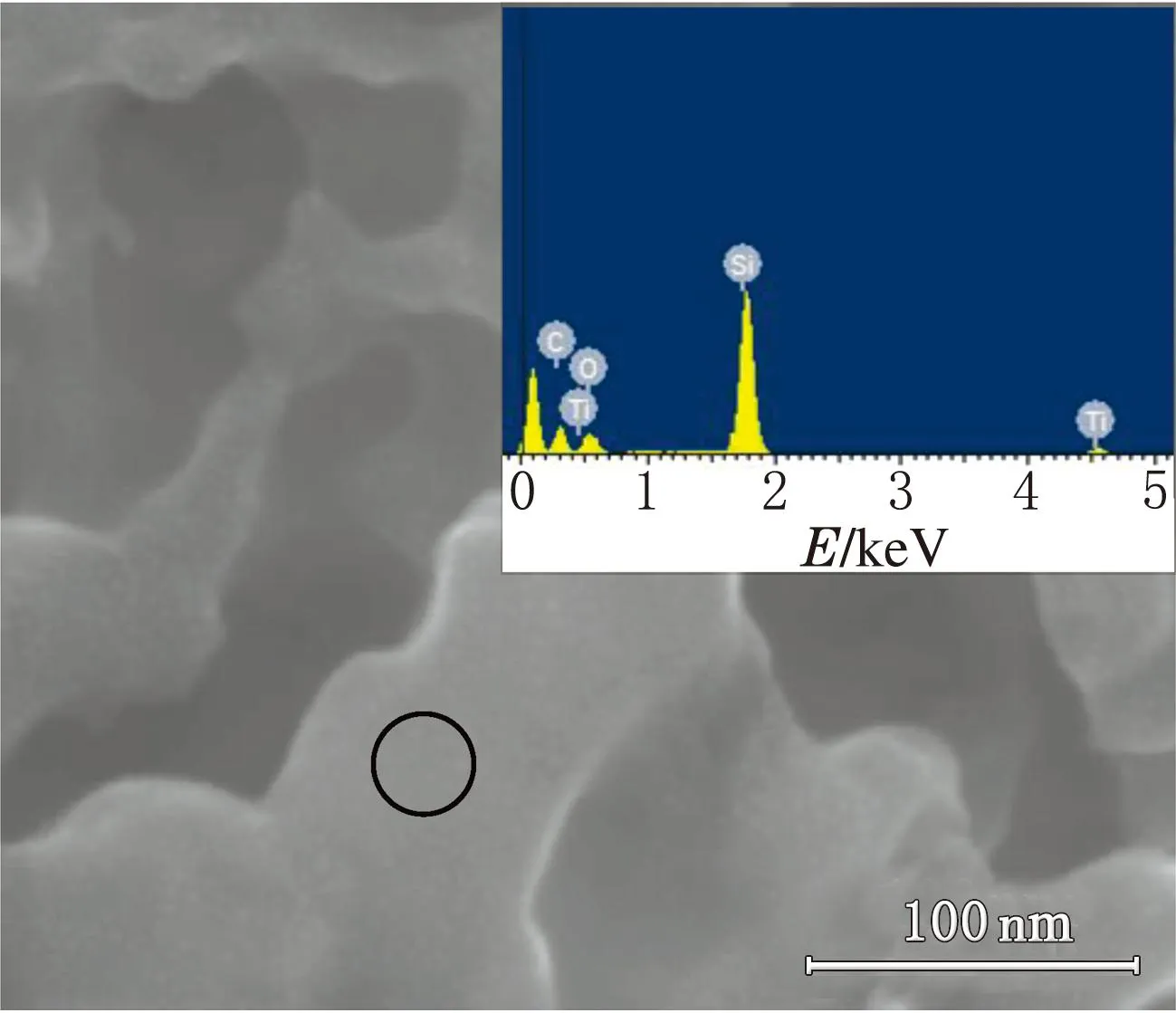
a 10%TiO2/SiC
由图6a可知,无法清晰观察到TiO2颗粒,是因为样品中w(TiO2)太少;由图6b可知,SiC纳米棒弯曲部分的直径约为300 nm,表面凹凸不平,铺满TiO2小颗粒,直径为20~40 nm,颗粒分布较为均匀;由图6c可知,SiC纳米棒表面可以观察到明显的颗粒,附着较均匀;由图6d可知,SiC表面TiO2分布不均匀,一部分有明显较多的TiO2颗粒,表明随着w(TiO2)的增加,TiO2纳米颗粒不能均匀分布在SiC纳米棒表面。能谱分析结果均显示样品中存在C、O、Ti、Si 4种元素,证明制备的样品均为TiO2/SiC复合材料。
2.3 SiC和TiO2及其复合材料的光致发光性能分析
对实验中合成的SiC、TiO2和TiO2/SiC复合材料进行光致发光性能分析,结果见图7。

λ/nm图7 样品的光致发光谱图
由图7可知,SiC在365 nm发射峰最大,该发射峰由SiC纳米棒表面堆积缺陷的量子限制效应产生,与文献[14]结论一致。TiO2在377、399和469 nm出现发射峰,前两者是由于带边自由激子发光形成,后者由束缚激子发光形成,均源于TiO2纳米颗粒表面的氧空位和缺陷等,与文献[15]结论一致。实验制备的TiO2纳米颗粒尺寸较小,表面存在大量氧空位,电子运动的平均自由程短,因此空穴束缚电子形成激子的概率大,激子发光信号强。
随着w(TiO2)增加,TiO2/SiC复合材料光致发光性能出现明显差异。样品均在约365 nm出现最大发射峰,与纯SiC发射峰位置基本一致。这是由于复合材料中w(TiO2)较少,光致发光性能主要由SiC决定。469 nm出现了明显的发射峰,与TiO2的发射峰位置基本一致;399 nmTiO2的发射峰变得较弱。w(TiO2)=10%,发射峰强度远大于纯SiC发射峰强度,主要是因为w(TiO2)较少,该发射峰依然由SiC纳米棒表面的堆积缺陷的量子限制效应而产生。由XRD和EDS分析结果可知,质量分数为10%的TiO2与SiC复合后,对SiC晶相影响较小,说明TiO2较均匀的分散在SiC表面。这可能会引入缺陷,当光照射到复合材料表面时产生了大量的电子空穴对,受到缺陷量子限制效应的影响,光生电子和空穴迅速复合,因此发射峰强度较强。较少量的TiO2纳米颗粒表面的氧空位能够束缚电子形成激子,表现出与TiO2一致的发射峰,但由于数量较少,因此399和469 nm的发射峰强度比纯TiO2发射峰强度低。w(TiO2)=20%,SiC纳米棒表面的TiO2均匀分布,SiC纳米棒大部分表面堆积缺陷被覆盖,量子限制效应导致的光生电子和空穴的复合几率减小,所以发射峰的强度比纯SiC发射峰强度小。TiO2纳米颗粒的均匀分布也使得氧空位和缺陷数量减少,光生电子与空穴的复合几率减小,因此发射峰强度减弱,表明两者复合后有效阻止了光生电子和空穴的复合。随着w(TiO2)继续增加,SiC纳米棒表面被TiO2纳米颗粒完全覆盖,光致发光性能主要由TiO2纳米颗粒表面的氧空位和缺陷等决定,由于SiC纳米棒表面w(TiO2)较少,因此发射峰强度较低,且随着w(TiO2)再增加,发射峰强度没有太大变化。
3 结 论
以石墨粉为碳源,正硅酸乙酯为硅源,通过溶胶-凝胶法和碳热还原法可以制得结晶性较好的绿色SiC纳米棒;以钛酸丁酯、SiC为原料,通过溶胶-凝胶法制备得到不同w(TiO2)的TiO2/SiC复合材料。讨论了w(TiO2)对TiO2/SiC复合材料光致发光性能的影响,w(TiO2)=10%,发射峰强度比纯SiC和TiO2发射峰强度大,主要与SiC和TiO2表面缺陷的量子限制效应有关。随着w(TiO2)增加,发射峰强度下降,w(TiO2)=30%,发射峰强度无明显变化,由于SiC纳米棒表面被TiO2纳米颗粒均匀覆盖,因此光致发光强度主要与TiO2纳米颗粒表面的氧空位和缺陷的量有关。
——潘桂棠光生的地质情怀

