体质量指数对前列腺癌合并心血管疾病的老年患者预后的影响及列线图构建
白盼盼,李春霞,卜星彭,,兰宁,陈还珍,3*
(1山西医科大学公共卫生学院,太原 030012;2山西白求恩医院综合医疗科,太原 030032;3山西医科大学第一医院心血管内科,太原 030001)
前列腺癌(prostate cancer,PCa)是一种常见的激素敏感性恶性肿瘤[1]。2020年GLOBOCAN数据示,前列腺癌发病和死亡的世界人口标化率分别为30.7/10万、7.7/10万,分别位列全球男性癌症谱的第2位和第5位[2]。我国目前处低发地区,但近年总体呈现上升趋势[3]。与一般人群相比,PCa患者更易合并心血管病[1](cardiovascular disease,CVD),且预后生活质量和生存率均下降[4],以致人们越来越关注肿瘤心脏病学科。
报告示CVD是前列腺癌症幸存者死亡的主要原因[5],癌症诊断后第1年死于心血管疾病和其他非癌症事件的发生率高于预期[6],体现早期预防的重要性。列线图被广泛用于癌症预后[7],可针对患者个体情况以可视化地方式呈现临床事件发生的概率[8]。对此,本研究通过回顾性分析前列腺癌合并CVD患者的临床资料,探索并构建前列腺癌伴CVD患者的预后列线图,为预后判断及个体化治疗提供依据。
1 对象与方法
1.1 研究对象
回顾性分析2019年5月至2021年5月于山西医科大学第一医院心血管内科、肿瘤科及泌尿外科住院治疗的237例前列腺癌合并CVD患者的临床资料。前列腺癌诊断标准见2019版《中国泌尿外科疾病诊断治疗指南》,心血管疾病诊断见《心血管内科疾病诊疗指南(第3版)》,包括冠状动脉疾病、中风、心肌炎、心力衰竭、心律失常、主动脉瘤、动脉粥样硬化和高血压等。所有患者均接受前列腺特异抗原(prostate specific antigen,PSA)、直肠指诊、经直肠超声(transrectal ultrasound,TRUS)检查、血液、尿液、心电图、心脏彩超等检查。纳入标准:(1)年龄≥60岁;(2)病理诊断为前列腺恶性肿瘤(前列腺癌、前列腺肉瘤、癌肉瘤);(3)合并心血管疾病;(4)临床资料、结局信息完整。排除标准:(1)多源性肿瘤;(2)合并多器官功能障碍;(3)信息不完整、生存时间不足1d、意外事故住院或入院原因不明确的病例。病历获取通过山西医科大学第一医院伦理委员会审核批准{[2020]伦审字(K071)号},患者知情同意豁免。
因体质量指数(body mass index,BMI)与心血管风险息息相关,本研究按照中国肥胖问题工作组推荐的划分标准将患者分为高BMI组(BMI≥24.0kg/m2)与低BMI组(BMI<24.0kg/m2)。
采用电子病历系统采集所有患者的人口学资料(包括年龄、心率、血压、BMI等)、既往史及合并症(高血压、冠心病、心肌梗死等)、实验室检验(血红蛋白、总胆固醇、甘油三酯、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、前列腺特异性抗原等)及再住院情况。
1.2 终点事件
研究期间所有病历从数字病历系统中获取,主要终点为1年内CVD再入院,以主要诊断为主,次要终点为1年内全因死亡。若患者在本院死亡或再入院,可从病历系统中获取;若在其他医院死亡或再次入院,则通过随访本或电话短信记录信息。研究截止至患者发生结局或固定日期(2021年6月1日),至截止日期仍存活的患者以研究截止日作截尾处理,对失访或再入院信息不完整者全部予以排除。考虑到慢病患者会反复住院,本研究只分析研究期间出院后首次CVD再入院。
1.3 统计学处理
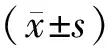
2 结 果
2.1 两组患者基线资料比较
符合纳入与排除标准的患者共255例,剔除失访和缺失过多的病历后,共237例前列腺癌合并CVD患者资料纳入统计分析。患者年龄60~93(75.58±7.54)岁;低BMI组127例,高BMI组110例。与高BMI组比较,低BMI组患者心率慢,舒张压、血红蛋白和甘油三酯水平低,生存时间短,但合并糖尿病者较少,差异有统计学意义(均P<0.05);其他资料比较,差异无统计学意义(均P>0.05;表1)。
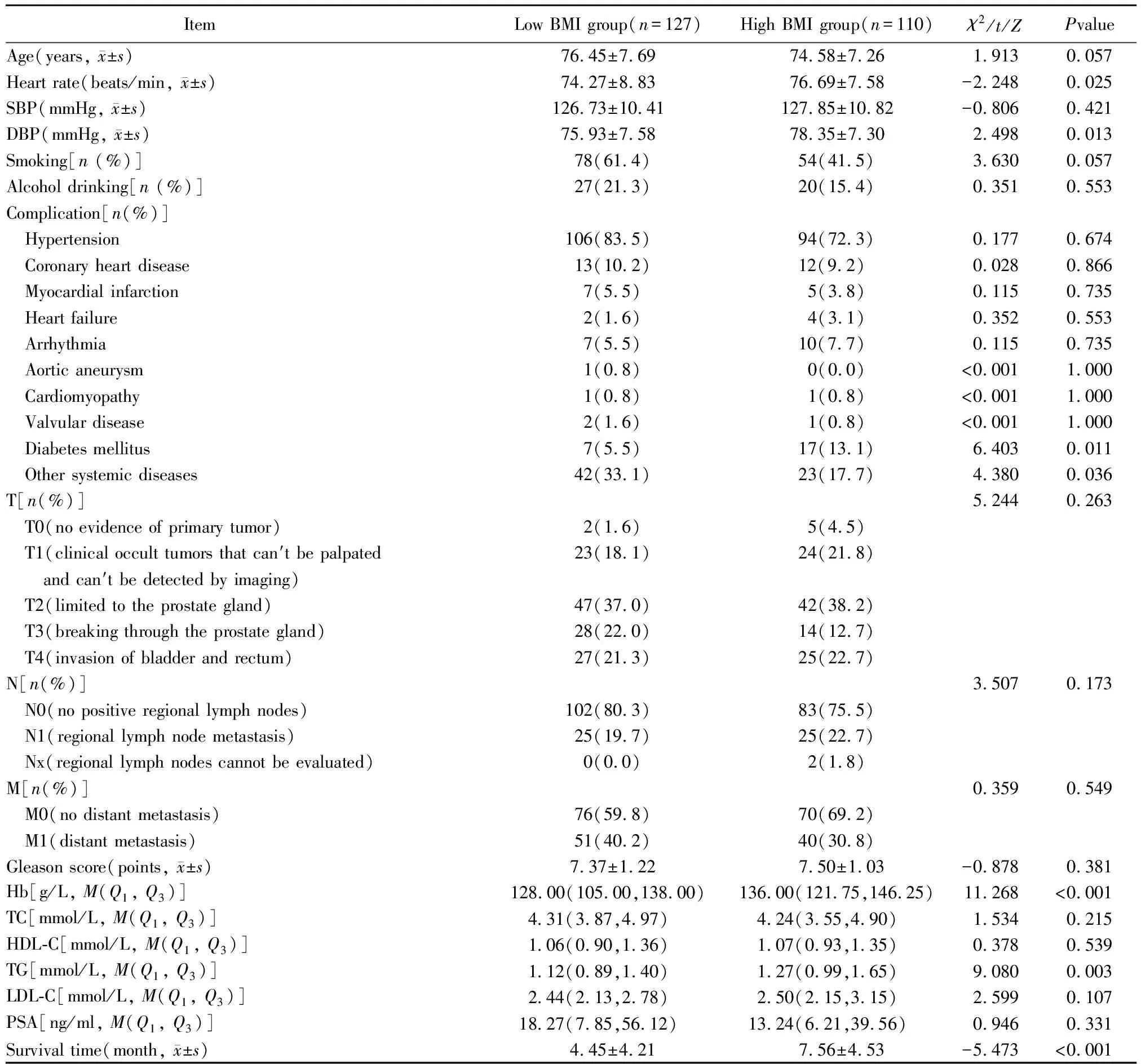
表1 两组患者基线资料比较
2.2 两组患者终点事件情况比较
1年内患者因CVD再入院共118例,其中低BMI组71例(55.9%),高BMI组47例(42.7%)。低BMI组再入院率高于高BMI组,尤其是因冠心病再入院患者,差异有统计学意义(P<0.05)。1年内全因死亡共4例(1.7%),其中低BMI组3例(2.4%),高BMI组1例(0.9%),两组比较,差异无统计学意义(P>0.05;表2)。
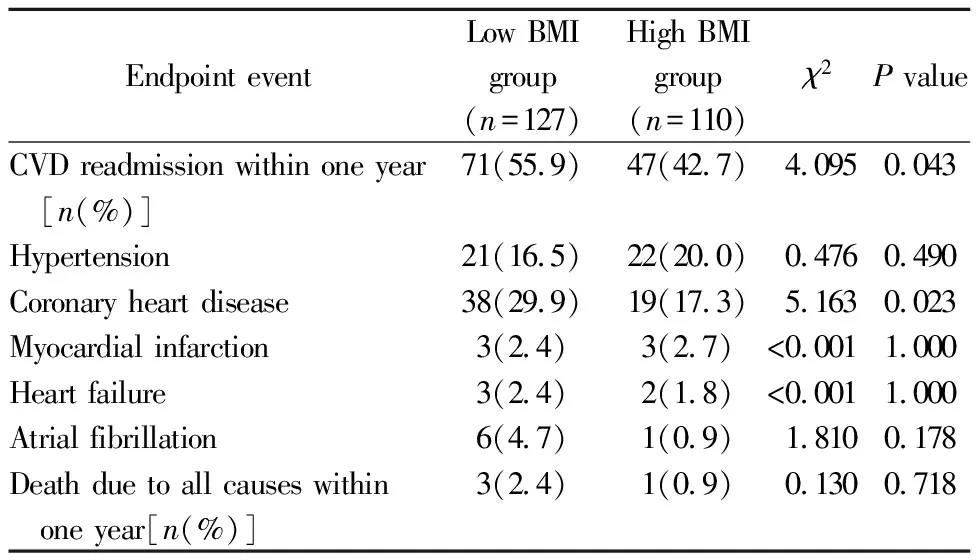
表2 两组患者终点事件情况比较
Kaplan-Meier生存曲线显示,低BMI组中位生存时间为6.6个月,高BMI组为11.6个月。与高BMI组比较,低BMI组1年CVD再入院率更高(HR=1.524,95%CI1.263~1.840;P<0.0001),且随时间延长,两组的差异越明显(图1)。
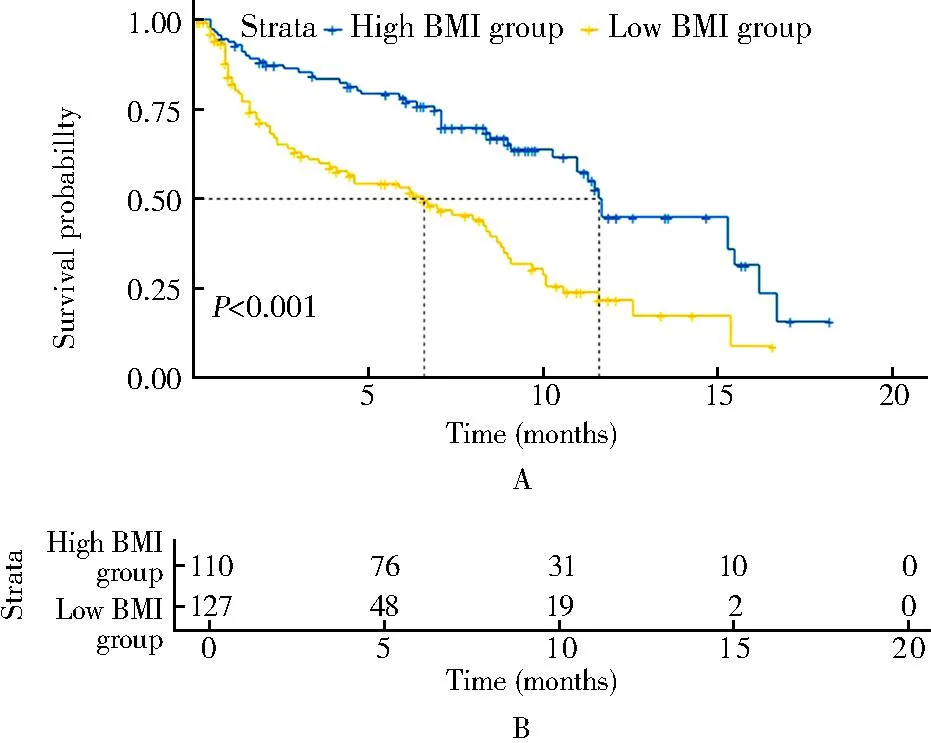
图1 患者CVD再入院的Kaplan-Meier生存曲线图Figure 1 Kaplan Meier survival curve of patients with CVD readmission A: Kaplan-Meier survival curves for two prognostic groups; B: the risk table, which refers to the number of people who did not have an outcome but may have an outcome. The two rows of figures in figure B correspond to the two curves in figure A respectively. CVD: cardiovascular disease.
2.3 Cox回归分析CVD再入院的影响因素
Cox单因素回归分析发现,高龄、吸烟、肿瘤转移、高总胆固醇、伴其他系统疾病与CVD再住院的发生风险增加相关,而高BMI和高水平高密度脂蛋白胆固醇是保护因素(均P<0.05)。Cox多因素回归分析发现,吸烟、其他系统疾病及高总胆固醇是独立危险因素;高BMI和高水平高密度脂蛋白胆固醇是CVD再住院发生的独立保护因素(均P<0.05;表3)。
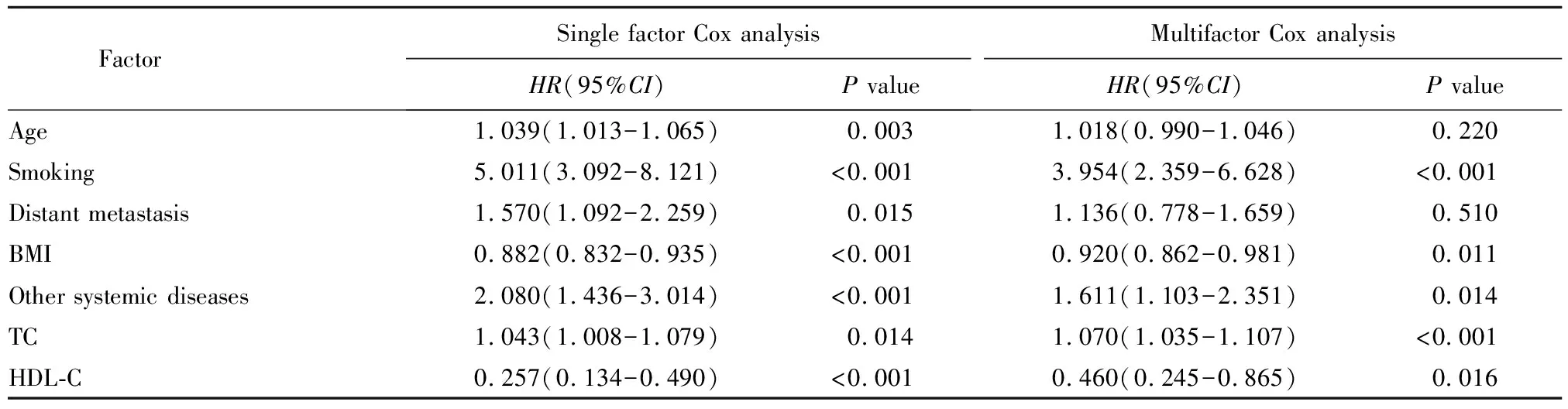
表3 患者CVD再入院的Cox多因素回归分析
2.4 列线图的构建与验证
将Cox多因素分析得出的5个独立预后因素(吸烟、BMI、其他系统疾病、总胆固醇和高密度脂蛋白胆固醇)纳入列线图的绘制,构建前列腺肿瘤伴CVD患者3、6、12个月CVD再入院概率的预测列线图。通过列线图可得到各预后因素对应标尺上的积分,在各积分的总分标尺上向下画一条,即可得到患者3、6、12个月的生存率。总分越高,预后越差。以数据集第10位患者为例绘制动态列线图,该患者64岁,吸烟、伴其他系统疾病,BMI 22.8kg/m2,总胆固醇1.24mmol/L,HDL-C 0.98mmol/L,则该患者3个月CVD再入院概率约为0.418,6个月CVD再入院概率为0.542,1年CVD再入院概率为0.925。
列线图C-index为0.731(95%CI0.686~0.776),3、6、12个月ROC曲线下面积分别为0.759(95%CI0.689~0.829)、0.767(95%CI0.699~0.834)和0.804(95%CI0.696~0.912),AUC值在0.671~0.804波动,表示模型具有良好的预测精度。采用Bootstrap内部检验1000次,显示列线图预测3、6、12个月的CVD再入院的红色校准曲线接近理想情况的黑色虚线,呈现较好的一致性,表示预测值与实际值具有较好的符合度(图2,图3)。
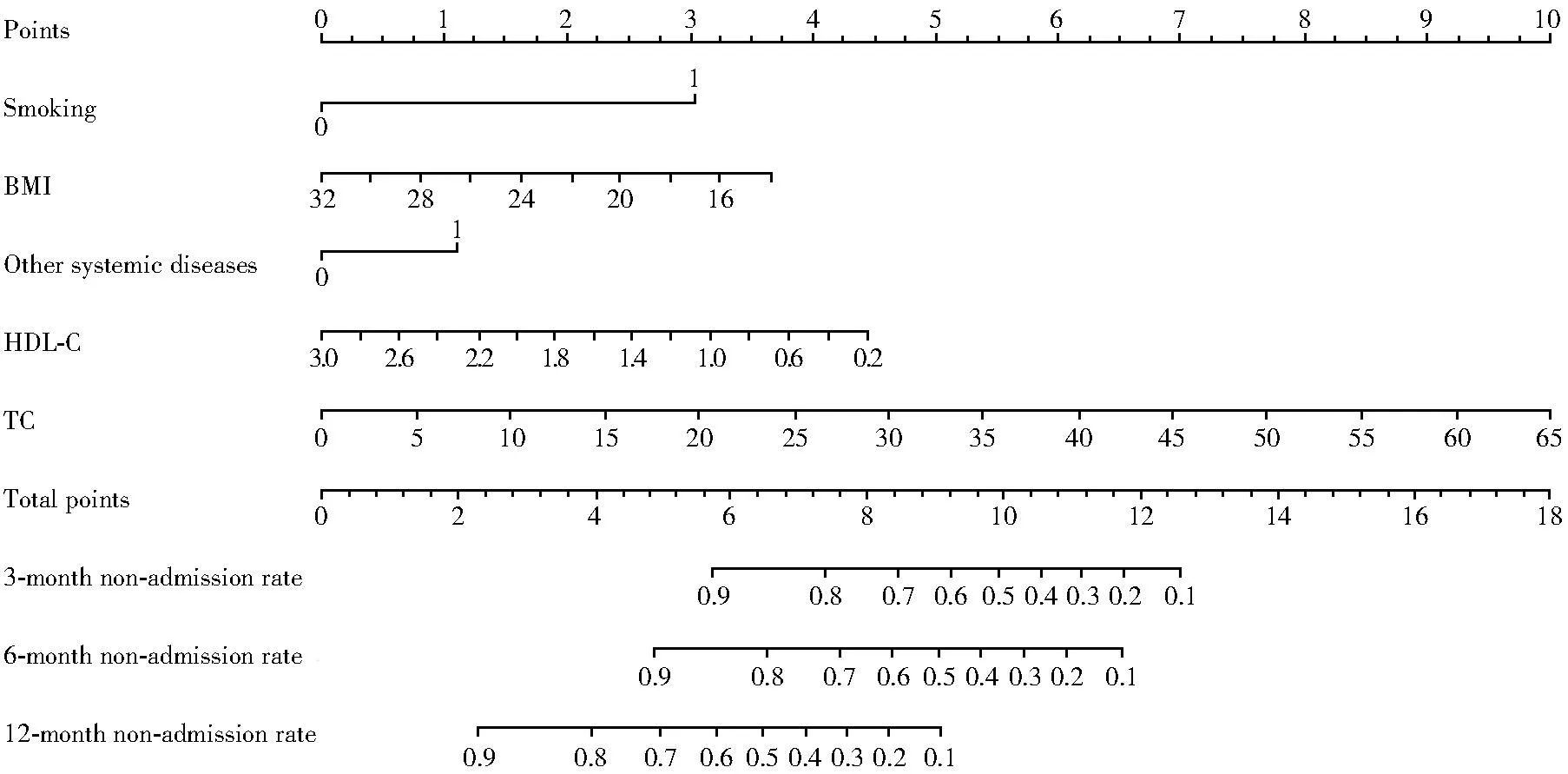
图2 患者CVD再入院的列线图(二分类项0代表否,1代表是)Figure 2 Nomogram of patient CVD readmission (binary item 0 represents no, 1 represents yes)CVD: cardiovascular disease; BMI: body mass index; HDL-C: high-density lipoprotein cholesterol; TC: total cholesterol.
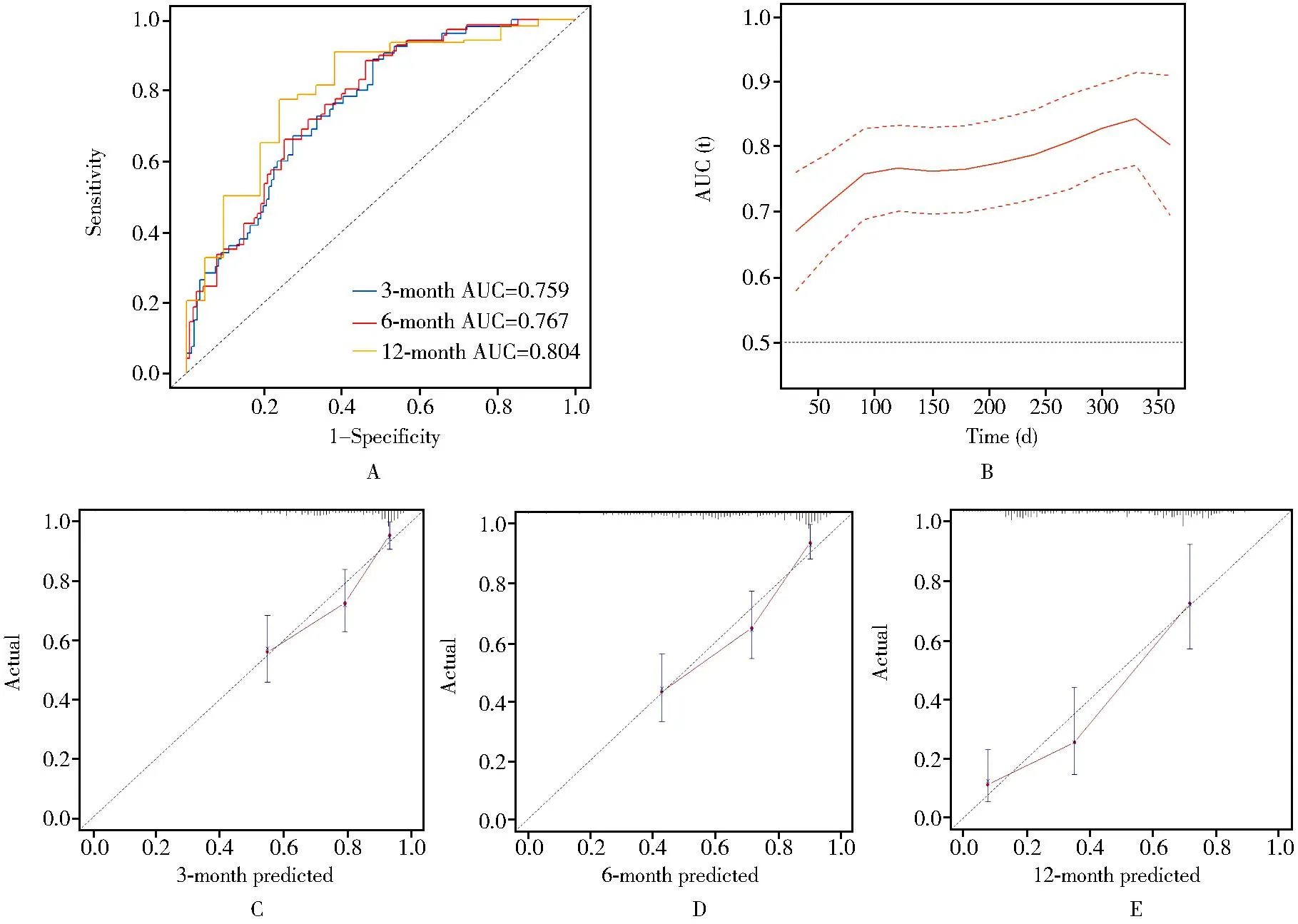
图3 列线图验证Figure 3 Line chart validation A: time ROC curve; B: time AUC curve; C: 3-month calibration curve; D: 6-month calibration curve ; E: 12-month calibration curve.AUC: area under the curve.
3 讨 论
心血管疾病是全球死亡、致残和医疗费用上涨的主要原因,已成为全球重大公共卫生问题[9]。尽管人们越来越意识到非传染性疾病对人类发展构成的威胁,但大多数国家的非传染性疾病控制进展缓慢[10]。《中国心血管健康与疾病报告2021概要》[11]中估计心血管病现患人数3.30亿,同时考虑到CVD发病率和死亡率的高流行率及前列腺疾病日益复杂的管理,患者存活率尤其重要[12]。传统的肿瘤分期(tumor node metastasis,TNM)不能很好地推测患者预后,更无法个体化地为患者预后提供指导。从患者的远期生存考虑,明确患者的预后因素并运用生存预测模型具有重要的临床意义。目前,国内外关于心脏肿瘤患者的生存预测仍缺乏可靠的模型。列线图作为临床疾病预测和预后评估的可视化工具,已被应用于评价多种疾病的预后,且都展示了良好的预测价值[13]。因此,本研究基于临床真实数据构建预测前列腺癌合并CVD患者预后的列线图,为预测预后差的患者及早提供更好的治疗方法,为具体的临床决策的制定提供参考依据。
本研究通过Cox多因素回归分析得出,吸烟、其他系统疾病、高总胆固醇是前列腺肿瘤合并CVD患者心血管病再入院的独立危险因素。有研究显示吸烟是前列腺肿瘤和CVD患者主要危险因素[14],与本研究结果基本一致。本研究中合并其他系统的慢病患者预后差,显而易见,疾病的叠加加强了各系统间的联系,使患者身体耐受性更差。本研究还发现总胆固醇水平不同的患者预后可能有差异,研究证实高总胆固醇与较高的总死亡率、心血管疾病和癌症死亡率相关,但需进一步的研究来证实[15]。此外,Cox多因素回归分析结果显示,高BMI、高HDL-C是CVD再入院的独立保护因素。HDL-C水平与全因死亡率、心血管疾病和癌症相关,呈J形剂量反应模式[16]。低浓度的HDL-C是心血管疾病的危险因素,与本研究结果一致。矛盾的是,极高的HDL-C水平同样也增加心血管风险,该研究发现HDL-C与CVD呈U型关系[17]。这种关联目前仍存在争议。关于HDL-C与前列腺肿瘤,有研究发现血清HDL-C升高与前列腺癌的风险增加有关[18]。然而,其他一些研究未发现HDL-C与前列腺肿瘤之间有任何关联[19]。这些不同的结果可能是由于所用的研究方法和随访差异有关,或数据中缺乏雄激素依赖性的相关指标,而本研究的研究对象是两种疾病的合并者,可能与两种疾病间的影响机制有关,目前也尚不明确。国外许多研究发现,BMI与肿瘤和CVD之间有潜在联系[20]。有研究表明,高BMI可以增加心血管疾病的死亡率,且与前列腺肿瘤的发病率呈正相关[21],而“肥胖悖论”则表明超重和轻度肥胖的患者对CVD和癌症具有潜在保护作用[22],可能与高BMI患者的身体更耐受疾病的消耗有关。既往研究发现前列腺癌和心血管疾病之间可能与代谢综合征有关[23]。代谢综合征的关键特征是由遗传风险因素、环境和生活方式暴露相互作用造成能量失衡。同样会使内皮依赖性血管舒张和动脉顺应性受损,进而动脉粥样硬化,由此产生的生理异常可能造成血栓和炎症状态。代谢综合征及其相关的心血管风险在前列腺癌的管理中变得越来越重要,特别是在对生活质量和健康资源利用的潜在影响的背景下[24]。因此,需要进一步研究前列腺疾病与CVD之间及与代谢综合征之间的潜在机制,以制定疾病预防策略。
高龄是心血管和前列腺疾病相关的危险因素之一,单因素Cox分析显示有显著差异,但多因素Cox分析未显示差异有统计学意义,可能是本研究纳入的对象均为60岁及以上的老年患者,各因素间相互作用使得年龄差异不明显。远处转移是肿瘤侵袭力的表现,但本研究将肿瘤转移纳入Cox多因素回归分析后,其未显示出与患者再入院的显著相关性。究其原因可能是本研究中部分对象肿瘤未进展或转移已经对肿瘤的恶性程度进行了一定的限定,也可能更多受其身体状况和多种慢病进展的影响,在较短的生存期中难以表现出差异。
综上,本研究基于临床真实数据,确定了前列腺癌合并心血管病患者预后的影响因素,构建了列线图模型,未来可运用到医疗系统中,为患者进行短期预后评估。从C-index、ROC和AUC曲线可以看出,该列线图内部验证预测效果良好,校准图显示预测的生存率与实际生存率符合度较高,呈现良好的一致性。但仍存在局限:本研究是一项单中心、回顾性分析,观察时间不长,虽得出有意义的结果,但仍需更大样本的研究进一步验证;临床资料中缺少家族史、肿瘤大小、治疗情况等;国内外关于CVD合并前列腺肿瘤患者的预后研究很少,缺乏相关参考依据。因此,本研究属于探索性研究,模型的实际应用还需通过多个中心扩大样本量以及前瞻性研究验证,以进一步提高模型的预测精度和推广价值。

