新条例实施后国产普通化妆品备案的问题与对策
谢化宏
摘要:文中通过对新备案平台运行起至2022年9月30日厦门市近一年国产普通化妆品备案技术审核发现问题的数据分析,剖析主要问题及其原因,并提出解决问题的对策,为化妆品备案人规范备案流程,提升备案质量提供参考。
关键词:国产普通化妆品备案;技术审查;产品执行的标准;安评资料
Challenges and Countermeasures of Filing Domestic Ordinary Cosmetics after the Implementation of the New Regulations
——Take Xiamen as an Example
XIE Huahong
( Xiamen Administration for Market Regulation, Xiamen 361004, Fujian, China )
Abstract: Through the data analysis of the problems found in the technical review of the filing of domestic ordinary cosmetics in Xiamen from the operation of the new filing platform to September 30, 2022, this paper analyzes the problems found, points out the crux of the problems, and puts forward the direction for solution and the focus for improvement, which provides a reference for cosmetic filers to standardize the filing process and improve the filing quality.
Key Words: Domestic ordinary cosmetics filings; Technical review; Standards implemented by products; Safety assessment data
0引言
《化妆品监督管理条例》[1](以下简称“《条例》”)于2021年1月1日实施后,以及《化妆品注册备案资料管理规定》[2](以下简称“《管理规定》”)、《化妆品安全评估技术导则》[3](以下简称“《技术导则》”)等一系列规范性文件的相继发布,要求国产普通化妆品备案人于2022年12月31日前完成历史产品的备案资料补录工作,对于2022年1月1日后提交普通化妆品备案的化妆品备案人可提交简化版产品安全评估报告,并于2024年5月1日以后提交完整版产品安全评估报告[3]。这些新的要求和规定旨在规范企业生产前的产品设计环节,提升企业产品质量是杜绝不安全的产品流向市场的源头性监管手段,但是在备案审查过程中,笔者发现备案企业提交的国产普通化妆品备案材料存在不完整、不规范、不科学等诸多问题,备案企业一次性通过率仅为6.7%,甚至有的企业提交多次都无法通过备案,这不但给企业造成了很大的困惑,也增大了监管部门的工作压力。文中以厦门市备案企业的产品审核情况为例,剖析现阶段国产化妆品备案企业产品备案过程中存在的难点问题,旨在指出问题症结所在并提出解决方向及改进着力点,指导备案企业更快更好的完成备案,提升国产化妆品行业备案水平。
1厦门国产普通化妆品备案产品审核概况
1.1备案审核总体情况
从新备案平台运行起至2022年9月30日,依据《管理规定》以及《技术导则》等规范性文件,并按国产普通化妆品备案平台系统报送项目:備案申请表、命名依据、产品配方、产品执行的标准、产品标签、检验报告和安评资料等七大版块对发现问题的描述,开展技术审查1355款产品,发现问题产品1264款,占比高达93.4%,通过率仅6.7%。
1.2七大版块发现问题统计
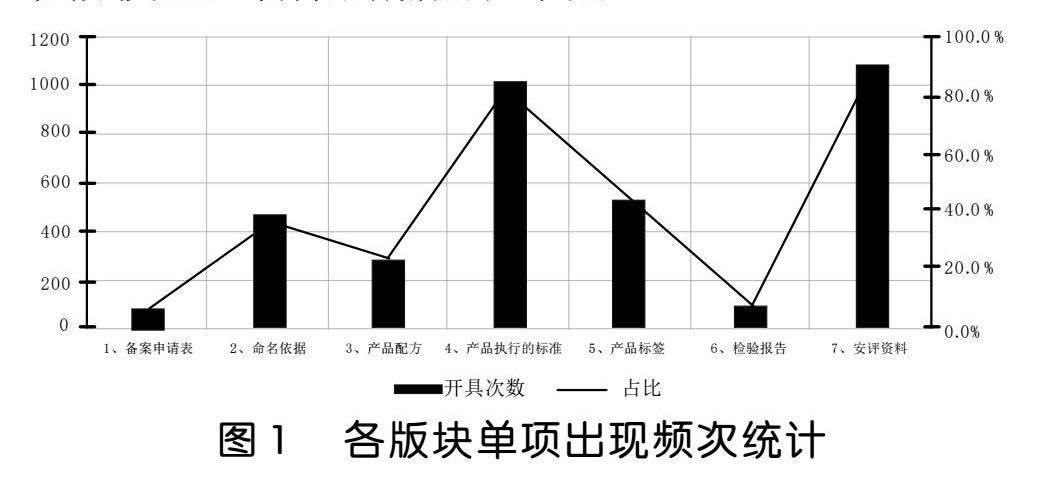
根据每款产品发现问题所含版块情况的数据统计分析,分别以每个产品发现问题的版块数和各版块单项出现频次进行统计。在1264款问题产品中,有1033款产品有2~4个版块发现问题,占总数的76.2%。其中,产品执行的标准和安评资料同时被开具有789款,占比76.3%。另外从各版块单项出现频次统计可知(见图1),在1264款问题产品中产品执行的标准和安评资料占比分别高达81.3%、86.6%,远高于位列第三产品标签的43.3%。进而可知,产品执行的标准和安评资料是现阶段企业备案的痛点和难点。
2 主要问题及原因分析
七大版块中被出具问题最多的版块是产品执行的标准和安评资料,这两个版块均是《条例》第十九条提出的新要求。产品执行的标准发现的问题是理化和微生物指标、感官指标以及产品生产工艺的规范性、合规性问题。安评资料发现的问题主要是由原料的辨识、生产工艺以及毒理学数据等问题所引发的,具体问题表现形式及其原因如下:
2.1产品执行的标准版块的问题
《条例》要求化妆品标签标注产品执行的标准编号,意在引导化妆品行业推行“一品一标”,运用标准管理的手段推动产品质量提升[4]。产品技术要求是产品执行的标准的前身,企业在制定产品执行的标准过程中,被原先制定技术要求所依据的推荐性国标、行标固化了思路,并在质量管理实践过程中未对各项目指标进行合理的质量评估、验证,以致于面对将各项目指标质量控制措施及其相关说明以备案资料的形式规范的上报要求,呈现出规范性问题频发的现象。
2.1.1理化和微生物指标与其质量控制设置
不合理
一是未根据产品配方情况设置质控指标进行描述,如配方中含有乙氧基结构原料但未设置二噁烷指标、使用了甲醛释放体类原料未设置游离甲醛指标等;二是采取检验质量管理控制措施的项目描述不规范,如未填写完整检验方法名称、未注明检验频次、使用的检验方法与《化妆品安全技术规范(2015年版)》[5](以下简称“《规范》”)不一致时未做相关合理说明等;三是采取非检验质量管理控制措施的项目描述不规范,如未明确具体的实施方案、未对合理性进行说明、指标内质量控制措施的简要说明未对向上游供方索要的原料质量规格证明如何符合《规范》指标的相关要求进行具体描述等;四是未对采取的质量管理控制措施的可操作性进行评估,如对微生物指标中致病菌和理化指标中的石棉、游离甲醛及二噁烷采取产品逐批检验的质控措施,但企业自身无对应项目的检验能力;五是未按《规范》要求对产品采取质量控制措施,如对配方中添加氢氧化钠或氢氧化钾等强碱但未根据原料在作为pH调节剂使用时《规范》中的“其他限值和要求”在质控指标或生产工艺中对产品pH值进行相应的控制;六是抱着“多做多错”和“严格按底线要求做”的心理,“严格”按法规要求设置了常规九项指标。未从保护消费者和对产品质量控制的实际出发,明确pH值等产品基础控制指标。
2.1.2感官指标填报不合理不规范
一是填报的指标内容与其他版块的内容前后不匹配,如感官指标的性状与备案申请表填报的剂型不一致、感官指标的颜色性状与检验报告出具的颜色性状描述不一致、感官指标的颜色与配方中着色剂使用情况无法匹配等;二是未按《管理规定》填报指标内容,如错误将产品性状透明状态归于颜色,使用贴、膜类载体材料的产品未描述贴、膜类材料的颜色、性状。
2.1.3产品生产工艺填报不规范
一是产品生产工艺未按《管理规定》填报温度和温度范围参数、投料和灌装等主要制作步骤;二是产品生产工艺表述无法反应所有原料投料情况或表述中的原料序号与填报的原料数量不匹配等。
2.2安评资料版块的问题
相较于新《条例》出台前化妆品安全评估主要参考2015年颁布的《化妆品安全风险评估指南》(征求意见稿)及2010年颁布的《化妆品中可能存在安全性风险物质风险评估指南》而言[6],安评资料是一个全新内容。又因为备案人对原料各方面知识的匮乏,安评资料的问题呈现显著的“牵一发(原料)而动全身”的态势,其中原料安全评估问题存在着“巧妇难为无米之炊”的状况。
2.2.1类别原料识别不准确
一是《表1产品配方表》未将pH调节剂以及《规范》的类别物料等在《规范》中的情况在备注栏中进行描述,如氢氧化钠、聚季铵盐-7、十二烷基苯磺酸TEA盐等;二是《表2各成分的安全评估》属于《规范》中限用组分、防腐剂、着色剂等原料未在《規范》要求栏中准确地对原料使用情况进行阐述,如既是限用物质也是防腐剂的月桂基三甲基氯化铵(C12)、水杨酸、吡硫鎓锌等,新批准的防腐剂月桂酰精氨酸乙酯盐酸盐,根据原料中文名称填报形式可以是着色剂又可以是防晒剂的CI77891(二氧化钛)和CI77947(氧化锌);三是《表3化妆品中安全性风险物质危害识别表》未对《规范》中有质量规格要求的类别原料进行识别,如椰油酰胺DEA、三乙醇胺、氨丁三醇等;四是误将原料识别成《规范》中的类别原料,如将椰油酰胺MEA识别成《化妆品限用组分》(表3)中的第44号原料。
2.2.2原料安评无相关毒理学数据或者获取难度大
一是未将产品的使用人群、使用部位、使用方法以及所用原料生产工艺、使用浓度等与所引用的证据类型进行比对的情况下,即下原料使用安全的结论,如使用《中华本草》(1999年版)、《中国药典》等作为证据类型时;二是原料使用浓度远高于采用的证据类型(《已使用化妆品原料目录(2021年版)》中的最高历史使用量(%))且未作合理说明,如玫瑰花水、棕榈酸乙基己酯、薰衣草(LAVANDULA ANGUSTIFOLIA)油等;三是未提供符合《技术导则》的任意一种证据类型,且未提供毒理学相关评估资料充分证明产品安全性等,如桃树脂提取物、鲟鱼子酱提取物、3-邻-乙基抗坏血酸等;四是“严格”按《技术导则》证据类型权重要求,对除了《规范》有要求原料外的所有原料安评均引用《已使用化妆品原料目录(2021年版)》的最高历史使用量(%)作为评估证据,而不在《表2各成分的安全评估》中填报国内外权威机构已有的评论结论。
2.2.3未对原料生产工艺或原料物理性状特征进行识别
一是对植物提取物识别及解释不到位,如未对植物类原料的生产工艺进行识别即判定该原料未含任何风险物质;二是在确认使用的植物类原料为经机械加工后直接使用但未提供农残相关证明文件;三是对其他特殊原料识别及解释不到位,如未对芦荟制品进行蒽醌的风险物质识别,未对α-熊果苷进行氢醌的风险物质识别(在强酸性以及强碱性环境下,α-熊果苷溶液中有氢醌检出,α-熊果苷在碱性条件下的稳定性比在酸性条件下弱[7])。
2.2.4 提供错误、虚假材料或刻意未对引用的证据类型进行详细描述
一是引用《美国CIR化妆品原料安全使用指南》为证据类型,其评估结论描述在未体现含量情况即下结论认为原料使用是安全的,但经查询后发现所使用的原料在CIR内描述使用的安全限量远低于原料在产品中的添加量;二是对“二裂酵母发酵产物溶胞产物”采用淋洗类的最高历史使用量(%)作为证据类型对驻留类产品进行原料安评;采用《已使用化妆品原料目录(2021年版)》驻留类的最高历史使用量(%)为证据类型进行安评时,用“二裂酵母发酵产物滤液”替代“二裂酵母发酵产物溶胞产物”对原料进行安评,因前者的最高使用量(89.55%)远高于后者的最高使用量(0.74064%)。
2.3原因分析
通过对产品执行的标准和安评资料存在主要问题的分析,发现国产普通化妆品备案材料存在诸多问题的原因有以下三方面:
1)在化妆品产品的快销品属性以及电商行业推陈出新的商业模式影响下,化妆品从业者认为愈发严谨严格的产品备案要求是阻碍其捕捉商机的绊脚石甚至是拦路虎,产生抵触情绪的同时导致其对法律法规逐渐失去敬畏之心。并在备案过程抱着“严格按底线要求做”的心理,虽在备案审核过程中符合法规规范要求,但在实际运用中则可能会出现适用性的问题。
2)在化妆品产品配方中,除个别在产品中用量占比较大的原料(如溶剂、填充剂、表面活性剂等)外,其他功效成分添加量也不大,即便是规上企业也存在采购的原料在上游供方眼里属于边缘客户的现象,从而导致化妆品从业者對原料生产企业或者原料供应商缺乏核心影响力,在原料的索证索票以及原料相关安全资料的索取上长期处于弱势地位。
3)安评资料对原料毒理学有技术性需求,但我国现阶段无相关完整的原料毒理学数据库以及相关日均使用量和人体毒理学评价基础数据,以致于行业内在产品安评的开展过程中只能引用国外数据(CIR、PCPC等),进而对安评人员的外语能力、查询数据成本和能力以及数据辨识等能力提出了极高要求。同时备案人缺乏既懂技术又懂法规的复合型人才。近五年来,国内大学新增设化妆品相关专业19个,部分高校以化学相关专业细分研究方向的方法开展化妆品专业教学,但却没有开设化妆品与法律交叉培养方向的院校[8],也是在备案过程中合规性频发原因之一。
3对策建议
3.1明晰主体责任,正确认识化妆品产品备案作用
完成产品备案只是履行了必要的法定义务,不应成为企业炫耀的资本。按法律法规要求提交备案资料是产品安全可信的必要但非充分条件,企业需对此有清醒的认识,备案只是监管的一种手段,是事中事后监管的起始,是监管的重要抓手,质量可控以及产品合规并举才是监管的目的。备案审核只是把握了原则性的底线,并不是产品专业化与否的评价性审查。
但企业在进行产品备案前,可通过产品研发、原辅料和包材的安全性研究以及严格的质量控制,不断积累完善相关资料,为保障良好的产品质控、科学可信的产品安全及功效宣称打下坚实基础,并合理通过备案公示的规则[9],在备案查询平台将成分、质控项目指标以及功效宣称证明文件等信息呈现给消费者,展现自身能力水平。在产品完成备案后,凭借着备案过程的细致严谨,如实上传备案所需资料,可通过备案系统留痕的特性,在遇到恶意投诉举报或假冒伪劣产品协查时,为自证清白提供有力保证。
3.2多管齐下,助力原料规范化管理原料质量是化妆品质量的源头[10]。原料规范化管理势在必行,建议从以下三个方面着手:
一是稳步推进原料报送工作的开展。对申报的原料相关数据进行汇总解析,明晰原料的生产工艺及其在生产过程中可能出现的风险物质,借力科研院校验证结果,逐步将笼罩在原料的迷雾吹散;二是借助技术赋能,持续优化备案平台的功能,降低原料申报审评的难度。增强产品配方版块的功能,将申报的原料名称、含量和使用目的等与产品执行的标准、产品标签、检验报告以及安评资料各版块进行有效串联,同时辅以《已使用化妆品原料目录》和《化妆品安全技术规范》等数据库并联比对,辅助企业规范备案申报并提升审评效能;三是探索性建立我国原料毒理数据库。借助科研院校、行业协会以及企业专家智慧,梳理国际原料毒理数据,为我国原料毒理数据库的建立筑牢基础。
3.3持续培训,深化产品备案专业化队伍建设
监管部门要用好国产普通化妆品备案质量抽查的工作机制,加强全国各地审评员的沟通交流进而细化审评标准细则、统一备案要求和审评尺度,群策群力解决行业痛点难点问题,为行业高质量发展不断加强技术审评能力。同时应持续组织质量安全负责人以及备案相关专题培训,宣贯法律责任,明确备案要求,落实主体责任,由表及里、由浅入深、层层递进地推进企业备案队伍建设。行业协会要做好沟通桥梁作用,积极协助监管部门组织相关培训,并积极收集专业数据以及企业反馈问题,为监管部门阶段工作成效的确认以及下一步工作开展提供技术支持。企业要积极参加国家、省、市组织的相关专题培训,并在参加外部学习后及时组织企业内部交流培训,持续完善备案人员知识结构,同步理解监管要求统一认识,助力行业的高质量发展。
4结语
总结备案过程遇到的问题,分析并正视自身短板是目前备案人的当务之急。文中对厦门市国产普通化妆品备案技术审核近千条数据进行全面剖析,找出现阶段备案人在备案过程中遇到的痛点,为化妆品备案人规范备案行为,提升备案质量提供参考。企业应正确认识备案工作,认真学习新颁布的化妆品法律法规以及规范性文件内容及精神,更好更快地适应化妆品新时代备案要求,为消费者提供安全可靠的化妆品,为行业高质量发展添砖加瓦。
参考文献
[1]国务院.《化妆品监督管理条例》(中华人民共和国
国务院令第727号)[EB/OL]. [2020-06-16]. http://www.
gov.cn/gongbao/content/2020/content_5525087.htm.
[2]国家药品监督管理局. 国家药监局关于发布《化妆品
注册备案资料管理规定》的公告(2021年第32
号)[EB/OL].[2021-02-26]. http://www.nmpa.gov.
cn/zhuanti/hzhpxch2021/hzhp2021fgwj/
20210304140747119.html.
[3]国家药品监督管理局.国家药监局关于发布《化妆品
安全评估技术导则(2021年版)》的公告(2021年
第51号)[EB/OL].[2021-04-08].http://www.nmpa.
gov.cn/xxgk/ggtg/qtggtg/20210409160436155.html.
[4]国家药品监督管理局.化妆品监督管理常见问题解
答(五)[EB/OL].[2022-07-20].http://www.nmpa.
gov.cn/hzhp/hzhpzcjd/20220720164418149.html.
[5]国家药品监督管理局.国家食品药品监督管理总局
关于发布化妆品安全技术规范(2015年版)的
公告(2015年第268号)[EB/OL].[2015-12-23].
http://www.nmpa.gov.cn/hzhp/hzhpfgwj/hzhpgzwj/
20151223120001986.html.
[6]唐颖, 张兆伦, 曹力化,等.《化妆品监督管理条例》
背景下《化妆品安全评估技术导则》的解读刍议[J].
轻工学报,2021,36,05:84-91.
[7]刘纲勇,刘旭峰,石莹莹.化妆品原料[M].北京:
化学工业出版社,2017:256-257.
[8]邓勇,吴雨桐.化妆品行业合规发展,亟待推进人才
队伍建设[J].中国化妆品,2022,07:46-47.
[9]国家药品监督管理局.国家药监局关于发布《化妆品
功效宣称评价规范》的公告(2021年第50号)[EB/OL].
[2021-04-08].http://www.nmpa.gov.cn/xxgk/ggtg/
qtggtg/20210409160321110.html.
[10]韩娟,贾娜,石磊,等.2019 年化妆品原料专项检查
情况分析[J].中国食品药品监管,2020,06:90-94.

