莪术油葡萄糖注射液灭菌前后指纹图谱相关性研究Δ
方洪壮,李睿,孙长海,李利,张宇(.佳木斯大学化学与药学院,佳木斯市 54007;.黑龙江科伦制药有限公司,庆安市 5400)
莪术油葡萄糖注射液灭菌前后指纹图谱相关性研究Δ
方洪壮1*,李睿1,孙长海1,李利2,张宇1(1.佳木斯大学化学与药学院,佳木斯市 154007;2.黑龙江科伦制药有限公司,庆安市 152400)
目的:研究灭菌前后的莪术油葡萄糖注射液指纹图谱的相关性,为建立莪术油葡萄糖注射液指纹图谱的检测标准提供依据。方法:采用高效液相色谱法分离测定,色谱柱为Zorbax Eclipse XDB-C18(250 mm×4.6 mm ID,5 μm),流动相为乙腈-0.1%磷酸水溶液(梯度洗脱),流速为1 mL·min-1,柱温为30℃,检测波长为210 nm。通过共有模式方法比较指纹图谱的相关性;用成对比较t检验法比较单一色谱峰强度的变化。结果:莪术油葡萄糖注射液灭菌后较灭菌前多数色谱峰峰面积明显变小,并增加了一些小峰。结论:莪术油葡萄糖注射液灭菌前后的指纹图谱间均有较好的相关性。
莪术油葡萄糖注射液;指纹图谱;相关性;高效液相色谱法
Δ黑龙江省教育厅科学技术研究项目(11521277)
*教授。研究方向:药物分析。电话:0454-8611265。E-mail:fhz-chjms@163.com
莪术油为温莪术经水蒸气蒸馏提取的挥发油[1],含多种药理活性成分。莪术油葡萄糖注射液为莪术油加葡萄糖和适当助溶剂制成的含药输液剂,作为抗病毒药收载于2005年版《中国药典》(二部)[2]。中药注射剂指纹图谱的相关性是中药指纹图谱研究的重要内容[3,4],有多个品种注射剂、提取物、中间体和药材之间相关性的研究报道[5~9],但未见注射剂灭菌前后之间的指纹图谱相关性研究。相关性的比较方法,现为整体上的共有模式间相似度计算和直观分析及单一色谱峰的直观比较。本试验测定灭菌前后莪术油葡萄糖注射液的高效液相色谱(HPLC)指纹图谱并比较它们之间的相关性;在单一色谱峰强度变化的比较上,引入了统计学检验方法,可克服单一色谱峰直观比较的误判。试验结果可为控制莪术油葡萄糖注射液的质量和提升其质量标准提供数据。
1 仪器与材料
1.1 仪器
1100系列HPLC仪,包括G1379A脱气机、G1311A四元泵、G1313A自动进样仪、G1316A柱温箱、G1315B DAD检测器(美国Agilent公司);BP211D型电子分析天平(德国Sartorius公司)。
1.2 试药
10批温莪术药材由天瑞制药有限公司提供,经佳木斯大学化学与药学院宗希明高级实验师鉴定为姜科植物温郁金Curcuma wenyujinY.H.Chen et C.Ling的干燥根茎,莪术油分别由各批温莪术药材粗粉加8倍量水,按《中国药典》挥发油提取甲法提取5 h制得,注射液按相应制剂工艺要求制成,分作不经灭菌部分和灭菌部分;莪术二酮标准品(上海沪云医药开发有限公司,纯度:99.6%);莪术醇、吉马酮、β-榄香烯对照品(中国药品生物制品检定所,批号分别为0080-20050521、10753-200212、00268-200401);葡萄糖粉、依地酸二钠、吐温-80均为注射用,乙腈、甲醇为色谱纯,磷酸、无水硫酸钠为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 注射液供试液:分别取灭菌前后莪术油葡萄糖注射液直接作为注射液供试品溶液,分别记为供试液A和供试液B。
2.1.2 阴性溶液:取0.36 g吐温-80,再加入5 mg依地酸二钠,用5%葡萄糖溶液定容至100 mL容量瓶中,0.45 μm微孔滤膜滤过,取续滤液作为不含莪术油的阴性溶液。
2.1.3 对照品溶液:分别取莪术二酮、莪术醇、吉马酮及β-榄香烯对照品适量,用甲醇制成4种对照品的混合溶液。
2.2 色谱条件
色谱柱:Zorbax Eclipse XDB-C18(250 mm×4.6 mm ID,5 μm),Zorbax Eclipse XDB C18保护柱(12.5 mm×4.6 mm ID,5 μm);柱温:30℃;流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(A相:0~5 min,55%;5~30 min,75%;30~45 min,90%;45~55 min,90%,55 min后,100%);流速:1 mL·min-1;注射液与挥发油供试液的光谱-色谱图显示,210 nm波长处的信号强度、分离度、峰形与柱效均较为理想,60 min后无明显色谱峰,故检测波长确定为210 nm;色谱记录时间为60 min。
2.3 成分的归属
取供试液A、对照品溶液和阴性溶液各20µL,分别进样,色谱见图1。

图1 HPLC指纹图谱A.供试品;B.对照品;C.阴性溶液;S1.莪术二酮;S2.莪术醇;S3.吉马酮;S4.β-榄香烯Fig 1 HPLC fingerprintsA.test sample;B.reference substance;C.negative solution;S1.curdione;S2.curcumol;S3.germacrone;S4.β-elemene
由图1可知,色谱中保留时间为13.5、18.8、25.5及51.6 min处的S1、S2、S3及S4色谱峰分别归属于莪术二酮、莪术醇、吉马酮及β-榄香烯;注射液中的葡萄糖和其它辅料对莪术油葡萄糖注射液的色谱峰无干扰。
2.4 方法学考察
2.4.1 精密度:取同一供试液A,按上述色谱条件连续进样5次,所得到的指纹图谱与其中位值的相关系数分别为0.997 2、0.999 5、0.998 1、0.999 7和0.995 5,均>0.99;相对应的RSD=0.17%。各图谱能够很好地重合,表明仪器精密度较好。
2.4.2 稳定性:取同一供试液A,分别在0、4、8、12、18和24 h进样。不同时间点测得的图谱与其均值的相关系数分别为0.998 9、0.995 8、0.998 1、0.999 5、0.994 0 和 0.990 4,均>0.99;相对应的RSD=0.35%,表明样品在24 h内较稳定。
2.5 指纹图谱的建立
按“2.2”项下色谱条件测定10批灭菌前后的莪术油葡萄糖注射液,按全谱方式以中位数法分别建立共有模式(见图2)。灭菌前后的注射液指纹图谱均选取9个共有峰,分别占总峰面积的83.42%和66.64%,其中2、4、6、8号峰分别为莪术二酮、莪术醇、吉马酮及β-榄香烯的特征峰。灭菌后10批样品与其共有模式的相关系数分别为0.962 9、0.992 3、0.995 2、0.926 8、0.992 0、0.996 3、0.997 6、0.989 8、0.995 0和0.976 3,均>0.92;灭菌前10批样品与其共有模式的相关系数分别为0.960 2、0.987 5、0.996 4、0.890 7、0.989 6、0.994 3、0.996 2、0.989 0、0.998 5和0.984 6,均>0.89。
2.6 指纹图谱相关性分析
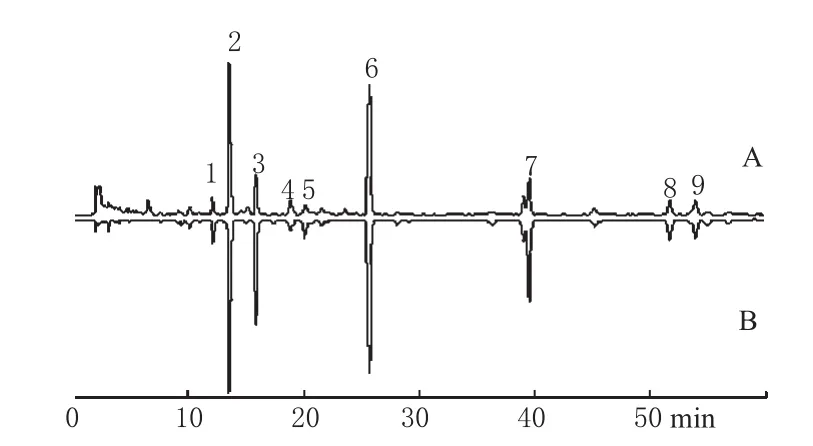
图2 灭菌后与灭菌前注射液指纹图谱的共有模式A.灭菌后;B.灭菌前Fig 2 Common fingerprints pattern of injection before and after sterilizationA.before sterilization;B.after sterilization
2.6.1 共有模式相关性:由图2的指纹图谱共有模式可见,注射液灭菌前后在HPLC指纹特征上相似。注射液灭菌后,色谱保留时间8 min前增加了一些小峰、出现了一些微量物质,部分特征峰的强度发生了一些变化。对灭菌前后的注射液指纹图谱的共有模式进行相似度计算得到,灭菌前后间的相关系数为0.936 0。
2.6.2 共有峰比较:图3为中位数共有模式下的共有峰面积柱型图,共有峰分别以1~9标记。由图3可见,莪术油注射液灭菌后的共有峰仅莪术醇(标记为4)峰面积变大,其余峰面积变小。共有峰面积统计学的成对比较t检验结果可知,各峰的检验计算值分别为7.99、27.0、11.1、12.0、9.19、18.9、8.88、8.76及15.2,均>检验的临界值3.25(P=0.01),表明灭菌前后共有峰面积间有高度显著差异。

图3 共有峰面积柱型图A.灭菌注射液;B.未灭菌注射液Fig 3 Columnar diagram of common peak areaA.sterilized injection;B.non-sterilized injection
3 讨论
3.1 共有峰的选择
莪术油葡萄糖注射液指纹图谱中,多数峰的强度较小,本试验选用峰面积最大的吉马酮为参照物,以超过其峰面积5%、保留时间和峰面积均比较稳定的色谱峰为共有峰。
3.2 相似性比较
中药的药材、提取物及制剂的色谱指纹图谱间单一共有峰相似性的比较,仅见直观比较,有时难以给出确切的判定。如灭菌前后的1号峰在直观上较接近,但统计学检验有显著差异,可见统计学方法可克服对峰强度变化的直观误判。
[1]国家药典委员会编.中华人民共和国药典(一部)[S].2005年版.北京:化学工业出版社,2005:279.
[2]国家药典委员会编.中华人民共和国药典(二部)[S].2005年版.北京:化学工业出版社,2005:592.
[3]王 旭,王国荣.中药注射剂指纹图谱研究的现状和分析[J].中国药品标准,2005,6(4):48.
[4]杨东风,梁宗锁.中药指纹图谱研究进展[J].中国药房,2008,19(6):467.
[5]饶春恺,罗顺德,雷嘉川,等.当归注射液指纹图谱初步研究[J].中成药,2003,26(10):775.
[6]游 松,王 亮,蒋雅红,等.银杏叶注射剂指纹图谱的研究[J].中草药,2002,33(3):216.
[7]兰燕宇,刘丽娜,王永林,等.注射用复方荭草(冻干粉针)指纹图谱研究[J].中国中药杂志,2005,30(6):440.
[8]罗远秀,文东旭,蒋受军,等.岩黄注射液与药材及提取物间指纹图谱相关性研究[J].药物分析杂志,2007,27(7):1 014.
[9]唐旭利,刘 静,李国强,等.注射用丹红(粉针)-中间体-药材HPLC指纹图谱相关性研究[J].中国海洋大学学报,2009,39(1):61.
Study on Fingerprints Correlation of Zedoary Turmeric Oil and Glucose Injection before and after Sterilization
FANG Hong-zhuang,LI Rui,SUN Chang-hai,ZHANG Yu(College of Chemistry and Pharmacy,Jiamusi University,Jiamusi 154007,China)
LI Li(Heilongjiang Kelun Pharmaceutical Co.,Ltd.,Qing’an 152400,China)
OBJECTIVE:To study fingerprints correlation of Zedoary turmeric oil and glucose injection before and after sterilization,and to provide reference for the establishment of detecting standard of fingerprints of Zedoary turmeric oil and glucose injection.METHODS:HPLC method was used.The separation was performed on Zorbax Eclipse XDB-C18(250 mm×4.6 mm ID,5 μm)column with mobile phase consisted of acetonitrile-0.1%phosphoric acid water(gradient elution)at flow rate of 1 mL·min-1.The column temperature was set at 30℃and detection wavelength was 210 nm.The fingerprints correlation was compared by the method of common pattern.The change of the unity chromatographic peak was analyzed by pairedt-test.RESULTS:After sterilization,the chromatographic peak areas of the injection were obviously diminished and some tiny chromatographic peaks appeared.CONCLUSION:There is a good relationship between the fingerprints of Zedoary turmeric oil and glucose injection before and after sterilization.
Zedoary turmeric oil and glucose injection;Fingerprints;Correlation;HPLC
R283.61;R927.2
A
1001-0408(2010)39-3702-03
2009-11-01
2010-04-09)

