一锅法合成2-硫脲嘧啶*
钟光祥, 陈婷婷, 周程程
(浙江工业大学 药学院,浙江 杭州 310032)
2-硫脲嘧啶(1)具有抗菌[1,2]、抗病毒[3,4]、抗甲状腺活性[5],它能抑制甲状激素合成、用于治疗甲状腺功能减退[6]。近年来研究发现1及其衍生物可以影响神经功能,是一新型的神经元型一氧化氮合酶的抑制剂[7],而且它又是多种抗菌、抗病毒、抗癌药物的主要合成单体[8],因此对其进行合成工艺的优化研究,具有非常重要的意义。
文献[9,10]方法虽然反应条件温和,但原料复杂,成本较高;龚宓等[11]用简便方法合成了1。我们重复文献[11]方法时,发现得到的产物为6-甲基-2-硫脲嘧啶(2),而不是所期待的1。因此,本文对1的合成过程(Scheme 1)进行了详细的研究,优化了反应条件,提高了收率,使其更适合于工业生产。
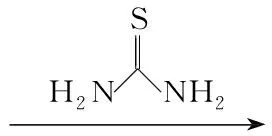
Scheme1
1 实验部分
1.1 仪器与试剂
X-4型数字显示显微熔点仪(温度计未经校正);Bruker AC-80 500 MHz型核磁共振仪(DMSO-d6为溶剂,TMS为内标)。
甲醇钠(Na 1.5 g, 甲醇30 mL)自制;其余所用试剂均为化学纯。
1.2 合成
硫脲2.5 g(33 mmol), 反应物摩尔比r=n(乙酸乙酯) ∶n(甲酸乙酯) ∶n(甲醇钠) ∶n(硫脲)=2.5 ∶1.5 ∶2.0 ∶1.0。
将乙酸乙酯缓慢滴加到甲醇钠(3.5 g)的甲苯(35 mL)溶液中,于80 ℃反应3 h;冷却后滴加甲酸乙酯,于25 ℃充分搅拌8 h;加入硫脲的乙醇(10 mL)溶液,回流(90 ℃)反应3 h。减压浓缩至干,残留物用热水溶解、醋酸酸化至pH 4,冷却后析出固体,过滤,滤饼用水洗涤,用水重结晶得米黄色针状晶体1,收率54.7%(以硫脲计算),纯度≥98%, m.p.>300 ℃ ;1H NMRδ: 5.81(d,J=7.5 Hz, 1H, 5′-H), 7.41(q,J=5.5 Hz, 7.5 Hz, 1H, 6′-H), 12.27(s, 1H, NH ), 12.44(s, 1H, NH)。
2 结果与讨论
重复文献[11]方法:硫脲3.8 g(50 mmol),r=3.8 ∶1.4 ∶2.4 ∶1.0。
在反应瓶中加入甲醇钠(6.5 g),搅拌下低于20 ℃滴加乙酸乙酯,滴毕,回流1.5 h;慢慢滴加甲酸乙酯,滴毕,于25 ℃反应1.5 h;加入研磨过的硫脲,于60 ℃反应2.5 h。减压浓缩至干,残留物用热水溶解、稀盐酸酸化,冷却后析出白色固体,过滤,滤饼干燥得2,收率70.1%, m.p.300 ℃(不熔) ;1H NMRδ: 2.06(s, 3H, CH3), 5.69(s, 1H, 5′-H), 12.26(s, 1H, NH), 12.32(s, 1H, NH)(确定2为6-甲基-2-硫脲嘧啶)。
为了合成1,本文对文献[11]方法作了改进。
2.1 第一步反应的改进
(1) 第一步反应的溶剂及其用量
为了合成1,我们对缩合反应的溶剂进行了研究,反应条件同1.2,实验结果见1。从表1可以看出,如果不加溶剂、或以DMF为溶剂,则产物为2;如果以甲苯作溶剂,则有1生成,且随着甲苯用量的增加,1的比例逐渐增加。其原因是当乙酸乙酯浓度过高、或在极性的介质中进行反应时,乙酸乙酯发生自身缩合反应生成乙酰乙酸乙酯,然后与硫脲环合生成2。因此,合成1需要加入一定量的非极性溶剂,使乙酸乙酯在反应体系中的浓度低于5%,这样才能避免自身缩合。因此,第一步反应宜选用甲苯(1 L·硫脲mol-1)为溶剂。

表 1 溶剂对缩合反应的影响*Table 1 Effect of solvent on condensation reaction
*硫脲2.5 g(33 mmol),r=n(乙酸乙酯) ∶n(甲酸乙酯) ∶n(甲醇钠) ∶n(硫脲)=3.8 ∶1.4 ∶2.4 ∶1.0;其余反应条件同1.2

表 2 r对1收率的影响*Table 2 Effect of r on the yield of 1
*第一步反应以甲苯为溶剂,其余同表1
(2)r
以甲苯为第一步反应的溶剂,其余反应条件同1.2,考察了r对1收率的影响,实验结果见表2。由表2可见,Entry 1收率低,这是因为反应温度为80 ℃,乙酸乙酯(b.p.77 ℃)会有损失,乙酸乙酯应过量。比较Entry 2和Entry 3的结果发现,甲醇钠用量也应当较理论值高,它在反应中即是缩合剂又是环合剂,并且甲酸乙酯会消耗部分的甲醇钠。如果乙酸乙酯用量过多(Entry 5),乙酸乙酯会发生自缩合,生成乙酰乙酸乙酯,为了防止副反应发生,乙酸乙酯要慢慢滴加,使其在反应体系中的浓度不高于5%。因此,Entry 4的收率最高,即宜选择r=2.5 ∶1.5 ∶2.0 ∶1.0。
2.2 第二步反应条件的改进
在改进第一步反应条件的基础上,考察了第二步反应的温度和溶剂对1收率的影响,结果见表3。由表3可见,加入对硫脲溶解性较好的甲醇或乙醇,对反应较为有利。以甲苯-乙醇为溶剂,于90 ℃反应3 h,收率可达54.7%。

表 3 第二步反应条件对1收率的影响*Table 3 Effect of 2nd-step reaction conditions on the yield of 1
*第一步反应以甲苯为溶剂,其余同表1
综上所述,采用一锅法合成了2-硫脲嘧啶,改进后的反应条件为: 硫脲33 mmol,n(乙酸乙酯) ∶n(甲酸乙酯) ∶n(甲醇钠) ∶n(硫脲)=2.5 ∶1.5 ∶2.0 ∶1.0;将乙酸乙酯缓慢滴加到甲醇钠的甲苯(35 mL)溶液中,于80 ℃反应3 h;冷却后滴加甲酸乙酯,于25 ℃充分搅拌8 h;加入硫脲和乙醇(10 mL),回流反应3 h,收率54.7%,纯度≥98%。
[1] Wyrzykiewicz E, Bartkowiak G, Kedzia B,etal. Synthesis ofanti-microbial properties ofS-substituted derivatives of 2-thiouracil[J].Farmaco,Poland,1993,48:979-988,CAN120:49663.
[2] Mohamed N R, Mohamed H E, Ali Y M,etal. Utility of 6-amino-2-thiouracil as a precursor for the synthesis of bioactive pyrimidine derivatives[J].Bioorganic & Medicinal Chemistry,2007,15:6227-6235.
[3] Nakamura M, Jonsson S. The effect of antimetabolites on the growth of Entamoebahistolyica[J].Archives of Biochemistry and Biophysics,1957,66:183-189.
[4] Fathalla O A, Awad S M, Mohamed M S. Synthesis of new 2-thiouracil-5-sulphonamide derivatives with antibacterial and antifungal activity[J].Archives of Pharmacal Research,2005,28(11):1205-1212.
[5] Okabe O, Fujiwara T, Yamagata Y, et al. Structure of a potent antithyroid drug,6-prooyl-2-thiouracil[J].Bulletin of the Chemical Society of Japan,1983,56:1543-1544.
[6] Andreson G W, Halverstadt I F, Miller W H,etal. Studies in chemotherapy.Ⅹ.Antithyroid compounds.Synthesis of 5- and 6-substituted 2-thiouracils fromβ-oxoesters and thiourea[J].Journal of the American Chemical Society,1945,67:2197-2200.
[7] Palumbo A, D’Ischia M. Thiouracil antithyroid crugs as a new class of beuronal bitric oxide synthase inhibitors[J].Biochemical and Biophysical Research Communications,2001,282:793-797.
[8] Fathalla O A, Zaghary W A, Radwan H H,etal. Synthesis of new 2-thiouracil-5-sulfonamide derivatives with biological ativity[J].Archives of Pharmacal Research,2002,25(3):258-269.
[9] Winckelmann I, Larsen E H. Improved one-step procedure for the preparation of 1-substituted and 1,3-cisubstituted uracils and 2-thiouracils[J].Synthesis,1986,12:1041-1044.
[10] Cassis R, Tapia R, Walderrama J A. New synthesis of uracil and 2- thiouacil[J].Synthetic Communications,1984,14(10):961-965.
[11] 龚宓,张善言. 简法合成2-硫脲嘧啶[J].化学研究与应用, 1999,11(4):442-443.

