Nb2O5/γ-Al2O3表面铌氧物种的分散状态与酸性特征
何 杰 范以宁
(1安徽理工大学化学工程学院,安徽淮南 232001;2南京大学化学化工学院,介观化学教育部重点实验室,南京 210093)
Nb2O5/γ-Al2O3表面铌氧物种的分散状态与酸性特征
何 杰1,2,*范以宁2
(1安徽理工大学化学工程学院,安徽淮南 232001;2南京大学化学化工学院,介观化学教育部重点实验室,南京 210093)
负载型Nb2O5是多种催化反应的有效催化剂.以草酸铌为前驱物,γ-Al2O3为载体,通过浸渍法制备不同负载量的Nb2O5/γ-Al2O3催化剂.采用粉末X射线衍射(XRD)、激光拉曼光谱(LRS)和吡啶吸附傅立叶变换红外(Py-IR)光谱方法对催化剂表面铌氧(NbOx)物种的分散特征、酸性特征进行表征,通过异丁烯(IB)与异丁醛(IBA)缩合生成2,5-二甲基-2,4-己二烯(DMHD)反应评价催化剂表面酸催化活性.结果表明,Nb在γ-Al2O3表面的单层分散容量(ΓNb)为7.6 μmol·m-2,与“嵌入模型”理论分析Nb5+分散在γ-Al2O3优先暴露晶面(110)上八面体空位中的单层分散容量值7.5 μmol·m-2接近,即分散的Nb5+离子键合在γ-Al2O3表面八面体空位中.在低负载量下,分散在γ-Al2O3表面的Nb2O5主要以孤立的NbOx物种形式通过Nb—O—Al键与载体表面键合,与LRS结果一致.处于孤立状态下的NbOx物种使表面Lewis酸位量下降.随负载量的增加,孤立的NbOx物种通过Nb—O—Nb键连接而聚集,并形成表面Brönsted酸位,随着NbOx聚集度增加,表面Brönsted酸密度增加,酸性增强,对IBA与IB缩合反应催化活性增加.当负载量超过单层分散容量时,NbOx物种呈现三维聚集状态,DMHD的转化频率(TOF)降低,同时表面Brönsted酸性增强,导致目标产物DMHD的选择性降低.Nb2O5/γ-Al2O3催化剂表面Brönsted酸特征与NbOx物种聚集状态密切相关.
表面酸性;Nb2O5/γ-Al2O3;表面NbOx物种;烯醛缩合反应
铌氧化物及其材料在许多催化应用领域均是有效的催化剂[1-5],如酸催化、选择性氧化、光催化等.除了直接用作催化剂外,铌氧化物还用于二维氧化铌覆盖层[6-11]、氧化物载体[12]或混合氧化物[13-14]以及催化剂的促进剂[15]等.在铌氧化物众多的催化反应中,酸催化是其重要应用之一.作为一种酸性氧化物,Nb2O5的酸性与大多数氧化物不同,晶相Nb2O5几乎不呈现酸性,以无定型态存在的铌酸(Nb2O5· nH2O)具有较强的酸性且对一些反应具有较高的酸催化活性,同时它具有很好的耐水性[16-17],如作为烯烃水合、醇脱水、脂肪酸与醇酯化以及烯醛缩合等反应的催化剂,因此,在有机合成及石油化工等领域铌酸作为酸催化剂有非常良好的应用前景.将Nb2O5负载于金属氧化物载体上,因表面NbOx物种与载体之间的相互作用使得表面铌氧化物的物理化学性质与本体相明显不同,并随着载体性质、负载量以及制备条件不同,表面铌氧化物的结构状态以及催化性质发生变化[7,9-10,18-19].负载型Nb2O5主要起酸催化剂的作用,表面NbOx物种的状态与酸特征之间存在着密切的关系[6,9-11],而酸性特征与催化性能密切联系.本研究在运用X射线衍射(XRD)相定量分析等方法讨论NbOx物种在TiO2表面分散状态的基础上[9],进一步采用该方法并结合激光拉曼光谱(LRS)技术以及“嵌入模型”研究Nb2O5/γ-Al2O3催化剂表面NbOx物种的分散状态及其与载体/γ-Al2O3之间的相互作用;通过异丁烯(IB)与异丁醛(IBA)缩合生成2,5-二甲基-2,4-己二烯(DMHD)反应的酸催化性能以及吡啶吸附红外光谱表征催化剂表面酸性特征,探讨γ-Al2O3表面NbOx物种的分散状态、表面酸性特征以及酸催化活性之间的关系.
1 实验部分
1.1 负载型Nb2O5/γ-Al2O3催化剂制备
将一定量铌酸(AR)溶于0.5 mol·L-1H2C2O4(AR)溶液制成草酸铌溶液,将直径约为2 mm的γ-Al2O3小球(天津化工研究院,SBET=232 m2·g-1)浸入计量的上述溶液中,于333-343 K旋转蒸发除去水分,再经393 K干燥12 h,在设定温度空气气氛中焙烧一定时间,得到负载型铌氧化物催化剂.高负载量的催化剂由多次浸渍焙烧方法制备.
1.2 催化剂表征
X射线粉末衍射(XRD)测定在Shimadzu XD-3A型X射线衍射仪上进行,Cu Kα,λ=0.15418 nm,Ni滤波,管电压35 kV,管电流15 mA.以晶相V2O5为内标求得不同负载量样品中Nb2O5(202)面与V2O5(001)面衍射峰的相对强度INb2O5(202)/IV2O5(001),用外推法求得Nb2O5在γ-Al2O3载体表面的单层分散容量.红外光谱测试在德国Bruker公司Vector 22型红外光谱仪上进行.催化剂样品经研磨后压成自支撑片(约6 mg)于573 K、10-3Pa下抽空处理2 h,降至室温后摄取本底红外光谱.处理后的样品室温下吸附吡啶饱和蒸汽(蒸汽压为612 Pa)30 min,然后分别于298、423和573 K下抽空1 h,冷却至室温摄谱.减去样品的本底谱即得样品吸附吡啶的红外光谱(Py-IR).分辨率4.0 cm-1,扫描次数:120.激光拉曼光谱(LRS)测试在法国JY公司JY HR800型激光Raman光谱仪上进行,激发光源波长546 nm.
1.3 催化性能评价
IB/IBA缩合生成DMHD反应在一台直型不锈钢反应装置上进行,反应条件见文献[20].
2 结果与讨论
实验考察Nb2O5在γ-Al2O3载体表面的分散状态以及晶相形成条件,将Nb负载量ΓNb为19.5 μmol·m-2的样品于不同温度焙烧24 h后,用XRD方法检测表面Nb2O5晶相形成温度.结果表明,在 873 K及以下温度未观察到明显的晶态Nb2O5形成,当焙烧温度达973 K时,Nb2O5在载体γ-Al2O3表面形成γ-Nb2O5晶相.
不同负载量的Nb2O5/γ-Al2O3样品经973 K焙烧24 h后的XRD测定结果示于图1.由图1可见,当Nb负载量在6.5 μmol·m-2以下时,未见晶相Nb2O5衍射峰,当Nb负载量达9.7 μmol·m-2时, XRD谱中出现了Nb2O5衍射峰,且其强度随着Nb2O5负载量增加而明显增强.以晶相V2O5为内标物测定Nb2O5/γ-Al2O3中Nb2O5(202)与V2O5(001)面衍射峰相对强度(INb2O5(202)/IV2O5(001))与Nb2O5负载量的关系,结果示于图2.用外推求得Nb在γ-Al2O3表面的单层分散容量为7.6 μmol·m-2.
Nb2O5/γ-Al2O3催化剂LRS谱示于图3.Nb负载量在分散容量7.6 μmol·m-2以下时,Nb2O5/γ-Al2O3催化剂仅在906 cm-1处出现一拉曼峰,该峰归属于载体γ-Al2O3表面八面体NbO6物种[21].随负载量增加,906 cm-1拉曼峰位置峰强度增加,这是由于载体表面NbO6物种浓度增加.当负载量超过单层分散容量时,Nb2O5/γ-Al2O3催化剂在600-700 cm-1范围出现一个宽的拉曼峰(图3d),该峰与无定形铌酸和晶相Nb2O5中聚集的NbOx物种Nb—O—Nb拉曼位移相近,表明超出分散容量的这部分铌氧物种以三维聚集体或晶相形式存在,结果与XRD结果一致.
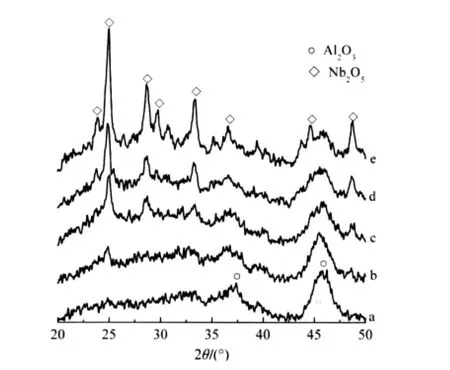
图1 不同负载量的Nb2O5/γ-Al2O3样品XRD图Fig.1 XRD patterns of Nb2O5/γ-Al2O3catalysts with different Nb2O5loadingΓNb/(μmol·m-2):(a)6.5,(b)9.7,(c)13.0,(d)16.2,(e)19.5
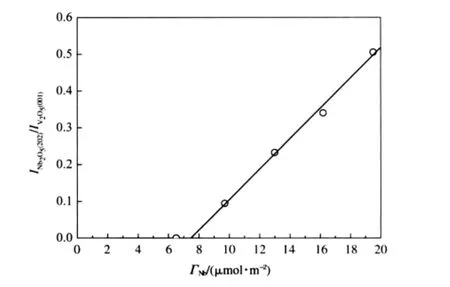
图2 Nb2O5/γ-Al2O3催化剂XRD定量分析结果Fig.2 XRD quantitative phase analysis result for Nb2O5/γ-Al2O3catalysts
研究氧化物与载体之间的相互作用,载体表面结构是一个不可或缺的重要因素,嵌入模型[22]从载体的优先暴露晶面讨论氧化物在载体上的分散.该模型认为,负载型离子化合物在载体表面上分散过程是其阳离子进入载体表面空位,相伴的阴离子定位其上以保持电中性.据此,离子型化合物在氧化物载体表面的分散容量与载体表面空位密切相关.
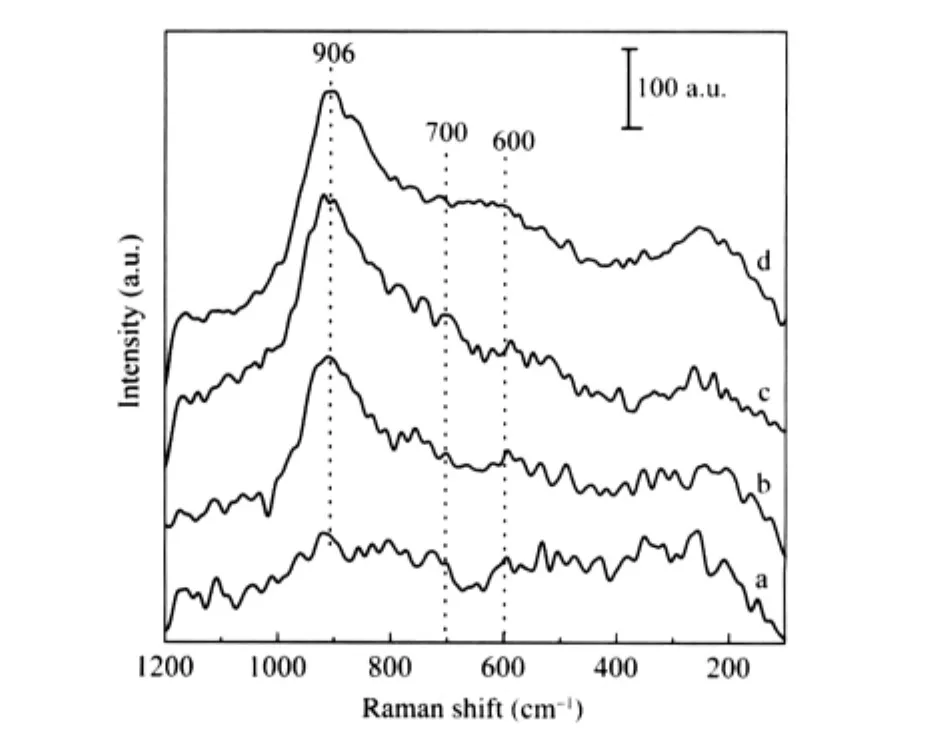
图3 Nb2O5/γ-Al2O3催化剂的LRS谱Fig.3 LRS of Nb2O5/γ-Al2O3samples with different Nb2O5loadingΓNb/(μmol·m-2):(a)1.7,(b)3.6,(c)5.7,(d)8.1
γ-Al2O3具有缺陷尖晶石结构[23],属立方晶系.在每一个单胞中含有32个O原子和64/3个Al原子,其中Al原子占据着四面体和八面体位置. Jimenez-Conzalez等[24]的研究表明,γ-Al2O3表面主要(约90%)呈(110)面取向.该面有两层结构:C层和D层,其离子排列方式示于图4.Schuit等[25]认为C层和D层所占比例相等.C层单位网格中有2个八面体(Oct.)空位和6个四面体(Tet.)空位,而D层单位网格中有2个八面体空位和8个四面体空位.按Al3+半径0.055 nm和O2-半径0.14 nm[26]可计算出γ-Al2O3的C层和D层结构中空位密度分别为31.2和 34.2 μmol·m-2.其中,八面体空位密度均为7.5 μmol·m-2.由于该载体表面存在四面体与八面体两种空位,半径大小不同的阳离子分散组分的嵌入存在着择位问题.已经发现,分散的金属阳离子优先占据γ-Al2O3表面的四面体空位还是八面体空位与被分散的金属氧化物的性质和负载量以及样品的焙烧温度有关[27].图3结果表明,NbOx氧物种在γ-Al2O3表面呈六配位的八面体结构,可以认为Nb5+进入八面体空位而形成具有八面体结构的NbOx物种.根据“嵌入模型”,在γ-Al2O3的C层与D层每嵌入1个Nb5+离子,将有2.5个O2-离子以保持电中性,当所有可用的八面体空位都被Nb5+离子占据后,覆盖O2-离子形成密置单层,如图4所示.据此可以估算出Nb在γ-Al2O3表面的分散容量为7.5 μmol·m-2,与实测值甚为一致.
为探讨Nb2O5/γ-Al2O3催化剂NbOx物种所处状态与催化性能的关系,以 IB与IBA缩合生成DMHD反应为探针,研究不同负载量的Nb2O5/γ-Al2O3催化剂对IB与IBA缩合反应催化性能.由于晶相Nb2O5表面几乎不具有酸性,在制备Nb2O5/γ-Al2O3系列催化剂,将焙烧温度控制在773 K,焙烧时间控制在6 h,以保证负载量超过单层分散容量时的Nb2O5在γ-Al2O3载体表面处于无定型状态.
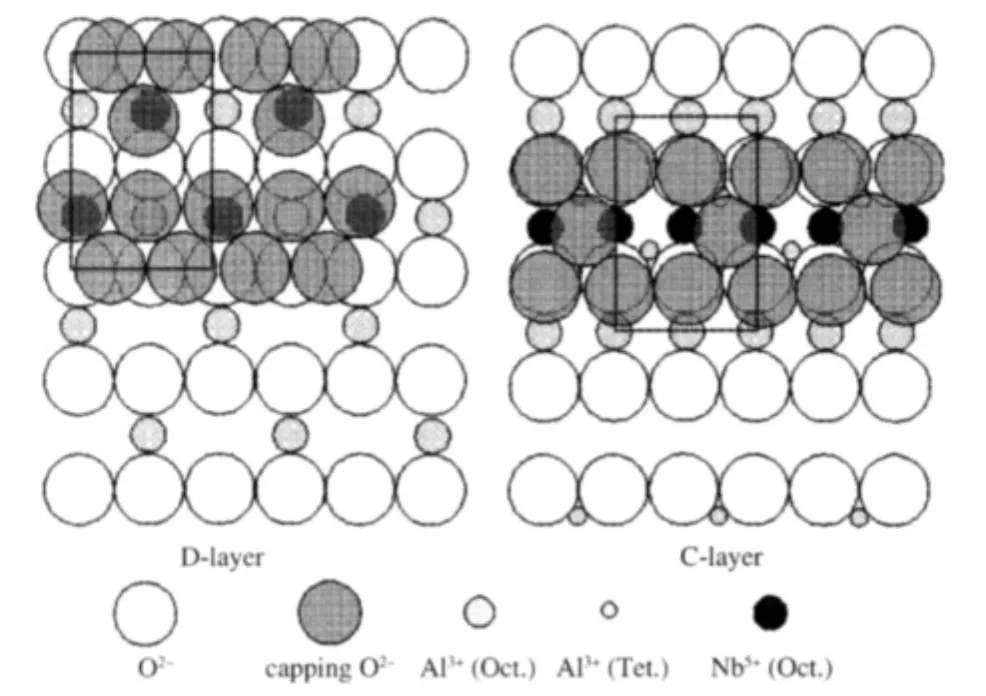
图4 Nb2O5在γ-Al2O3的(110)面上分散的示意图Fig.4 Schematic structure of the dispersed Nb2O5on γ-Al2O3(110)
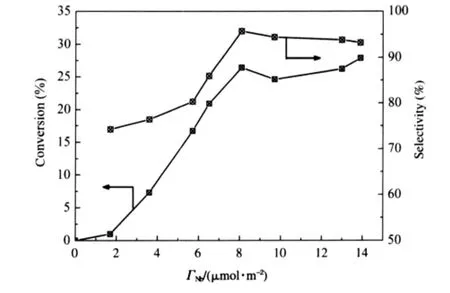
图5 Nb2O5/γ-Al2O3催化剂的IB与IBA缩合生成DMHD的催化性能Fig.5 Catalytic acitivity of Nb2O5/γ-Al2O3catalysts for condensation reaction of IB and IBA to DMHD
载体γ-Al2O3对IB与IBA缩合反应几乎不具有催化活性,而晶相Nb2O5虽有一定催化活性但反应物IBA的转化率(10.0%)和产物DMHD的选择性(51.4%)均明显偏低,而在无定型形态的铌酸上,IBA的转化率和产物DMHD的选择性分别为66.2%和86.8%,均比晶相Nb2O5的高得多.负载型Nb2O5/γ-Al2O3催化剂对IB与IBA缩合反应的催化活性和产物DMHD的选择性与Nb2O5负载量密切相关,结果示于图5.以催化剂单位时间每个Nb5+离子的DMHD产物收率估算催化活性(转化频率TOF),结果示于图6.随负载量的增加,TOF呈线性上升,当负载量超过单层分散容量时TOF值下降,这是催化剂表面NbOx物种利用率降低的结果.图中还显示,随样品中Nb的负载量不同,这种变化表现为两条斜率不同的直线线形变化,两线相交于7.5 μmol· m-2附近,与XRD测定和按嵌入模型所预测的Nb2O5在γ-Al2O3上的分散容量相近.
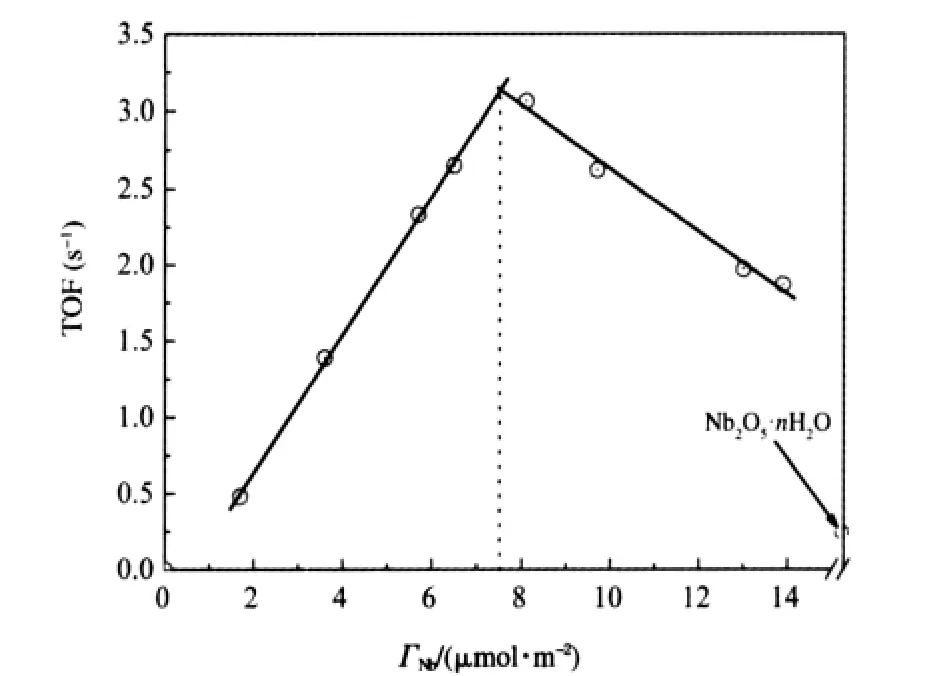
图6 Nb2O5/γ-Al2O3催化剂上IB与IBA缩合成DMHD的TOF随Nb2O5负载量的变化Fig.6 Turnover frequency(TOF)of DMHD from IB and IBA condensation on Nb2O5/γ-Al2O3catalysts with Nb2O5loading
IB与IBA缩合形成DMHD反应是一典型的酸催化反应[9,20,28].为考查负载量不同的Nb2O5/γ-Al2O3催化剂中表面NbOx物种酸催化性能的差异,测定了一系列催化剂样品吸附吡啶后的红外光谱(Py-IR),分别以1440-1460和1535-1550 cm-1特征吸收峰面积与样品表面积之比表示L酸位和B酸位相对酸量,并以不同温度下的酸量变化反映酸强度变化[20,28],结果示于图7.从图7可见,载体γ-Al2O3表面未观察到B酸位,但具有最大的L酸位量.将Nb2O5分散到γ-Al2O3表面后,导致Nb2O5/γ-Al2O3样品表面可检测到的L酸位量下降,这可能是Nb5+填充到γ-Al2O3表面八面体空位的结果.在单层分散之前,样品表面L酸位量随着Nb2O5负载量的增加先下降而后增加.在单层分散后,样品的表面酸特征由NbOx物种控制.Nb2O5负载到γ-Al2O3表面后在改变催化剂表面L酸位量的同时,在较高的负载量下形成了B酸位.Nb负载量为1.7 μmol·m-2的样品未检测到PyH+振动吸收峰,可以认为其表面B酸位量低于检测范围,负载量为3.6 μmol·m-2的样品表面B酸位量很小,而负载量为5.7 μmol·m-2的样品表面B酸位量明显增加,此后,增加Nb2O5的负载量,表面B酸位量进一步增加.
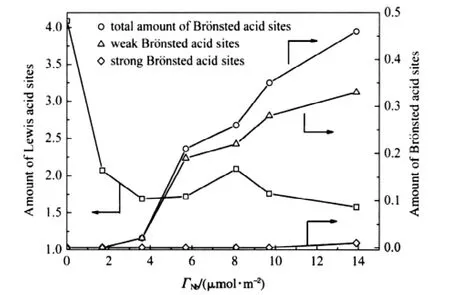
图7 Nb2O5/γ-Al2O3催化剂表面酸特征与负载量的关系Fig.7 Acidity feature of the Nb2O5/γ-Al2O3catalyst with Nb2O5loading
从图7还可见,Nb负载量为3.6 μmol·m-2的样品表面只有强度较弱的B酸位.随着负载量的增加,在B酸位浓度增加的同时强度增加,Nb负载量为13.9 μmol·m-2的样品上出现了类似于铌酸表面较强的B酸位.因此,Nb2O5/γ-Al2O3催化剂表面的B酸位量与Nb2O5在γ-Al2O3表面的分散状态密切相关.
负载型氧化物催化剂表面的B酸位来自于其表面的可质子化羟基.Kataoka等[29]认为,表面羟基是否具有B酸酸性可通过其键强度大小来判断,只有键强度在0.1-0.4 v.u.(valence unit)之间的羟基才有可能产生B酸性,键强度越接近于0.1 v.u.,B酸酸性越强.在负载型Nb2O5/γ-Al2O3催化剂表面存在着Al—OH、Nb—OH端羟基和Al—OH—Al、Nb—OH—Al、Nb—OH—Nb桥羟基[18,30-31].按Kataoka等方法计算,端羟基Al—OH和Nb—OH的键强度分别为1.50和1.17 v.u.,表明这些端羟基不具有B酸酸性.桥羟基Al—OH—Al、Nb—OH—Al和Nb—OH—Nb的键强度分别为1.0、0.67和0.33 v.u.,只有Nb—OH—Nb桥羟基的键强度在0.1-0.4 v.u.范围,即在这些桥羟基中,只有Nb—OH—Nb桥羟基呈现明显的B酸酸性,而Nb—OH—Al桥羟基几乎不呈现B酸性,理论预测与实验结果一致.这一结果表明,在Nb2O5/γ-Al2O3催化剂表面,B酸位由Nb—OH—Nb桥羟基产生.在低负载量下,Nb2O5在γ-Al2O3表面以孤立的NbOx物种形式存在,与表面形成Nb—O—Al键,因而没有可观测到的B酸位.随着Nb2O5负载量增加,相邻的Nb—O—Al键间形成Nb—O—Nb键,从而在催化剂表面形成了B酸位.结果表明,当负载量增加到一定值时,载体γ-Al2O3表面孤立的NbOx物种结合形成了聚集态NbOx的物种,即形成Nb—O—Nb键,这一值即为表面B酸位形成的阈值,超过这一阈值表面出现了可观测量的B酸位,并且B酸位量随Nb2O5负载量的增加,表面NbOx物种聚集程度增加,B酸量增加,同时B酸位强度增强.在单层分散容量以上,NbOx物种聚集体向三维方向增长,形成了多层Nb—O—Nb键结构,结果每一个Nb原子周围的Nb原子数增加,有利于B酸位的形成,表面B酸位增加,强度增强,并出现了较强的B酸位,具有无定型体相结构的铌酸(Nb2O5·nH2O)具有最大的表面B酸位量和最强的B酸强度.
IB与IBA缩合生成DMHD的反应是B酸催化反应[20,28],催化剂表面B酸位量与催化活性呈现良好的相关性,通过比较图5与图7结果可以看出这一相关性,即在Nb2O5/γ-Al2O3催化剂上,随着Nb2O5负载量的增加,表面Nb—O—Nb物种增加,表面B酸位量增加,导致IB与IBA反应生成DMHD的TOF值增加.在单层分散容量以上,由于表面形成了较强的B酸位,使DMHD的选择性降低.我们认为,在IB与IBA缩合生成DMHD的反应中,聚集状态NbOx物种形成的Nb—OH—Nb桥羟基比孤立的NbOx物种形成的Nb—OH—Al桥羟基具有更高的催化活性.
3 结 论
(1)由XRD定量分析方法测得Nb在γ-Al2O3表面的单层分散容量为7.6 μmol·m-2,与“嵌入模型”按Nb5+离子进入γ-Al2O3优先暴露面(110)面C层和D层的八面体空位估算值7.5 μmol·m-2一致.
(2)当Nb2O5的负载量远低于其分散容量时,高度分散于γ-Al2O3表面八面体空位的NbOx物种主要通过Nb—O—Al键与γ-Al2O3表面连接,随着负载量的增加,孤立的NbOx物种倾向于与近邻的NbOx通过Nb—O—Nb键相连而聚合.当Nb2O5的负载量超过其单层分散容量,表面NbOx物种通过Nb—O—Nb键聚合形成三维聚集态NbOx物种结构.
(3)Nb2O5/γ-Al2O3催化剂表面的B酸位特征与载体表面NbOx物种聚集状态密切相关.只有聚集状态的NbOx物种形成的Nb—OH—Nb桥羟基才呈现明显的B酸酸性.随着负载量增加,NbOx物种聚合度增大,更多的Nb—O—Al键转化为Nb—O—Nb键,表面B酸酸量增加,强度增强,IB与IBA缩合形成DMHD转化频率(TOF)增加.
(4)当Nb2O5的负载量超过其单层分散容量,其中只有部分NbOx物种位于表面,与二维NbOx物种相比较其表面利用率下降,Nb2O5/γ-Al2O3催化剂活性(TOF)下降,同时表面出现较强的B酸位,导致DMHD的选择性降低.
1 Izabela,N.;Maria,Z.Chem.Rev.,1999,99:3603
2 Ziolek,M.Catal.Today,2003,78:47
3 Tanabe,K.Catal.Today,2003,78:65
4 Ding,Q.P.;Yuan,Y.P.;Xiong,X.;Li,R.P.;Huang,H.B.;Li,Z. S.;Yu,T.;Zou,Z.G.;Yang,S.G.J.Phys.Chem.C,2008,112: 18846
5 Jang,J.S.;Kim,H.G.;Reddy,V.R.;Bae,S.W.;Ji,S.M.;Lee,J. S.J.Catal.,2005,231:213
6 Abdel-Rehim,M.;Santos,A.C.B.;Camorim,V.L.L.;Faro Jr.,A. C.Appl.Catal.A-Gen.,2006,305:211
7 Onfroy,T.;Manoilova,O.V.;Bukallah,S.B.;Hercules,D.M.; Clet,G.;Houalla,M.Appl.Catal.A-Gen.,2007,316:184
8 Braga,V.S.;Dias,J.A.;Dias,S.C.L.;Macedo,J.L.Chem. Mater.,2005,17:690
9 He,J.;Fan,Y.N.;Qiu,J.H.;Chen,Y.Acta Chim.Sin.,2004,62: 1311 [何 杰,范以宁,邱金恒,陈 懿.化学学报,2004,62: 1311]
10 Onfroy,T.;Clet,G.;Houalla,M.J.Phys.Chem.B,2005,109: 14588
11 Sumiya,S.;Oumi,Y.;Sadakane,M.;Sano,T.Appl.Catal.A-Gen., 2009,365:261
12 Chary,K.V.R.;Srikanth,C.S.;Rao,V.V.Catal.Commun., 2009,10:459
13 Carreon,M.A.;Guliants,V.V.;Guerrero-Perez,M.O.;Baöares, M.A.Catal.Commun.,2009,10:416
14 Martos,M.;Julián,B.;Dehouli,H.;Gourier,D.;Cordoncillo,E.; Escribano,P.J.Solid State Chem.,2007,180:679
15 Guerrero-Pérez,M.O.;Bañares,M.A.Catal.Today,2009,142: 245
16 Tanabe,K.;Okazaki,S.Appl.Catal.A-Gen.,1995,133:191
17 Okuhara,T.Chem.Rev.,2002,102:3641
18 Burcham,L.J.;Datka,J.;Wachs,I.E.J.Phys.Chem.B,1999, 103:6015
19 Carniti,P.;Gervasini,A.;Marzo,M.J.Phys.Chem.C,2008,112: 14064
20 He,J.;Fang,Y.N.;Qiu,J.H.Acta Petrolei Sinica(Petroleum Processing Scetion),2006,22:18 [何 杰,范以宁,邱金恒.石油学报(石油加工),2006,22:18]
21 Jehng,J.M.;Wachs,I.E.J.Phys.Chem.,1991,95:7373
22 Dong,L.;Chen,Y.Chin.J.Inorg.Chem.,2000,16:250 [董 林,陈 懿.无机化学学报,2000,16:250]
23 Chen,Y.;Zhang,L.F.Catal.Lett.,1992,12:51
24 Jimenez-Conzalez,J.;Schmeiber,D.Surf.Sci.,1991,250:59
25 Schuit,G.A.;Gates,B.C.AIChE J.,1973,19:417
26 Zhang,X.Y.Handbook of applied chemistry.Beijing:National Defense Industry Press,1988:25 [张向宇.应用化学手册.北京:国防工业出版社,1988:25]
27 Xia,W.S.;Chen,Y.;Wan,H.L.J.Mol.Catal.A-Chem.,1999, 138:185
28 He,J.;Fan,Y.N.;Qiu,J.H.;Chen,Y.Chin.J.Inorg.Chem., 2004,20:789 [何 杰,范以宁,邱金恒,陈 懿.无机化学学报,2004,20:789]
29 Kataoka,T.;Dumesic,J.A.J.Catal.,1988,112:66
30 Bernholc,J.;Horsley,J.A.;Murrell,L.L.;Sherman,L.G.;Soled, S.J.Phys.Chem.,1987,91:1526
31 Turek,A.M.;Wachs,I.E.;DeCanio,E.J.Phys.Chem.,1992,96: 5000
August 28,2009;Revised:December 3,2009;Published on Web:January 4,2010.
Dispersion and Acidity of Niobia on Nb2O5/γ-Al2O3
HE Jie1,2,*FAN Yi-Ning2
(1School of Chemical Engineering,Anhui University of Science and Technology,Huainan 232001,Anhui Province,P.R.China;2Key Laboratory of Mesoscopic Chemistry of the Ministry of Education,School of Chemistry and Chemical Engineering, Nanjing University,Nanjing 210093,P.R.China)
Supported niobium pentoxide materials are effective catalysts for a variety of reactions.Nb2O5/γ-Al2O3catalysts with different Nb2O5loadings were prepared by aqueous solution impregnation using niobium oxalate as a precursor on γ-Al2O3.The samples were characterized with respect to the dispersion state of the niobium oxide species on γ-Al2O3by X-ray power diffraction(XRD)and laser Raman spectroscopy(LRS).The nature of the surface acidity was investigated using Fourier-transform infrared spectroscopy of pyridine adsorption(Py-IR).The catalytic activity of the as-prepared catalysts was evaluated by the condensation reaction of iso-butene(IB)and iso-butyraldehyde(IBA)to form 2,5-dimethyl-2,4-hexadiene(DMHD).Results reveal that the dispersion capacity(ΓNb)of Nb on γ-Al2O3is about 7.6 μmol·m-2.This value is almost identical to the density of the octahedral vacant sites of the preferentially exposed (110)plane(7.5 μmol·m-2)on the surface of the γ-Al2O3support.Additionally,the“incorporated model”suggests that Nb5+cations are located on the vacant sites of the(110)plane on γ-Al2O3.These results suggest that isolated niobia (NbOx)species are present and are bound to the surface of the γ-Al2O3support through Nb—O—Al bonds at a loading well below that corresponding to monolayer dispersion.This is consistent with the result from LRS.The formation of isolated NbOxspecies,which binds to the surface of the support through Nb—O—Al bonds,causes a decrease in the amount of surface Lewis acid sites(LAS)on the Nb2O5/γ-Al2O3catalysts.With an increase in Nb2O5loading,polymeric NbOxspecies are formed by the Nb—O—Nb bridging of neighboring isolated NbOxspecies and Brönsted acid sites(BAS)are generated.We found that the catalytic activity towards the condensation reaction of IB and IBA to form DMHD increased because the amount and strength of the Brönsted acid sites increased as the number of polymeric niobia species increased.When the loading exceeds the monolayer dispersion capacity,the catalytic activity(turnoverfrequency(TOF)ofDMHD)decreasedbecause of the formation of the three-dimensional NbOxspecies. Additionally,the selectivity of DMHD decreased because of an increase in the strength of the Brönsted acid sites.We suggest that the strength of the Brönsted acid sites are related to the state of NbOxon the surface of the Nb2O5/γ-Al2O3catalysts.
Surface acidity; Nb2O5/γ-Al2O3; NbOxsurface species; Olefin-aldehyde condensation
[Article] www.whxb.pku.edu.cn
*Corresponding author.Email:jhe@aust.edu.cn;Tel:+86-554-6668497.
The project was supported by the National Key Basic Research Program of China(G1999022400).
国家重点基础研究发展计划(G1999022400)资助项目
O643

