清热除湿颗粒提取工艺研究
朱建新,王宏,何薇*
(1.首都医科大学附属北京中医医院,北京100010;2.北京市中医研究所,北京100010)
首都医科大学附属北京中医医院皮肤科常用协定处方——清热除湿汤是由已故著名中医皮外科专家赵炳南教授根据龙胆泻肝汤化裁而来,为皮肤科临床应用多年的经验方剂,该方对急性湿疹、接触性皮炎、带状疱疹、药疹等皮肤病急性湿热症有较好的疗效,同时体现了中医异病同治治疗原则的临床优越性。方中龙胆性寒,味苦,归肝、胆经,具有清热燥湿,泻肝胆火的功效,为君药;黄芩性寒,味苦,归肺、胆、脾、大肠、小肠经,具有清热燥湿,泻火解毒,止血,安胎等作用,为臣药;车前草性寒,味甘,归肝、肾、肺、小肠经,具有清热利尿通淋,祛痰,凉血,解毒的作用,为佐药。本实验通过正交试验设计,对其提取工艺进行了实验研究,确定影响提取工艺的显著性因素。已有的研究表明[1-3],龙胆、黄芩等有效成分在乙醇中有较高溶解度,故这几味药材均采用乙醇提取;白茅根[4-5]等药材含有丰富的多糖具有水溶性,故采用水提。结果报告如下。
1 仪器与试药
1.1 仪器Agilent1100高效液相色谱仪(G1312A型泵,G1365B型检测器);SK7210HP超声波清洗机;DU 800紫外分光光度计;ZK-072型真空干燥箱(上海市实验仪器总厂);METTLER TOLEDO精密电子天平。
1.2 试药龙胆苦苷、黄芩苷、无水葡萄糖对照品(由中国药品生物制品检定所提供,批号分别为:110770-200409;110715-201016;110833-200904);大车前苷对照品(由上海华壹生物科技有限公司提供,经HPLC分析,纯度≥98%,CAS:104777-68-6);甲醇(色谱纯,Fisher Scientific公司提供);乙腈(色谱纯,CNW公司提供)。其他试剂均为分析纯。
2 实验方法与结果
2.1 醇提工艺考察方法
2.1.1 龙胆苦苷测定方法
2.1.1.1 色谱条件[6]色谱柱为Kromasil 100-5 C18(150 mm×4.6 mm);流动相为水-甲醇(75∶25);体积流量1.0 mL/min;检测波长270 nm;柱温为室温;理论塔板数按龙胆苦苷计算应不低于4 000;在此条件下,供试品中龙胆苦苷峰与其他峰能达到基线分离,结果见图1。
2.1.1.2 标准曲线制备取龙胆苦苷对照品适量,精密称定,加甲醇制成每1 mL含0.5 mg的溶液,即得。精密移取上述龙胆苦苷对照品溶液0.5、1.0、2.0、3.0、4.0、5 mL,置5 mL量瓶中,甲醇定容,进样量为5 μL,依法测定。以对照品进样量(μg)与峰面积作图,进行回归处理,得龙胆苦苷回归方程为:Y=1 035.8X+10.136(r=0.999 8),表明龙胆苦苷在0.25~2.5 μg范围内与峰面积呈良好线性关系。
2.1.2 黄芩苷测定方法
2.1.2.1 色谱条件[6]色谱柱为Kromasil 100-5PHENYL(250 mm×4.6 mm);流动相为0.2%磷酸溶液-甲醇(53∶47);体积流量为1.0 mL/min;检测波长为280 nm;柱温为室温;理论塔板数为按黄芩苷计算应不低于2 500;在此条件下,供试品中黄芩苷峰与其他峰能达到基线分离,结果见图2。

图2 黄芩苷和样品HPLC色谱图
2.1.2.2 标准曲线制备精密称取已干燥(60℃减压干燥4 h)的黄芩苷对照品0.010 2 g,用甲醇定容于25 mL量瓶中,制成0.408 0 mg/mL的对照品溶液。精密吸取上述黄芩苷对照品溶液0.2、0.3、0.4、0.5、1.0、2.0 mL,置5 mL量瓶中,甲醇定容,滤过,分别注入液相色谱仪,进样量为5 μL,按上述条件测定黄芩苷峰面积,分别以黄芩苷峰面积积分值为纵坐标(Y),以进样量为横坐标(X),进行回归处理,得回归方程为:Y=3 630.5X-198.27(r=0.999 9),表明黄芩苷在0.081 6~0.816 0 μg范围内呈良好线性关系。
2.1.3 大车前苷测定方法[7]
2.1.3.1 色谱条件色谱柱为Kromasil 100-5PHENYL(250 mm×4.6 mm);流动相为0.1%甲酸溶液-乙腈(81∶19);体积流量1.0 mL/min;检测波长330 nm;柱温为室温;理论塔板数按大车前苷计算应不低于3 000;在此条件下,供试品中大车前苷峰与其他峰能达到基线分离,结果见图3。

图3 大车前苷和样品HPLC色谱图
2.1.3.2 标准曲线制备精密称取大车前苷对照品0.002 53 g,用60%甲醇定容于25 mL量瓶中,制成0.101 2 mg/mL的对照品溶液。精密吸取上述大车前苷对照品溶液0.5、1.0、2.0、3.0、4.0、5.0、6.0 mL,置10 mL量瓶中,60%甲醇定容,滤过,进样量为30 μL,依法测定。以对照品进样量(μg)与峰面积作图,进行回归处理,得大车前苷回归方程为:Y=1 129.7X+8.376 4(r=0.999 6),表明大车前苷在0.151 8~1.821 6 μg范围内与峰面积呈良好线性关系。
2.1.4 正交设计筛选最佳提取工艺
2.1.4.1 提取因素及水平的确定拟以A含乙醇量(%)、B乙醇用量(倍)、C提取时间(h)、D提取次数(次)为主要考察因素,选用L9(34)正交表设计试验,各因素的相关水平见表1。

表1 醇提工艺因素水平
2.1.4.2 提取方法及结果分析按处方称取龙胆、黄芩、车前草等药材,按照正交设计条件提取,试验结果见表2。

表2 醇提工艺正交试验结果
经直观分析和方差分析可知,影响该工艺的因素依次为D>C>B>A,A、B、C、D四个因素的差异均具有显著性(P<0.01),结果见表3。最佳提取工艺为A2B3C3D3,即70%乙醇,12倍量,提取3次,每次1.5 h。

表3 综合评分方差分析
2.1.5 验证实验称取处方量的龙胆等药材5份,按最佳工艺进行提取,龙胆苦苷的平均质量分数为3.70%,RSD为0.95%(n=5);黄芩苷的平均质量分数为9.15%,RSD为1.03%(n=5);大车前苷的平均质量分数为0.51%,RSD为1.07%(n=5),浸膏平均得率为35.28%。该条件下指标成分质量分数较稳定,因此该工艺是合理可行的。
2.2 水提取工艺的考察
2.2.1 多糖含有量测定方法
2.2.1.1 最大吸收波长的确定[8]取适量显色后的对照品溶液,于300~600 nm范围内扫描,在485 nm处有最大吸收,故选定最大吸收波长为485 nm。
2.2.1.2 标准曲线制备[9]精密称取105℃干燥至恒质量的无水葡萄糖对照品50 mg,置于50 mL量瓶中,加蒸馏水至刻度,配制成1 mg/mL的葡萄糖对照品溶液。精密量取上述对照品溶液0、1.0、2.0、3.0、4.0、5.0、6.0 mL分别置于50 mL量瓶中,加蒸馏水稀释至刻度,摇匀。精密量取上述各溶液2 mL置具塞试管中,分别加入1.0 mL 5%苯酚溶液,再垂直快速加入浓硫酸5 mL,充分振摇,置沸水浴上加热15 min,取出,置冷水浴中冷却30 min,于485 nm波长处测定吸光度,以吸光度Y为纵坐标,质量浓度X为横坐标,绘制标准曲线,回归方程为:Y=0.055 6X-0.098 9,r=0.999 3,葡萄糖在5~30 μg/mL范围内呈良好的线性关系。
2.2.2 浸膏得率测定称取干燥至恒质量的各样品,按下式计算浸膏得率:浸膏得率(%)=浸膏质量/样品质量×100%。
2.2.3 试验方法及结果分析
2.2.3.1 正交设计筛选提取工艺[10]拟以A提取次数(次)、B提取时间(h)、C加水量(倍)为主要考察因素,选用L9(34)正交表设计试验,各因素的相关水平见表4。

表4 水提工艺因素水平
2.2.3.2 样品制备及测定取处方量的白茅根、茯苓、生地黄等药材,按照L9(34)正交表进行实验,回流提取,滤过,合并滤液,浓缩,移至200 mL量瓶中,加水定容至刻度,摇匀。精密吸取50 mL,在搅拌状态下,加入4倍量无水乙醇沉淀多糖,4℃冰箱静置24 h,过滤,取沉淀,60℃减压干燥至恒质量,精密称量,即得。精密称取样品5 mg,置于50 mL量瓶中,加蒸馏水溶解并稀释至刻度。精密量取1 mL置于具塞试管中,按2.2.1.2项下方法测定样品的吸光度,代入回归方程,计算多糖的含有量,结果见表5。
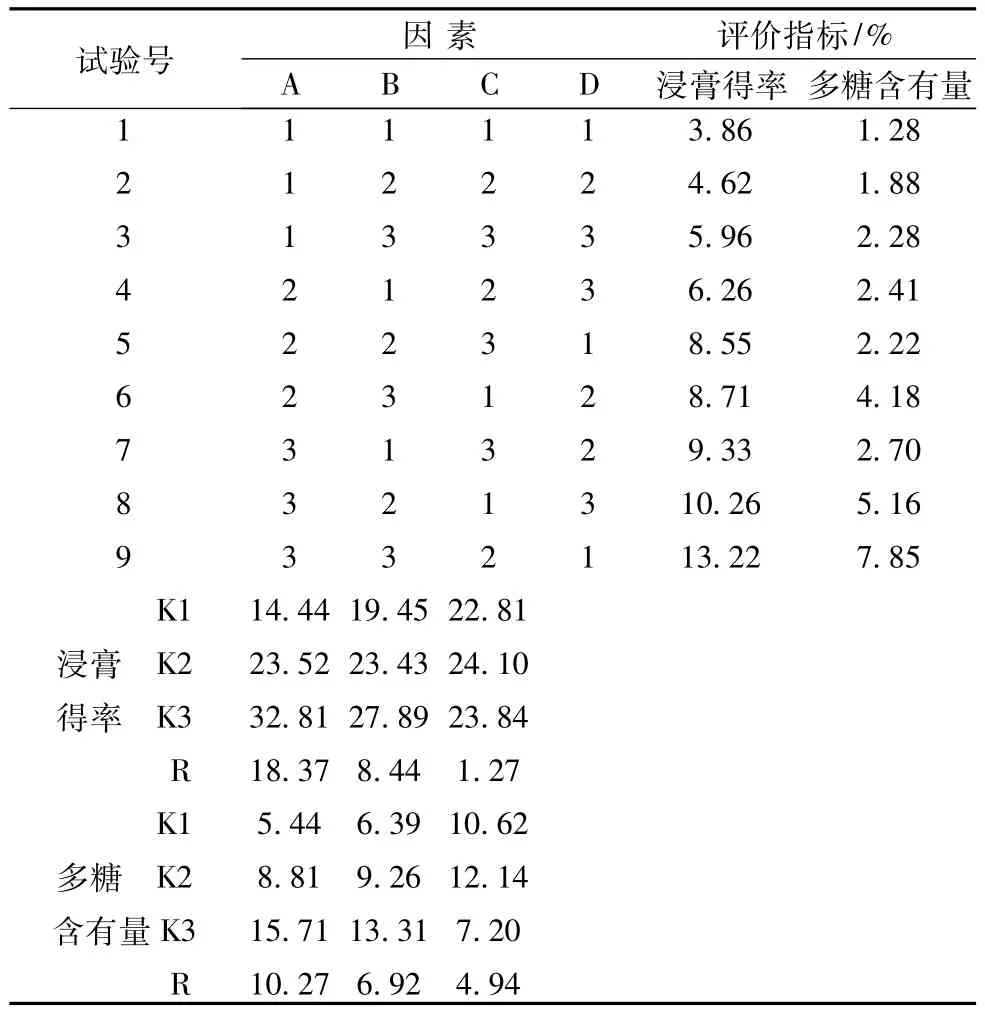
表5 水提工艺正交试验结果
2.2.3.3 结果分析由表5的直观分析可以看出,3因素中A即提取次数对实验结果影响最大,为多糖提取工艺的主要影响因素,影响次序依次为A>B>C。进一步的方差分析表明,A因素对浸膏得率的影响具有统计学意义(P<0.05),对多糖含有量的影响无统计学意义(P>0.05),B、C因素对浸膏得率和多糖含有量的影响都无统计学意义。综合考虑工艺成本,在多糖的提取工艺中,最佳提取工艺为A3B2C1,即加8倍量的水提取3次,每次2 h。结果见表6、表7。

表6 浸膏得率方差分析

表7 多糖含有量方差分析
2.2.3.4 验证试验按处方称取白茅根、茯苓等六味药,按照最佳提取条件A3B2C1提取多糖,计算多糖平均含有量为6.02%,RSD为0.69%(n=5),浸膏得率平均为11.59%,RSD为1.37%(n=5),说明优化后的工艺条件,多糖产率高,重复性好。
3 讨论
3.1 前期通过抗炎药效学实验[11]确定清热除湿颗粒的提取方法。实验结果表明,两种方法(传统水煎法、分类提取法)提取的清热除湿汤均可显著抑制小鼠耳肿胀,与模型对照组比较,存在显著性差异(P<0.01);分类提取法提取的清热除湿颗粒的抗炎效果优于传统水煎法。因此,确定了清热除湿汤的提取方法为分类提取法。
3.2 由于本方为治疗急性湿疹、皮炎,故该类制剂产品应便于患者携带和贮存;另外,整个处方的出膏率为17.4%,出膏量为22 g,即使在不加辅料的情况下,也很难制备成片剂或胶囊剂,故选择为颗粒剂。
3.3 清热除湿颗粒为中药复方制剂,成分复杂,龙胆苦苷为本方中君药龙胆的主要有效成分,黄芩苷为臣药黄芩的主要有效成分。用单一考察指标筛选中药提取工艺条件并不全面,单一指标的优劣并不能完全代表中药制剂整体质量的优劣[12]。因此,本实验在清热除湿颗粒醇提取工艺的优选实验中,采用了3指标评价法,以综合考察提取工艺的优劣。
3.4 水提取工艺中多糖的含有量测定,实验原理[13]为多糖在浓硫酸作用下水解成单糖并迅速脱水生成糖醛,然后与苯酚缩合成有色化合物,用分光光度法测定其含有量。本法显色稳定,灵敏度高。苯酚试剂应为新鲜配置,且冷藏避光保存,否则以蒸馏水作空白对照时颜色加深,对实验结果有干扰。
[1]杨维霞,周乐,耿会玲,等.龙胆科药用植物化学成分的研究现状[J].西北植物药学,2008,23(12):2235-2240.
[2]孙凤娇,廖克俭,丛玉风.黄芩提取工艺的优化研究[J].精细石油化工进展,2008,9(11):51-52.
[3]熊淑华,熊爱珍,方晓,等.正交试验设计法优选黄芩的提取工艺[J].中国医药导报,2008,5(2):46-47.
[4]刘荣华,付丽娜,陈兰英,等.白茅根化学成分与药理研究进展[J].江西中医学院学报,2010,22(4):80-83.
[5]王莹,孟宪生,包永睿,等.白茅根多糖提取工艺优化及含量测定[J].亚太传统医药,2009,5(11):24-26.
[6]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[7]孙虔,耿放,程雪梅,等.车前草中大车前苷的定性和定量分析[J].中国中药杂志,2010,35(16):2095-2098.
[8]张亚环,陈萍,王小芳,等.正交试验法优选黄芪多糖的水提工艺研究[J].化学世界,2007(6):345-347.
[9]刘依.板蓝根有效成分的提取分离及含量测定[D].北京:中国农业大学,2002:21-22.
[10]张国华,李邵平,季晖,等.正交设计优化冬虫夏草多糖的提取工艺[J].安徽医药,2004,8(6):404-405.
[11]朱建新,何薇.清热除湿汤提取方法的实验研究[C]//中华中医药学会制剂分会世界中联中药药剂专业委员会学术年会论文集.昆明:中华中医药学会制剂分会世界中联中药药剂专业委员会,2011:131-133.
[12]罗友华,程刚,李成付,等.正交试验法优选咽舒宁颗粒剂的提取工艺[J].中国药剂学杂志,2009,7(4):299-304.
[13]陈惠红,冯艳玲,苏艳妮.正交试验优选神光源颗粒剂的提取工艺[J].现代中药研究与实践,2007,21(5):46-48.

