不同证型颈动脉粥样硬化患者Hp感染状况及相关基因检测分析
刘丽芳,窦逾常,于红霞
(1.长春中医药大学附属医院 神经内科,吉林 长春 130021;2.吉林大学中日联谊医院 中医科,吉林 长春 130033;3.空军航空大学门诊部,吉林 长春 130000)
传统的脂质浸润学说和损伤反应学说认为动脉粥样硬化的形成与高血压、高血脂、糖尿病和吸烟等因素相关,并且是缺血性脑卒中发病的主要病因。我们发现Hp感染与缺血性脑卒中有一定的相关性[1],Hp感染及相关基因是否参与了不同证型颈动脉粥样硬化的形成尚未清楚,为此本文对此进行研究,为动脉粥样硬化的防治提供科学依据。
1 资料与方法
1.1 临床资料 治疗组103例均为2009年2月-2011年8月长春中医药大学附属医院神经内科住院的缺血性脑卒中合并颈动脉粥样硬化患者,男65例,女38例,年龄54~78,平均年龄(63.3±10.1)岁,均为48 h之内发病患者。对照组为同期年龄、性别、体质量指数、居住环境和生活习惯的频数相匹的健康体检合并颈动脉粥样硬化者136例,男85例,女51例,年龄52~79,平均年龄(62.5±11.4)岁。观察对象4周内均未接受过抗生素治疗。
诊断标准符合国家中医药管理局制定的《中风病诊断疗效评定标准》(试行)和中华医学会修订的《各类脑血管疾病诊断要点》。颈动脉内膜中层厚度(IMT)的检测结果作为颈动脉粥样硬化的判定标准,采用飞利浦IU-22型彩色多普勒对颈内外动脉分叉处及其上、下1.0~1.5 cm的范围内进行检测,以1.0 mm≤IMT<1.5 mm为颈动脉硬化病变期;IMT≥1.5 mm,且增厚的内膜向血管腔内凸出确定为有斑块形成。参照国家中医药管理局制定的《中医病证诊断疗效标准》,将颈动脉粥样硬化辨证为精髓亏虚证、痰浊内阻证、气血滞瘀证、气血两虚型。
1.2 实验方法
1.2.1 血清抗-Hp-IgG、抗-Hp CagA-IgG及抗-Hp VacA-IgG的检测 研究对象均以间接酶联免疫法(ELISA)测定抗-Hp-IgG来判断Hp感染率,试剂由郑州华美生物工程公司提供;对抗-Hp-IgG阳性血清均以免疫印记法(Weston-Blotting)测定抗-Hp CagA-IgG和抗-Hp VacA-IgG,判定Hp不同毒力亚型感染率,试剂由上海元谷科技发展有限公司提供。
1.2.2 动脉粥样斑块螺杆菌16SrRNA和Hp CagA、VacA和glmM基因检测 对6例CagA+VacA+菌株感染的患者,经颈动脉内膜切除术获得的动脉粥样斑块,用3S柱提取法,以Hp的SS1菌株为阳性对照,去离子水代替模板作为阴性对照,进行PCR方法扩增,将扩增产物进行凝胶电泳、DNA测序分析。
1.3 统计学方法 样本均数的比较采用t检验,率的比较采用χ2检验和Fisher精确检验;并用条件logistic回归进行多因素分析;所有统计分析用SPSS 16.0软件完成。
2 结果
2.1 2组及不同证型患者血清抗-Hp-IgG、抗-Hp CagA-IgG及抗-Hp VacA-IgG的检测结果比较 见表1。
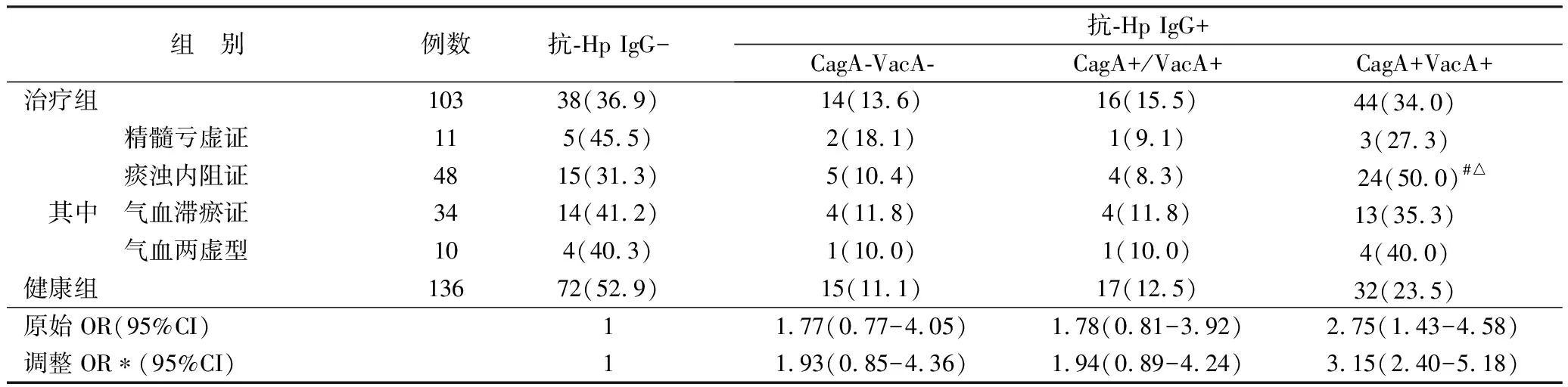
表1 2组及不同证型患者血清抗HP-IgG、抗-Hp CagA-IgG及抗Hp-VacA-IgG检测结果比较 例(%)
表1结果显示颈动脉粥样硬化组Hp感染率(63.1%)明显高于健康对照组(47.1%)(P<0.05);CagA+VacA+感染率(34.0%)明显高于CagA-VacA-(13.6%)和CagA+/VacA+(15.5%)(P<0.05),其中痰浊内阻证CagA+VacA+感染率(50.0%)优势更加明显(P<0.05)。
2.2 2组动脉粥样斑块螺杆菌16SrRNA和HpCagA、VacA和glmM基因检测 对6例CagA+VacA+菌株感染的患者的动脉粥样斑块,用3S柱提取法,经进行PCR方法扩增,将扩增产物进行凝胶电泳、DNA测序分析,结果显示均阴性。
3 讨论
近年来,由于对Hp感染和动脉粥样硬化的相关性认识存在着争议[2-3],研究者一直致力于在动脉粥样斑块组织中寻找Hp-DNA,但未得到有力和可信的证据[4]。结合以前的研究,对不同证型颈动脉粥样硬化患者Hp感染状况及相关基因进行了分析,结果发现痰浊内阻证型颈动脉粥样硬化患者是Hp感染的主要证候,且CagA+VacA+感染率具有更显著的优势;虽然未检出螺杆菌16SrRNA、Hp CagA、VacA和glmM相关基因,但不能否认此相关性。
中医学认为,动脉粥样硬化和毒邪、痰浊、血瘀密切相关。外感邪毒,内伤脾胃,转输失利,津液不行,痰瘀相关,痰浊内生,阻于脉络,血行不畅,痰瘀互结,郁久腐化,渐而形成毒、痰、瘀相互交结之病机,故以痰浊内阻证型为主要症候。Hp和动脉硬化形成的机制可能是:1)Hp感染时常引起全身或局部血管炎症反应,或促进TNF-α、IL-1、6、8及细胞间黏附因子以及E-选择素水平升高,诱导单核细胞黏附到血管内皮、趋化白细胞聚集并损伤血管内皮,加重局部炎症反应导致动脉粥样硬化血栓的形成[5]。2)Hp作为外源性抗原可增强动脉局部免疫应答,激活局部的免疫反应,诱导动脉内膜损伤,或通过增高氧自由基水平来介导免疫机制;尤其CagA阳性菌株可通过加重免疫炎症反应,参与早期动脉粥样硬化的形成,或通过抗原模拟与血管壁的表面抗原发生交叉反应诱导血管损伤,在动脉粥样硬化机制中起重要作用[6]。3)Hp感染的低度炎症可诱导体内脂质过氧化,引起低密度脂蛋白升高和高密度脂蛋白下降,导致血小板持续激活和不可逆性聚集,促进血栓形成[7]。
本研究通过对不同证型颈动脉粥样硬化患者Hp感染状况及相关基因的分析,Hp感染有可能通过诱导免疫和炎症反应,导致脂质代谢紊乱,促进动脉粥样硬化的发生发展。Hp感染可能是痰浊内阻证型颈动脉粥样硬化患者的危险因素,其中CagA+VacA+优势显著。
[1]李霞,窦逾常.缺血性中风患者幽门螺旋杆菌感染状况调查[J].北京中医药大学学报,2008,31(2):138-144.
[2]Sawayama Y,Ariyama I,Hamada M,et al.Association between chronic Helicobacter pylori infection and acute ischemic stroke:Fukuoka Harasanshin Atherosclerosis Trial(FHAT)[J].Atherosclerosis,2005,178(2):303-309.
[3]Khairy P,Rinfret S,Tardif JC,et al.Absence of association between infection agents and endothelial function in healthy young men[J].Circulation,2003,107:1966-1971.
[4]Manolakis A,Kapsoritakis AN,Potamianos SP,et al.A review of the postulated mechanisms concerning the association of Helicobacter pylori with ischemic heart disease[J].Helicobacter,2007,12(4):287-297.
[5]Innocenti M,Thoreson AC,Ferrero RL,et al.Helicobacter pylori-induced activation of human endothial cells[J].Infect Immun,2002,70(8):4581-4590.
[6]Masoud SA,Arami MA,Kucheki E.Association between Infection with Helicobacter Pylori and Cerebral Non cardioembolic Ischemic Stroke [J].Neurol India,2005,53(3):303-306.
[7]Harangi M,Seres I,Magyar MT,et al.Association between human paraoxonase 1 activity and intima-media thickness in subjects under 55 years of age with carotid artery disease[J].Cerebrovasc Dis,2008,25(1-2):122-8.

