铝灰中AlN的水解行为
姜 澜,邱明放,丁友东,苏 楠,姚 泉
(东北大学 多金属共生矿生态化冶金教育部重点实验室,沈阳 110819)
铝灰(或铝灰渣)是原铝生产、铝合金以及废铝回收过程中产生的一种渣。与其他重金属熔炼产生的炉渣不同,铝灰会浮在熔体表面并呈现出松散的灰渣状。据统计,每生产1 000 kg铝,就会产生25~50 kg的铝灰[1-2]。全世界每年产生约500万t的铝灰[3]。随着铝及铝合金产量的提高,铝灰的生成量也随之增大。因此,铝灰的绿色循环利用便成为了人们关注的热点。目前,铝灰的利用基本上只是回收其中的金属铝,提取金属铝后的残灰大部分直接堆存或填埋处理,少部分用于制造建筑材料的填料。回收金属铝后的残灰可用来生产氧化铝[4]、制备净水剂[5]、合成或制备Al-Si合金[6-7]、合成耐火材料[8-9]等,但大部分残灰的利用尚处于试验研究阶段。
通过对铝灰的组成进行分析发现[3,10],铝灰中除含有Al、Al2O3外,还含有大量的AlN。铝灰中的AlN很不稳定,能与水发生反应放出氨气,造成残灰利用过程中的材料性能不稳定、溶液酸碱度发生变化;在堆存和填埋后,也会造成环境污染。因此,研究铝灰中AlN与水的反应行为,对铝灰的循环利用和避免环境污染具有重要的现实意义。
AlN和水反应会生成氢氧化铝和氨气。过去,这个反应被用来生产氨水。随着人们逐渐发现它所具有的独特性能(高导热系数、高电导率、低介电常数等)[11-12],AlN开始引起更多人的注意。控制AlN水解反应已经成为粉末处理过程中的主要问题。对于AlN水解反应,国内外学者进行了大量研究[13-16]。SVEDBERG等[14]研究了在不同pH值条件下,AlN在85 ℃的水中恒温反应1 h后的水解情况,并通过XRD检测到具有不同比例的 AlOOH和Al(OH)3相生成。KRNEL和KOSMAC[15]研究发现,AlN发生水解反应之前存在诱导期,该诱导期随着温度的升高而缩短,随着溶液pH值的降低而延长。FUKUMOTO等[16]研究了在室温到100 ℃条件下,粉末和用该粉末烧结的AlN陶瓷块体的水解行为。该研究同样发现AlN在发生水解反应之前存在诱导期,诱导期随着温度的升高而缩短;烧结后的AlN陶瓷块体在室温下不发生水解,在373 K下有轻微的水解,水解后的pH值仅达到8。通过对不同温度的水解产物分析可知,AlN的水解行为在351 K时会发生改变:在这一温度以下,拜耳石为主要结晶相;而当温度高于此温度时,便形成了结晶的勃姆石。
以上关于AlN水解的研究主要集中在AlN粉末和AlN陶瓷的水解行为。该两种AlN和铝灰中的AlN的生成条件完全不同,而铝灰中AlN水解行为尚未见报道。针对电解铝厂产生的铝灰,本文作者研究了反应时间、反应温度、铝灰粒度、液固比和搅拌速度等条件对其中的AlN水解程度的影响,旨在为铝灰堆存过程中减少环境污染和铝灰中资源二次利用提供理论依据。
1 实验
1.1 原料及预处理
本实验所用铝灰来源于中国铝业抚顺分公司。从工厂取回的铝灰先预处理后再进行分析测试和实验研究。预处理过程为:将铝灰中大块金属铝分离去除,剩余部分棒磨处理,并选择60目标准筛进行筛分,取筛下物(粒度小于0.25 mm)作为实验原料。铝灰筛下物的形貌如图1所示。用激光粒度仪对筛下物进行粒度分析,结果见图2。

图1 两种粒度铝灰的SEM照片Fig.1 SEM images of aluminum dross: (a) Big particles;(b) Small particles
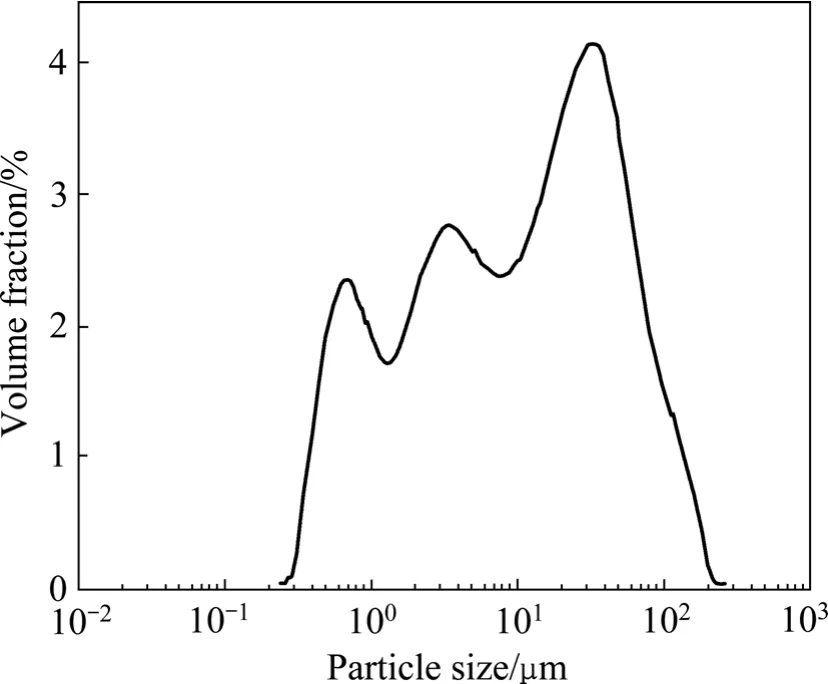
图2 铝灰粒度分布Fig.2 Particle size distribution of aluminum dross
从粒度分析结果可知,预处理后的铝灰粒度分布在0.3~100 μm范围内。从图1所示的扫描电镜照片可以看出,铝灰中的大颗粒多为团聚体,多孔疏松。铝灰预处理过程也表明,大颗粒物料较疏松、易粉碎。X射线衍射分析结果表明铝灰的物相组成为 Al2O3、MgAl2O4、AlN、NaAl11O17和K1.6Al11O17。铝灰的化学组成见表1。
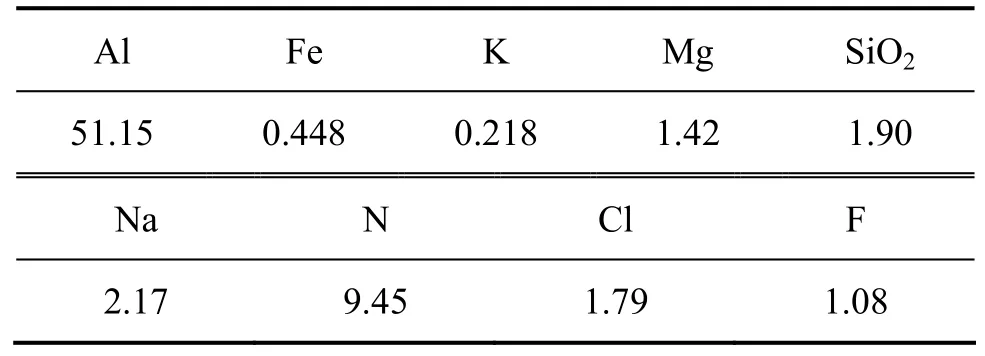
表1 铝灰的化学组成Table1 Chemical composition of aluminum dross ( mass fraction, %)
1.2 实验过程
将经预处理后的铝灰原料(以下简称为铝灰)进行水解实验,实验过程如下。
将一定量的铝灰加入预热至设定温度的去离子水中,进行水解实验,定时测定水解浆料的 pH值。分别测定了在不同水解温度、搅拌速度和物料粒度等条件下的铝灰浆料的pH值以及铝灰中剩余AlN含量随时间的变化规律;物料粒度条件实验需将铝灰原料研磨至能全部通过对应条件的筛网。在水解反应结束后进行真空过滤,滤渣在50℃下烘干并称重,然后测定滤渣中剩余AlN含量,并进行物相分析。
1.3 分析测试方法
利用PW3040/60型X射线衍射分析仪对样品进行物相分析,利用SSX-550型扫描电子显微镜对粉体的微观形貌进行观察。
采用蒸馏分离-中和滴定法测定氮含量,测定方法如下。
1) 测量原理及过程
准确称取一定量的铝灰或滤渣W(g)于蒸馏瓶中,加入 NaOH溶液进行蒸馏,铝灰渣中的 AlN可溶于NaOH溶液中并放出氨气,发生如下反应:
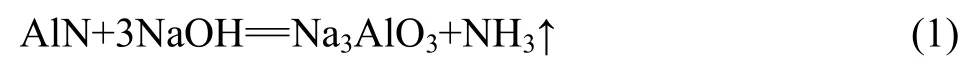
用硼酸吸收溜出液,并以甲基红-溴甲酚绿为指示剂,用浓度为C的硫酸溶液进行滴定,滴定终点为亮绿色变为酒红色,并记录所消耗硫酸的量V1。用相同的方法做空白实验,记录所消耗硫酸的量V2。
2) 测量结果计算
铝灰渣中AlN含量ωAlN可用如下公式进行计算:ωAlN=0.082C(V1-V2)/W。
2 结果与讨论
2.1 AlN水解过程热力学
本实验中,通过对生成物进行 XRD物相分析,可以确定氮化铝水解反应方程式为
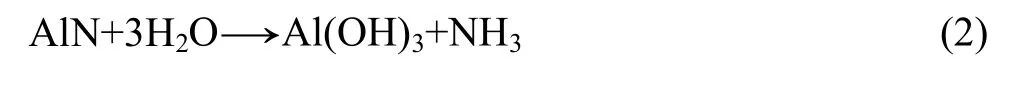
不同温度下的反应吉布斯自由能(ΘΔG)计算采用如下公式计算:
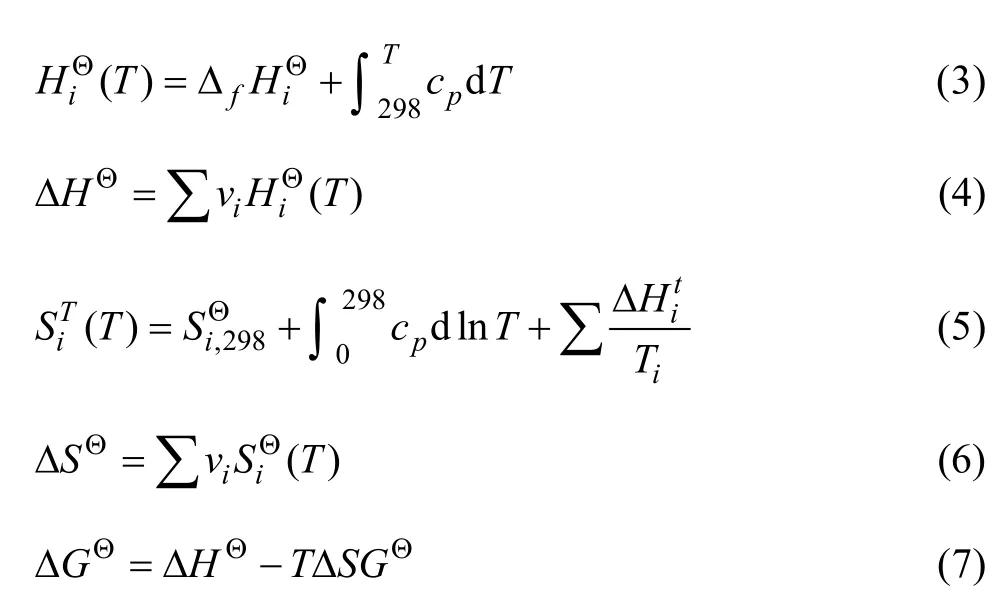
式中:HiΘ为i物质在温度T下的生成焓;ΔfHiΘ为i物质标准摩尔生成焓;ΔHΘ为化学反应焓变;υi为i物质的化学计量数;SiΘ为i物质在温度T下的熵;cp为等压热容;ΔSΘ为化学反应熵变。
参与反应的各物质的热力学数据见表2。

表2 物质的热力学数据Table2 Thermodynamic parameters of substances
计算结果如下:

计算 0~100 ℃(298~373 K)范围内的ΔGΘ时,在此范围内SiT(T)的变化很小,因此,可以忽略其变化,全部采用298 K的熵。
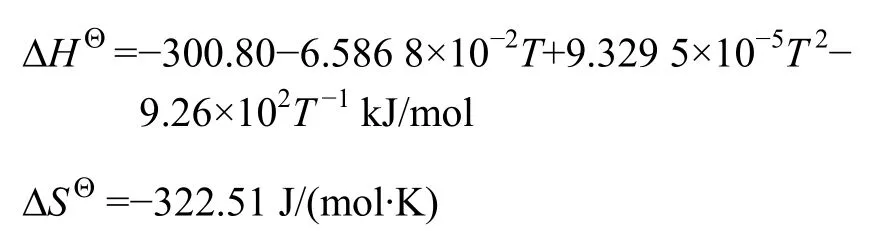
由化学反应吉布斯自由能计算公式:
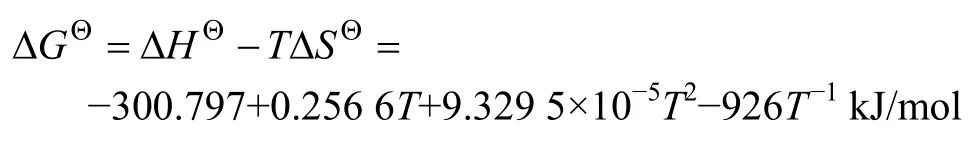
可计算出298~373K下ΘΔG的数据,结果列于表3。
由表3可以看出,在298~373 K时,AlN的水解反应吉布斯自由能变化均小于零,在热力学上均能朝正方向进行。

表3 不同温度下反应方程式(2)ΘΔG与T之间的关系Table3 Relationship between Gibbs free energy and temperature for reaction (2)
2.2 铝灰中AlN水解过程中pH的变化
进行水解温度、液固比、物料粒度、搅拌速度等单因素实验,考察各因素对铝灰浆料的 pH值影响。实验结果见图3~6。
实验所用去离子水的pH值为6.7。图3所示为温度条件实验结果,固定实验条件为物料粒度小于0.25 mm,搅拌速度200 r/min,液固比10。可以看出,加入铝灰后溶液的pH值均明显上升,在水解0.2 h后pH值均超过了9;在8 h内,298 K下水解所能达到的最高pH值为9.61,而在373 K温度下水解所达到的最高pH值为10.38。可见,温度越低,水解后的料浆pH值越低;温度越高,pH值越高。表明温度对水解过程有显著影响。图4所示为298 K温度下液固比为2.5~15的实验结果,其中物料粒度小于0.25 mm,搅拌速度200 r/min。从实验结果可以看出,液固比较小的水解pH值高于液固比较大的水解pH值。这是因为在其他条件一定的情况下,液固比越小,AlN的浓度相对越高,此时AlN水解生成的NH3溶解在水中,所以表现为液固比越小,水解pH值越高。
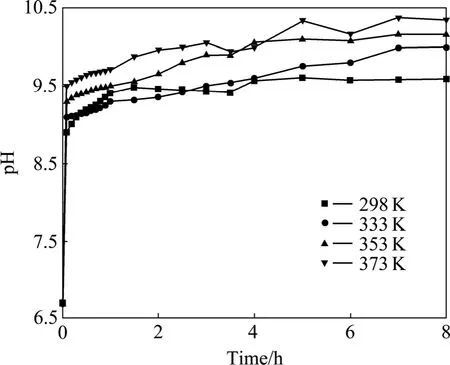
图3 温度对铝灰水解过程中溶液pH值的影响Fig.3 Effect of temperature on pH value of suspension in aluminium dross hydrolysis process
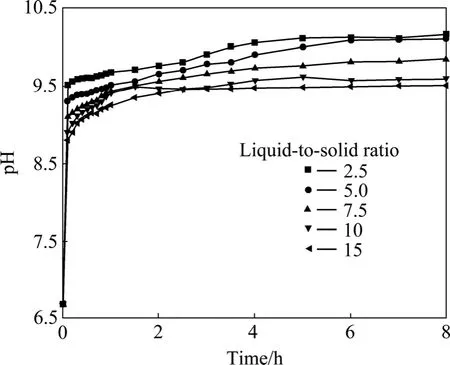
图4 液固比对铝灰水解过程中溶液pH值的影响Fig.4 Effect of ratio of liquid to solid on pH value of suspension in aluminium dross hydrolysis process
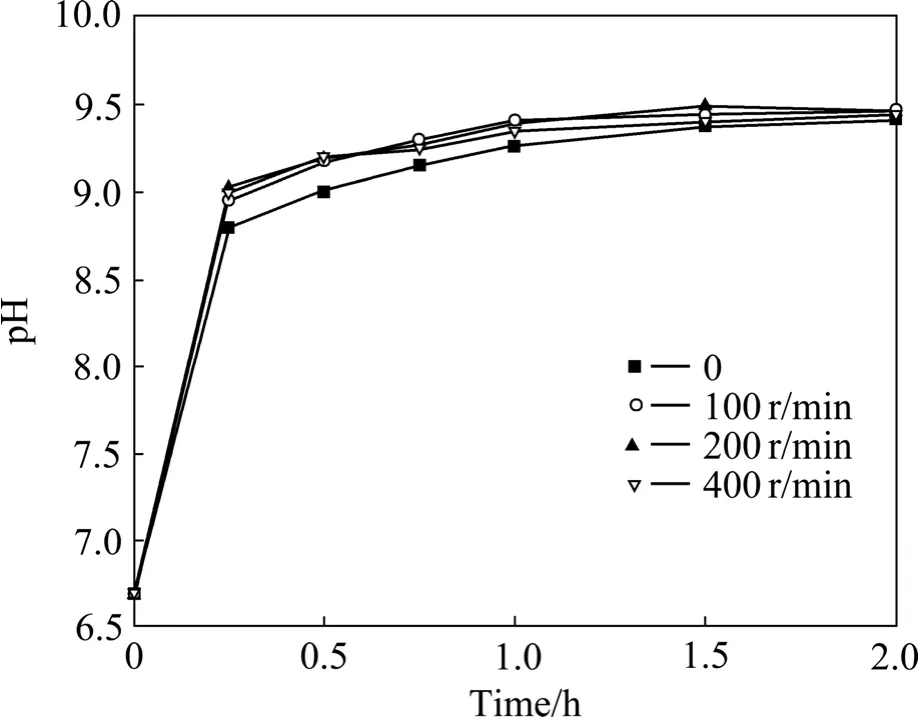
图5 搅拌速度对铝灰水解过程中溶液pH值的影响Fig.5 Effect of stirring rate on pH value of suspension in aluminium dross hydrolysis process
图5所示为在298 K温度下,将粒度小于 0.25 mm、液固比为10的物料,在不同搅拌速度下进行水解的实验结果。可以看出,在水解初期,无搅拌条件下的pH值低于有搅拌水解的pH值,最后pH值趋于一致。而搅拌速度为100、200和400 r/min时的水解pH值并无明显差别。由于搅拌有利于铝灰颗粒悬浮于液体中,也有利于AlN与H2O反应生成的NH3和H2O的混合,从而加快化学反应和传质过程的进行,因此搅拌在一定程度上可以加速水解的进行。
表4所列为铝灰筛分分析结果及各粒度级别的物料AlN含量。图6所示为在温度298 K、液固比10、搅拌速度200 r/min条件下,不同粒度的物料水解实验结果。该实验是先将物料分别进行研磨,使其全部通过各粒度级别的筛网,然后取相同质量的磨后物料进行水解。可以看出,粒度小于0.075 mm的铝灰水解pH值稍高于其他粒度的pH值;但从4个粒度级别的水解结果总体来看,粒度对水解pH没有明显影响。从表4中可以看出,大部分AlN存在于粒度较小的铝灰中;粒度小于0.12 mm的铝灰中,AlN含量占全部含量的80%以上。粒度对水解pH值影响较小的原因是:铝灰中的AlN大多集中在小粒度物料中,而研磨只是磨细了铝灰中的其他大粒度物质(主要含氧化铝)。
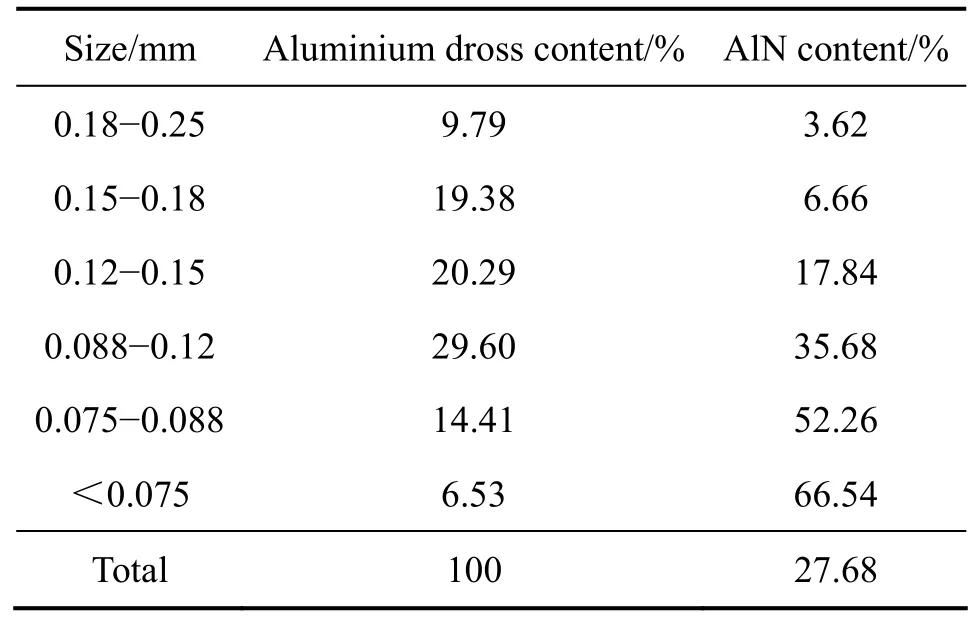
表4 铝灰筛分分析结果及AlN含量Table4 Sieve analysis and AlN content of aluminium dross
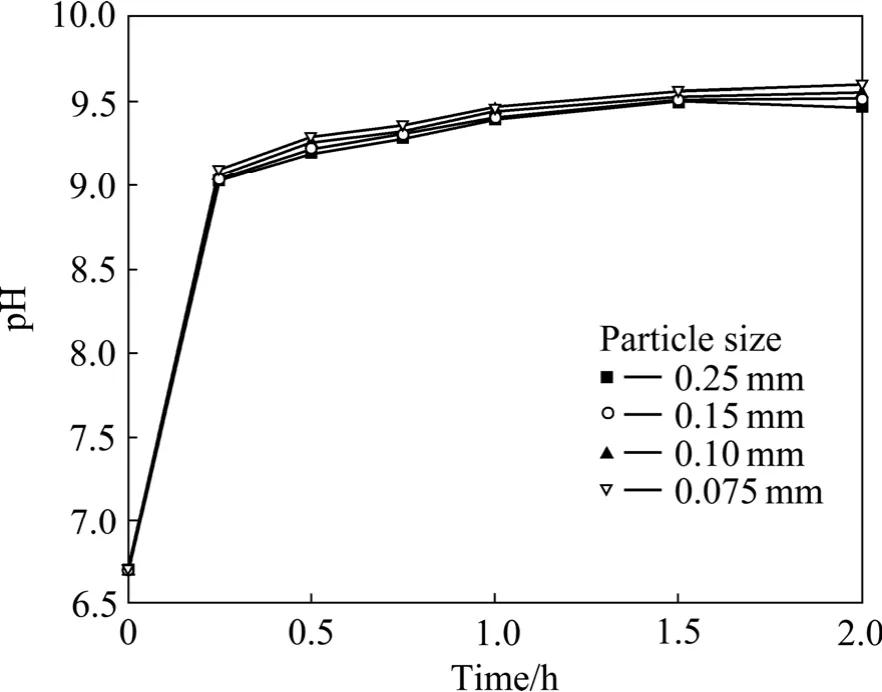
图6 粒度对铝灰水解过程溶液pH值的影响Fig.6 Effect of particle size on pH value of suspension in aluminium dross hydrolysis process
2.3 AlN水解后铝灰中剩余AlN含量
考察了不同温度下铝灰水解过程中的剩余AlN含量(如图7所示)。每次实验所用原料为粒度小于0.25 mm的铝灰100 g(AlN含量为27.68%),搅拌速度为200 r/min,液固比为10。结果表明:随着反应时间的延长,铝灰中的AlN含量逐渐降低。在298 K下水解24 h后的滤渣,烘干后其AlN含量为27.01 g,水解曲线接近水平直线,可见在室温下AlN的水解速度很慢。随着水解温度的升高,水解速度显著升高。在313、333和353 K温度下水解24 h,滤渣中AlN的含量分别为20.15、6.46和3.89 g;在373 K温度下AlN的水解反应速度很快,0.4 h后滤渣中AlN的含量为12 g,1 h后AlN含量为5 g,8 h后AlN含量为0.92 g,24 h后为仅为0.52 g。
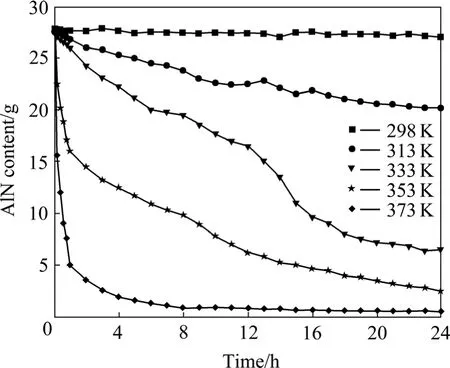
图7 温度对铝灰水解滤渣中AlN含量的影响Fig.7 Effect of temperature on AlN content in aluminium dross residue during hydrolysis process
2.4 分析与讨论
在铝灰与水反应的实验过程中,用湿润的石蕊试纸在反应容器口进行检测发现,红色的石蕊试纸会变成蓝色,说明反应过程中有氨气生成。又根据水解产物物相分析结果(图8)可知,产物中出现了Al(OH)3相,此即验证了铝灰中AlN的反应是按反应式(2)进行的。当铝灰加入到水中后,悬浮液的pH值开始升高,并且随着温度的变化,达到最高值所需时间不同。由反应
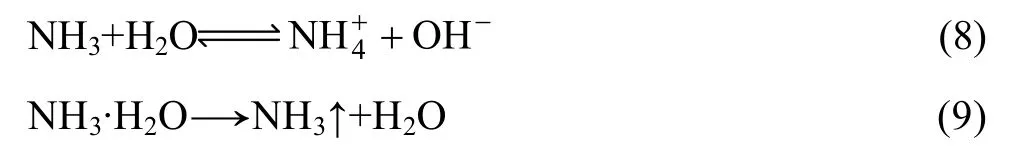
可知,AlN水解产生的 NH3溶于水并电离形成NH4+和OH-,这一反应使溶液的pH值迅速升高。另外,在不同温度下,NH3在水中的溶解度有很大的差别[17],因此溶液的pH值总会达到一个最大值。这也就是在图7中在高温下有很多AlN反应生成了NH3,而在图3中pH却没有很明显提高的原因。
AlN粉末水解过程中存在较长的诱导期[15-16],在298 K温度下的诱导期约为10 h,而AlN陶瓷块体仅在373 K下有轻微的水解。与这两者相比,铝灰中的AlN的活性更大一些,在同样反应条件下,不存在明显的诱导期(298 K条件下,0.1 h的水解pH就超过了9)。相对AlN粉末的制备条件,铝灰中的AlN是在较低温度下生成的,呈多孔、疏松团聚状,比表面积大,因而更活泼,易于水解反应。
从水解产物的物相分析结果(见图8)也可以看出两种AlN水解的区别。铝灰中的 AlN水解产物只有Al(OH)3相,未见AlOOH相的存在。此结果说明铝灰中AlN水解生成稳定的 Al(OH)3相,而没有过渡相AlOOH。
为了避免铝灰中AlN发生水解反应,在铝灰或回收金属铝后的残灰堆存过程中,首先应尽量避免铝灰与水(如空气中的水蒸气、雨水等)相接触,其次要将铝灰放置在温度较低的环境中,目的是降低铝灰水解的反应速度;在铝灰的再利用过程中,可以将铝灰氧化焙烧成稳定的耐火材料(如氧化铝、铝镁尖晶石等),再加以利用;采用湿法配料,也要考虑 AlN水解的问题。
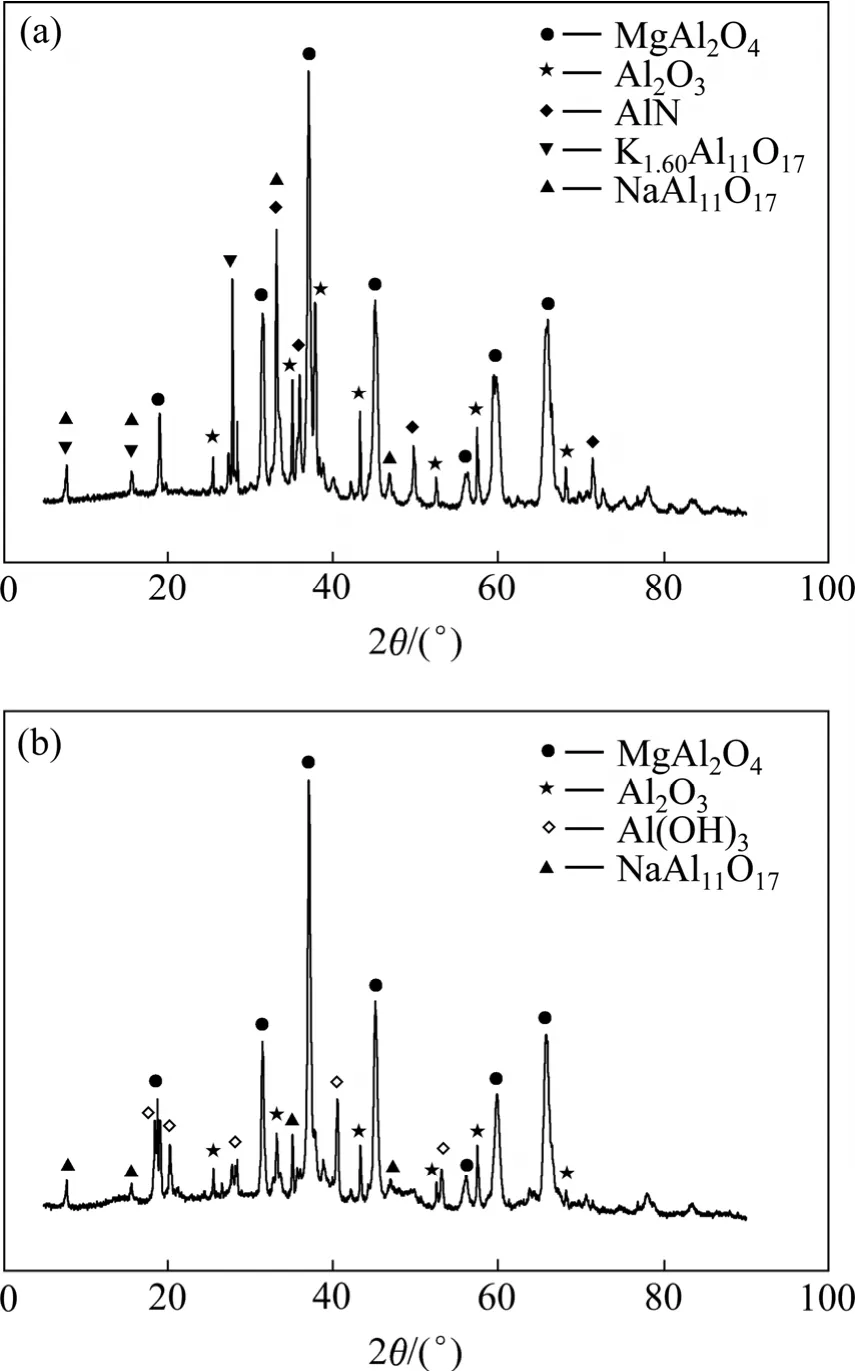
图8 铝灰及其水解产物物相分析Fig.8 Phase anylysis of aluminum dross and its hydrolyzed products: (a) Aluminum dross; (b) Hydrolyzed products under condition of 80 ℃ for 24 h
3 结论
1) 铝灰中的AlN和水接触时,会发生水解反应,水解后AlN中的氮元素以氨气的形式释放出来。
2)在相同温度下,随着水解时间的延长,溶液pH逐渐升高,直到达到平衡;水解8 h以内,温度越高,溶液 pH越大;温度越高、反应时间越长,铝灰中AlN的反应越充分。在373 K下水解24 h后,AlN几乎完全转变成Al(OH)3。在298 K温度下,在2.5~15的液固比范围内,液固比越小,水解 pH值越高;搅拌可以在一定程度上加速水解的进行;粒度对水解pH没有明显影响。
3) 与AlN粉末和AlN陶瓷块体相比较,铝灰中的AlN活性更高,不存在诱导期。AlN粉末水解产物是AlOOH和Al(OH)3混合物,而铝灰中AlN的水解产物只有Al(OH)3相,未见AlOOH相的存在。
[1]周长祥, 王 卿, 张文娟, 赵 伟.铝渣灰中氨氮的回收[J].矿产保护与利用, 2012, 3(6): 38-41.ZHOU Chang-xiang, WANG Qing, ZHANG Wen-juan, ZHAO Wei.The recovery of ammonia nitrogen from aluminum slag ashes[J].Conservation and Utilization of Mineral Resources,2012, 3(6): 38-41.
[2]石 健, 邹开云.利用铝灰制备聚合氯化铝工艺参数的优化[J].南通大学学报, 2011, 10(3): 31-34.SHI Jian, ZOU Kai-yun.Optimization on process parameters about preparation of polyaluminum chloride from aluminum ash[J].Journal of Nantong University, 2011, 10(3): 31-34.
[3]MURAYAMA N, MAEKAWA I, USHIRO H, MIYOSHI T,SHIBATA J, VALIX M.Synthesis of various layered double hydroxides using aluminum dross generated inaluminum recycling process[J].International Journal of Mineral Processing,2012, 110/111: 46-52.
[4]DAS B R, DASH B, TRIPATHY B C, BHATTACHARYA I N,DAS S C.Production ofβ-alumina from waste aluminium dross[J].Minerals Engineering, 2007, 20: 252-258.
[5]李小忠, 许晓路, 申秀英, 袁向红.以炼铝灰渣为原料制备絮凝剂及其应用[J].环境科学与技术, 2002, 27(21): 100-102.LI Xiao-zhong, XU Xiao-lu, SHEN Xiu-ying, YUAN Xiang-hong.Preparation of aluminium mortar based flocculants and its application[J].Environmental Science & Technology,2002, 27(21): 100-102.
[6]KIMA J, BISWASA K, JHONB K W, JEONGB S Y, AHNA W S.Synthesis of AlPO4-5 and CrAPO-5 using aluminum dross[J].Journal of Hazardous Materials, 2009, 169: 919-925.
[7]HONG Jian-ping, WANG Jun, CHEN Hai-yan, SUN Bao-de, LI Jia-jing, CHEN Chong.Process of aluminum dross recycling and life cycle assessment for Al-Si alloys and brown fused alumina[J].Transactions of Nonferrous Metals Society of China,2010, 20: 2155-2161.
[8]YOSHIMURA H N, ABREU A P, MOLISANI A L.Evaluation of aluminum dross waste as raw material for refractories[J].Ceramics International, 2008, 34: 581-591.
[9]曾令可, 李得家, 刘艳春, 王 慧.利用铝加工废渣制备堇青石材料[J].材料导报, 2009, 23(1): 90-92.ZENG Ling-ke, LI De-jia, LIU Yan-chun, WANG Hui,Application of industrial sludge of aluminum[J].Factory in Producing Cordierite, 2009, 23(1): 90-92.
[10]HISAYUKI K, ATSUTA Y, DAMON H, FUJIE K.Stabilization of aluminum dross by using hydrothermal reaction[J].Journal of Japan Institute of Light Metals, 2009, 59(11): 627-631.
[11]ZHANG Y, BINNER J G P.Characterisation of a surface treated AlN powder in aqueous media[J].International Journal of Inorganic Materials, 1999, 1: 219-227.
[12]OLIVEIRA M, OLHERO S, ROCHA J, FERREIRA J M F.Controlling hydrolysis and dispersion of AlN powders in aqueous media[J].Journal of Colloid and Interface Science, 2003,261: 456-463.
[13]KOCJAN A, KRNEL K, KOSMAC T.The influence of temperature and time on the AlN powder hydrolysis reaction products[J].Journal of the European Ceramic Society, 2008,28(5): 1003-1008.
[14]SVEDBERG L M, ARNDT K C, CIMA M J.Corrosion of aluminum nitride (AlN) in aqueous cleaning solutions[J].Journal of the American Ceramic Society, 2000, 83: 41-46.
[15]KRNEL K, KOSMAC T.Reactivity of AlN powder in an aqueous environment[J].Key Engineering Materials, 2004,264/268(1): 29-32.
[16]FUKUMOTO S, HOOKABE T, TSUBAKINO H.Hydrolysis behavior of aluminum nitride in various solutions[J].J Mater Sci,2000, 35: 2743-2748.

