丝氨酰组氨酰赖氨酸三肽的合成*
徐常龙,曹小华,严 平,柳闽生,张爱东,张 岩
(1.九江学院生命科学学院,江西九江 332000;2.南京晓庄学院化学系,江苏 南京 210017;3.华中师范大学农药与化学生物学教育部重点实验室,湖北武汉 430079)
含His-Lys序列的肽是一种具有不同生物功能的内源性多肽,可由多种组织细胞表达和分泌,发挥多种生物学功能[1~4],其化学合成是研究热点[5~7]。研究发现丝氨酰组氨酰赖氨酸三肽[ZSer-His(Trt)-Lys-Z-OBzl,1]具有细胞生长因子的功能[8],并且由于其中丝氨酸具有羟基侧链,在一定条件下可与糖或卤代糖形成O-糖肽链[9]。糖肽是糖蛋白活性中心的结构区域,在细胞免疫学和医学上可用于抗原与受体的识别作用,在生物学上可用于对细胞间相互作用和遗传学研究[10],因此,1的合成有重要的生物学意义。
本文利用液相合成法,L-丝氨酸(L-Ser),L-组氨酸(L-His)和L-赖氨酸(L-Lys)经活化后缩合合成了1(Scheme 1),其结构经1H NMR,IR和GC-MS确证。
1 实验部分
1.1 仪器与试剂
XT4A型显微熔点仪;Mer-curyPlus-400型核磁共振仪(CDCl3为溶剂,TMS为内标);Nicolet 470型红外光谱仪;Trace MS型质谱仪。
3[5],A-B[6,11]按文献方法合成;L-Ser,L-His,L-赖氨酸盐,苄氧甲酰氯,N-羟基琥珀酰亚胺,N,N-二环己基碳二亚胺(DCC),化学纯,上海吉尔生化公司;其余所用试剂均为分析纯,其中Et3N使用前重蒸,EtOAc和MeOH经无水处理。
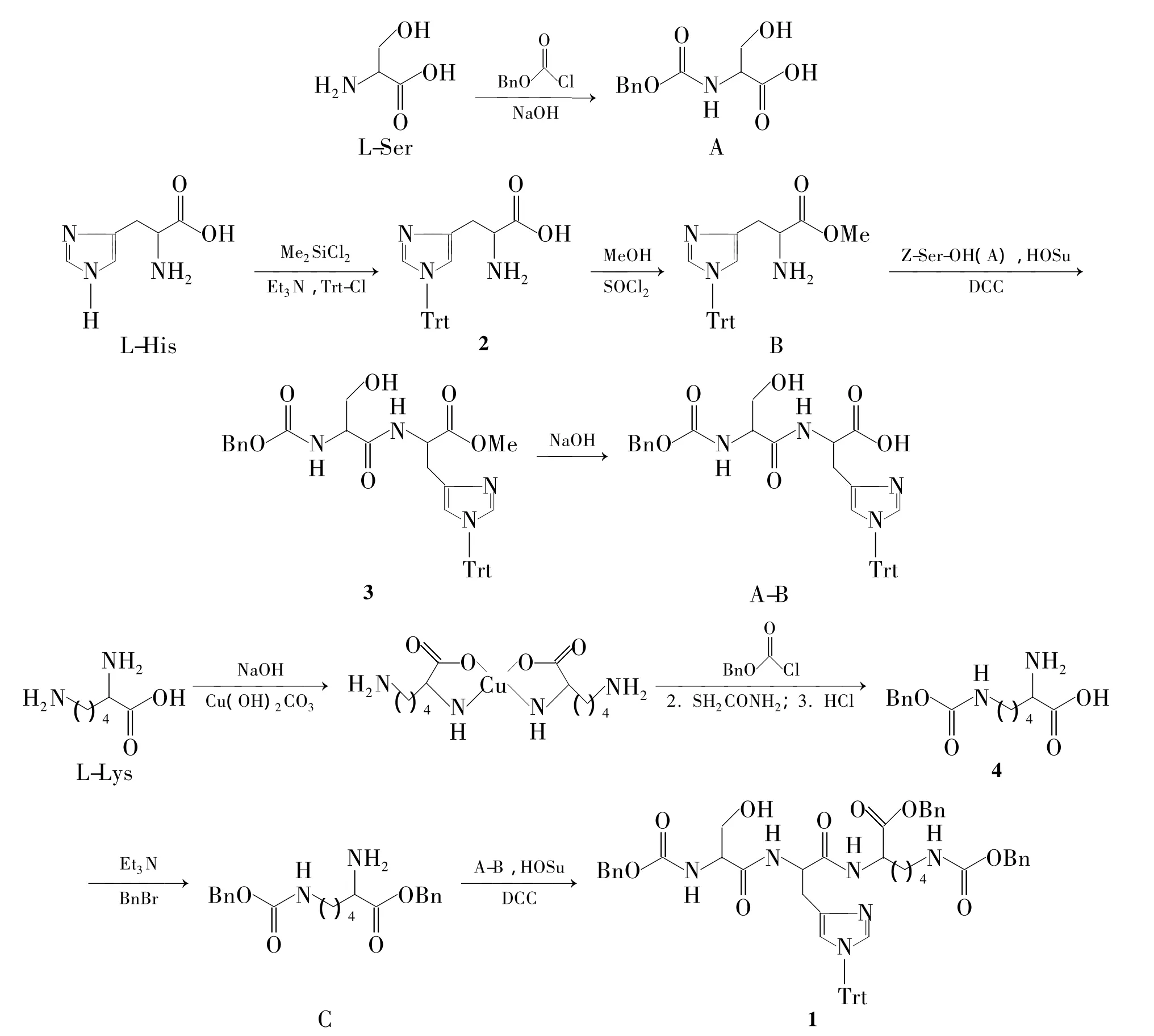
Scheme 1
1.2 合成
(1)Z-Ser-OH(A)的合成
在反应瓶中加入L-Ser 6.0 g(57 mmol)和2 mol·L-1NaOH溶液33 mL,冰浴冷却,搅拌下缓慢滴加苄氧酰氯12.8 mL(90 mmol),滴毕,用2 mol·L-1NaOH 溶液(约 45 mL)调至 pH 8.0,反应8 h。撤去冰浴,反应过夜。用乙醚(50 mL)洗涤,冰浴下用浓盐酸(约6 mL)调至pH 3.0(出现白色沉淀),静置(冰箱)3 h;过滤,滤饼用水(4×20 mL)洗涤,真空干燥过夜得白色固体A 8.5 g,产率62.2%,m.p.99 ℃ ~ 101 ℃;1H NMR δ:3.84~3.87(m,2H,CH2),4.27(m,1H,CH),5.10~5.14(m,2H,CH2),7.28~7.38(m,5H,PhH);IR ν:3 424,3 338,3 329,3 211,3 030,1 746,1 692,1 600,1 535,1 401,911,750,697 cm-1。
(2)H-His(Trt)-OH(2)的合成
在反应瓶中依次加入 L-His 3.0 g(19.3 mmol)和 CH2Cl215 mL,搅拌下加入 Me2SiCl22.33 mL(19.3 mmol),于室温反应 5 h;加入 Et3N 2.68 mL(19.3 mmol),反应 15 min;依次加入 Et3N 1.39 mL(10 mmol)和三苯基氯甲烷(Trt-Cl)5.38 g(4.2 mmol)的 CH2Cl2(10 mL)溶液,反应 2 h。加入过量无水MeOH,旋蒸脱溶,加水10 mL,用Et3N 调至 pH 8.0 ~8.5,加入 CHCl320 mL,过滤,滤液依次用水(20 mL)和乙醚(20 mL)洗涤,用混合溶剂[V(THF)∶V(H2O)=1 ∶1]重结晶,真空干燥48 h 得白色固体2 4.2 g,产率54.%,m.p.218 ℃ ~ 221 ℃;1H NMR δ:2.92 ~ 3.16(m,2H,CH2),3.79 ~3.82(m,1H,CH),6.85(s,1H),7.12 ~7.41(m,5H,PhH);IR ν:3 414,3 050,2 966,1 629,1 597,1 491,1 246,1 230,753,701 cm-1。
(3)H-His(Trt)-OMe(B)的合成
在反应瓶中加入甲醇8 mL,冰盐浴冷却至-10℃,搅拌下缓慢滴加SOCl21 mL,滴毕,加入2 4.0 g,于20℃反应2 h;回流反应(70℃ ~80℃)30 min(组氨酸完全溶解)。旋蒸脱溶,加无水乙醚30 mL~40 mL(大量晶体析出),于冰箱中静置1 h~2 h,抽滤,滤饼用无水乙醚洗涤,真空干燥得白色固体B 3.05 g,产率40.3%,m.p.118℃ ~ 121 ℃;1H NMR δ:3.10(s,3H,CH3),3.15~3.30(m,2H,CH2),4.13(m,1H,CH),6.96(s,1H),7.15 ~7.76(m,5H,PhH);IR ν:2 937,2 928,1 631,1 182,1 057 cm-1。
(4)H-Lys(Z)-OH(4)的合成
在反应瓶中依次加入盐酸赖氨酸10 g(56 mmol)的水(75 mL)溶液,碱式碳酸铜 12.7 g,搅拌下回流反应4 h。加热水(60℃ ~70℃)50 mL,过滤,滤液冷却至0℃,用固体Na2CO3调至pH 9,恒温(0℃)下滴加苄氧甲酰氯58 mL(约1 h,用固体 Na2CO3控制 pH≈9),于室温反应12 h;过滤得蓝色固体[12],加水 200 mL,加入硫代乙酰胺8.42 g(112 mmol),于50℃反应3 h。用2 mol·L-1盐酸调至 pH 2,煮沸5 min,过滤(除去CuS沉淀[13]),滤液浓缩至 60 mL(析出白色沉淀),过滤,真空干燥48 h得白色固体4 2.3 g,产率 20.1%,m.p.246 ℃ ~ 248 ℃;1H NMR δ:1.42 ~1.53(m,6H,CH2),1.78 ~1.80(m,3H,CH2N),3.12(m,2H,PhCH2),3.31~3.51(m,2H,NH2),7.28 ~ 7.38(m,5H,PhH);IR ν:3 345,3 338,3 319,3 054,3 034,1 582,1 513,1 419,940,1 692,747,697 cm-1。
(5)H-Lys-(Z)-OBzl(C)的合成
在反应瓶中加入4 2.0 g(7.1mmol)和AcOEt 45 mL,搅拌使其完全溶解;依次加入Et3N 1.0 mL(7.1mmol)和 PhCH2Br 0.8 mL(35.7 mmol),回流反应6 h。抽滤[14],滤饼用乙酸乙酯洗涤,合并滤液与洗液,依次用0.5 mol·L-1碳酸氢钾溶液(2×20 mL)、饱和氯化钠溶液(2×20 mL)和1.17 mol·L-1氯化钠溶液(50 mL)洗涤至中性,用无水Na2SO4干燥,旋蒸脱溶得油状液体C 2.1 g,产率 67.8%。
(6)1的合成
在反应瓶中依次加入A-B 9.74 g(15 mmol),N-羟基琥珀酰亚胺(HOSu)1.78 g(15.5 mmol)和四氢呋喃21 mL,搅拌使其完全溶解;冰浴冷却下滴加DCC(3.18 g)的 THF(6 mL)溶液,滴毕,反应6 h。自然升至室温,静置过夜,过滤(除去N,N-二环已基脲)得溶液(E)备用。
在反应瓶中加入C 1.82 g(4.5mmol)和THF 10 mL,搅拌使其完全溶解;加入E,冰浴冷却下反应2 d。旋蒸脱溶得黄色黏稠状物,加乙酸乙酯20 mL,分别用饱和 NaHCO3溶液(3×20 mL)、柠檬酸溶液(3×20 mL)和饱和NaCl溶液(3×20 mL)洗涤,无水Na2SO4干燥,旋蒸脱溶后经硅胶柱层析[洗脱剂:V(CH3Cl3)∶V(CH3OH)=5 ∶1]纯化得淡黄色固体 1 1.3 g,产率 42.1%;1H NMR δ:3.38 ~3.48(m,8H,CH2),3.85(m,1H,NH),3.12(m,2H,PhCH2),7.55 ~8.92(m,10H,PhH);EI-MSm/z:898(M+),551,243,91。
2 结果与讨论
2.1 合成
肽的化学合成法包括液相合成和固相合成法。两者各有优缺点,对于较小的肽,液相反应比固相反应较方便,纯化较容易。在肽的化学合成中,主要是酰胺键的形成和侧链基团的保护。肽的液相合成法发展至今,运用较为广泛的主要有混合酸酐法[16]、活化酯法[17]和缩合剂法[18]。缩合剂法中最为普遍使用的是二环已基碳二亚胺(DCCI)法,反应中氨基的活化通常加入有机碱如三乙胺、N-甲基吗啉等,能抑制副反应且提高收率,本文采用此种方法。
在1的合成中,由于其中的氨基酸均为三官能团的氨基酸,给合成带来一定困难,因此选择合适的保护基显得极为重要,也是能否合成较纯产物肽的关键。本文采用HOSu-DCCI法合成1,用N-甲基吗林调节体系pH至9。在制备保护氨基酸时,考虑到1含有L-Ser,其侧链羟基可和溴代葡萄糖反应形成糖肽[19],三肽上所有的保护基在糖肽形成后才脱除,由于O-糖所含肽键在酸性和碱性条件下均会断裂,因此氨基酸的侧链氨基和羧基的保护基,必须在温和条件下容易脱去,且在脱保护反应中对肽链的酰氨键和糖肽中O-糖肽键的影响很小。因此本文采用苄酯保护L-Lys的羧基,苄氧甲酰氯保护L-Ser的氨基和L-LysE位上的氨基,而苄基和苄氧甲酰基可在在中性条件用催化氢化法除去[7],且氢化还原彻底,同时除掉了两种保护基团,简化反应步骤。
在甲酯B的合成中,采用SOCl2酰化L-His的羧基,会产生一定的副反应,Trt基在酸性条件下会脱除,因此控制SOCl2的加入量十分重要。本文对文献[20]方法进行了改进,减少 SOCl2用量,延长反应时间,并在反应中升温回流之前,加入NaHCO3调节体系pH至中性,制得咪唑基上的氨基保护的组氨酸甲酯。
本文合成了具有细胞生长因子功能的丝氨酰组氨酰赖氨酸三肽,以其为原料可合成具有重要生物功能的分子糖肽。为研究其对细胞生长的影响状况奠定了基础,提供了其在医学及免疫学中应用的可能。
[1]Boucher J,Masri B,Daviaud D,et al.Apelin,a new lyidentified adipokine up-regulated by insulin and obesity[J].Endocrinology,2005,146(4):1764 -1771.
[2]Simpkin J C,Yellon D M,Davidson S M,et al.Apelin-13 and apelin-36 exhibit direct cardioprot ective activity against ischemia-reperfusion injury[J].Basic Rescardiol,2007,102(6):518 -528.
[3]钱凯先.生物进化中的多肽生长因子探讨[J].浙江大学学报,1994,28(5):549 -554.
[4]吴文清.多肽生长因子与糖尿病肾病[J].中国实用内科杂志,2000,20(8):508 -509.
[5]彭小三,陈均辉,张昕等.甘氨酰组氨酰赖氨酸(GHK)的液相合成及其酶促降解[J].中国生物化学与分子生物学学报,2003,19(3):406~409.
[6]赵明,彭师奇,迪丽努尔,等.含RGD四肽的合成与功能[J].药学学报,1997,32(4):271 -277.
[7]邱凯,万昌秀,赵强,等.精氨酸-甘氨酸-天门冬氨酸三肽的合成与生物活性检测[J].四川大学学报,2002,39(4):734 -737.
[8]Pickart L.The use of glycylhistidy llysine in culture systems[J].In Vitro,1981,17(6):459 -466.
[9]Ivone Carvalho,Shona L Scheuer,K PRavindranathan Kartha,et al.Practical synthesis of the 2-acetamido-3,4,6-tri-O-acetyl-2-deoxy-beta-D-glucosides of fmocserine and fmoc-threonine and their benzyl esters[J].Carbohydrate Research,2003,338(10):1039 -1041.
[10]Medhurst A D,Jennings C A,Robbins M J,et al.Pharmacological and immunohisto chemical characterization of the APJ receptor and its endogenous ligand apelin[J].J Neurochem,2003,84(5):1162 -1172.
[11]K Barlos,DpapaioannouD.The odorpoulos“efficientone-pot”synthesis ofN-tritylamino acids[J].J Org Chem,1982,47:1324 -1326.
[12]Navdeep,B Malkar Janeller,L Lauer-fields,et al.Convenient synthesis of glycosylated hydroxylysine derivatives for use in solid-phase synthesis[J].Tetrahedron Letters,2000,41(8):1137 -1140.
[13]姚志勇,杨大成,范莉,等.O-苄基丝氨酸苄酯盐酸盐的制备方法研究[J].中国药物化学杂志,2003,13(1):16 -20.
[14]J R Vaughan,R L Osato.Preparation of peptides using mixed carbonic-carboxylic acid anhydrides[J].J AM Chem Soc,1952,74:676.
[15]F H C Stewart.The preparation of someN-alkylsydnones containing a functional group in the side chain[J].J Chem,1962,27(2):687 -689.
[16]G W Anderson,J E Zimmernanand,F M Callahna.N-Hydroxysuccinimide esters in peptide synthesis[J].J Am Chem Soc,1964,86(9):1839 -1842.
[17]D F DeTar,R Silverstein.Reactions of carbodiimides.Ⅰ.The mechanisms of the reactions of acetic acid with dicyclohexylcarbodiimide1,2[J].J Am Chem Soc,1966,88(5):1020 -1023.
[18]许家喜,杨俊海.糖肽的合成[J].化学通报,1998,(3):23 -30.
[19]Hong Zhang,Yali Wang,Wolfgang Voelter.A new strategy for the synthesis of Asp-Gly units-containing glycopeptides using Fmoc/Bzl protection[J].Tetrahedronletters,1995,36(48):8767 -8770.
[20]思洋,刘乐乐,张廊,等.氨基酸甲乙酯的合成及纯化[J].内蒙古医学院学报,2005,27(1):33-34.

