响应面法优化提取杨梅果渣中矢车菊-3-葡萄糖苷的研究
成纪予,杨虎清
(浙江农林大学农业与食品科学学院,浙江临安311300)
杨梅(Myrica rubra Sieb.et zucc.)属于浆果,果实富含花青素,色泽诱人,酸甜适宜,风味独特,具有宜人的香气。矢车菊-3-葡萄糖苷是杨梅中主要的花青素类物质,占95% 以上[1],是主要的活性有效成分,具有抗氧化、调节免疫、抗癌等方面的功能作用[2-4]。杨梅可鲜食,也可以加工成饮料、果酒、果脯等多种产品形式,其中以果汁产品为主。随着加工量的增加,每年会产生占鲜重25%左右的杨梅果渣。目前这些果渣还未能得到充分有效的利用,造成资源的巨大浪费,同时也严重污染环境。而杨梅果渣中含有丰富的矢车菊素-3-葡萄糖苷[5],且对于杨梅果渣中矢车菊素-3-葡萄糖苷的提取研究尚未见报道。因此,本研究以杨梅果渣为原料,采用有机溶剂浸提并结合超声波处理提取矢车菊-3-葡萄糖苷,在单因素实验的基础上,采用响应面优化法确定适宜的提取条件,为今后的杨梅果渣的深度开发和综合利用提供参考依据。
1 材料与方法
1.1 材料与仪器
杨梅(品种:荸荠) 采摘后立即运送到实验室,经榨汁去核后,得到新鲜的杨梅果渣,干燥、粉碎,过60 目筛备用;矢车菊-3-葡萄糖苷 Sigma 公司;甲醇、乙腈、甲酸 均为色谱纯;乙醇 分级纯;实验室用水均为超纯水。
DFT-200 手提式高速中药粉碎机 温岭市大德中药机械有限公司;Waters 2695 液相色谱色谱仪 美国Waters 公司;KQ-250B 型超声波清洗机超声 江苏昆山超声仪器有限公司。
1.2 提取方法
准确称取5g 杨梅渣,转入100mL 容量瓶内,用提取溶剂定容到100mL,置于超声波发生器固定位置,超声波的水位亦要固定,在设定的温度和时间进行超声波(40kHz,250W)处理。提取结束,真空抽滤,滤液待测。
1.2.1 单因素影响
1.2.1.1 乙醇浓度 分别以20%、40%、60%、80%、95%的乙醇溶液为提取溶剂,提取温度为40℃,超声40min。
1.2.1.2 提取温度 以60%乙醇溶液为提取溶剂,分别在30、40、50、60、70、80℃下提取,超声40min。
1.2.1.3 提取时间 以60%乙醇溶液为提取溶剂,在60℃下,分别超声20、30、40、50、60、70、90、110min。
1.2.2 Box-Behnken 实验设计 根据Box-Behnken实验设计原理,以乙醇浓度、提取温度、提取时间作为考察因子,进行响应面优化组合,因素与水平见表1。

表1 因素与水平表Table 1 Table of factors and levels
1.3 矢车菊-3-葡萄糖苷含量的测定
将提取液经微孔滤膜(0.45μm)过滤后,用高效液相色谱测定矢车菊-3-葡萄糖苷含量。色谱条件[6]:ODS 柱(250mm ×4.6mm i.d.,5μm),流动相A为0.1%的甲酸水溶液,流动相B 为80%乙腈水溶液;采用梯度洗脱:0~30min,流动相B 由0 变化为66%;检测波长为520nm,流速为1.0mL/min,柱温为30℃,进样量为10μL。矢车菊-3-葡萄糖苷对照品的高效液相图谱如图1 所示。根据出峰面积建立矢车菊-3-葡萄糖苷浓度(x,mg/mL)与峰面积(y)之间的回归方程:y =1E +9x-42795(R2=0.9994)。根据下式计算矢车菊-3-葡萄糖苷得率:
得率(mg/g)= 矢车菊- 3 - 葡萄糖苷浓度(mg/mL)×提取液体积(mL)/原料质量(g)
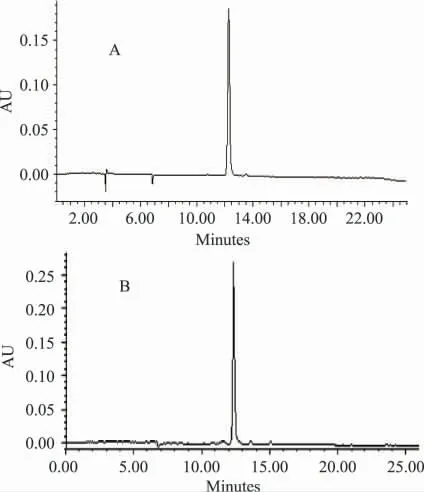
图1 矢车菊-3-葡萄糖苷对照品(A)及样品(B)的HPLC 图谱Fig.1 HPLC chromatograms of cyanidin-3-glucoside standard(A)and sample(B)
2 结果与分析
2.1 乙醇浓度对矢车菊-3-葡萄糖苷得率的影响
由图2 可知,含有适量水的乙醇溶液有利于增加杨梅渣中矢车菊-3-葡萄糖苷的得率。当乙醇浓度从20%增加到60%时,矢车菊-3-葡萄糖苷的得率从2.88mg/g 提高到3.95mg/g。当乙醇浓度达到80%,得率降低到3.65mg/g。当用95%的乙醇溶液提取时,一些极性较低的物质同时被提取,这可能导致降低了杨梅渣中矢车菊-3-葡萄糖苷的得率。
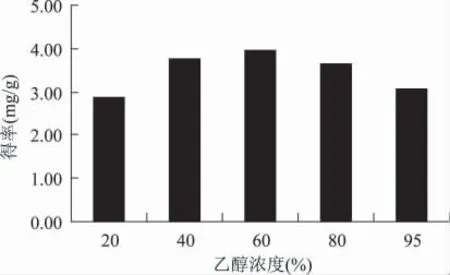
图2 乙醇浓度对矢车菊-3-葡萄糖苷得率的影响Fig.2 Effect of ethanol concentration on extraction rate of cyanidin-3-glucoside
2.2 提取温度对矢车菊-3-葡萄糖苷得率的影响
提取温度对杨梅渣中矢车菊-3-葡萄糖苷得率的影响见图3。在30~60℃温度范围,矢车菊-3-葡萄糖苷的得率随着温度增高而逐渐提高,从3.68mg/g 增加到4.28mg/g。但在更高的温度下,一方面矢车菊-3-葡萄糖苷容易受到破坏,另一方面使其它物质的溶出量增加,从而导致得率降低。

图3 提取温度对矢车菊-3-葡萄糖苷得率的影响Fig.3 Effect of extraction temperature on extraction rate of cyanidin-3-glucoside
2.3 提取时间对矢车菊-3-葡萄糖苷得率的影响
提取时间对杨梅渣中矢车菊-3-葡萄糖苷得率的影响见图4。提取时间从10min 延长到70min,可观察到矢车菊-3-葡萄糖苷的得率增加,从2.14mg/g提高到4.35mg/g。提取时间从70min 延长到90min,得率的增加不明显。提取时间进一步延长,发现得率反而略微降低,这可能是因为矢车菊-3-葡萄糖苷在长时间的热和光作用下容易被破坏所致。
2.4 响应面法优化实验条件
在以上单因素实验结果的基础上,采用Box-Behnken 三因素三水平实验设计,其实验结果见表2。根据所得实验结果,利用Design-Expert 7.0.0软件回归拟合实验数据,获得以下的三元二次回归模型。

图4 提取时间对矢车菊-3-葡萄糖苷得率的影响Fig.4 Effect of extraction time on extraction rate of cyanidin-3-glucoside

表2 Box-Behnken 实验结果Table 2 Results of Box-Behnken experiment

由表3 的方差分析结果可知,本实验所选用的模型极显著(p <0.001),方程失拟项不显著(p =0.0818 >0.05),且该模型决定系数R2=0.9983,表明回归方程的拟合程度较好,预测值和实测值之间具有高度的相关性,说明各因素值与响应值之间的关系可以用此模型来函数化,可以应用于杨梅渣中矢车菊-3-葡萄糖苷提取的理论预测。由F 检验可知,各因素的贡献率为:提取温度>提取时间>乙醇浓度。乙醇浓度和提取温度、乙醇浓度和提取时间、提取温度和时间之间存在着交互作用,如图5所示。
应用响应面法对回归模型进行分析,预测的最优工艺参数为:乙醇浓度53%,温度67℃,时间67min,响应面最优值为5.32mg/g。为验证响应面法所得结果的可靠性,在响应面法优化的最佳条件下进行3 次平行实验,矢车菊-3-葡萄糖苷得率为5.25mg/g,与预测值非常接近,说明响应值的实际测量值与回归模型预测值吻合度好。

图5 各因素交互作用对矢车菊-3-葡萄糖苷得率的影响规律Fig.5 Effect rules of interaction of factors on extraction rate of cyanidin-3-glucoside
3 结论
本文在单因素实验的基础上,采用Box-Behnken实验设计法对杨梅渣中矢车菊-3-葡萄糖苷的提取工艺进行了响应面优化。研究结果表明,乙醇浓度和提取温度、乙醇浓度和提取时间、提取温度和时间之间存在着交互作用;最佳工艺参数为:乙醇浓度53%,温度67℃,时间67min。经过验证实验可知,在最优提取工艺条件下,矢车菊-3-葡萄糖苷得率可达5.25mg/g,与回归模型的预测值相比,相对误差<1%,可为进一步的中试以及工业化制备提供理论基础。
[1]叶兴乾,陈健初,苏平.荸荠种杨梅的花色苷组分鉴定[J].浙江农业大学学报,1994,20(2),188-190.
[2]曾林钗,高洁,张瑞.矢车菊素-3-葡萄糖苷抑制体内外卵巢癌生长的作用[J].中国中药杂志,2012,37(11):1651-1654.
[3]Shih P H,Yeh C T,Yen G C.Effects of anthocyanidin on the inhibition of proliferation and induction of apoptosis in human gastric adenocarcinoma cells[J].Food and Chemical Toxicology,2005,43(10):1557-1566.

表3 回归模型的方差分析Table 3 Variance analysis of regressive model
[4]Meiers S,Kemény M,Weyand U,et al.The anthocyanidins cyanidin and delphinidin are potent inhibitors of the epidermal growth- factor receptor[J].Journal of Agricultural and Food Chemistry,2001,49(2):958-962.
[5]Zhou S Z,Lü Y,Chen J,Liu D,et al. Phenolics and antioxidant properties of bayberry(Myrica rubra Sieb.et Zucc.)pomace[J].Food Chemistry,2009,112:394-399.
[6]Fang Z X,Zhang M,Wang L X.HPLC-DAD-ESIMS analysis of phenolic compounds in bayberries(Myrica rubra Sieb.et Zucc.)[J].Food Chemistry,2007,100:845-852.

