磺酰脲受体的合成及阴离子识别性能*
瞿金清 万文 勇雪 苏铭健 严轶琛 刘瑞源
(1.华南理工大学化学与化工学院,广东 广州510640;2.南方医科大学药学院,广东广州510515)
阴离子在生物学、病理学和环境监测等领域都起着重要作用[1-3].许多阴离子半径大、电荷密度低、几何构型各异且溶剂化作用强,对介质pH值较为敏感,因此设计合成选择性好、灵敏度高的阴离子受体比较困难.近年来,阴离子受体的设计合成受到了极大的关注[4-5].比色和荧光阴离子受体能简便地通过“裸眼识别”定性鉴别阴离子,甚至能提供定量信息,是一类广受欢迎的受体[6-7].该类受体通常由结合阴离子的信号报告基团和识别基团两部分组成,两者直接相连或由连接臂连接.识别基团通过氢键作用和/或去质子化作用结合阴离子,使信号报告基团的吸收光谱或者荧光光谱发生变化,达到识别阴离子的目的.氢键具有良好的方向性和选择性,是识别基团键合阴离子的主要作用力之一.酰胺[8]、脲/硫脲[9-11]、吡咯[12]和酚羟基[13]等都可作为氢键供体,已广泛应用于阴离子受体设计和合成.磺酰脲同时含有磺酰基和脲基,磺酰基增强了脲基和阴离子的结合能力;但是,将磺酰脲应用于阴离子识别却鲜见报道.磺酰脲常见于高效除草剂和抗糖尿病等药物分子中[14-15].文中将磺酰脲用作阴离子识别基团,设计合成了一种新型的磺酰脲阴离子受体双-(4'-硝基苯基)磺酰脲,检测其对阴离子的裸眼识别能力;并通过紫外-可见分光光度滴定法进一步测定了其与阴离子的结合能力.
1 实验
1.1 仪器与试剂
DMX 400-MHz型核磁共振仪,美国布鲁克公司生产;UV-2450型紫外-可见吸收光谱仪(1cm石英液池),日本岛津公司生产;FTIR-8100型红外光谱仪(KBr压片),日本岛津公司生产;Vario EL III元素分析仪,德国Elementar公司生产.
4-硝基苯异氰酸酯、磺酰胺、四正丁基硫酸氢铵、四正丁基醋酸铵和四正丁基硝酸铵,均为分析纯,百灵威科技有限公司生产;四正丁基氟化铵、四正丁基氯化铵和四正丁基溴化铵,均为分析纯,阿达玛斯试剂有限公司生产;N,N-二甲基甲酰胺(DMF)、二氯甲烷、乙酸乙酯和正己烷,均为分析纯,广州市金华大化学试剂有限公司生产.以上试剂均未经进一步纯化而直接使用.
1.2 受体分子合成与表征
室温下向100 mL烧瓶中加入4-硝基苯异氰酸酯(4.92 g,30 mmol)、磺酰胺(1.44 g,15 mmol)和50mLCH2Cl2,搅拌24 h.将所得二氯甲烷溶液依次用1mol/L的盐酸、饱和NaHCO3水溶液和饱和NaCl水溶液洗涤3次,有机层在无水MgSO4中干燥,然后旋蒸除去溶剂.残余物用正己烷与乙酸乙酯体积比为1∶2的混合物作洗脱剂经硅胶柱层析分离纯化,重结晶得到黄色固体4.46g,收率70%.合成路线如图1所示.

图1 受体分子的合成路线Fig.1 Synthetic route of the receptor
C14H12O8N6S元素分析得C、H、N的计算值分别为 39.59%(质量分数,余同)、2.89%、19.75%;实测值分别为 39.63%、2.85%、19.80%.IR(KBr),波数(cm-1):3369,3340,3231,2886,1736,1619,1598,1 578,1 554,1 500,1 331,1 302,1 181,849,752.1H NMR(CD3COCD3-d6)δ:4.05(s,2H,NH),7.82(m,4H,Ar),8.20(d,4H,Ar),11.65(s,2H,NH);13C NMR(CD3COCD3-d6)δ:120.9,124.5,142.9,144.0,188.5.
1.3 紫外-可见吸收光谱分析
首先配制2 mmol/L的受体的DMF溶液,然后分别配制 NO-3、Br-、Cl-、HSO-4、CH3CO-2、F-浓度为100mmol/L的四正丁基铵盐的DMF溶液,备用.
分别移取0.5mL受体的DMF溶液和0.5mL阴离子四正丁基铵盐的DMF溶液于10 mL容量瓶中,定容,使阴离子浓度为受体浓度的50倍,混合均匀后静置,于25℃下测其紫外-可见吸收光谱(DMF作参比).
分别移取0.5mL受体的DMF溶液和不同体积的阴离子四丁基铵盐的DMF溶液于10 mL容量瓶中定容,得到受体浓度恒定、阴离子浓度不同的溶液,测其紫外-可见吸收光谱,然后测量计算阴离子与受体浓度比及其对应的吸光度,并作峰值曲线.
利用Jobs法测受体分子与阴离子的配位比.使受体分子和客体分子的总浓度保持为700 mmol/L,分别改变受体与客体的摩尔分数,以未加客体的受体溶液作参比溶液,于25℃下测其测其紫外-可见吸收光谱.
2 结果与讨论
2.1 受体对不同阴离子的识别能力
受体的DMF溶液颜色及加入不同阴离子后的颜色如图2(a)所示.由图2(a)可见,受体的DMF溶液为无色;加入F-后溶液变为棕黄色;加入CH3后溶液变为淡黄色,颜色变化不明显;而加入、Br-、Cl-、后溶液颜色几乎没有变化.受体显示出对F-的裸眼识别能力.
利用紫外-可见分光光度法进一步测试了受体对 F-、、Br-、Cl-、CH3的选择性识别性质,结果如图2(b)所示.由图2(b)可见,加入F-后,受体溶液的吸收光谱的最大吸收峰从351 nm红移到 480 nm;而加入、Br-、Cl-、HSO4-和CH3后,受体溶液的吸收光谱仅仅发生微小红移.由此可见,受体对F-显示出良好的选择性.

图2 受体的DMF溶液加入不同的阴离子后的颜色变化及紫外-可见吸收光谱Fig.2 Color change and UV-vis absorption spectra of the DMF solution of receptor after addition of different anions
2.2 受体与阴离子的结合能力
受体的DMF溶液中加入不同浓度的F-时其紫外-可见吸收光谱如图3所示(0~40.0eq表示F-浓度是受体浓度的0~40倍).由图3可见,随着F-浓度的增大,受体溶液在351nm处的吸光度逐渐减小,吸收峰发生红移,同时在480 nm处出现一组新的吸收峰,此峰为受体分子与阴离子形成的配合物的吸收峰,峰值相应增大.
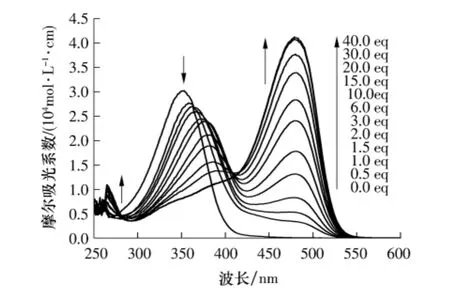
图3 受体的DMF溶液中加入不同浓度F-的紫外-可见吸收光谱Fig.3 UV-vis absorption spectra of DMF solutions of the receptor after addition of different concentrations of F-
根据阴离子配合物最大吸收峰的峰值随阴离子浓度的变化曲线,拟合得到加入不同阴离子后受体的DMF溶液的最大吸收峰的峰值曲线,如图4所示.由图4可知,受体与F-形成的配合物对紫外光谱较其他阴离子更为敏感,因而可说明受体对F-有较高的灵敏度和较强的识别能力.经最小二乘法曲线拟合程序Reactlab Equlibria计算得到受体与阴离子的配合常数lgKa,见表1.

图4 加入不同阴离子后受体的DMF溶液的峰值曲线Fig.4 Peak value curves of DMF solution of the receptor after addition of different anions

表1 受体分子与不同阴离子的结合常数lgK1)aTable 1 Binding constant lgKaof the receptor with different anions
2.3 识别机理探讨
利用Jobs法检测受体分子和F-的结合模式,结果如图5所示.从图5可看出,吸光度差值最大值对应的受体摩尔分数为0.33,说明受体分子与F-形成摩尔比1∶2的配合物.

图5 受体分子与F-的Jobs曲线Fig.5 Jobs plot of receptor and F-
磺酰脲是优良的氢键供体,可以和阴离子结合形成氢键配合物.为探讨受体分子和阴离子之间的氢键作用,测定了甲醇对受体分子和F-配合物的紫外光吸收光谱的影响,结果如图6所示.由图6可见,含有受体分子和F-的DMF溶液在480 nm处有较强的吸收峰;添加甲醇后,480 nm处的吸收峰消失,而在351 nm处出现新的吸收峰,其结果和未加入F-的受体DMF溶液相近.这是由于甲醇分子与阴离子竞争受体分子中氢键的结合位点所致,它破坏了受体和F-间形成的氢键.这一结果揭示了阴离子与受体分子间的氢键作用本质.

图6 甲醇对受体分子和F-配合物的紫外光吸收光谱的影响Fig.6 Influence of methyl alcohol on the absorption spectra of complex of receptor and F-
3 结论
利用简便的方法合成了一种新型的磺酰脲阴离子受体,并考察了其对一价阴离子的识别能力.结果表明,F-的引入使受体溶液变为棕黄色,CH3的引入使受体溶液变为淡黄色,实现了裸眼检测,而引入其他阴离子(如、Br-、Cl-、)受体溶液颜色无明显的变化;受体与F-形成的配合物相比于受体与其他阴离子形成的配合物对紫外光谱更为敏感,受体对F-有较高的灵敏度和较强的识别能力;受体分子与F-通过氢键结合形成摩尔比1∶2的配合物.
[1]Caltagirone C,Gale P A.Anion receptor chemistry:highlights from 2007 [J].Chemical Society Reviews,2009,38:520-563.
[2]Ayoob S,Gupta A K.Fluoride in drinking water:a review on the status and stress effects[J].Critical Reviews Environmental Science Technology,2006,36(6):433-487.
[3]Bassin E B,Wypij D,Davis R B,et al.Age-specific fluoride exposure in drinking water and osteosarcoma(United States)[J].Cancer Causes and Control,2006,17(4):421-428.
[4]Cametti M,Rissanen K.Recognition and sensing of fluoride anion [J].Chemical Communications,2009(20):2809-2829.
[5]Duke R M,Veale E B,Pfeffer F M,et al.Colorimetric and fluorescent anion sensors:an overview of recent developments in the use of 1,8-naphthalimide-based chemosensors[J].Chemical Society Reviews,2010,39(10):3936-3953.
[6]Gunnlaugsson T,Glynn M,Tocci G M,et al.Anion recognition and sensing in organic and aqueous media using luminescent and colorimetric sensors [J].Coordination Chemistry Reviews,2006,250(23/24):3094-3117.
[7]Kubo Y,Yamamoto M,Ikeda M,et al.A colorimetric and ratiometric fluorescent chemosensor with three emission changes:fluoride ion sensing by a triarylborane porphyrin conjugate[J].Angewandte Chemie International Edition,2003,42(18):2036-2040.
[8]Piatek P,Jurczak J.A selective colorimetric anion sensor based on an amide group containing macrocycle[J].Chemical Communications,2002(20):2450-2451.
[9]Cho E J,Moon J W,Ko S W,et al.A new fluoride selective fluorescent as well as chromogenic chemosensor containing a naphthalene urea deriva-tive[J].Journal of the American Chemical Society,2003,125(41):12376-12377.
[10]Bondy C R,Gale P,Loeb S J.Metal?organic anion receptors:arranging urea hydrogen-bond donors to encapsulate sulfate ions[J].Journal of the American Chemical Society,2004,126(16):5030-5031.
[11]Kwon J Y,Singh N J,Kim H N,etal.Fluorescent GTP-sensing in aqueous solution of physiological pH [J].Journal of the American Chemical Society,2004,126(29):8892-8893.
[12]Sessler J L,Camiolo S,Gale P A.Pyrrolic and polypyrrolic anion binding agents[J].Coordination Chemistry Reviews,2003,240(1/2):17-55.
[13]Devaraj S,Saravanakumar D,Kandaswamy M.Dual chemosensing properties of new anthraquinone-based receptors toward fluoride ions[J].Tetrahedron Letters,2007,48(17):3077-3081.
[14]Kang S,Chang N,Pan C P,etal.Development of a method for the simultaneous determination of six sulfonylurea herbicides in wheat,rice,and corn by liquid chromatography tandem mass spectrometry[J].Journal of Agricultural Food Chemistry,2011,59(18):9776-9781.
[15]Zwaveling-Soonawala N,Hagebeuk E E,Slingerland A S,et al.Successful transfer to sulfonylurea therapy in an infant with developmental delay,epilepsy and neonatal diabetes(DEND)syndrome and a novel ABCC8 gene mutation [J].Diabetologia,2011,54(2):469-471.
[16]Pizzoli G,Lobello M G,Carlotti B,et al.Acid base properties of the N3 ruthenium(II)solar cell sensitizer:a combined experimental and computational analysis[J].Dalton Transactions,2012,41:11841-11848.

