不同程度奶牛乳腺炎的相关性试验
程艳艳,张志刚,刘本君,高 利
(东北农业大学动物医学学院,黑龙江 哈尔滨150030)
奶牛乳房炎通过影响牛奶的产出率和质量对奶业造成巨大的经济损失。乳房炎是源于细菌感染或挤奶方式不正确造成机体产生免疫应答[1],有报道称,机体的免疫反应会导致机体氧自由基的产生增多[2]及许多相关因子的变化[3-4]。自由基在体内有很强的氧化反应能力,一旦体内的自由基产生过多,易对蛋白质、脂质和核酸等产生伤害,从而引起机体的氧化应激和脂质过氧化[5]。过氧化物酶被认为是细胞内抵御氧化损伤的第一道防线,因此它的活性直接体现了机体抗氧化能力[6]。但是目前关于不同程度奶牛乳房炎和奶牛抗氧化能力关系的报道非常有限,本试验通过研究二者的相关性并探讨所测定的指标是否可以作为判定乳腺损伤的依据。
1 材料与方法
1.1 试验动物分组 利用乳汁体细胞计数仪检测法对40头试验奶牛进行分组,分为4组:C组(SCC<5×105个/mL)、Ⅰ组(5×105<SCC<1.5×106个/mL)、Ⅱ组(1.5×106<SCC<5×106个/mL)和Ⅲ组(SCC>5×106个/mL)。
1.2 血样的采集 选择阿城区某奶牛示范基地的荷斯坦奶牛40头(年龄和泌乳期相近)。颈静脉采集C组、Ⅰ组、Ⅱ组、Ⅲ组各10头奶牛的血液,采样前消毒取血部位,对每头牛约取15mL血液。对采集血样的奶牛和试管进行号码标记,将采集的血样室温下静止。
1.3 乳样的采集 采集C组、Ⅰ组、Ⅱ组、Ⅲ组各10头奶牛的乳汁,采样前对乳区进行清洗,然后用70%酒精消毒乳区,弃掉头2把乳汁,进行全天采样,从早上6点开始,每间隔5h进行取样,取样3次,每次20mL,最后混入无菌奶瓶中。将采集的乳样放到有冰块的泡沫箱中,将乳样带回实验室检测。
1.4 血样的处理及测定 颈静脉采集血液,在室温下自然凝固1~2h,冰浴30min,然后3 000r/min离心10min,分离血清,4℃保存,待测。样品采用南京建成生物工程研究所超氧化物歧化酶 (superoxide dismutase,SOD)、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)和丙二醛 (malonal-dehyde,MDA)试剂盒进行测定。
1.5 乳样的处理及测定 将乳样3 000r/min离心5min,除去上层乳脂,然后于16 000r/min高速离心机中离心10min,收集上清,4℃保存,待测。如检测时间较长,要将样品置于-80℃冰箱中保存备用。样品采用南京建成生物工程研究所SOD、GSH-Px和MDA的试剂盒进行测定。
1.6 数据分析 利用软件SPSS 13.0软件统计分析进行分析处理,数据用±SD表示。
2 结果
2.1 血清中SOD、GSH-Px活性及MDA水平 见图1~3。

图1 血清各组中SOD活性

图2 血清各组中GSH-Px活性
由图1、2可看出,本试验中Ⅰ、Ⅱ、ⅲ组相比于对照组SOD、GSH-Px酶活性依次降低,且P<0.05。由图3可得出,Ⅰ、Ⅱ、Ⅲ组相比于对照组MDA水平依次升高,且P<0.05。

图3 血清各组中MDA含量
2.2 乳清中SOD、GSH-Px活性及MDA水平 见图4~6。

图4 乳清各组中SOD含量
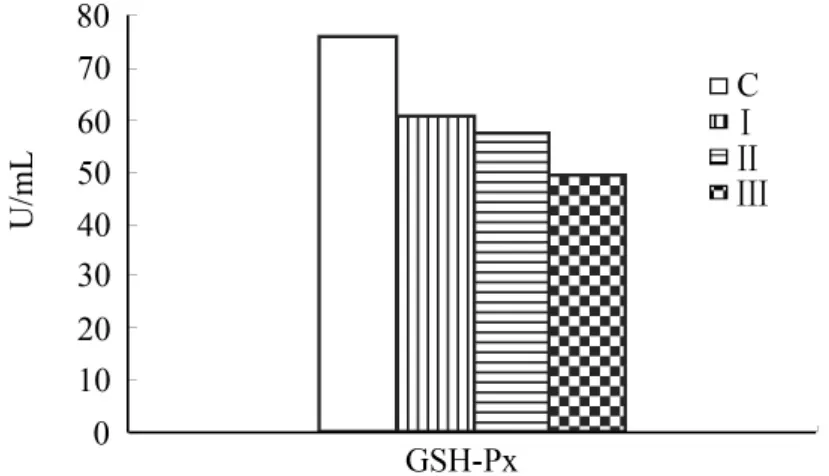
图5 乳清各组中GSH-Px含量
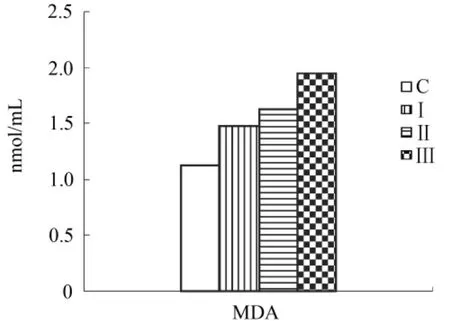
图6 乳清各组中MDA含量
由图4、5可看出,与对照组相比,Ⅰ、Ⅱ、Ⅲ组SOD、GSH-Px酶活性依次降低(P<0.05)。图6显示,Ⅰ、Ⅱ、Ⅲ组相比于对照组MDA水平依次升高(P<0.05)。
3 讨论
在试验中奶牛患有乳腺炎时,血清及乳清中SOD、GSH-Px的活性显著低于对照组,且随着炎症程度的加重,SOD、GSH-Px的活性也逐渐降低,说明奶牛在患有乳腺炎时,机体内抗氧化酶活力显著降低。这主要是因为奶牛发生乳腺炎时,体内大量的自由基异常生成并超过了机体的清除能力,于是机体内的SOD和GSH-Px被大量消耗[7]。
MDA水平的增加可能源于自由基产生过多,SOD和GPX-Px酶活性降低,致使机体产生氧化损伤,细胞内的自由基受内源性的过氧化物酶如SOD和GPX-Px等控制,然而自由基产生突破抗氧化防线,细胞内则发生氧化应激,MDA是氧化应激引起的脂质过氧化的产物[8]。本试验结果提示,奶牛在患有乳腺炎时过氧化物和自由基参与了乳腺炎的发生过程,并且使机体组织细胞受到氧化损伤。
奶牛发生乳腺炎时,动物机体和乳腺组织均产生了过多的自由基,机体的总抗氧化能力下降,抗氧化系统活性物质严重不足,已经不能有效地清除体内过多的自由基,导致乳腺上皮细胞的细胞膜无法有效防御自由基的攻击,以至于过多的自由基使乳腺上皮细胞细胞膜的通透性异常,从而引起乳腺细胞分泌异常乳。因此,检测血液中和乳汁中SOD和GSH-Px酶活性和MDA的含量变化可以指示乳房炎的严重程度,这些指标也可以作为判定乳腺炎奶牛乳腺损伤的依据。
[1] 刘春元,铁焕录.奶山羊乳房炎的综合防治[J].中国兽医杂志,2012,48(1):37-38.
[2] Bouwstra R J,Nielen M,Newbold J R,etal.Vitamin E supplementation during the dry period in dairy cattle.Part II:Oxidative stress following vitamin E supplementation may increase clinical mastitis incidence postpartum [J].J Dairy Sci,2010,93:5696-5706.
[3] 李晓蕾,张宇,刘本军,等.不同程度乳腺炎血清中相关细胞因子的试验[J].中国兽医杂志,2011,47(10):7-8.
[4] 张宇,王洪伟,魏成威,等.不同乳腺炎乳中部分相关酶变化的试验[J].中国兽医杂志,2011,47(3):23-25.
[5] Kaufmann J A,Bickford P C,Taglialatela G.Free Radical-Dependent Changes in Constitutive Nuclear Factor Kappa B in the Aged Hippocampus[J].Neuroreport,2002,13:1917-1920.
[6] Jomova K,Jenisova Z,Feszterova M,etal.Arsenic:toxicity,oxidative stress and human disease[J].J Appl Toxicol,2011,31:95-107.
[7] Mukherjee R.Selenium and vitamin E increases polymorphonuclear cell phagocytosis and antioxidant levels during acute mastitis in riverine buffaloes[J].Vet Res Commun,2008,32:305-313
[8] Halliwell B.Free radicals and antioxidants:apersonal view[J].Nutr Rev,1994,52:253-267.

