价电子对互斥理论与电价理论相结合判定分子的共轭类型*
吴贵升 袁联群
(上海应用技术学院化学与环境工程学院 上海 201418 )
共轭效应为有机化学与结构化学的重要理论之一,可以有效分析具有共轭效应化合物分子、离子或自由基的稳定性,酸碱性以及反应活性,同时,也可以解释该类分子的颜色效应[1-2]。通常只含碳原子化合物的共轭效应比较简单,但是对于一些包含杂原子并且共轭π键不是特别明显的有机分子或离子,共轭效应判定较为困难,这也是学生学习的难点之一。
分子轨道理论、价键理论和配位场理论是近代研究化学键的3大基本理论,其中分子轨道理论能解释许多其他理论不能解释的实验事实,它认为原子轨道依据一定的规则线性组合成一组全新的分子轨道,偏重于对整个分子进行分析[1-2]。价键理论则偏重于对成键原子间的价电子对进行分析,其中杂化轨道理论和价电子对互斥理论又为价键理论的补充内容,关于二者的关联和互补已有不少文献阐述,其基本出发点都是基于分子中中心原子的价电子对采取何种构型使分子能量最低[3-8]。但是利用分子轨道理论和价键理论相结合来讨论分子化学键则鲜有报道。
在分析共轭π键时,其先决条件是分子中所有参加共轭的原子必须在同一个平面上,其次是π电子数小于参加成键的p轨道的2倍[1-2]。因此判定哪些原子在同一平面,并且确定共轭电子数为分析共轭π键形成的两大重要步骤,但仅通过分子轨道理论有时较难处理。本文通过价电子互斥理论,先确定中心原子的电子对结构,并得出哪些原子处于同一平面;然后根据杂化轨道理论得出中心原子的杂化类型,排除σ键,仅分析π键,并根据价键理论确定参加共轭的原子对共轭π键所贡献的电子数,最终达到确定分子共轭类型的目的。
1 价电子对互斥(VSEPR) 理论要点
VSEPR理论认为[1-2]分子的几何构型由中心离子或原子周围的价电子对决定,即总是采取电子对排斥作用最小的几何结构,从而保持分子的能量最低。价电子对包括成键电子对和孤对电子,当知道成对电子和孤对电子的数目时,可以很方便地判定分子的构型。
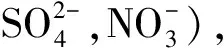
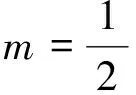



根据总电子对的数目,可以初步判定总电子对的空间构型以及中心原子或离子的杂化类型,与本文相关的类型见表1。

表1 总电子对的数目、空间构型以及中心原子杂化类型之间的关系
2 化合物共轭类型的判别
2.1 判别规则
对于一个共轭类型的化合物,其共轭类型可以根据以下步骤进行判别:
1) 确定中心原子或离子,化合物中不止包含一个中心离子,要逐一判别;
2) 根据VSEPR理论,求其总电子对数,判定杂化类型,并确定其σ键以及孤对电子;
3) 确定摒除杂化轨道所用的p轨道,确定其所剩余的p轨道(pz或py和pz,简称p剩)的电子数;
4) 根据价键理论,分析中心原子或离子相连的原子的p剩电子数,并确定其共轭中心数目;
5) 确保中心原子的σ键的成键键电子对数和孤对电子数目为2的前提下,体系所剩余的电子均放到共轭π键上,最终确定共轭电子数。
2.2 实例分析
2.2.1 中心离子仅包含碳原子的体系
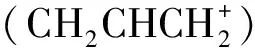
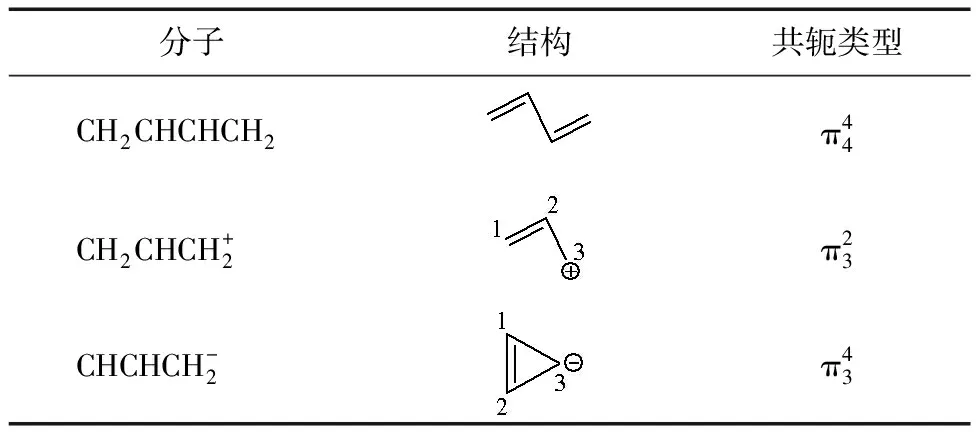
表2 碳原子体系的分子结构与共轭类型
2.2.2 含杂原子的体系

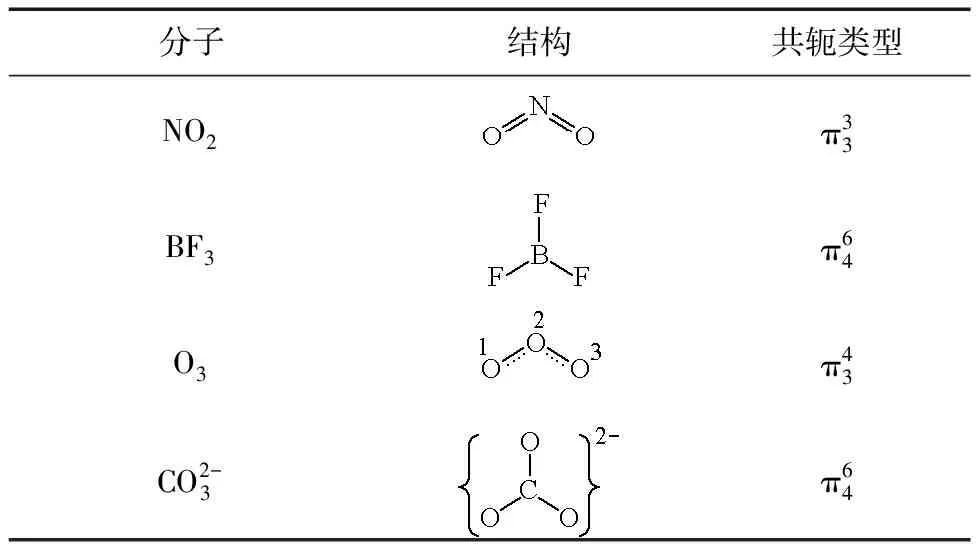
表3 含杂原子体系的分子结构与共轭类型
2.2.3 含有多个共轭体系
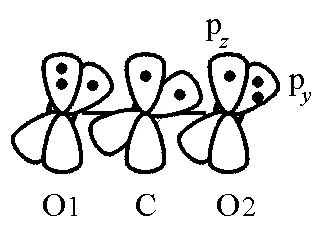
图1 CO2的分子结构以及共轭类型
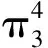
3 结论
采用价电子互斥理论与杂化轨道理论相结合的方法,首先确定中心原子或离子的杂化类型以及总电子对的结构,判定哪些原子在同一平面;然后根据杂化轨道理论得出中心原子的杂化类型,然后摒除σ键,仅分析π键,并根据价键理论,确定参加共轭的原子对共轭π键所贡献的电子数,最终达到确定分子共轭类型的目的。虽然价键理论和分子轨道理论是两种不同的理论,但是两者结合可以简化对分子,尤其是含有杂原子分子共轭类型的判别。
参 考 文 献
[1] 夏少武.简明结构化学教程.第2版.北京:化学工业出版社,2008
[2] 潘道凯,赵成大,郑载兴.物质结构.第2版.北京:高等教育出版社,1987
[3] 冯军.中学化学教学参考,2008(Z1):41
[4] 朱斌.四川师范学院学报(自然科学版),2003,24(2):240
[5] 邓玉良.武警学院学报,2007,23(2):86
[6] 王福民.渭南师范学院学报,2002,17(5):29
[7] 席改卿.邯郸师专学报,2000,10(3):46
[8] 张文广,王祖浩.化学世界,2008(3):189
[9] 陈益.化学教学,2007(6):73

