葡萄糖酸钠的分光光度法测定*
翁艳军,林凯,辛嘉英*
(1.哈药集团制药总厂,黑龙江哈尔滨150086;2.哈尔滨商业大学食品科学与工程重点实验室,黑龙江哈尔滨150076)
分析测试
葡萄糖酸钠的分光光度法测定*
翁艳军1,林凯2,辛嘉英2*
(1.哈药集团制药总厂,黑龙江哈尔滨150086;2.哈尔滨商业大学食品科学与工程重点实验室,黑龙江哈尔滨150076)
利用葡萄糖酸钠在强酸性条件下形成内酯,通过羟胺-三氯化铁显色法生成红棕色异羟肟酸-Fe3+络合物,进行分光光度检测。建立标准曲线,其线性方程为y=113.0833χ+0.1162,R2=0.9999,检测波长为500nm,在1×10-3~9×10-3mol·L-1范围内具有良好的线性关系,平均加标回收率为99.79%,并且该方法能够检测Au/γ-Al2O3催化葡萄糖氧化反应液中葡萄糖酸钠的含量。
葡萄糖酸钠;分光光度法;羟胺-三氯化铁法
葡萄糖酸及其盐是葡萄糖氧化的主要产物,因其具有良好的生物相容性和生物可降解性,已广泛应用于医药、食品、造纸和混凝土等工业[1]。葡萄糖酸是机体代谢中间产物,对肠道有益菌群双歧杆菌具有增值作用;葡萄糖酸钠对维持细胞渗透压,调节人体内酸碱平衡、恢复神经正常功能具有重要作用;其钙盐在医药上用于消除过敏、补充钙质;葡萄糖酸锌能够改善生长发育迟缓、营养不良等症状。目前,生物发酵法是工业化生产葡萄糖酸的主要方式。但随着负载型金催化剂在催化葡萄糖氧化方面研究的不断深入,探索葡萄糖酸高效合成的新方法已引起人们的重视[2]。本课题组已在利用甲烷氧化菌素(methanobactin,Mb)还原法制备纳米金方面进行了初步探索[3,4]。由于葡萄糖酸不具有灵敏的紫外吸收,通常需要对其进行衍生化等操作,并且检测仪器昂贵。羟胺-三氯化铁法作为检测具有酰胺键和内酯类化合物已得到广泛应用[5-9]。该方法具有操作方法简便、检测结果重复性和灵敏度良好等优点。其反应机理见图1。

图1 羟胺-三氯化铁法检测葡萄糖酸钠反应机理[10]Fig.1 Mechanism for the determination of sodium gluconate by the hydroxylamine-ferric chloridemethod
本文建立了利用羟胺-三氯化铁法检测葡萄糖酸钠的方法,考察了测定过程中的影响因素,并应用于Au/γ-Al2O3催化葡萄糖氧化反应液中葡萄糖酸钠含量的测定。
1 实验部分
1.1 仪器及主要试剂
UV-2550紫外-可见分光光度计(岛津);电热鼓风干燥箱(上海一恒科学仪器有限公司);箱式电阻炉(上海跃进医疗器械有限公司);油浴锅(天津市欧诺仪器仪表有限公司)。
葡萄糖(A.R.天津市天力化学试剂有限公司);葡萄糖酸钠(G.R.天津市科密欧化学试剂有限公司);盐酸羟胺(A.R.天津市福晨化学试剂厂);NaOH(A. R.天津市光复科技发展有限公司);FeCl·36H2O(A. R.天津市天力化学试剂有限公司)。
1.2 实验方法
1.2.1 试剂配制
标准溶液用葡萄糖酸钠配制1×10-3、3×10-3、5×10-3、7×10-3、9×10-3mol·L-1的标准溶液,并用4 mol·L-1HCl调pH值至1.5。
羟胺碱试剂4mol·L-1盐酸羟胺和4mol·L-1NaOH等体积混合,并用适量以上溶液调节pH值至8,该试剂应现用现配。
FeCl3试剂称取10g FeCl·36H2O,用0.1mol·L-1HCl溶液定容至100mL,即为0.37mo·lL-1FeCl3试剂。1.2.2操作步骤向10mL带有磨口塞的试管中加入1mL 1×10-3~9×10-3mol·L-1葡萄糖酸钠标准溶液,调节溶液pH值为1.5,置于沸水浴中加热30min,冷却至室温,依次加入2mL羟胺碱试剂,1m L 4mol·L-1HCl和1m LFeCl3试剂显色,迅速振摇去除气泡。空白组用1mL去离子水代替试样,其余试剂及用量不变。用1cm石英比色皿以空白组为对照,进行可见光谱扫描,并在500nm处测定吸光度(OD500)。测定工作需在10min内完成。
2 结果与讨论
2.1 可见光谱扫描和标准曲线的绘制
按1.2方法对葡萄糖酸钠标准溶液进行可见光谱扫描。结果见图2。产生的红棕色异羟肟酸-Fe3+络合物在500nm附近有最大吸收峰。因此,本实验选取500nm为测定波长,并绘制葡萄糖酸钠标准曲线。
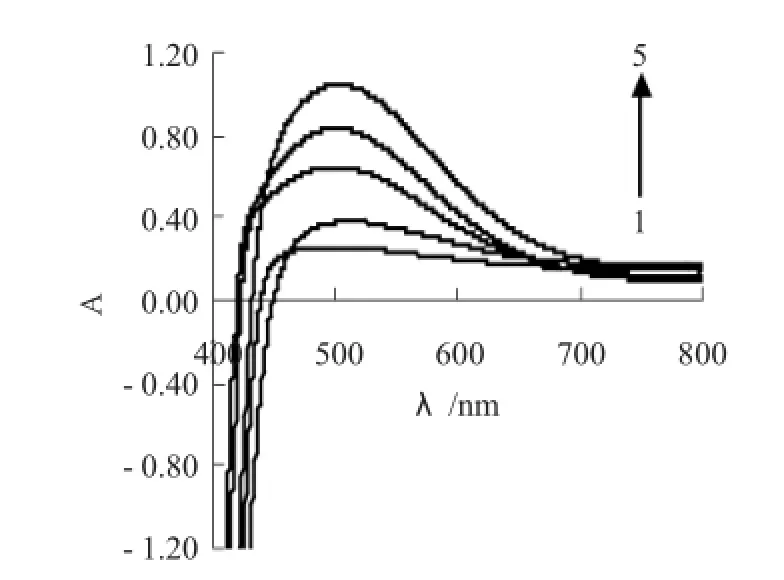
图2 标准曲线吸收光谱Fig.2 Standard curve of absorption spectrum
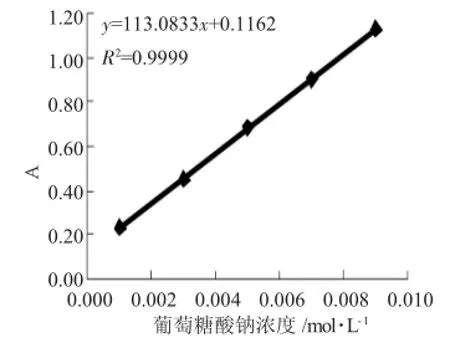
图3 葡萄糖酸钠标准曲线Fig.3 Standard curve of sodium gluconate
由图3可知,葡萄糖酸钠标准溶液浓度在1× 10-3~9×10-3mol·L-1范围内与OD500呈现良好的线性关系。线性方程为:y=113.0833χ+0.1162,R2=0.9999。

2.2 显色时间对测定结果的影响
葡萄糖酸钠标准溶液按实验方法显色后,放置不同时间,测定其对吸光度影响。
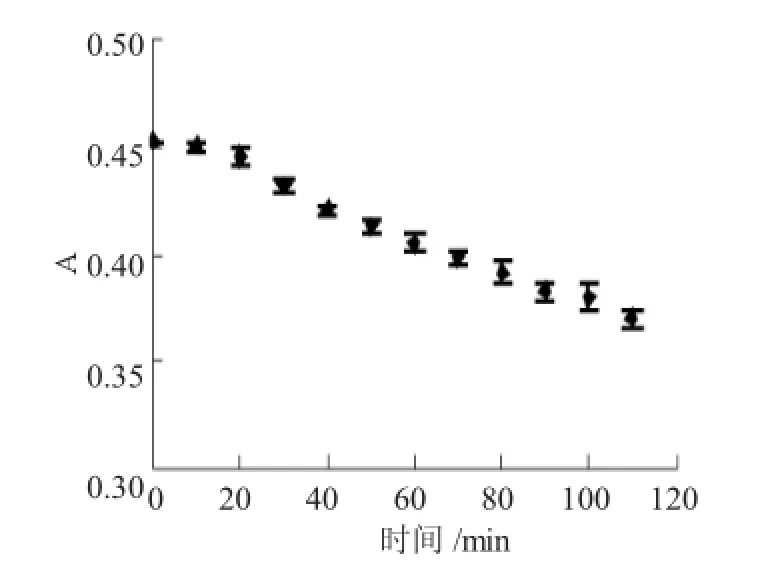
图4 显色时间对测定结果的影响Fig.4 Effectof time on absorbance
由图4可知,充分振摇去除气泡后,随时间的增加,棕红色铁络合物吸光度逐渐减小,表明异羟肟酸-Fe3+络合物稳定性较差。因此,测定时间应控制在样品显色后10min内完成。若大批进行样品分析时,应分批加入FeCl3试剂进行显色,减小误差[9]。
2.3 葡萄糖对测定结果的影响
在Au/γ-Al2O3催化葡萄糖氧化过程中,催化反应液中会残存未反应的葡萄糖。由于葡萄糖也会发生类似的显色反应,从而影响测定结果[10]。为考察葡萄糖对测定结果是否存在干扰,本文研究了在3× 10-3mol·L-1葡萄糖酸钠标准溶液中加入3×10-3、6× 10-3、9×10-3、12×10-3mol·L-1的葡萄糖,测定葡萄糖酸钠的含量,其结果见表1。

表1 葡萄糖对葡萄糖酸钠测定的影响Tab.1 Effectof glucose on the determination of sodium gluconate
由表1可知,在葡萄糖酸钠浓度4倍量范围内,葡萄糖对测定结果影响不大,因此,可用于催化反应液中葡萄糖酸钠含量的测定。
2.4 催化反应液中葡萄糖酸钠的测定
2.4.1 催化剂的制备及反应过程γ-Al2O3在马弗炉中焙烧(500℃)处理5h后,置于干燥器内冷却至室温。将焙烧处理过的γ-Al2O3在HAuCl4中浸渍1h,置于鼓风干燥箱(110℃)内烘干,制得Au负载量为0.5%的Au3+/γ-Al2O3。然后向Au3+/γ-Al2O3加入Mb溶液(mb∶Au3+=10∶1(V/V)),置于30℃恒温摇床振荡10h[3]。原位还原后用去离子水洗涤催化剂去除Cl-1,直至向滤液中滴加AgNO3无沉淀产生,50℃烘干催化剂,500℃焙烧活化催化剂2h,制得Au/γ-Al2O3催化剂[10]。
向三口烧瓶内加入葡萄糖12mmol,调整溶液pH值至9,加入制备的Au/γ-Al2O3催化剂500mg,分批加入H2O248mmol,反应温度50℃,磁力搅拌反应24h。
2.4.2 回收率实验反应结束后将Au/γ-Al2O3催化氧化制得的葡萄糖酸钠催化反应液离心,取上层清液并进行适当稀释,按照1.2所述实验方法显色后,进行吸收光谱扫描,并测定样品加标回收率。

图5 催化反应液中葡萄糖酸钠吸收光谱Fig.5 Absorption spectrum of sodium gluconate in catalytic reaction solution(1.control group 2.experimental group)
由图5可知,用该方法检测催化反应液中葡萄糖酸钠时,在500nm处出现异羟肟酸-Fe3+络合物吸收峰。通过4批次加标回收实验发现(表2),其平均加标回收率为99.79%,说明该方法能够用于检测mb原位还原制备Au/γ-Al2O3催化葡萄糖氧化反应液中葡萄糖酸钠含量。
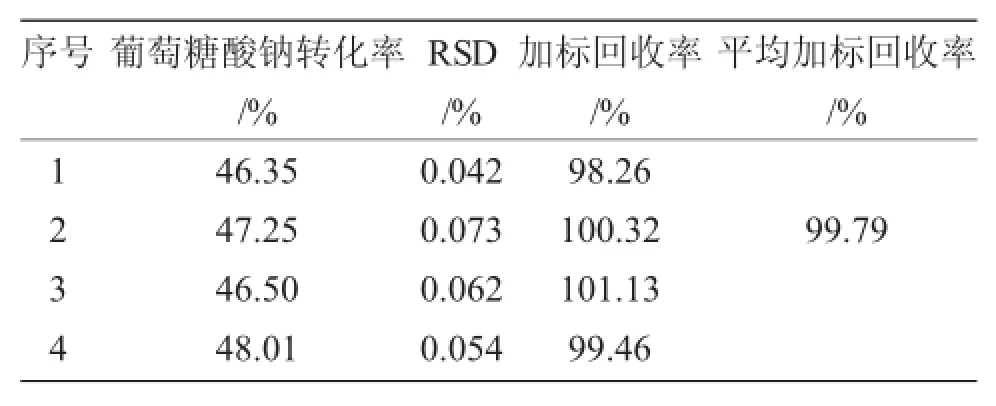
表2 反应催化液中葡萄糖酸酸钠的测定及回收率Tab.2 Determination of sodium gluconate in catalytic reaction solution and recoveries of themeasured results
3 结论
(1)葡萄糖酸在酸性条件下形成内酯,通过羟胺-三氯化铁显色法生成红棕色异羟肟酸-Fe3+络合物,建立了葡萄糖酸钠分光光度检测法。实验证明,在葡萄糖酸钠浓度为1×10-3~9×10-3mol·L-1范围内,标准曲线具有良好的线性范围。实验发现,异羟肟酸-Fe3+络合物稳定相较差,应在显色后10min内进行测定。同时考察了葡萄糖对测定反映的影响,发现在少于或等于4倍葡萄糖酸钠范围内,葡萄糖对测定结果影响不大。
(2)本实验成功将羟胺-三氯化铁法应用于检测Au/γ-Al2O3催化反应液中葡萄糖酸酸钠含量,平均加标回收率为99.79%。
[1]Delidovich IV,Moroz B L,Taran OP,et al.Aerobic selective oxi-dation ofglucose to gluconate catalyzed by Au/Al2O3and Au/C:impact of the mass-transfer processes on the overall kinetics[J]. Chemical Engineering Journal,2012,223(1):921-931.
[2]林凯,辛嘉英,陈丹丹,等.负载型纳米金催化葡萄糖氧化研究进展[J].分子催化,2014,28(1):1-7.
[3]Xin J,Cheng D,Zhang L,et al.Methanobactin-mediated one-step synthesis ofgold nanoparticles[J].International journal ofmolecular sciences,2013,14(11):21676-21688.
[4]张铁男,辛嘉英,张秀凤,等.甲烷氧化菌素催化纳米金合成[J].分子催化,2013,27(2):192-197.
[5]邹路易,肖静静,顾文秀,等.催化反应液中氨基葡萄糖酸的光度法测定[J].现代化工,2011,31(11):93-95.
[6]毕小健.分光光度法测定大气中的己内酰胺[J].山西化工,2007, 27(3):41-43.
[7]彭彦峰,吴兆亮,李英杰,等.分光光度法测定微生物发酵液中D-核糖浓度及其机理[J].分析化学,2002,(8).
[8]李玉萍,范衍琼.改良羟胺-三氯化铁法测定己内酰胺中毒物[J].中国职业医学,2001,28(6):44-45.
[9]LuoW,Zhu C,Su S,et al.Self-catalyzed,self-limiting growth of glucose oxidase-mimickinggold nanoparticles[J].ACSnano,2010, 4(12):7451-7458.
[10]Rakitzis E T,Papandreou P.Reactivity of 6-phosphogluconolactonewith hydroxylamine:the possible involvementof glucose-6-phosphate dehydrogenase in endogenous glycation reactions[J]. Chemico-biological interactions,1998,113(3):205-216.
[11]1996W ST.中华人民共和国卫生行业标准全血胆碱酯酶活性的分光光度测定方法羟胺三氯化铁法[S].
[12]Huang J,Liu C,Sun D,et al.Biosynthesized gold nanoparticles supported over TS-1 toward efficient catalyst for epoxidation of styrene[J].Chemical Engineering Journal,2014,235:215-223.
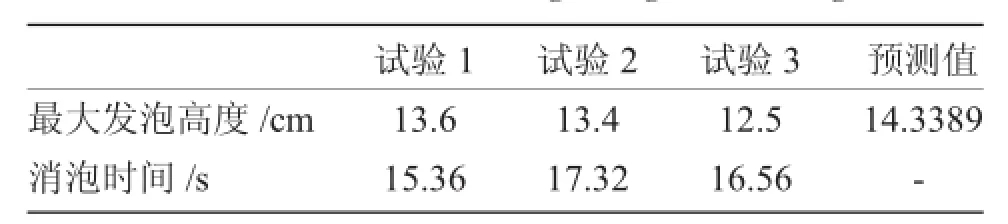
表7 最大发泡高度验证性试验Tab.7 Verification testing of highest foaming
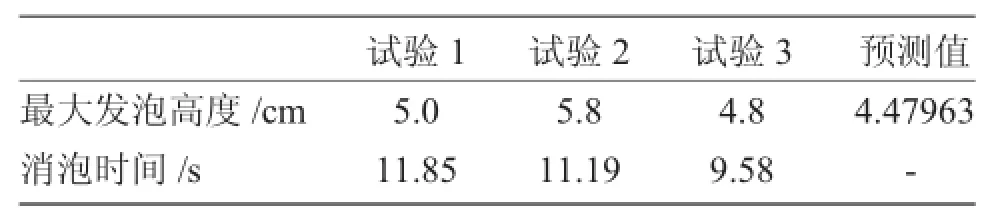
表8 最小发泡高度验证性试验Tab.8 Verification testing ofminimum foaming
验证性试验结果表明,实际MDEA溶液测试结果与预测值接近,表明上述多因素影响试验的工程推断是合理、可信的。
利用minitab软件预测出的最大(小)发泡高度的各个影响因子的水平进行验证性试验,结果表明测定结果与预测值接近,验证了上述各因素影响发泡高度的准确性。
5 结论
(1)采用Minitab软件进行多因素试验对MEDA脱硫溶液的发泡性能(发泡高度)与5个影响因素进行关联分析,确定了影响因素的排序为:温度>Fe(NO3)3>MgCl2>甲酸钠>环戊烷。
(2)与单因素试验比较,在多因素共存时,各因素相互作用和影响,导致各因素对发泡性能(发泡高度)发生了明显改变。
(3)控制好系统操作温度,对抑制MEDA溶液发泡至关重要。
参考文献
[1]吴新民.甲基二乙醇胺(MDEA)脱硫溶液发泡影响因素和机理研究[J].天然气化工,2008,33(6):31-36.
[2]常宏岗.气体脱硫装置胺溶液发泡原因及认识[J].石油与天然气化工,1995,24(1):60-63.
[3]付敬强,王鸿宇.脱硫溶液污染原因分析[J].石油与天然气化工,2001,30(6):293-294.
[4]叶庆国,李宁.脱硫工业中氧对N-甲基二乙醇胺的降解影响及对策研究[J].化学反应工程与工艺,1999,115(2):219-221.
[5]石油天然气行业标准SY/T 6538-2002配方型选择性脱硫溶液[S].
Determ ination of sodium gluconate by spectrophotometry*
WENG Yan-jun1,LIN Kai2,XIN Jia-ying2*
(1.Harbin Pharmaceutical Group Co.Ltd.General Pharm.Factory,Harbin 150086,China;2.Key Laboratory for Food Science and Engineering,Harbin University of Commerce,Harbin 150076,China)
Based on the ability of sodium gluconate can form the corresponding lactone at pH 1.5,then glucolactone can reactwith hydroxylamine-ferric trichloride to form red-brown hydroxamate Fe3+comp lex,so the content of complex can be determined by colorimetry and the standard curve is established.The corresponding linear equation is y=113.0833χ+0.1162,R2=0.9999.Themaximum absorbance of the complex is at 500nm.There is a well linearity in the range of 1×10-3~9×10-3mol·L-1and the average recovery is 99.79%.Thismethod can be successfully applied to the detection of sodium gluconate which is formed by the oxidation of glucose over Au/γ-Al2O3.
sodium gluconate;spectrophotometry;hydroxylamine-ferric trichloride
O657.32
A
1002-1124(2014)07-0022-04
2014-03-12
国家自然科学基金(21073050);黑龙江省杰出青年科学基金项目(jc201106);黑龙江省应用技术研究与开发计划项目(GC13C111)
翁艳军(1971-),男,副高,生物化学工程。
辛嘉英(1966-),男,教授,博士,研究方向:生物催化。

