hi FGF2真核表达载体的构建及其高表达对细胞凋亡的影响
陈钟琳,姜红岩,洪晓冰,陈中华,郑燕珊,徐 涵,石刚刚,黄展勤
(1.汕头大学医学院附属肿瘤医院,2.汕头大学医学院药理学教研室,广东汕头 515041)
成纤维细胞生长因子2(fibroblast growth factor-2,FGF-2),也称作碱性成纤维生长因子(basic fibroblast growth factor,bFGF),广泛参与细胞的生长、分化、迁移、血管生成及肿瘤的发生等过程。FGF-2基因定位于人类染色体的4q26,全长38kb,含有3个外显子和2个内含子。由于其mRNA有多个翻译起始位点,可以产生18 ku的低分子量亚型(lo FGF2)和23 ku的高分子量亚型(hi FGF2),低分子量亚型在细胞质和细胞膜中表达,高分子量亚型则主要直接进入细胞核中发挥作用。具有活性的FGF-2可通过肝素硫酸盐蛋白多糖(heparin sulfate proteoglycans,HSPG),与酪氨酸激酶受体性质的成纤维细胞生长因子受体(fibroblast growth factor receptor,FGFR)结合,激活 PKC、Ras/Raf/MEK/ERK、P13K、JAK/STAT等信号传导通路,参与调节细胞增殖,分化和恶性转化[1-2]。
在心血管系统,有研究结果证明FGF-2参与了压力负荷和血管紧张素引起的心肌肥厚[3];AngⅡ与受体结合刺激心肌细胞和心肌成纤维细胞分泌FGF-2,并激活MAPK信号通路导致心肌肥厚,心脏功能恶化[4-5]。但是,也有研究表明 FGF-2可以引起细胞染色质浓缩,抑制增殖和引起细胞凋亡[6]。显然,FGF-2在心血管中的作用尚不完全明了。
为了进一步研究hi FGF2的生物学意义及其机制,本实验构建 hi FGF2的真核表达载体,并在HEK293细胞中过表达后,观察其对HEK293细胞凋亡的影响。
1 材料与方法
1.1 试剂与仪器 重组质粒hi FGF2(23 ku)-pD-sRed1-N1(由德国 Hannover大学 Prof.Dr.Peter Claus馈赠),HEK293细胞株(中国细胞库),LipofectamineTM2000 Reagent(Invitrogen公司),E.coli Trans1-T1感受态细胞(北京全式金公司),Nhel限制性内切酶、EcoRI限制性内切酶(美津生物技术公司),胶回收试剂盒(天根生物技术公司),质粒小提/中提试剂盒(BIOMIGA公司),高糖DMEM培养液、胎牛血清(HyClone公司),Annexin V-FITC/PI双染法细胞凋亡检测试剂盒(Mbchem公司),兔抗大鼠FGF-2单克隆抗体(Epitomics公司)。
1.2 实验分组 实验分成3组:正常组(Control)、转染空载体(Vector)组、转染质粒(hi FGF2)组。
1.3 pDsRed1-N1真核表达载体的构建 质粒FGF2(23 ku)-pDsRed1-N1的 cDNA用 Nhel和 Eco-RI双酶切后,琼脂糖凝胶电泳后根据载体DNA片段大小切胶(约4 700 bp),用胶回收试剂盒回收纯化所切片段,得到少量载体DNA。载体DNA用感受态细胞Trans1-T1进行转化,在LB固体培养基中扩增长出菌落,最后用去内毒素质粒小提试剂盒抽提纯化出质粒DNA,即构建出pDsRed1-N1真核表达载体。用Nhel和EcoRI进行酶切鉴定,琼脂糖凝胶电泳。
1.4 FGF2在HEK293细胞中的转染 200 ml的DMEM(无血清)中加入4.0μg DNA,柔和混匀;200 μl/孔无血清 DMEM稀释10μl/孔 lipofectamin 2000试剂,轻轻混匀,室温放置5 min;将稀释好的DNA和lipofectamin 2000试剂轻柔混匀,室温放置20 min。将400μl上述复合物加入到细胞中,细胞在37℃、5%CO2培养箱中孵育24 h后可通过倒置荧光显微镜观察到荧光,检测转染效率。
1.5 FGF2在HEK293细胞中过表达后的检测FGF2在HEK293细胞中转染48 h内提取总蛋白进行Western blot检测。一抗为兔抗FGF2单克隆抗体,二抗为羊抗兔多克隆抗体,化学发光液为底物。
1.6 检测过表达hi FGF2后细胞凋亡 用Annexin V-FITC/PI双染法细胞凋亡试剂盒检测过表达hi FGF2后细胞凋亡的情况。pDsRed1-N1-hi FGF2质粒转染至HEK293细胞后24 h,用不含EDTA的胰酶消化收集,用冷PBS洗涤细胞两次,每次2 000 r·min-1,5 min离心收集细胞;用400μl 1×Binding Buffer悬浮细胞;在细胞悬液中加入5μl Annexin VFITC,轻轻混匀避光孵育15 min;加入10μl PI后轻轻混匀避光孵育5 min;1 h内用荧光显微镜检测。细胞分组:阴性组,单染FITC组,单染 PI组,双染FITC-PI组。
1.7 统计学方法 实验结果用SPSS 13.0统计软件分析,结果以±s表示,采用单因素方差分析进行组间比较。
2 结果
2.1 HI FGF2的鉴定及真核表达载体的构建HEK293细胞RNA经逆转录聚合酶链反应法得到约1 000 bp的DNA条带,酶切克隆至pDsRed1-N1中,PCR扩增hi FGF2质粒在23 ku的基因片段,琼脂糖凝胶电泳检测得到含hi FGF2 cDNA的真核表达载体,条带指示约在5500 bp和90 bp(Fig1)。DNA测序证实其全长开放读码框与真核表达载体的读码框吻合,得到pDsRed1-N1-hi FGF2。
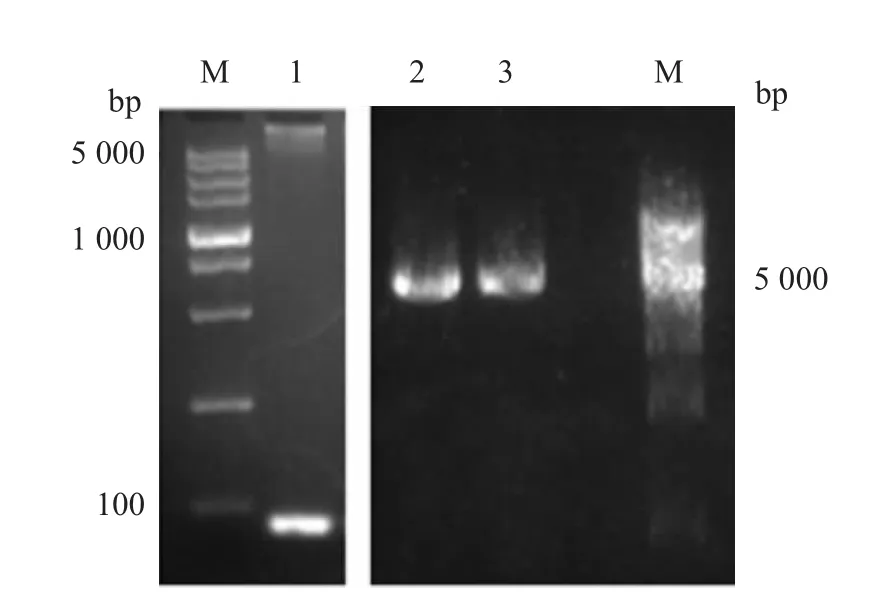
Fig 1 hi FGF2 plasmid and p DsRed1-N1 vector was detected by gel Agarose gel electrophoresis1:The hi FGF2-pDsRed1-N1 DNA,the bands are about 5 500bp and 90bp.2,3:The pDsRed1-N1 DNA,the band is about 5 000 bp.
2.2 荧光倒置显微镜观测HI FGF2的转染效率由于目的基因片段插入载体pDsRed1-N1中,且带红色荧光蛋白,所以进行质粒hi-FGF2-pDsRed1-N1转染后,有质粒转入的细胞在荧光倒置显微镜下可观测到红色荧光,从而判断质粒的转染效率(Fig 2)。

Fig 2 Transfection of hi FGF2-pDsRed1-N1 in HEK293 cellsThe red fluorescence represents that hi FGF2-pDsRed1-N1 has been transfected into the HEK293 cells.
2.3 Western blot检测HI FGF2在HEK293细胞中的表达 Westerm blot检测pDsRed1-N1-hi FGF2转染的HEK293细胞中hi FGF2的表达,在约50 ku处出现了特异性免疫反应条带(Fig 3),而未经转染细胞对照无相应条带,表明 hi FGF2成功转入HEK293细胞中,并表达hi FGF2重组蛋白。

Fig 3 Over-expression of hi FGF2-pDsRed1-N1 in HEK293 cells1:Nomal cultured HEK293 cells;2:HEK293 cells which were transfected with hi FGF2-pDsRed1-N1.
2.4 表达HI FGF2引起细胞凋亡 FITC-Annexin V/PI双染法检测细胞凋亡。在流式细胞散点分析图上划十字门,正常细胞FITC及PI均低染(FITCPI-),图上显示为左下区细胞簇;早期凋亡细胞FITC高染而PI低染(FITC+PI-),图上显示为右下区细胞簇;晚期凋亡及死亡细胞FITC及PI均高染(FITC+PI+),图上显示为右上区细胞簇(Fig 4 A,B,C)。比较早期凋亡和晚期凋亡,空载体转染组(Vector组)(Fig 4B)比正常未转染组(Control组)(Fig 4A)凋亡细胞增多,其差别有统计学意义(P<0.05),质粒转染组(Fig 4C)比正常未转染组和空载体转染组细胞凋亡明显增多,差异均有统计学意义(P<0.05)。说明当过表达质粒 pDsRed1-N1-hi FGF2时,明显促进细胞凋亡。

Fig 4 Over-expression of Hi-FGF2 induced cell apoptosisA:Normal cultured HEK293 cells(Control);B:HEK293 cells which were transfected with empty vector pDsRed1-N1(Vector);C:HEK293 cells which were transfected with hi FGF2-pDsRed1-N1(hi FGF2).*P<0.05,**P<0.01 vs control;#P<0.05 vs vector
3 讨论
HEK293细胞是一种来源于人体肾脏的细胞株,且比较容易转染,是一个很常用的研究表达外源基因的细胞株。综合大量的文献和前期研究,选择HEK293细胞株作为初步研究转染和生物活性的功能性细胞,是一个最佳选择[7]。本实验选用HEK293细胞株作为实验载体,并成功进行 pD-sRed1-N1-hi FGF2的转染,为研究hi FGF2的生物学功能奠定基础。
已有研究表明,hi FGF2过表达会使半胱氨酸天冬氨酸蛋白激酶3(caspase-3)活化,同时下调Akt磷酸化水平。Miyamoto等[8]指出,多种病理损伤,包括缺血和再灌注、压力超负荷、缺氧、低血糖和心脏毒性药物能够激活Akt,阻止心肌细胞凋亡。Akt磷酸化水平一旦降低,其促细胞存活的作用也将随之降低,加上执行caspase-3的激活,标志细胞凋亡的引发[9]。本实验结果证实 hi FGF2转染到HEK293细胞过表达后会导致细胞凋亡。
本实验重组质粒hi FGF2-pDsRed1-N1的成功构建,为我们的下一步深入研究提供有利的实验条件。在本实验结果基础上,我们将进一步扩展研究hi FGF2导致细胞凋亡可能的作用机制,如对细胞中Akt磷酸化水平的影响,以及B23、p68、C1QBP等多种蛋白质的相互作用后所产生的生物效应。
参考文献:
[1] Turner N,Grose R.Fibroblast growth factor signaling:development to cancer[J].Nat Rev Cancer,2010,10(2):116-29.
[2] Liao S,Bodmer J,Pietras D,et al.Biological functions of the low and high molecular weight protein of fibroblast growth factor-2 in cardiovascular development and disease isoforms[J].Devel Dynam,2009,238(2):249-64.
[3] Detillieux K A,Sheikh F,Kardami E,et al.Biological activities of fibroblast growth factor-2 in the adult myocardium[J].Cardiovasc Res,2003,57(1):8-19.
[4] Pellieux C,Foletti A,Peduto G,et al.Dilated cardiomyopathy and impaired cardiac hypertrophic response to angiotensinⅡin mice lacking FGF-2[J].J Clin Invest,2001,108(12):1843-51.
[5] Kim H.Assignment of the human basic fibroblast growth factor gene FGF2 to chromosome 4 band q26 by radiation hybrid mapping[J].Cytogenet Cell Genet,1998,83(1-2):73.
[6] Hirst C,Herlyn M,Cattini P,et al.High levels of CUG-initiated FGF-2 expression cause chromatin compaction,decreased cardiomyocyte mitosis,and cell death[J].Mol Cell Biochem,2003,246(1-2):111-6.
[7] 孙 颖,蔡海燕,沈敬山,等.5-羟色胺1A受体激动剂高通量筛选模型的建立[J].中国药理学通报,2012,28(5):731-6.
[7] Sun Y,Cai H Y,Shen JS,et al.Establishment of high throughput screening system of 5-HT1A receptor agonists[J].Chin Pharmacol Bull,2012,28(5):731-6.
[8] Miyamoto S,Rubio M,Sussman M.Nuclear and mitochondrial signalling Akts in cardiomyocytes[J].Cardiovascul Res,2009,82(2):272-85.
[9] Kothakota S,Azuma T,Reinhard C,et al.Caspase-3-generated fragment of gelsolin:effector of morphological change in apoptosis[J].Science,1997,278(5336):294-8.

