酵母水解物对草鱼生长性能和体成分的影响
■曾本和向 枭杨文娇吴 振 张 禛 张腾云王 强吕光俊
(1.西南大学荣昌校区水产系淡水鱼类资源与生殖发育教育部重点实验室水产科学重庆市市级重点实验室,重庆 402460;2.唐山拓普生物科技有限公司,河北唐山063021)
酵母水解物(yeast hydrolysate,YHY),是以新鲜啤酒酵母为原料,采用现代生物工程技术,经除杂、自溶、酶解、喷雾干燥等工艺精制而成。酵母水解物富含核酸、核苷酸、小肽、细胞壁多糖(免疫多糖)、游离氨基酸及丰富的B族维生素。氨基酸和小肽易于消化吸收,在动物蛋白质营养中优势显著,因此酵母水解物是一种非常理想的功能性蛋白源,可以作为饲料中优质蛋白原料(如鱼粉)的替代物。其中小肽能改善胃肠环境和菌群结构,促进胃肠对饲料营养物质的分解、合成、消化、吸收和利用,从而增加采食量,提高动物对饲料的利用率,改善生产性能;同时,酵母水解物中的甘露寡糖,能够吸附病原菌和霉菌毒素,并且仅能被含有β-糖苷酶的有益菌所利用,因此能有效抑制病源性微生物的繁殖,协助机体消除毒素及其代谢产物,增强机体免疫和抗病力。本试验通过在饲料中添加不同含量的酵母水解物(yeast hydrolyzate,YHY)探讨其对草鱼幼鱼生长性能及体成分的影响,以期为YHY在水产饲料中的推广应用提供参考。
1 材料和方法
1.1 试验饲料
以鱼粉为动物蛋白源,豆粕、菜粕、花生粕、玉米蛋白粉等为植物蛋白源,用麸皮和面粉等来平衡饲料能量水平,酵母水解物(YHY)(由唐山拓普生物科技有限公司提供)的添加量分别为0、0.5%、0.9%、1.3%、1.7%和2.1%。用玉米蛋白粉来调整饲料蛋白含量,配制成6种等氮(蛋白质含量30.00%)、等脂(脂肪含量为7.00%)的草鱼试验饲料。各饲料原料均粉碎过60目筛,称重后混匀,量少的组分采用逐级扩大法混合,制成直径1 mm颗粒饲料,自然晾干后保存备用,各试验组试验饲料配方见表1。
1.2 试验鱼及饲养管理
试验草鱼幼鱼购自重庆市荣昌县梅石坝养殖场,为同一批繁殖的幼鱼。购回后先用5%的食盐水消毒后放入暂养池(暂养池尺寸2.1 m×1.2 m×0.8 m),用商品饲料暂养两周。试验开始时,选取体格健康、无畸形、体重为(8.19±0.27)g的草鱼540尾随机放入18个水族箱中。每个水族箱放30尾鱼,随机安排每3个水族箱为一个试验组(每个处理组设3个重复组),养殖周期为60 d。养殖期间定点、定时、定质、定量投喂。每天按5%的投饵率早、中、晚(7:00、12:00、17:00)各投喂一次,投饵1 h后将残饵捞出烘干称重并扣除。试验期间保持微流水。试验用水为曝气后的自来水,每日监测水温、水质、试验鱼的摄食行为和死亡数量等,并根据水温和鱼体生长等情况调整投饲量。试验期间,水温维持在26~28℃,溶氧高于6 mg/l,氨氮含量小于0.3 mg/l,pH值为7.0~7.5。试验结束时停食1 d。

表1 试验饲料配方及主要营养成分(风干基础)(%)
1.3 生长性能指标及肌肉营养成分测定
1.3.1 生长性能指标测定
试验开始时,测定试验鱼的初始体重,试验结束后,停食1 d,测定各组试验鱼体重,计算其增重率和特定生长率,依据养殖期间饲料的投喂量、饲料蛋白含量及试验鱼的增重计算增重率、特定生长率、饲料系数、蛋白质效率等指标。

式中:W0——试验开始时鱼体重(g);
Wt——试验结束时鱼体重(g);
F——饲料摄入量(g);
P——饲料粗蛋白质质量分数(%);
t——养殖天数(d)。
1.3.2 鱼体成分分析
胴体粗蛋白质采用凯氏定氮法(GB5009.5—2010)测定;粗脂肪采用索氏抽提仪测定法(GB/T 6433—2006)测定;水分采用干燥法(105 ℃)(GB/T 6435—2006)测定;灰分采用马弗炉灼烧(550℃)法(GB/T 6438—2007)测定。
1.4 数据处理和分析
试验数据用Excel 2010计算,采用SPSS Statistics 19.0统计软件中one-way ANOVA进行方差分析,若组间差异显著,再用Duncan's法进行多重比较,差异显著水平为P<0.05。试验数据以“平均值±标准差(Means±SD)”表示。
2 结果
2.1 酵母水解物对草鱼生长性能的影响(见表2及图1~图4)

表2 酵母水解物对草鱼生长性能的影响(平均值±标准差)

图1 草鱼增重率与YHY添加水平的关系

图2 草鱼特定生长率与YHY添加水平的关系

图3 草鱼蛋白质效率与YHY添加水平的关系
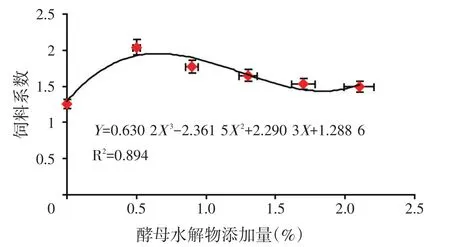
图4 草鱼饲料系数与YHY添加水平的关系
由表2可知,YHY对草鱼生长有影响。随着YHY的增加,草鱼增重率(WGR)、特定生长率(SGR)、蛋白质效率(PER)均呈先降低后升高再降低的变化趋势。草鱼增重率(WGR)、特定生长率(SGR)和蛋白质效率(PER)均在YHY添加量为1.7%达到最高(分别为245.16%、2.07%/d和324.35%),显著高于其他试验组(P<0.05)。以三次方程回归可知(图1~图3),草鱼的WGR、SGR、PER分别为:Y=-144.03X3+444.24X2-302.61X+157.93(R2=0.818 8);Y=-0.913 5X3+2.822 6X2-1.931 9X+1.560 9(R2=0.851 9);Y=-269.3X3+812.05X2-577.63X+261.98(R2=0.868 1)。草鱼WGR、SGR、PER最优时YHY的添加水平分别为1.62%、1.61%、1.53%。因此满足草鱼WGR、SGR、PER最佳时YHY的添加水平为1.53%~1.62%。
草鱼饲料系数(FCR)的变化趋势同WGR、SGR、PER相反(图4),随着YHY添加量的升高呈先升高后降低并趋于稳定的变化趋势。根据三次回归方程可知,草鱼FCR回归方程为Y=0.630 2X3-2.361 5X2+2.290 3X+1.288 6(R2=0.894),FCR最优时YHY添加水平为1.75%。
2.2 酵母水解物对草鱼体成分的影响(见表3)

表3 酵母水解物对草鱼体成分的影响(%)
如表3所示,试验草鱼机体粗蛋白随YHY添加量的升高而呈先升高后降低的变化趋势,且在YHY的添加量为1.3%时最高(15.03%),显著高于对照组(Diet 1)及其他试验组(P<0.05)。而草鱼机体粗脂肪随YHY添加量的升高而呈先降低后升高的变化趋势;粗脂肪在YHY的添加量为1.7%时最低(4.39%)(P<0.05),显著低于对照组(Diet 1)及其他试验组(P<0.05)。随着YHY添加量的升高,试验草鱼机体水分和粗灰分差异不显著(P>0.05)。
3 讨论
3.1 酵母水解物对草鱼生长性能的影响
本试验中,随着YHY的增加,草鱼WGR、SGR、PER均呈先降低后升高再降低的变化趋势,而FCR则随着YHY添加量的升高呈先升高后降低再趋于稳定的变化趋势。说明添加低剂量(添加量<0.9%)的YHY会导致WGR、SGR、PER降低,FCR升高。这与李自金等的研究结果有一定的差异。这可能与饲料成分、酵母的来源、组成、养殖品种、生长阶段等有关,具体原因有待进一步证明。随着YHY进一步增加,草鱼WGR、SGR、PER均呈升高趋势,FCR呈降低趋势,且在YHY添加量为1.5%~1.7%时获得最佳WGR、SGR、PER,说明适量YHY能明显改善草鱼的生长状况和饲料转化利用率。这与Sanderson、程光平等的研究结果一致。可能是由于酵母水解物所含的丰富小肽、游离氨基酸等活性物质,提高了饲料的适口性和鱼类的摄食量,同时其中含有的β-葡聚糖、小肽等可提高鱼类小肠微绒毛高度及吸收面积,从而提高了鱼类对饲料营养物质的消化利用率,提高其生长速度。当YHY添加量大于1.7%时,草鱼WGR、SGR、PER均呈降低趋势,FCR有升高趋势,说明过量饲料YHY会影响草鱼生长。在对胡子鲶(Clarias fuscus)、中华鳖等的研究中同样发现高剂量的酵母会影响水产动物的摄食和生长。可能是因为高剂量的饲料酵母导致肠道完整性被破坏,对营养物质的吸收能力降低,从而影响鱼类生长发育;也可能是高浓度的酵母引起鱼体的免疫反应过度,导致用于生长的能量和营养素减少的缘故。
3.2 酵母水解物对草鱼体成分的影响
酵母水解物是酵母细胞的水解产物,含有大量的氨基酸、小肽、丰富的B族维生素、谷胱甘肽及核苷酸类物质,对水产动物营养平衡及肌肉营养品质有着重要作用。向枭等对鲤鱼的研究发现,随着酵母核苷酸添加量的增加,鱼体中粗蛋白质和粗脂肪含量呈先上升后降低趋势,说明适量的饲料酵母能改善鲤鱼肌肉品质。在本试验中,YHY对草鱼胴体中粗灰分和水分的含量无显著影响(P>0.05),但添加适宜YHY能显著提高加州鲈胴体中粗蛋白含量和降低胴体粗脂肪含量(P<0.05),说明YHY能有效改善加州鲈肌肉品质。这与向枭等对鲤鱼的研究结果基本一致。可能是由于酵母水解物所含的丰富的草鱼生长所需的氨基酸,使鱼体氨基酸达到平衡,促进了蛋白质合成;同时酵母水解物中丰富的小肽,能阻碍脂肪吸收,促进脂质代谢消耗。但与崔敏对大菱鲆等的研究结果存在差异,这可能与鱼的种类、生长阶段、饵料成分有关。
4 结论
适量的YHY能提高草鱼生长性能,改善其肌肉营养品质。为了在养殖过程中获得最佳的生长性能,建议草鱼饲料中YHY的添加水平应为1.53%~1.75%。
(参考文献19篇,刊略,需者可函索)

