三元体系KBr-K2SO4-H2O在373 K的相平衡研究*
卢啟富,桑世华,张 海,李 婷
(1.贵州省地矿局一一三地质大队,贵州六盘水,553001;2.成都理工大学材料与化学化工学院;3.成都理工大学地球化学系)
研究与发展
三元体系KBr-K2SO4-H2O在373 K的相平衡研究*
卢啟富1,2,桑世华2,张 海1,3,李 婷2
(1.贵州省地矿局一一三地质大队,贵州六盘水,553001;2.成都理工大学材料与化学化工学院;3.成都理工大学地球化学系)
采用等温溶解平衡法研究了三元体系KBr-K2SO4-H2O在373 K时的相平衡关系,测定了相应温度条件下饱和溶液的溶解度及密度。研究发现:该三元体系为简单共饱和型,无复盐及固溶体形成。根据溶解度数据绘制了相应的平衡溶解度曲线,相图中有1个共饱点,2条单变曲线,2个平衡固相结晶区分别为溴化钾和硫酸钾;对不同温度条件下的KBr-K2SO4-H2O的溶解度做了对比分析和讨论,结果表明:溴化钾对硫酸钾有强烈的盐析作用。此外还简要讨论了该三元体系的密度变化规律。
水盐体系;相平衡;硫酸钾;溴化钾;溶解度
钾盐矿主要用于制造钾肥,硫酸钾是农业不可缺少的三大肥料之一。目前,农业用钾肥严重不足,主要依赖进口,大力发展钾矿资源的勘探和开发是中国工农业发展的基础,因此,钾盐矿被国家列入急缺矿种之一。中国有很多高矿化度的盐湖卤水是天然存在于地表的富钾液态矿产资源,其主要分布在西藏、青海、新疆等省区,例如青海察尔汗盐湖、西藏扎布耶盐湖、罗布泊富钾卤水等。此外,中国部分省区还储藏有巨量的地下卤水资源。四川盆地的地下层卤水独具特色,其中含有K+、Na+、Ca2+、Mg2+、Cl-、B4O72-等多种成分,并伴有Sr、Li、Br、I等多种组分。这些卤水中钾的含量大多为7.18~25.95 g/L,平均钾含量为18.86 g/L,最高可达53.27 g/L,是中国重要的液态钾矿资源。深埋地下的卤水和地表盐湖卤水一样,均是高矿化度的液态矿产资源,开发利用丰富的液态矿产资源对中国农业和工业的发展具有重要意义。盐湖卤水和地下卤水资源的成矿和开发过程中,均存在盐类矿物-溶液的动态固液相平衡过程。有关卤水体系多温相平衡的研究是卤水资源综合利用的基础,为卤水资源的开发工艺提供基础相平衡数据。通常采用相分离的技术手段,例如蒸发、结晶、盐析、加热、冷却等工艺过程实现卤水资源的分离提纯。因此,开展该地下卤水高温固液相平衡的研究可以揭示液态矿产的成矿规律,指导卤水资源的开发利用。
在中国现有地下卤水资源中,四川盆地西部的气田卤水颇具代表性。在前期的研究中,课题组已针对四川盆地西部气田卤水的化学组成,开展了不同温度条件下的氯化盐、硫酸盐、硼酸盐和溴盐等体系的多温溶解度和固液相平衡的研究[1-12],从而揭示了卤水中盐类矿物的赋存形式和结晶析出条件。
该三元体系为川西地下卤水复杂多组分体系中的三元子体系,课题组的研究温度条件为多温323~373 K区间,而高温相平衡的研究目前是固液相平衡的研究热点和难点,该三元体系KBr-K2SO4-H2O在373 K条件下的高温相平衡实验还鲜见报道。因此,课题组在前期研究基础上对该三元体系相平衡关系做了详细的实验研究,测定了373 K条件下该体系的溶解度及密度,绘制了相应的溶解度曲线图和密度关系图,确定了高温条件下的盐矿结晶析出的固相结构,揭示了钾盐矿在高温373 K时的结晶溶解和平衡规律,为卤水中钾盐的提取分离提供了基础化学热力学相平衡数据。
1 实验部分
1.1 试剂与仪器
试剂:KBr、K2SO4,均为分析纯;去离子水(pH≈6.6,电导率<1×10-4S/m,实验过程中配制溶液和分析用标液均用此水,配制溶液前煮沸除去CO2气体)。
仪器:AL104型电子天平(精度值为0.000 1 g)、SHA-GW型数显恒温油浴振荡器(±0.1 K)。实验时先设定实验温度为373 K,待稳定后再用精密温度计(±0.01 K)测量实验的油浴温度,根据实际测量的温度对恒温油浴微调,保证实验油浴温度变化在(373±0.1)K范围内。
1.2 实验方法
该三元体系在373 K时的相平衡研究采用等温溶解平衡法在密封性能良好的玻璃瓶中进行。根据二元体系共饱点的溶解度数据进行三元体系相平衡样品的配置:例如从KBr-H2O共饱点开始逐渐加入K2SO4;所配料液密封于磨口玻璃瓶中,放入恒温油浴振荡器中振荡以促进平衡,振荡一定时间后,取上层清液做化学分析,当上层清液的化学组成不变时,即视为达到平衡。高温条件下平衡时间较短,一般为4~7 d,平衡后取液相做化学分析,并对相应的平衡固相做分析鉴定。平衡溶液密度采用密度瓶法测定,取样的移液枪枪头先预热至373 K以上,再用移液枪快速取样,测定前用373 K条件下的纯水对密度瓶和测量的天平加以校正,并换算相应的校正系数。
1.3 分析方法[6]
Br-的测定采用AgNO3容量法;SO42-的测定采用茜素红-S法;K+的测定采用四苯硼钠-季胺盐容量法。
2 结果与讨论
2.1 相平衡实验结果
表1为三元体系溶解度的测定结果,图1、图2分别为依据表1数据绘制的该体系在373 K时的等温溶解度相图和密度曲线。
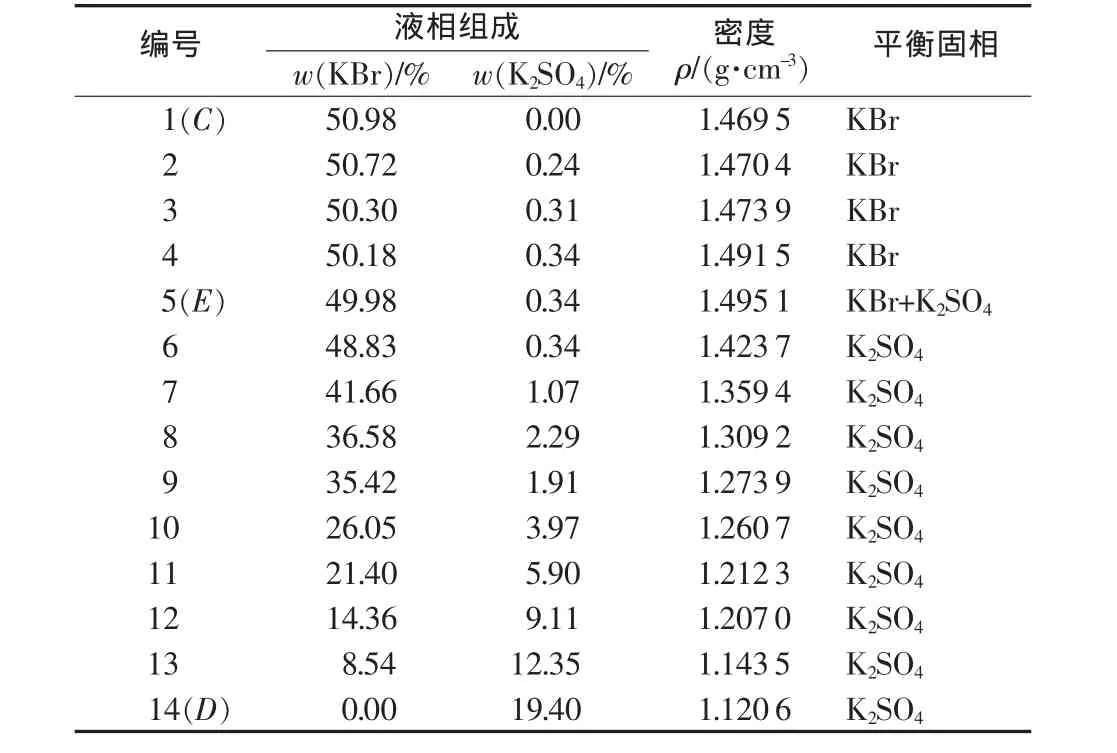
表1 三元水盐体系KBr-K2SO4-H2O 373K溶解度和密度
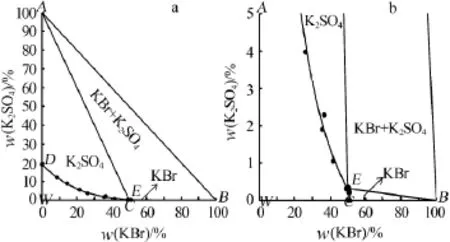
图1 三元水盐元体系KBr-K2SO4-H2O 373K等温溶解度曲线(a)及局部放大图(b)

图2 三元水盐元体系KBr-K2SO4-H2O 373K密度-质量分数图
由图1、表1可知,三元体系KBr-K2SO4-H2O在373 K的等温溶解度图中无复盐和固溶体生成,属于简单共饱和型,该等温溶解度图有1个共饱点,2条溶解度曲线,2个结晶区。共饱点E对应的平衡固相为KBr+K2SO4,其液相中w(KBr)=49.98%、w(K2SO4)= 0.34%。溶解度曲线CE对应的平衡固相为KBr,溶解度曲线DE对应的平衡固相为K2SO4。2个结晶区:CEBC区为KBr的结晶区,DEAD区为K2SO4的结晶区。图1a中该体系在373K下的KBr结晶区非常小,需在图1b局部放大图中才能看到,而K2SO4有较大结晶区,则KBr在该三元体系中有较大溶解度,而K2SO4在该三元体系中有较小溶解度。分析表1数据可知,当溶液中KBr的质量分数逐渐增大时,K2SO4的质量分数则迅速减小,从二元体系在373 K时的共饱点的溶解度w(K2SO4)=19.40%下降到该体系共饱点E4处w(K2SO4)=0.34%,这说明KBr对K2SO4有强烈的盐析作用。
综合表1和图2可知,液相的密度总体随着溶液中KBr质量分数的增大而增大,到达共饱点E后,液相的密度在共饱点处达到最大值。
2.2 不同温度的对比讨论
课题组将373 K条件下的单盐和共饱和点溶解度数据与早期文献报道的该三元体系KBr-K2SO4-H2O在273、298、323 K条件下的溶解度数据[13]做了对比分析,如表2所示。由表1和表2数据对比可知,在从低温273 K到高温373 K,KBr-H2O的饱和溶解度从34.11%增至50.98%,K2SO4-H2O的饱和溶解度则从6.78%增至19.40%,溴化钾和硫酸钾溶解度的随着温度的增加而增大;对比表2中不同温度下共饱和点溶解度数据可见,溴化钾对硫酸钾具有强烈的盐析作用,这为后期利用温度条件和盐析作用的分离提取硫酸钾提供了科学依据。
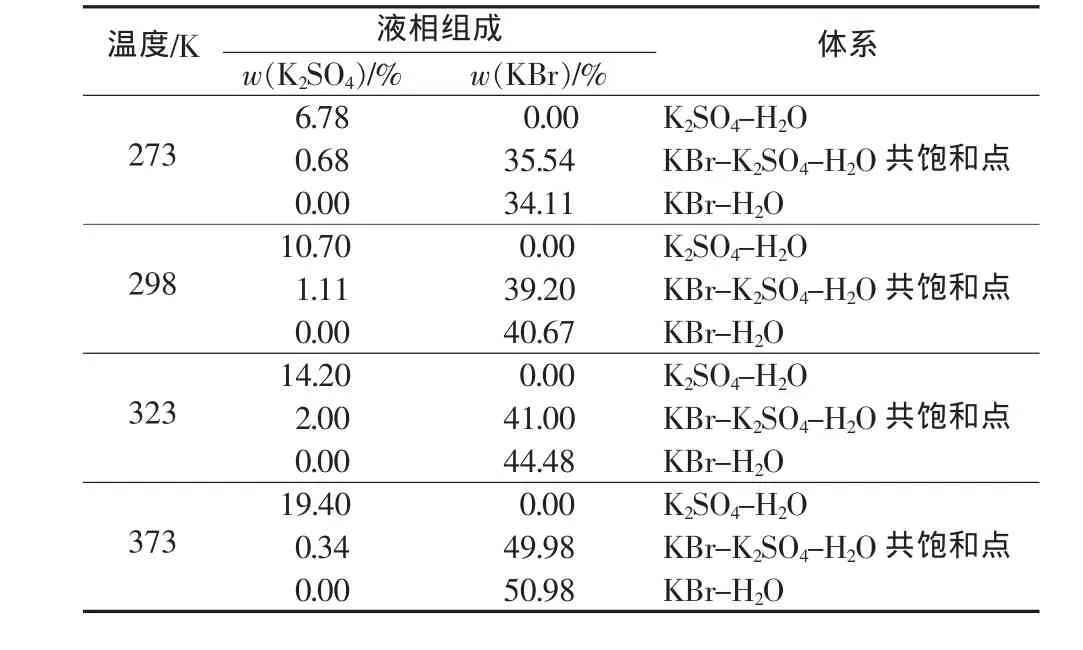
表2 三元水盐体系KBr-K2SO4-H2O在273、298、323K和373K共饱和点溶解度数据
3 结论
1)通过等温溶解平衡法得到了三元体系KBr-K2SO4-H2O在373 K时的溶解度数据,并测定了相应的平衡液相的密度,绘制了等温溶解度曲线及组成-密度曲线。2)研究发现,该三元体系为简单共饱和型,平衡固相为K2SO4和KBr。3)随着温度的增加,单盐KBr-H2O和K2SO4-H2O的溶解度均显著增加,在该三元体系中,溴化钾对硫酸钾具有强烈的盐析作用,导致硫酸钾的溶解度在共饱和点处明显下降。
[1] 桑世华,殷辉安,倪师军,等.三元体系K2B4O7-KBr-H2O在298 K的相平衡研究[J].成都理工大学学报:自然科学版,2006,33(4):414-416.
[2] 桑世华,虞海燕.三元体系Na2B4O7-NaBr-H2O 298 K相平衡研究[J].海湖盐与化工,2006,35(2),4-5,8.
[3] Sang Shihua,Zhang Hai,zhong Siyao,et al.Experimental study of the solubility in ternary Na2B4O7-NaBr-H2O and in quaternary Na2B4O7-Na2SO4-NaBr-H2O systems at 323 K[J].Fluid Phase Equilibria,2014,361:171-174.
[4] 王丹,桑世华,曾晓晓,等.KCl-KBr-K2SO4-H2O四组分物系323K相平衡[J].石油化工,2011,40(3):285-288.
[5] 桑世华,孙明亮,李恒,等.Na+,K+∥Br-,SO42--H2O四元体系323K相平衡研究[J].无机化学学报,2011,27(5):845-849.
[6] 孙明亮,桑世华,李恒,等.NaBr-Na2SO4-H2O三元体系323K相平衡研究[J].化学工程,2010,38(7):67-70.
[7] 张晓,桑世华,赖晨焕,等.Na2B4O7-Na2SO4-NaCl-H2O四元体系323K相平衡研究[J].化学工程,2009,37(11):44-46,50.
[8] 桑世华,李婷,崔瑞芝.三元水盐体系KBr-K2B4O7-H2O 348K相平衡研究[J].盐湖研究,2013,21(2),29-32.
[9] Cui Ruizhi,Sang Shihua,Zhang Kaijie,et al.Phase equilibria in the ternary systems K2SO4-K2B4O7-H2O and Na2SO4-Na2B4O7-H2O at 348K[J].J.Chem.Eng.Data,2012,57(12):3498-3501.
[10] Li Ting,Sang Shihua,Cui Ruizhi,et al.Phase equilibria of quaternary system NaCl-NaBr-Na2B4O7-H2O at 348 K[J].Chemical Research inChineseUniversities,2013,29(2):311-313.
[11] Cui Ruizhi,Sang Shihua,Hu Yongxia,et al.Phase equilibria in the ternarysystemsKBr-K2B4O7-H2Oand KCl-K2B4O7-H2Oat373K[J]. ActaGeologicaSinica,2013,87(6):1668-1673.
[12] Cui Ruizhi,Sang Shihua,Hu Yongxia,et al..Liquid-solid equilibria
in the quaternary systems KCl-KBr-K2B4O7-H2O and KCl-KBr-K2SO4-H2Oat373K[J].J.Chem.Eng.Data,2013,58(2):477-481.
[13] Silcock H L.Solubilities of inorganic and organic compounds[M]. Oxford:Pergamon Press,1979.
Research ofphaseequilibrium in ternary system KBr-K2SO4-H2O at373K
Lu Qifu1,2,SangShihua2,ZhangHai1,3,LiTing2
(1.No.113GeologicalBrigade,Guizhou ProvincialGeologicalProspectingBureau,Liupanshui553001,China;2.CollegeofMaterials,and Chemistry&ChemicalEngineering,Chengdu UniversityofTechnology;3.DepartmentofGeochemistry,Chengdu UniversityofTechnology)
Thesolid-liquid equilibriain ternary system KBr-K2SO4-H2Oat373Kwerestudied,and thesolubilitiesand densities of solution in the ternary system were determined.Research showed that the ternary system was of simple eutectic type and no double salt or solid solution was found;the solubility diagram of the ternary system had one invariant point,two univariant curves,and two fields of crystallization(KBr and K2SO4).The solubilities of KBr-K2SO4-H2O at different temperatures were compared and analyzed.Results showed that potassium bromide had a strong salting-out function on potassium sulfate obviously. Thedensity changing ruleofthe KBr-K2SO4-H2Owasalsodiscussed simply.
salt-watersystem;phaseequilibrium;potassium sulfate;potassium bromide;solubility
TQ131.13
A
1006-4990(2015)02-0013-03
2014-08-13
卢啟富(1964— )男,高级工程师,学士,主要从事实验室测
桑世华
国家自然科学基金(41373062、40973047)、高等学校博士学科点专项科研基金(20125122110015)联合资助项目。
试研究工作,已公开发表文章10余篇。
联系方式:sangsh@cdut.edu.cn

