羟自由基对三聚铝酸根离子(Al3 -B基团)环合反应的影响
尹周澜,丁治英,李 俊,张牧群
(中南大学 化学化工学院,长沙 410083)
铝酸钠溶液的分解是氧化铝生产的重要环节,由于溶液分解速度缓慢,分解率较低,铝酸钠溶液的分解成为氧化铝生产的瓶颈[1-2]。深入研究铝酸钠溶液的分解机理,对调控铝酸钠溶液的分解过程,保证分解产品质量具有重要意义。李小斌等[3]经过大量的研究认为,铝酸钠溶液分解过程中有利于氢氧化铝析出的含铝离子是Al(O,调控溶液中其他复杂含铝离子结构向该类结构转变则有利于氢氧化铝析出;李洁等[4-5]将量子化学计算与实验相结合研究了铝酸钠溶液分解的微观机理,提出有利生长基元的形成是溶液分解的关键,其中,四配位Al(O离子通过质子转移形成六配位的生长基元[Al(OH)4(O,以及三聚铝酸根离子(Al3-B基团)间环合反应形成六元环[Al6(OH)22(H2O)2]4-是铝酸钠溶液,其中三聚铝酸根离子间环合反应的活化能高达158.0 kJ/mol,其转化过程如下:

该六元环铝酸根离子很容易转变为有利生长基元[Al6(OH)18(H2O)6],从而不断叠合形成氢氧化铝晶体。
因此,铝酸钠溶液强化分解的关键就是找到促进生长基元形成的方法。ZHANG等[6]、WU等[7]和孙文乐等[8]研究发现经超声波处理后的种分精液有利于提高溶液分解率、缩短分解时间。关于超声场强化溶液分解的原因,多数学者认为是由于超声波在液体中产生空化效应,当超声功率达到空化阈值时,溶剂媒质中的空泡发生瞬间崩溃,在其周围产生局部高温高压,这一极端的物理化学环境可以致使某些化学键迅速断裂,导致自由基的形成[9-10]。张牧群等[11]应用电子顺磁共振(EPR)以及自由基捕获技术,检测到铝酸钠溶液在超声波空化作用下产生羟自由基(·OH)。尹周澜等[12]采用半经验量子化学计算方法AM1分析了超声场作用下产生的羟自由基可促进铝酸钠溶液中Al(III)配位数的增加,形成生长基元单体[Al(OH)4(OH2)2]-,即促进铝酸钠溶液分解的第一个控制步骤的反应。
为了探究超声场产生的羟自由基(·OH)是否能强化三聚铝酸根离子(Al3-B基团)间的环合反应,以促进有利生长基元[Al6(OH)18(H2O)6]的形成,本文作者采用量子化学计算方法分析羟自由基(·OH)参与三聚铝酸根离子间环合反应的活化能、反应途径、过渡态等,为超声场强化铝酸钠溶液的分解过程提供理论支撑。
1 计算方法
在DFT/BLYP/DND水平下,对Al3-B基团环合反应进行反应势能面(PES)扫描研究,分析反应路径上各驻点的几何构型,并利用振动频率分析确认反应的过渡态(TS)和中间体(IM)。然后通过判断能量的变化,正确关联反应物、中间体、过渡态以及生成物。为了得到更可靠的相对能量值,在BLYP/DND优化的基础上进一步选用精度较高的DNP进行模型体系的单点能计算,利用零点振动能(ZPVE)校正获得反应的活化能。所有的工作均在中南大学化学化工学院Sigworkstation量子化学工作站Cerius24.6的Dmol3计算模块中完成。
2 结果与讨论
2.1 Al3-B基团及其生成物六元环[Al6(OH)22(H2O)2]4-的几何构型
根据李洁[4]对过饱和铝酸钠溶液自发成核的研究,四配位Al(O离子通过两次质子转移聚合形成三聚体铝酸根离子(Al3-B基团),该三聚体中所有铝的配位数均为6。通过三聚体间的缩合,最终形成有利生长基元[Al6(OH)22(H2O)6]。为了研究羟自由基对该环合反应的影响,首先对反应物Al3-B基团和生成物六元环[Al6(OH)22(H2O)2]4-进行几何优化,在Cerius2程序中选用OFF的Universal1.02力场对模型体系进行初步优化,再采用DFT/BLYP/DND方法进行条件优化,最后改用精度更高的DNP基组求其单点能,并采用FORCE分析得到模型的振动频率和零点振动能(ZPVE)。Al3-B基团的优化几何构型和相关几何参数分别见图1和表1,[Al6(OH)22(H2O)2]4-的优化几何构型见图3(f)所示。
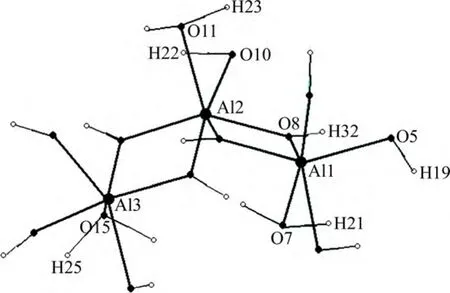
图1 Al3-B基团的优化几何构型示意图Fig.1 Schematic diagram showing optimized geometric structures ofAl3-B cluster
优化后的Al3-B基团属于C1点群,Al1和Al3上的—OH、—OH2以及 —OH—基团的几何结构性质十分相似。分析表1中的部分结构参数可知,Al3-B基团的Al1—OH中Al—O的键长大致为1.8Å左右,小于端基Al—O(H2)的键长,另外该键与相邻Al—O键之间的夹角明显小于端基Al—O(H2)与相邻键的夹角。类似地,Al2上的Al—OH也有同样的情况。根据配位化学中配位键之间的相互作用等相关原理[13],可以说明Al2上的Al—OH所受的排斥力比端基的相同键要小,因而该位置上的键能相对较大。比较端基铝上的Al—OH2和Al—OH,可以看出键Al—O(H2)的键长要比键Al—O(H)的键长大约0.2Å,可能前者的键能要比后者弱。此外,对比体系中的O—H键的键长发现端基铝上配位水分子中的O—H键的键长最大,为0.96Å左右。所以通过几何参数分析可以初步得出,端基上配位的水分子中O—H键容易断开。根据计算所得的模型结构参数对比文献,李洁[4]对铝酸钠溶液作X射线衍射分析时得出,溶液中Al—O(H)的键长约为1.82Å。KUBICKI等[14]在对聚合铝酸根离子进行理论计算求得的结构参数分别为Al—O(H)的键长平均值为1.83 Å;Al—O(H2)的键长平均值为1.99 Å。本实验中计算的Al—O(H)的键长平均值为1.81 Å,AlO(H2)的键长平均值为1.98 Å,与这些文献值符合得很好,说明该计算方法及所选模型结构合理可靠。
自由基具有的特性(如顺磁性等)与自由基中存在的未成对电子有关。根据STEMMLER[15]和CABRAL等[16]对自由基反应的研究表明,在气相或液相中发生的自由基反应十分相似,即溶剂化作用造成的影响不大。因此,本文作者在理论模拟计算时忽略了离子的溶剂化效应。通过分析羟自由基和Al3-B基团的前线轨道能量、电荷分布以及自旋密度,确定Al3-B基团与自由基发生反应的活性中心位置,以探讨两个基团的相互作用。
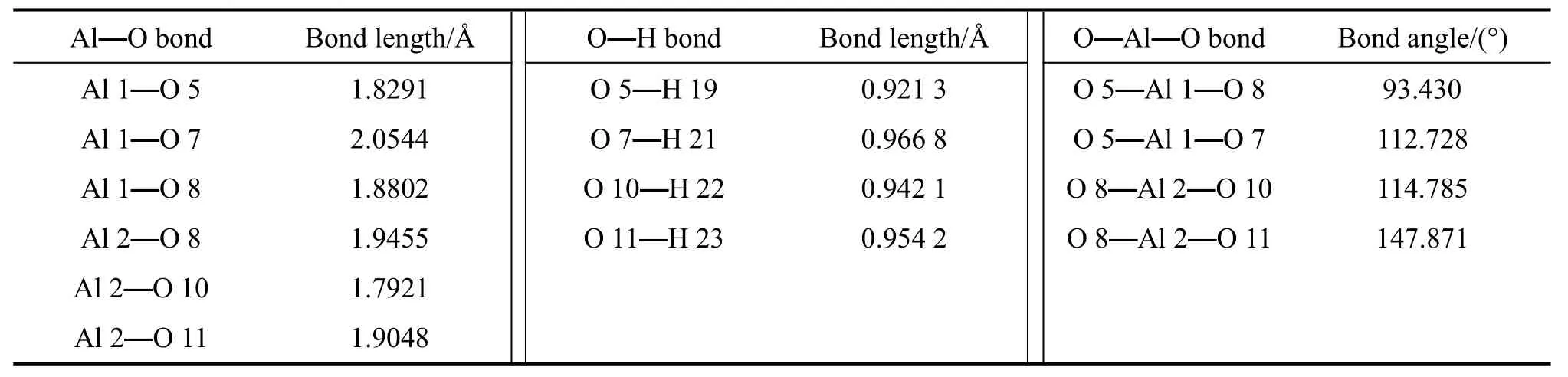
表1 Al3-B基团的部分几何结构参数Table 1 Partial optimized geometric parameters ofAl3-B cluster

表2 Al3-B基团和羟自由基的总能量、前线轨道能量及能级差Table 2 Total energy,frontier molecular orbital energy and energy gapsofAl3-B clusterand ·OH radicalunder DFT/BLYP/DNP level

图2 Al3-B基团和·OH自由基的前线轨道Fig.2 Frontier molecular orbitals of Al3-B cluster and·OH radical
2.2 模型体系反应活性中心的分析
不同方法计算模型体系Al3-B基团所得到的总能量、前线轨道能量及能级差列于表2。在BLYP/DNP水平下计算所得总能量要略低于UHF/6-31G水平下计算值,但两者相差不大。分析Al3-B基团的前线轨道能级及能级差可知,LUMO(最低空分子轨道)具有较高的能量,不易获得电子;而HOMO(最高占据分子轨道)具有相对低的能量,不易给出电子。HOMO与LUMO之间的能级差较大,不易发生电子跃迁。另外,从图2中Al3-B基团的前线轨道电子云分布情况来看,HOMO的电子云主要集中在两个端基的—O位置,这表明羟自由基易与该吸引电子的活性部位结合。LUMO的电子云主要分布于铝原子和氢原子上,且具有较强的排斥电子能力,故当自由基与端基上—OH2结合后,自由电子很难发生转移。
表3所列为模型体系Al3-B基团在DFT/BLYP/DNP水平下计算的部分原子净电荷分布情况。由表3可见,模型体系的正电荷分布于Al原子和H原子上。其中Al1、Al2和Al3原子的正电荷分别为1.7355、1.8811和1.7322,原子具有相对强的吸电子能力。但从基团的几何结构分析,Al原子分布在离子内层,外面包裹着O原子。因此,暴露在离子基团外面的氢原子成为自由基进攻的对象。其中端基—OH2中的氢原子因带正电荷较高,其自旋密度大于0,且相对较大,成为羟自由基与离子结合的活性部位。
2.3 羟自由基参与Al3-B基团环合反应的中间体和过渡态
羟自由基参与Al3-B基团的环合反应生成六元环状的[Al6(OH)22(H2O)2]4-产物,首先应是自由基与端基上—OH2中H结合,并迅速释放出水分子[17-18]。同时又与另一相同特性的基团发生聚合,形成[Al6(OH)22(H2O)2]4-产物。通过对反应势能面(PES)的研究,分别采用反应活性部位中O—O原子的距离以及O—Al原子的距离为变量,通过BLYP/DNP优化构型为基础,进行反应物、中间体以及过渡态的结构关联研究,图3所示为反应路径上的中间体与过渡态的几何构型,其相应的能量如表4所列。
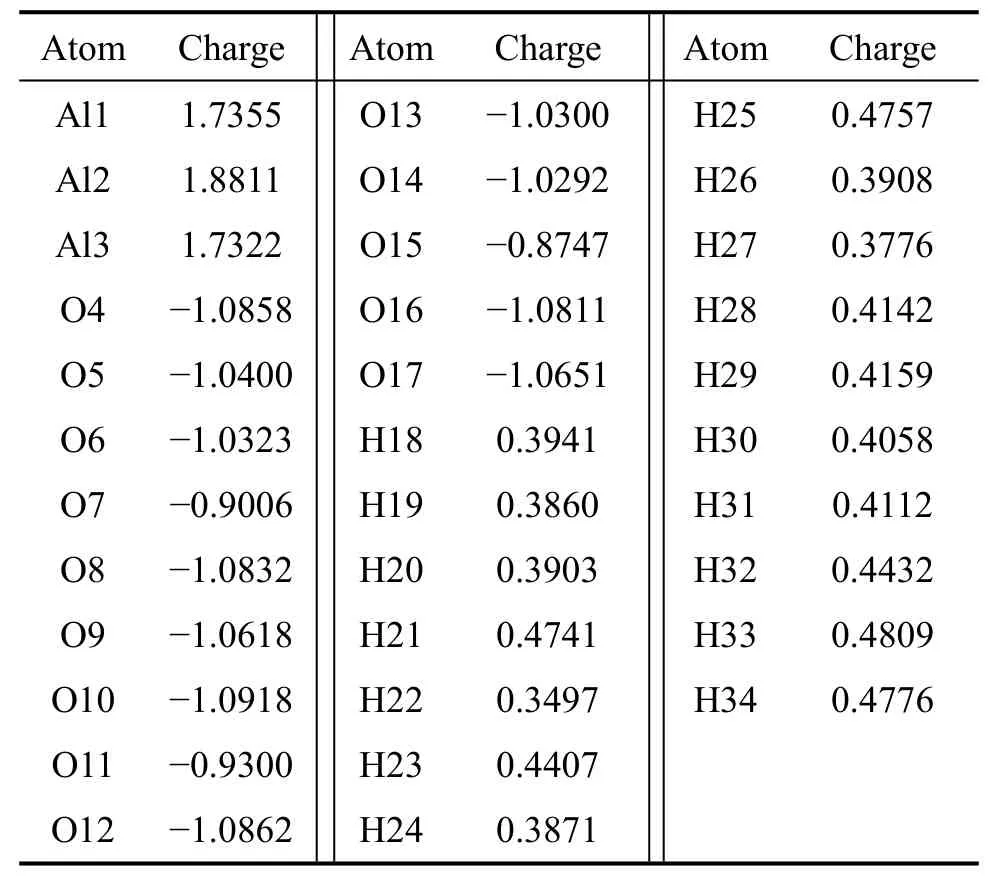
表3 Al3-B基团的电荷分布Table 3 Total atomic net-charge forAl3-B cluster
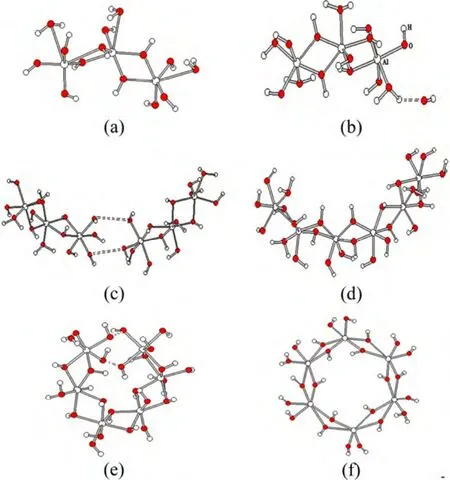
图3 反应各据点的几何构型示意图Fig.3 Schematic diagrams of optimized geometries of various species:(a)Al3-B cluster;(b)IM1;(c)TS1;(d)IM2;(e)TS2;(f)[Al6(OH)22(H2O)2]4-
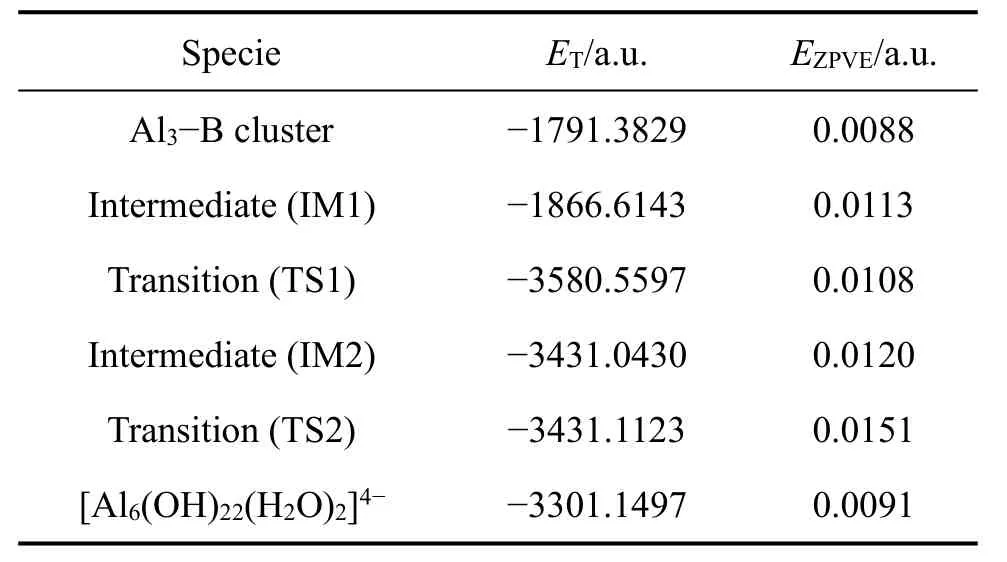
表4 各种物质的零点振动能和单点能Table 4 Zero-point vibration energy and total energy of species under DFT/BLPY/DNP level
2.4 反应通道的设计
通过对Al3-B基团活性部位和—OH基团的振动频率分析可知,铝酸根聚合离子端基上的—OH基团易参与质子化或去质子化反应。过饱和中等浓度铝酸钠溶液自发成核时,铝酸根离子之间经过配位体上的质子转移而发生相互聚合,即羟自由基可与Al3-B基团端基上OH2配位体的H结合发生系列反应,如图4所示。图4中反应(2)为Al3-B基团端基上的OH2中一个H与带有单电子的羟自由基结合。从反应势能面的能量信息得知:生成物处于能量的最低点,但对其进行力分析时,总存在多个负值,可以推断该物质为不稳定的中间产物。当端基上OH2连接一个带单电子的羟自由基时,该自由基夺去一个氢形成水分子,从而使该端基上OH2失去一个氢原子和一对孤电子对,因此,该基团迅速进行下一步反应。反应(3)表示有空轨道的—OH基团与另—个Al3-B基团端基上的OH结合成键,使两个铝酸根离子在终端形成桥连。含有[—HO------OH—]的生成物在反应势能面上处于另一个能量低点,但通过BLYP/DNP水平下的振动频率分析得知,该物质为反应过渡态。反应(4)是两个[—HO------OH—]与相连的Al原子发生结构重组,从第一过渡态中脱去H2O2,使铝酸根离子形成稳定的桥连。同时,通过类似的分析可以确认第二中间物质。同样地,当聚合体铝酸根离子另一端基上的OH2经自由基激活后,会发生相同的反应,从而形成了首尾相连的六元环基团。该六元环聚合离子容易与水合钠离子发生质子交换作用,生成有利生长基元,最后叠合成晶体而析出。
同理,根据羟自由基在端基上的OH2中夺取氢原子的特性,对反应路径作PES计算。发现当同时在一个氧上脱氢时,反应的活化能高达210 kJ/mol,反应直接从过渡态转变为产物。理论上,该反应路径很难发生(如图5路径(4))。当羟自由基同时夺取不同端基上OH2的氢原子时,反应将遵从反应物→IM2→TS2→产物,其反应活化能为109 kJ/mol(见图5路径(3))。
为了对比羟自由基对Al3-B基团环合反应的影响,在DFT/BLYP/DNP水平下,计算了无自由基参与的Al3-B基团环合反应活化能。通过对反应过渡态的确认与单点能的精确计算,采用零点振动能校正后,计算反应的活化能约为178 kJ/mol,这与李洁[4]的计算结果(156 kJ/mol)相差不大。
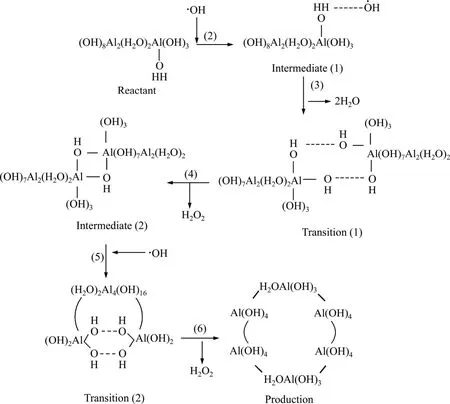
图4 Al3-B基团环合反应机理示意图Fig.4 Schematic diagrams showing possible reaction mechanism of Al3-B clusters polymerizing
2.5 反应势能面及机理
通过对反应通道的分析与计算,根据各物质的能量,作出在羟自由基存在下Al3-B基团环合成六元环状离子,再形成有利生长基元的势能剖面图(见图5)。图中路径(1)表示没有羟自由基参与反应,其活化能为178 kJ/mol;路径(2)表示由于羟自由基参与环合反应而改变了反应路径,反应活化能降低至109 kJ/mol,降低了约70 kJ/mol。反应路径(3)与(2)类似,只是当两个自由基同时进攻时,Al3-B基团直接转化为IM2态。路径(4)的活化能高达210 kJ/mol,该反应路径不可能进行。因此,该羟自由基参与Al3-B基团环合反应有两条可能的反应路径(路径(2)和(3)),且其活化能相同,为109 kJ/mol。

图5 Al3-B基团环合反应的势能面Fig.5 Schematic potential energy surface of reactions(R is reactant;P is product)
3 结论
1)Al3-B基团端基上OH2的H易与羟自由基(·OH)结合,使该部位成为羟自由基进攻的活性中心。
2)羟自由基参与Al3-B基团环合反应有两条可能的反应路径,其活化能为109 kJ/mol,比无自由基参与时降低约70 kJ/mol。
[1] LI Xiao-bin,WANG Dan-qin,ZHOU Qiu-sheng,LIU Gui-hua,PENG Zhi-hong.Concentration variation of aluminate ions during the seeded precipitation process of gibbsite from sodium aluminate solution[J].Hydrometallurgy,2011,106(1/2):93-98.
[2] ZHANG Ying,ZHENG Shi-li,DU Hao,XU Hong-bin,WANG Shao-na,ZHANG Yi.Improved precipitation of gibbsite from sodium aluminate solution by adding methanol[J].Hydrometallurgy,2009,98(1/2):38-44.
[3] 李小斌,赵东峰,王丹琴,阎 丽.铝酸钠溶液分解过程的理论及技术研究进展[J].中国有色金属学报,2011,21(10):2577-2593.LI Xiao-bin,ZHAO Dong-feng,WANG Dan-qin,YAN Li.Research progress in theory and technology ofgibbsite precipitation from sodium aluminate solution[J].The Chinese JournaI of Nonferrous Metals,2011,21(10):2577-2593.
[4] 李 洁.过饱和铝酸钠溶液结构及分解机理的研究 [D].长沙:中南大学,2002:86-110.LI Jie.Study on the struetural characteristies and decomposition mechanism of supersaturated sodium aluminate solution[D].Changsha:Central South University,2002:86-110.
[5] 吴争平,尹周澜,陈启元,李 洁.氢氧化铝有利生长基元[Al6(OH)18(H2O)6]n微观叠合的DFT计算[J].中南大学学报(自然科学版),2009,40(3):592-600.WU Zheng-ping,YIN Zhou-lan,CHEN Qi-yuan,LI Jie.DFT calculation on microcosmic combination of favorable growth unit of gibbsite[Al6(OH)18(H2O)6][J].Journal of Central South University(Science and Technology),2009,40(3):592-600.
[6] ZHANG Bin,LIJie,CHEN Qi-yuan,CHEN Guo-hui.Precipitation of Al(OH)3crystals from supersaturated sodium aluminate solution irradiated with ultrasonic sound[J].Minerals Engineering,2009,22(9/10):853-858.
[7] WU Yu-sheng,QU Yan-ping,ZHANG Lin-nan,LIU Mo.Effect of αkon aluminium trihydroxide crystallization from sodium aluminate soluntion under ultrasound[C]//Physical and Numerical Simulation of Material Processing VI,PTS 1 AND 2.Materials Science Forum.Switzerland:Transaction Technical Publications Limited,2012:364-369.
[8] 孙文乐,张 扬,马淑花,王月娇,丁 健,唐振华,郑诗礼.超声波强化铝酸钠结晶工艺[J].过程工程学报,2013,13(6):992-997.SUN Wen-le,ZHANG Yang,MA Shu-hua,WANG Yue-jiao,DING Jian,TANG Zhen-hua,ZHEN Shi-li.Crystallization process of sodium aluminate enhanced by ultrasonic wave[J].The Chinese Journal of Process Engineering,2013,13(6):992-997.
[9] 刘吉波,张牧群,尹周澜,张平民,陈启元.铝酸钠溶液性质对超声空化作用及种分过程超声强化的影响[J].中国有色金属学报,2004,14(6):1047-1052.LIU Ji-bo,ZHANG Mu-qun,YIN Zhou-lan,ZHANG Ping-min,CHEN Qi-yuan.Effectofphysicalpropertiesofsodium aluminate solution on ultrasonic cavitation and enhancement during precipitation process[J].The Chinese JournaI of Nonferrous Metals,2004,14(6):1047-1052.
[10]HU Yu-fei,ZHANG Zhu-jun,YANG Chun-yan.Measurement of hydroxyl radical production in ultrasonic aqueous solutions by a novel chemiluminescence method[J].Ultrasonics Sonochemistry,2008,15(5):665-672.
[11] 张牧群,尹周澜,陈启元.铝酸钠溶液中超声诱致自由基的检测[J].中国稀土学报,2004,22(z1):207-211.ZHANG Mu-qun,YIN Zhou-lan,CHEN Qi-yuan.Inspection of the free radicals in sodium aluminate solution coursed by ultrasound[J].Journal of The Chinese Rare Earth Society,2004,22(z1):207-211.
[12] 尹周澜,花书贵,张牧群,李 洁,陈启元.超声场强化铝酸钠溶液种分过程的理论研究[J].中国稀土学报,2004,22(z1):188-191.YIN Zhou-lan,HUA Shu-gui,ZHANG Mu-qun,LI Jie,CHEN Qi-yuan.Theoretical research on the precititation of sodium aluminate solutions enhanced by ultrasound[J].Journal of The Chinese Rare Earth Society,2004,22(z1):188-191.
[13]朱龙观.高等配位化学[M].上海:华东理工大学出版社,2009:280-310.ZHU Long-guan. Advanced coordination chemistry[M].Shanghai:East China University of Science and Techmology Press,2009:280-310.
[14]KUBICKI J,APITZ S.Molecular cluster models of aluminum oxide and aluminum hydroxide surfaces[J]. American Mineralogist,1998,83:1054-1066.
[15]STEMMLER K,vonGUNTEN U.OH radical-initiated oxidation of organic compounds in atmospheric water phases:part 2.Reactions of peroxyl radicals with transition metals[J].Atmospheric Environment,2000,34(25):4253-4264.
[16]CABRALC,GUEDESRC,COSTACABRALBJ,MARTINHO SIMÕES J A.The hydration of the OH radical:Microsolvation modeling and statistical mechanics simulation[J].The Journal of Chemical Physics,2003,119(14):7344-7355.
[17]GOVIND N,PETERSEN M,FITZGERALD G,KING-SMITH D,ANDZELM J.A generalized synchronous transit method for transition state location[J].Computational Materials Science,2003,28(2):250-258.
[18]PARADAS M,CAMPAÑA A G,JIMÉNEZ T,ROBLES R,OLTRA J E,BUÑUEL E,JUSTICIA J,CÁRDENAS D J,CUERVA J M.Understanding the exceptional hydrogen-atom donor characteristics of water in Ti(Ⅲ)-mediated free-radical chemistry[J].Journal of the American Chemical Society,2010,132(36):12748-12756.
