金属-有机骨架材料制备及其吸附净化挥发性有机物应用
任柳芬,陈曙光,杨 坤*
(1.浙江大学环境科学系,杭州 310058; 2.浙江省有机污染过程与控制重点实验室,杭州 310058)
挥发性有机化合物(Volatile Organic Compounds,VOCs)由于排放量大、毒性高,是环境空气污染的主要污染物之一,已被世界各国列为优先控制污染物。根据世界卫生组织(WHO)的定义,挥发性有机化合物是指沸点介于50~260 ℃之间、室温下饱和蒸汽压超过133.32 Pa,常温下以气体形式存在于空气中的一类有机化合物[1],包含烷烃类、烯烃类、卤代烃类、芳香烃类、酯类、醛类等。在天然环境中,VOCs主要来自于海洋、土壤、植物等的散发[2-4]。人为排放是造成当前环境空气VOCs污染的主要原因,包括石化等工业行业有机废气排放、汽车尾气排放、农业废弃物不完全燃烧废气排放、烹饪油烟排放、家装涂料挥发等[5-6]。VOCs会刺激人的呼吸系统、中枢神经系统[7]、黏膜系统[8],造成慢性或急性中毒,甚至诱发癌症[9]。VOCs也是城市光化学烟雾的前驱物,可能形成毒性更大的二次污染物[10]。扩散到平流层的卤代烃类VOCs还会破坏臭氧层,形成臭氧空洞[11]。
目前VOCs的控制净化方法主要有吸收法、吸附法、光催化、焚烧、冷凝以及生物降解等[12]。其中,吸附法是最常用且有效的方法之一,其关键是选择一种高效的吸附剂。目前常用的吸附剂主要有分子筛[13-14]、吸附树脂[15]、活性炭及其衍生物等[16-17]。通常,高效VOCs吸附材料具有高比表面积和大孔容的特征。金属有机骨架材料(Metal-Organic Frameworks,MOFs)是近20年快速发展起来的一类新型多孔材料。由于具有大的孔容及高比表面积,这类材料在催化[18]、气体储存与分离[19-20]及环境有害气体吸附[21-22]等方面的应用得到了广泛研究。因此,本论文概述了MOFs材料的发展历程,重点介绍了MOFs材料合成方法及其吸附VOCs的研究进展,并讨论了相关研究工作尚存在的科学技术问题和展望了未来的研究方向。
1 金属-有机骨架材料
金属-有机骨架材料又称多孔配位聚合物[23],是由含氧或含氮的有机配体与金属盐通过金属-配体络合作用自组装而成具有周期性网络结构的晶体。从微观视角看,金属-有机骨架材料先由金属盐在空间形成三维次级构筑单元(Secondary Building Units),再由有机配体将金属构筑单元通过配位键(甚至超分子作用)连接,从而形成具有永久孔隙度的空间有序网状结构[24]。因金属次级构筑单元和有机配体的多样性、两者配位位置的不同等原因,合成的MOFs材料具有立方、砖壁、金刚石、石英、梯状、格子等多种形状结构的骨架[25]。21世纪以来,MOFs合成呈现出飞速的发展态势(图1)[26],每年都有上千种MOFs材料被研发出来。由于其在气体吸附分离、多相催化、药物贮藏与缓释、光电磁等领域[27-34]都具有潜在应用前景,MOFs已经成为当前材料领域的研究前沿和热点之一(图2)。
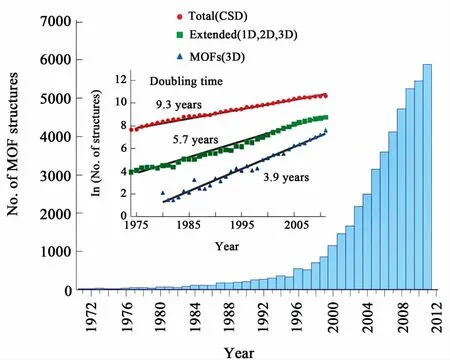
图1 1971~2011年收录于CSD(Cambridge Structural Database)中的MOFs结构统计图[26]Fig.1 MOFs structures reported in the Cambridge Structural Database(CSD) from 1971 to 2011[26]
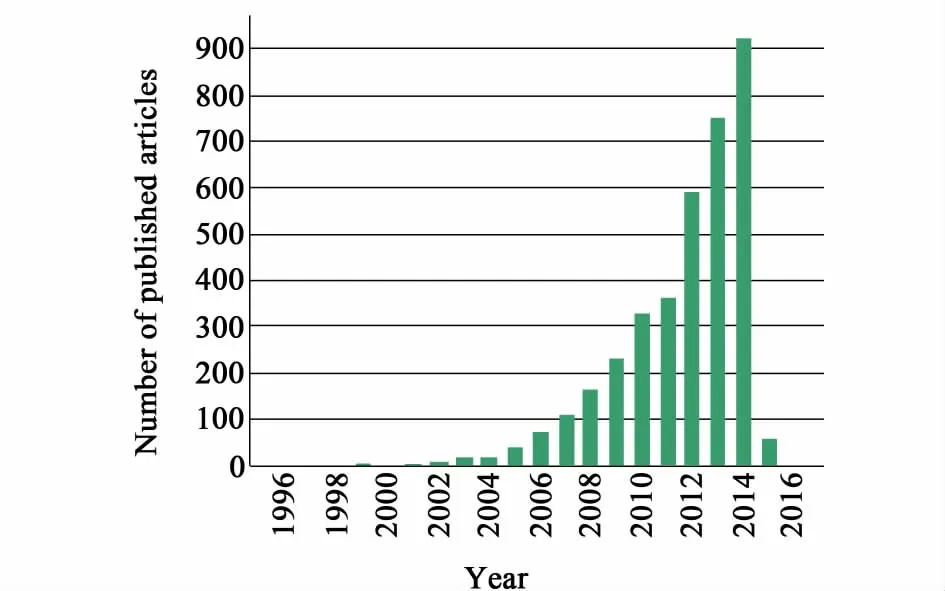
图2 Web of Science上以“MOFs”为主题关键词统计的出版文章数Fig.2 “MOFs” as keywords, the statistics number of published articles on Web of Science
金属-有机骨架材料的开发最早可以追溯到1706年发现的普鲁士蓝,其三维网状结构由Ludi等科学家于1977年才确定[35]。1959年,Kinoshita等[36]使用过渡金属络合物[Cu(adiponitrile)2]和硝酸根阴离子合成了具有三维网状结构的双己二腈硝酸亚铜结构晶体。这是有关MOFs合成的最早文献记载。但直到20世纪80年代末90年代初,随着“晶体工程”概念[37]和拓扑理论[38-39]在材料合成领域的引入,具有独特优良性质的金属-有机骨架材料才开始被研究者大量合成出来。1989年,Robson等根据拓扑理论设计并实验合成出了有金刚石型结构的金属-有机骨架材料CuI[C(C6H4·CN)4]BF4[40]和NMe4[CuZn(CN)4][41]。但这些材料的结构会随填充模板剂的移除而坍塌,且自身网络结构存在相互贯穿的现象,缺乏稳定的孔隙等结构功能特性[19,42-43]。
1995年,Yaghi团队发现用Co金属盐和刚性有机配体均苯三甲酸合成的MOFs在移除模板试剂后骨架结构仍能保持稳定,没有或仅有少量的网络结构发生相互贯穿或坍塌[44]。从此,MOFs合成开启了新纪元。随后,Yaghi团队又合成了许多种MOFs材料[45-47],其中最具有代表性的就是于1999年以Zn(NO3)2和对苯二甲酸为原料合成的MOF-5材料[47],其比表面积(N2吸附Langmuir比表面积最高达3 917 m2/g[48])和孔径(~0.8 nm)超过大部分传统多孔分子筛,成为MOFs发展历程上的里程碑。在MOF-5基础上,Yaghi团队合成了IRMOF(Isoreticular Metal-Organic Framework)系列材料(结构见图3)[27],发现通过改变二羧酸有机配体的长度及配体苯环上的取代基,能使合成的MOFs具有更大的孔径尺寸。其中,IRMOF-16有效孔径可达2.88 nm,是首个报道孔径尺寸达到中孔的MOFs材料[27]。随后,Yaghi等[49]和Ferey等[50]分别于2004年和2005年以Zn(NO3)2·6H2O与H3BTB(4,4′,4″-benzene-1,3,5-triyl-tribenzoic acid)为原料合成了Langmuir比表面积高达4 500 m2/g 的MOF-177金属-有机骨架材料和以Cr(NO3)3·9H2O与对苯二甲酸为原料合成了比表面积高达5 900 m2/g、内部尺寸达2.9~3.4 nm的MIL-101金属-有机骨架材料。Furukawa等[51]于2010年通过不断增长有机配体长度的方法合成的MOF-210是目前报道的比表面积最大的材料,其BET和Langmuir比表面积分别为6 240和10 400 m2/g。
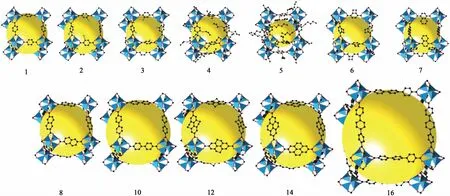
图3 MOF-5(IRMOF-1)及IRMOF-n(n=1~16)空间结构示意图[27]Fig.3 The spatial structure diagram of MOF-5(IRMOF-1) and IRMOF-n(n=1~16)[27]
根据除去客体分子后材料内部结构是否稳定,可以将配位聚合物分成三代[52]:第一代配位聚合物的结构靠客体分子支撑,移除客体分子后会发生不可逆的坍塌;第二代材料具有比较稳定、坚固的孔结构,在移除客体分子后不会发生结构坍塌,仍能保持原结构;第三代材料具有灵活可控的孔结构,当外界有光、电、客体分子等外界刺激的时候,材料孔道可以发生可逆性的转变。含多齿型羧基有机配体与金属离子桥接构成的MOFs材料多属于第二代多孔材料,而含氮杂环类有机配体与金属离子桥接构成的MOFs材料多属于第三代多孔材料。目前得到广泛研究具有应用前景的MOFs材料主要为骨架结构稳定的第二、三代配位聚合物材料。
2 金属-有机骨架材料制备
MOFs材料一般采用一步法在液相中合成。在纯溶剂或适当的混合溶剂中,金属盐和有机配体可以通过结构单元的自组装形成有序、网状结构的晶体骨架结构MOFs材料。决定和影响MOFs材料合成及结构性能的主要包括原材料与溶剂类型、合成反应条件和合成方法三方面因素。
2.1 原材料与溶剂类型
金属盐和有机配体是合成MOFs的主要原材料。几乎所有2到4价态的稳定态金属盐都可以成为合成MOFs材料的金属配体[53]。目前常用的金属配体包括过渡金属、碱金属、碱土金属、主族金属和稀土金属,如Zn[54]、Cu[55]、Ag[56]、Cd[57]、Co[58-59]、Pt[60]、Ni[61]和Cr[50]等。其中,Zn和Cr是目前合成高表面积和孔容MOFs的最主要金属配体[27,47,49-51,54]。根据与金属配位能力,多选择带有共轭体系的中性或带电负性有机分子作为有机配体,使得合成的MOFs材料具有较高的稳定性、结晶度和孔隙率。带正电的有机配体由于和金属配体配位能力弱,很少使用。有机配体应至少含有1个多齿型官能团,如 COOH、CS2H、NO2、SO3H和PO3H等,常用的有机配体包括多羧酸芳香有机物(如对苯二甲酸、均三苯甲酸、苯四羧酸等)、吡啶、多硫唑嘌呤杂环类分子(咪唑类、三唑类、四唑类、嘧啶和吡嗪以及它们的衍生物等)[49-50,53,62-64]。含有2个或2个以上多齿型官能团的有机配体,通常能与金属离子形成多种配位模式。以对苯二甲酸为例,在不同合成条件下,2个羧基的去质子化程度不同,可以形成图4所示几种不同的配位模式[65]。通常情况下,有机配体中参与配位作用的原子越多,所形成的MOFs骨架结构就越稳定。对有机配体进行改性和修饰,可以得到不同几何构型、不同长度和引入不同取代基多齿型官能团的有机配体,从而可能合成出具有更加稳定的结构和更大表面积等性能的MOFs材料[66]。此外,对于芳环和含氮杂环配体,环之间的π-π作用也可能影响骨架的结构[67]。

图4 羧基配位模式[65]Fig.4 Coordination models of carboxyl[65]
除了选择合适的有机配体和金属离子配体,溶剂的选择对MOFs合成也是至关重要。常用的溶剂包括水、有机胺类物质以及乙醇等有机溶剂[68],一般为单一纯物质溶剂或者几种溶剂的混合物。溶剂能促进合成反应的顺利进行。如,Friscic等[69]采用氧化锌和反丁烯二酸为原料,在不使用任何溶剂的条件下合成反应无法进行,而当使用水和乙醇作为溶剂时,则得到了4种产物。多数有机配体是固体,金属盐在碱性情况下容易形成沉淀。溶剂在合成反应中主要起溶解作用,可以促进有机配体分子和金属离子的相互接触及反应。例如,在金属离子和苯羧酸类有机配体配位前,加入碱性有机胺类溶剂不仅可以使苯羧酸类有机配体的羧基功能团去质子化[57,70],而且可以通过氨基的络合作用降低金属离子的沉淀形成[71],从而提高有机配体和金属离子溶解度及配位反应活性。目前,使用较多的去质子化碱性有机胺类物质有三乙胺 (TEA)、N, N-二甲基甲酰胺(DMF)、N,N-二乙基甲酰胺(DEF)、N-甲基吡咯烷酮等[72-73]。近年来也发现可以在水中加入氢氧化钠等强碱去质子化[74]。使用不同性质的溶剂,不仅能增加合成线路的多样性,而且由于其极性和pH值不同,对有机配体的去质子化程度不同,使得配体与金属离子的配位方式发生改变,从而可以合成不同骨架结构的MOFs材料[75]。例如,Vaidhyanatha等[76]使用氧化锌(ZnO)和草酸(H2C2O4)为原料,分别以1,3-二氨基丙烷(1, 3-diaminopropane,DAP)和N-丙胺(N-propylamine,PA)为溶剂,合成出了Zn2O15C9N2H18和Zn2O15C12N2H26两种不同结构的MOFs材料。Tian等[77]使用Zn2+和咪唑配体为原料,分别以N,N-二甲基甲酰胺(N, N-dimethylformamide,DMF)、N,N-二甲基乙酰胺DMA(dimethylacetamide,DMA)、N,N-二乙基甲酰胺(diethylformamide,DEF)、N-甲基吡咯烷酮(N-methylpyrrolidone,NMP)等为溶剂,合成出了7种不同结构的MOFs材料。混合溶剂经常用于调节体系的极性,改变溶剂与有机配体间的相互作用,进而调节MOFs材料的骨架结构[75]。例如,Friscic等[69]研究发现:当水和乙醇的质量比例为0∶1时,反应产物为Zn(C4H2O4);当水和乙醇的质量比例为1∶1时,反应产物为Zn(C4H2O4)·2H2O;而当水和乙醇的质量比例为1∶0时,反应产物为Zn(C4H2O4)·5H2O和Zn(C4H2O4)·4H2O。此外,非水性溶剂也能作为配体与金属离子进行配位,或与有机配体形成氢键等弱相互作用,存在于合成的MOFs材料骨架中。通过加热或真空干燥的方法,可以破坏溶剂分子与材料骨架形成的弱相互作用但不破坏MOFs材料骨架结构,从而使得溶剂分子以气体形式散逸出来,增大MOFs材料的孔隙和孔容[78-79]。近年来,也有研究者使用离子液体(ILs)和低温共熔溶剂(DESs)做为溶剂合成MOFs材料[80-82]。离子液体是在常温下即为液态的低温熔融盐,无挥发性能,具有良好导电性能和溶剂化属性,热稳定性高,不易燃烧,可溶解多种固体盐和有机配体等优点[83-84]。低温共熔溶剂是由2个或以上化合物混合组成的熔点低于任何一个组分的物质,表现出来的溶剂性质与离子溶液非常相似[80-82]。与离子液体相比,低温共熔溶剂更容易提取产物,成本更低。研究者以氯化胆碱/二甲脲混合低温共熔物为溶剂,用超声法合成了HKUST-1[82]。
2.2 合成条件
2.3 合成方法
MOFs材料合成方法主要有溶剂扩散法、水(溶剂)热法、微波辅助合成法、超声合成法、机械合成法、电化学法及近年发展起来的干凝胶转化法等[95]。不同的合成方法得到的MOFs材料性质各异,包括颗粒大小、孔径分布、孔径大小及晶体形态等都会受到一定影响。溶剂扩散法是将金属盐、有机配体和溶剂按一定比例混合,置于1个小玻璃瓶中,将此玻璃瓶放入1个加有去质子化溶剂的大玻璃瓶中,封住大瓶瓶口,静置反应一段时间生成MOFs晶体的方法[96-99]。该方法可以通过调整溶剂的扩散速度、改变配体和金属离子的浓度、调节溶剂的极性等方式控制反应物质的接触程度达到控制晶核生长速度和效率的效果[96]。目前通过溶剂扩散法可成功合成MOF-5、MOF-74、MOF-177、HKUST-1、ZIF-8等多种典型MOFs材料[97-99]。溶剂扩散法反应条件温和,易获得高质量单晶材料,但耗时太长、产率低,并且要求反应物溶解性好(如室温下就可以溶解)。水(溶剂)热法是将金属盐、有机配体和溶剂按一定比例加入到密封反应容器(如带有聚四氟衬里的不锈钢反应器或玻璃试管)中加热反应结晶生成MOFs材料的方法[71,100]。水(溶剂)热反应温度一般在100~200 ℃。随着温度升高,溶剂在密封容器中挥发可提高容器内压力,一些难溶或不溶的反应物溶解度会在密封容器的高温高压下增大,从而加快反应速度和效率。水(溶剂)热法反应时间较短,并且解决了反应物室温下溶解度和反应活性低的问题。因此,溶剂热法合成MOFs材料具有晶体产率高、设备简单、节省能量等优点,已成为近年来最常使用的制备方法[71]。微波辅助合成法与水(溶剂)热法相比较,只是一种加热方式的改变。由于微波可以通过电磁波辐照对溶液(反应物)直接反应加热,因此可以均匀、迅速地加热,使反应有更高的成核率,结晶速率快,生成的MOFs材料孔径分布集中、纯度高[101]。微波辅助合成MOFs的反应温度一般都在100 ℃以上,反应时间控制在1 h以内,超过最优的反应时间反而会造成晶体损坏[102]。和溶剂热法相比,微波辅助合成法制备MOFs材料的时间明显缩短,晶体颗粒更小[25,103]。超声合成法是一种通过超声震荡促进金属和有机配体在溶剂中反应合成MOFs的方法,常用超声频率介于20~10 MHz之间。该方法的原理是高能超声在液体中能形成低压/高压循环交替区域并产生局部气体孔穴,在气体孔穴生长和破灭的过程中,不仅能提高对液体中颗粒物的分散,而且能形成局部高温(5 000 K)和高压(1×108Pa),导致快速的加热和冷却,从而促进MOFs合成反应的进行[104]。电化学合成法由BASF公司的研究者于2005年提出[105]。该方法通过导电液连接金属阳极和不溶性阴极反应介质,在金属阳极放出金属离子参与液相合成反应,常添加质子溶剂避免金属沉积在阴极。该方法的主要优点是合成过程中不用直接添加金属盐(可排除金属盐阴离子的影响)、可以持续运行、运行效率高,但合成过程中会产生H2,存在安全隐患。机械化学法是将配体与金属盐混合,在球磨机研磨下破碎分子推动化学转变合成MOFs的方法[106-107]。该方法最大的优势是无需溶剂,而且可以使用金属氧化物代替金属盐作为金属配体。干凝胶转化法是在水和挥发性胺的蒸汽环境下,金属盐和有机配体直接反应生成MOFs材料的方法。该方法具有废物排放少、反应体积和转化成均匀晶体的产率高等突出优势。目前,已有研究者用此方法合成了ZIF-8[108]和Fe-MIL-100[109]。
3 MOFs吸附净化挥发性有机物的应用研究
MOFs材料能够成为VOCs气体净化潜在优良吸附剂的一个重要特性是其具有巨大的比表面积和孔容。表1列出了典型MOFs吸附材料的比表面积和孔容等性质。
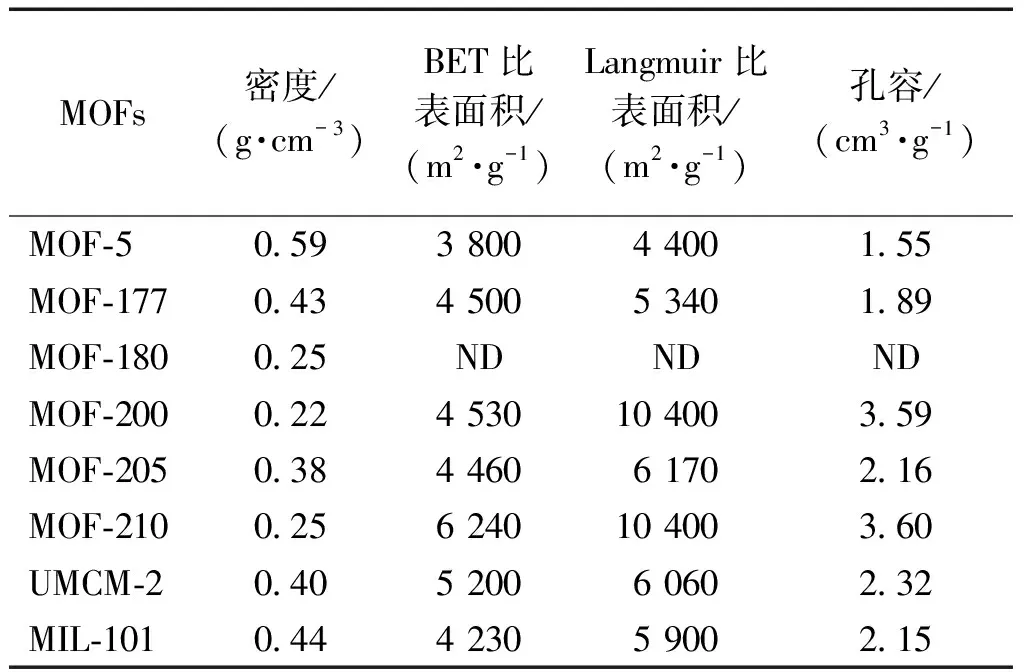
表1 典型MOFs吸附材料的比表面积和孔容等性质[51]
传统的多孔吸附材料,如活性炭和分子筛等的BET比表面积通常在100~1 000 m2/g[110]。近年来开发的KOH活化改性活性炭的BET比表面积可以达到3 000~4 000 m2/g[104,111]。与这些材料相比,MOF-210等典型MOFs吸附材料在比表面积上具有很大的优势(表1)。因此,典型MOFs材料对VOCs的吸附容量远大于现有的多孔吸附材料[28,47,102,112-113]。例如,1999年Yaghi等[47]研究发现MOF-5对CH2Cl2、CHCl3、C6H6、CCl4和C6H12等VOCs的饱和吸附量分别可达1 211、1 367、802、1 472和703 mg/g,是活性炭、沸石分子筛等传统吸附剂的4~10倍。他们进一步比较研究发现,MOF-74 和MOF-199对四氢噻吩、C6H6、CH2Cl2和环氧乙烷4种VOCs的吸附容量比沥青基活性炭(BPL)高一个数量级,最高可达59倍[112]。2007年,Ferey等[102]研究发现MIL-101对苯的吸附容量可达16.7 mmol/g (p/p0=0.5),远高于活性炭、HZSM-5分子筛以及介孔硅SBA-15。我们课题组研究也发现,MIL-101对丙酮、苯、甲苯、乙苯、对二甲苯、邻二甲苯及间二甲苯的吸附量分别达到1 291、1 291、1 096、1 105、727、758 和1 067 mg/g,远高于现有分子筛、吸附树脂、活性炭等对这些VOCs吸附容量的报道数据[113]。MOFs骨架上存在的不饱和金属配位点以及孔道结构上存在的疏水基团和亲水基团数量都会影响其对VOCs的吸附容量[68,112]。有机配体修饰上—Br,—NH2,—OC3H7,—OC5H11等功能性基团也可以增加合成的MOFs材料对VOCs及其它气体的吸附和选择性[115]。除了吸附容量大外,MOFs材料能够成为VOCs气体净化潜在优良吸附剂的另一个优点是吸附速率快。2006年,Stallmach等[114]用核磁共振检测方法研究发现,在相同温度下,正己烷和苯在MOF-5上的有效自扩散系数仅略小于它们在纯净液体中的扩散系数,扩散能力很强。2007年,Ferey等[102]研究发现MIL-101(40)和MIL-101(CH) 对苯完全吸附的时间仅需253和300 s,比活性炭(500 s)快1倍。与传统吸附材料(如二氧化硅SBA-15、MCM-41)相比,MIL-101等MOFs材料在气体相对压力很低的情况下仍能对VOCs有很高的吸附量和吸附速率[115],表明它们在环境中低浓度VOCs吸附净化处理上有很大的应用前景。
MOFs材料对VOCs的主要吸附机制为微孔填充,吸附容量和吸附速率均由MOFs材料的孔径尺寸和VOCs分子大小决定[113,116-119]。我们课题组研究发现,MIL-101和MOF-177对丙酮、苯、甲苯、乙苯、对二甲苯、邻二甲苯及间二甲苯的吸附体积容量与分子横截面积呈负相关(图5),表现出明显的分子尺寸筛选效应[113,118]。Yaghi等[117]研究发现,随着CH2Cl2(0.4 nm)、C6H6(0.58 nm)、CCl4(0.6 nm)和C6H12(0.62 nm)分子尺寸增大,MOF-11对其吸附速率逐渐减小。Trung等研究也发现短链的烷烃在MIL-100和MIL-101上的吸附和脱附都快于长链烷烃[119]。除了VOCs分子的尺寸大小外,VOCs分子形状(如二甲苯上甲基的排列方式)引起的其进入MOFs材料孔隙方式改变也会影响吸附[117]。例如,我们课题组研究发现,丙酮、苯、甲苯、乙苯及对二甲苯以尺寸最小的截面进入MIL-101材料孔隙,而间二甲苯和邻二甲苯则是以尺寸最大的截面进入孔隙。与对二甲苯相比,间二甲苯和邻二甲苯的2个甲基间存在一定倾斜角度,会从空间上阻碍间二甲苯和邻二甲苯分子进入空隙,从而造成它们吸附体积相近但小于以线性形状排列甲基的对二甲苯以及甲苯和乙苯(图6)[113]。基于孔填充吸附机制,MOFs材料不能吸附分子尺寸大于其孔径的VOCs。由于MOFs材料孔径通常集中于微孔(<2 nm,目前报道唯一能达到中孔的IRMOF-16有效孔径为2.88 nm)[28],因此MOFs材料只能适用于小分子VOCs化合物吸附。
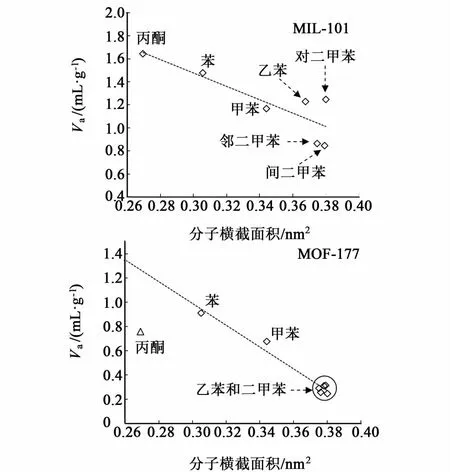
图5 MIL-101[113]和MOF-177[118]对VOCs的吸附体积与VOCs分子横截面积的关系Fig.5 Volume capacity (Va) of VOCs sorption on MIL-101[113] and MOF-177[118] versus their molecular cross-sectional areas

图6 乙苯、对二甲苯、邻二甲苯及间二甲苯进入MIL-101孔隙的示意图[113]Fig.6 Scheme of ethylbenzene, p-xylene, o-xylene and m-xylene entering into MIL-101 pores[113]
环境中VOCs通常共同存在,而且也与气态水分子(湿度)共存。研究发现,湿度会显著抑制MOFs对VOCs的吸附,其主要机理为气态水分子与VOCs分子间会产生竞争吸附[91,120-121]。Zhao等研究发现,当相对湿度从13%增加到34%,HKUST-1对苯的吸附去除率从94.7%下降至72.9%[120]。我们研究也发现[88],随着相对湿度从0 增加到90 %,苯在MIL-101上的饱和吸附量从937.4 mg/g下降到649.9 mg/g[见图7a)]。当相对湿度大于54% 时,苯饱和吸附量随相对湿度增加其降低的程度逐渐减缓[见图7a)]。在相对湿度为70% 和90 % 时,苯的饱和吸附量基本保持不变,为0湿度时苯在 MIL-101上饱和吸附量的68.6%,说明MIL-101在高湿度条件下对苯仍具有很大的吸附容量,可以在高湿度环境中吸附净化VOCs[88]。此外,我们研究发现,湿度主要抑制高浓度VOCs吸附,降低MIL-101对苯的吸附容量,对低浓度苯的吸附抑制很小[见图7b)][88]。这可能是由于MOFs孔隙表面同时存在疏水性点位和亲水性点位造成的结果:低浓度VOCs分子优先吸附在MOFs孔隙表面的疏水性点位上,随着VOCs浓度增加,VOCs分子逐渐会吸附到MOFs孔隙表面的亲水性点位上并占据全部孔隙空间;而气态水分子只能吸附在MOFs孔隙表面的亲水性点位上,从而和高浓度VOCs分子在亲水性点位上形成竞争。共存VOCs分子间也会在MOFs孔隙产生竞争吸附[88,122-123]。共存VOCs分子(如苯与甲苯)在MOFs(如MIL-101)孔隙上的竞争不仅会降低它们在高浓度时的吸附容量,而且会降低它们在低浓度时的吸附量[88]。这可能是VOCs分子都能优先吸附在MOFs孔隙表面的疏水性点位上从而产生竞争所致。该竞争吸附行为可以用理想吸附理论(Ideal Adsorption Theory, IAT)进行预测[88]。当吸附达到饱和时,共存VOCs(以及气态水分子)在MOFs材料上的吸附体积容量总和基本保持不变[88],符合孔填充吸附机制[120,124]。

图7 相对湿度(RH)对苯在MIL-101上饱和吸附量及吸附等温线的影响[88]Fig.7 Variation of adsorption capacity and isotherms of benzene on MIL-101 with relative humidity (RH)[88]
4 总结与展望
MOFs材料具有巨大的比表面积和孔容。已有研究表明,MOFs材料与传统吸附材料相比,对VOCs不仅有很高的吸附量、很快的吸附速率,而且湿度对其吸附低浓度VOCs的影响较小。因此,MOFs材料是一种新型的潜在优良吸附材料,在VOCs吸附净化领域具有广阔的应用前景。但是,MOFs材料现有研究成果要真正应用到VOCs吸附净化工程,尚有很多限制。
首先,现已发现的具有高表面积和孔容MOFs材料合成的原材料类型无法满足实际工程的需要。目前合成的高表面积和孔容MOFs材料的金属配体主要为Zn和Cr离子,这些金属离子具有很高的毒性,在合成生产、使用和最终处置过程中造成环境污染和健康危害。因此,需要以相对无毒的Ca、Mg、Fe和Al等金属离子为配体,开发高表面积和孔容的MOFs材料。部分MOFs材料如MOF-177和MOF-210的有机配体尚未工业化生产,无法大量购买并导致价格成本高昂。因此,研究价廉易得工业化生产的有机配体合成开发高表面积和孔容MOFs材料也是今后需要努力的方向。
其次,现有MOFs材料的合成方法条件很难工业化和规模化生产。现有合成方法不仅反应产率低,而且通常需要稀溶液低浓度反应合成才能得到高质量均匀的MOFs晶体,导致单位体积反应容器合成效率低下,溶剂使用和损耗量大,工业化价值有待提高。因此,目前统计的成千上万种MOFs材料,大部分合成的规模仅用于实验室的结构表征分析,没有工业化生产。此外,溶剂扩散法等合成MOFs材料存在反应速率慢、耗时等问题,水热法、微波辅助合成法、超声合成法、电化学合成法等合成MOFs材料存在对生产设备要求高、现有设备反应容积小、耗电量大等问题,机械化学合成法存在合成MOFs产品不均匀等问题,这些问题也限制着MOFs材料的工业化生产。另外,MOFs材料合成的控制条件需要进一步研究精细化,提高合成MOFs材料性能的重现性。对于同一种MOFs材料,现有研究中,不仅不同实验室合成的产品性质千差万别,而且即使是控制相同制备条件下不同批次合成的MOFs材料性质也存在很大差异。
第三,现有高表面积和孔容MOFs材料的稳定性尚有待提高。低热稳定性是MOFs材料的一个明显缺陷,温度过高会导致骨架结构的坍塌,大多数MOFs最高只能承受300~400 ℃,很少有能耐受500 ℃以上高温的MOFs材料。很多MOFs材料如MOF-177不能耐受湿度的影响,在接触空气一段时间后,其骨架结构就会坍塌。因此,研究高表面积和孔容MOFs材料在高温、高湿、酸碱及有机溶剂环境下的稳定性是今后工作的重要方面。
最后,现有高表面积和孔容MOFs材料对VOCs的吸附应用研究成果尚很欠缺。合成的MOFs材料通常为粉体材料,其要应用到吸附工程,还需要研究其黏结造粒成型方法,提高其在工程使用中的分离回收和避免粉体材料流失损失。现有研究对MOFs材料吸附VOCs的容量、速率及吸附机制和竞争影响已做了一些探索,但对吸附后MOFs材料的再生回收方法尚未有研究。此外,现有研究的VOCs主要集中在苯系物和烷烃,对其它VOCs如醛酮类等的研究尚有待进一步完善。除了气态VOCs的吸附研究,MOFs对水中VOCs的吸附净化应用可行性也需要开展研究[102,125-126]。
参考文献:
[1]WHO. Indoor air quality organic pollutants. Euro reports and studies No. 111[S]. 1989
[2]Barletta B, Meinardi S, Sherwood R F,etal. Volatile organic compounds in 43 Chinese cities[J]. AtmosEnviron, 2005, 39(32): 5 979-5 990
[3]闫雁, 王志辉, 白郁华, 等. 中国植被VOC排放清单的建立[J]. 中国环境科学, 2005, 25(1): 110-114
Yan Yan, Wang Zhihui, Bai Yuhua,etal. Establishment of vegetation VOC emission inventory in China[J]. China Environmental Science, 2005, 25(1): 110-114(in Chinese)
[4]Wang Z, Bai Y, Zhang S. A biogenic volatile organic compounds emission inventory for Beijing[J]. Atmos Environ, 2003, 37(27): 3 771-3 782
[5]王宝庆, 马广大, 陈剑宁. 挥发性有机废气净化技术研究进展[J]. 环境污染治理技术与设备,2003, 4(5): 47-51
Wang Baoqing, Ma Guangda, Chen Jianning. Development in research of technology for purifying volatile organic compounds from exhaust gases[J]. Techniques and Equipment for Environmental Pollution Control, 2003, 4(5): 47-51(in Chinese)
[6]Jones A P. Indoor air quality and health[J]. Atmos, Environ,1999, 33: 4 535-4 564
[7]Wolkoff P, Wilkins C K, Clausen P A,etal. Organic compounds in office environments-sensory irritation, odor, measurements and the role of reactive chemistry[J]. Indoor Air, 2006, 16: 7-19
[8]Bernstein J A, Alexis N, Bacchus H,etal. The health effects of nonindustrial indoor air pollution[J]. J Allergy Clin Immun, 2008, 121: 585-591
[9]Cometto-Muniz J E, Cain W S, Abraham M H. Detection of single and mixed VOCs by smell and by sensory irritation[J]. Indoor Air, 2004, 14: 108-117
[10]林立, 鲁君, 马英歌, 等. 国内外VOCs排放管理控制历程[J]. 环境监测管理与技术, 2011, 23(5): 12-16
Lin Li, Lu Jun, Ma Yingge,etal. Reviews of VOCs control at home and abroad[J]. The Administration and Technique of Environmental Monitoring, 2011, 23(5): 12-16(in Chinese)
[11]德利克·埃尔森. 烟雾警报城市空气质量管理[M]. 北京: 科学出版社, 1999
[12]Parmar G R, Rao N N. Emerging control technologies for volatile organic compounds[J]. Crit Rev Environ Sci Technol, 2009, 39: 41-78
[13]Pires J A, Carvalho M B. Adsorption of volatile organic compounds in Y zeolites and pillared clays[J]. Micropor Mesopor Mat, 2001, 43: 277-287
[14]Cheng H, Reinhard M. Sorption of trichloroethylene in hydrophobic micropores of dealuminated Y zeolites and natural minerals[J]. Environ Sci Technol, 2006, 40: 7 694-7 701
[15]Liu P, Long C, Li Q,etal. Adsorption of trichloroethylene and benzene vapors onto hypercrosslinked polymeric resin[J]. J Hazard Mater, 2009, 166: 46-51
[16]Das D, Gaur V, Erma N. Removal of volatile organic compound by activated carbon fiber[J]. Carbon, 2004, 42: 2 949-2 962
[17]Gupta K N, Rao N J, Agarwal G K. Gaseous phase adsorption of volatile organic compounds on granular activated carbon[J]. Chem Eng Commun, 2015, 202: 384-401
[18]Lee J Y, Farha O K, Roberts J,etal. Metal-Organic framework materials as catalysts[J]. Chem Soc Rev, 2009, 38: 1 450-1 459
[19]Murray L J, Dinca M, Long J R,etal. Hydrogen storage in metal-organic frameworks[J]. Chem Soc Rev, 2009, 38(5): 1 294-1 314
[20]Li J, Sculley J, Zhou H. Metal-Organic frameworks for separations[J]. Chem Rev, 2012, 112(2): 869-932
[21]Li J, Kuppler R J, Zhou H. Selective gas adsorption and separation in metal-organic frameworks[J]. Chem Soc Rev, 2009, 38(5): 1 477-1 504
[22]Khan N A, Hasan Z, Jhung S H. Adsorptive removal of hazardous materials using metal-organic frameworks (MOFs): A review[J]. J Hazard Mater, 2013, 244/245: 444-456
[23]The IUPAC project “Coordination polymers and metal organic frameworks: Terminology and nomenclatureguidelines”[R]. Chemistry International. Jan-Feb 2010, 32 (1) and www.iupac.org/web/ins/2009-012-2-200
[24]Yaghi O M, Keeffe M O, Ockwing N W,etal. Reticular synthesis and the design of new materials[J]. Nature, 2003, 423: 705-714
[25]Kitagawa S, Kitaura R, Noro S. Functional porous coordination polymers[J]. Angew Chem Int Ed, 2004, 43(18): 2 334-2 375
[26]Furukawa H, Cordova K E, Yaghi O M,etal. The chemistry and applications of metal-organic frameworks[J]. doi:10.1126/science, 1230444
[27]Llewellyn P L, Bourrelly S, Serre C,etal. High uptakes of CO2and CH4in mesoporous metal-organic frameworks MIL-100 and MIL-101[J]. Langmuir, 2008, 24: 7 245-7 250
[28]Eddaoudi M, Kim J, Rosi N,etal. Systematic design of pore size and functionality in isoreticular MOFs and their application in methane storage[J]. Science, 2002, 295: 469-472
[29]Rosi N L, Eckert J, Eddaoudi M,etal. Hydrogen storage in microporous metal-organic frameworks[J]. Science, 2003, 300: 1 127-1 129
[30]Liu Y, Xuan W, Cui Y. Engineering homochiral metal-organic frameworks for heterogeneous asymmetric catalysis and enantioselective separation[J]. Adv Mater, 2010, 22(37): 4 112-4 135
[31]Allendorf M D, Abauer C. Luminescent metal-organic frameworks[J]. Chem Soc Rev, 2009, 38(5): 1 330-1 352
[32]Rosseinsky M J. Recent developments in metal-organic framework chemistry: Design, discovery, permanent porosity and flexibility[J]. Micropor Mesopor Mat, 2004, 73(1/2): 15-30
[33]Kurmoo M. Magnetic metal-organic frameworks[J]. Chem Soc Rev, 2009, 38(5): 1 353-1 379
[34]Meek S T, Greathouse J A. Metal-Organic frameworks: A rapidly growing class of versatile nanoporous materials[J]. Adv Mater, 2011, 23(2): 249-267
[35]Buser H J, Schwarzenbach D, Petter W,etal. Crystal-Structure of Prussian blue-Fe4[Fe(CN)6]3·xH2O[J]. Inorg Chem, 1977, 16: 2 704-2 710
[36]Kinoshita Y, Matsubara I, Higuchi T,etal. The crystal structure of bis(adiponitrilo)-copper(I) nitrate[J]. Chem Soc Jpn, 1959, 32: 1 221-1 226
[37]Wells A F. Three dimensional nets and polyhedral[M]. New York: Raven Press, 1977
[38]Schmid G M. Crystal engineering in porous materials[J]. J Pure Appl Chem, 1971, 27: 647-651
[39]Wells A F. Structrual inorganic chemistry[M]. New York: Oxford University Press, 1983
[40]Hoskins B F, Robson R. Infinite polymeric frameworks consisting of 3 dimensionally linked rod-like segments[J]. J Am Chem Soc, 1989, 111: 5 962-5 964
[41]Hoskins B F, Robson R. Design and construction of a new class of scaffolding-like materials comprising infinite polymeric frameworks of 3-D-linked molecular rods-a reappraisal of the Zn(CN)2and Cd(CN)2structures and the synthesis and structure of the diamond-related frameworks [N(CH3)4][CuZn (CN)4] and Cu[4,4′,4″,4‴-tetracyano tetraphenylmethane] BF4·xC6H5NO2[J]. J Am Chem Soc, 1990, 112: 1 546-1 554
[42]Schnobrich J K, Koh K, Sura K N,etal. A framework for predicting surface areas in microporous coordination polymers [J]. Langmuir, 2010, 26: 5 808-5 814
[43]Chen B, Eddaoudi M, Hyde S T,etal. Interwoven metal-organic framework on a periodic minimal surface with extra-large pores[J]. Science, 2001, 291: 1 021-1 023
[44]Yaghi O M, Li G, Li H. Selective binding and removal of guests in a microporous metal-organic framework[J]. Nature, 1995, 378: 703-706
[45]Yaghi O M, Jernigan R, Li H L,etal. Construction of a new open-framework solid from 1,3,5-cyclohexanetri carboxylateand zinc(II) building blocks[J]. J Chem Soc, 1997: 2 383-2 384
[46]Eddaoudi M, Li H, Yaghi O M,etal. Design and synthesis of metal-carboxylate frameworks with permanent microporosity[J].Topic in Catalysis, 1999, 9: 105-111
[47]Li H, Eddaoudi M, Yaghi O M,etal. Design and synthesis of an exceptionally stable and highly porous metal-organic framework[J]. Nature, 1999, 402: 276-279
[48]Saha D, Wei Z, Deng S. Hydrogen adsorption equilibriumand kinetics in metal-organic framework (MOF-5) synthesized with DEF approach[J]. Sep Purif Technol, 2009, 64(3): 280-287
[49]Chae H K, Siberio-Perez D Y, Kim J,etal. A route to high surface area, porosity and inclusion of large molecules in crystals[J]. Nature, 2004, 427: 523-527
[50]Ferey G, Draznieks C M, Serre C,etal. A chromium terephthalate-based solid with unusually large pore volumes and surface area[J]. Science, 2005, 309: 2 040-2 042
[51]Furukawa H, Ko N, Go Y B,etal. Ultrahigh porosity in metal-organic frameworks[J]. Science, 2010, 329: 424-428
[52]Kitagawa S, Kondo M. Functional micropore chemistry of crystalline metal complex-assembled compounds[J]. Bull Chem Soc Jpn, 1998, 71(8): 1 739-1 753
[53]Corma A, García H, Xamena F X. Engineering metal organic frameworks for heterogeneous catalysis[J]. Chem Rev, 2010, 110 (8): 4 606-4 655
[54]Feng P, Bu X, Stucky G D. Hydrothermal syntheses and structural characterization of zeolite analogue compounds based on cobalt phosphate[J]. Nature, 1997, 388: 735-741
[55]Chui S S Y, Lo S M F, Charmant J P H,etal. A chemically functionalizable nanoporous material [Cu3(TMA)2(H2O)3]n[J]. Science, 1999, 283: 1 148-1 150
[56]Yan B, Ma R, Chu Z,etal. 2D Cationic metal-organic frameworks of Ag with mixed ligands (semi-rigid dipyridyl, 3-pmpmd, and diphosphine, dppe) [J]. J Inorg Organomet Polym Mater, 2010, 20: 809-815
[57]Habib H A, Sanchiz J, Janiak C. Magnetic and luminescence properties of Cu(II), Cu(II)4O4core, and Cd(II) mixed-ligand metal-organic frameworks constructed from 1, 2-bis(1, 2, 4-triazol-4-yl)ethane and benzene-1, 3, 5-tricarboxylate[J]. Inorg Chim Acta, 2009, 362: 2 452-2 460
[58]Chen J, Natarajan S, Thomas J M,etal. A novel open-framework cobalt phosphate containing a tetrahedrally coordinated cobalt(II) center: CoPO4·0.5 C2H10N2[J]. Angew Chem Int Edit, 1994, 33: 639-640
[59]Natarajan S,Neeraj S,Choudhury A,etal. Three-Dimensional open-framework cobalt(II) phosphates by novel routes[J]. Inorg Chem, 2000, 39: 1 426-1 433
[60]Szeto K C,Prestipino C,Lamberti C,etal. Characterization of a new porous Pt-containing metal-organic framework containing potentially catalytically active sites: local electronic structure at the metal centers[J]. Chem Mater, 2006, 19: 211-220
[61]Guillou N,Gao Q,Nogues M,etal. Zeolitic and magnetic properties of a 24-membered ring porous nickel(II) phosphate, VSB-1[J]. Comptes Rendus de I′Académie des Sciences-Series II C-Chemistry, 1999, 2: 387-392
[62]Hou K, Bai F, Xing Y,etal. A novel family of 3D photoluminescent lanthanide-bta-flexible MOFs constructed from 1,2,4,5-benzene tetracarboxylic acid and different spanning of dicarboxylate acid ligands[J]. Cryst Eng Comm, 2011, 13: 3 884-3 894
[63]Bux H, Liang F, Li Y,etal. Zeolitic imidazolate framework membrane with molecular sieving properties by microwave-assisted solvothermal synthesis[J]. J Am Chem Soc, 2009, 131: 16 000-16 001
[64]Aromí G, Barrios L A, Roubeau O,etal. Triazoles and tetrazoles: Prime ligands to generate remarkable coordination materials[J]. Coordin Chem Rev, 2011, 255: 485-546
[65]魏文英, 方键, 孔海宁, 等. 金属有机骨架材料的合成及应用[J]. 化学进展, 2005, 17: 1 110-1 115
Wei Wenying, Fang Jian, Kong Haining,etal. Synthesis and applications for materials of metallorganic frameworks[J]. Progress in Chemistry, 2005, 17: 1 110-1 115(in Chinese)
[66]Gadipelli S, Guo Z. Postsynthesis annealing of MOF-5 remarkably enhances the framework structural stability and CO2uptake[J]. Chem Mater, 2014, 26: 6 333-6 338
[67]Walton K S, Snurr R Q. Applicability of the BET method for determining surface areas of microporous metal-organic frameworks[J]. J Am Chem Soc, 2007, 129(27): 8 552-8 556
[68]Ferey G. Hybrid porous solids: Past, present, future[J]. Chem Soc Rev, 2008, 37: 191-214
[69]Friscic T, Fabian L. Mechanochemical conversion of a metal oxide into coordination polymers and porous frameworks using liquid-assisted grinding (LAG) [J]. Cryst Eng Comm, 2009, 11: 743-745
[70]Cabrera M F, Nicholson D M, Sumpte B G. Electronic structure and properties of isoreticular metal-organic frameworks: The case of M-IRMOF (M=Zn,Cd,Be,Mg, and Ca)[J]. J Chem Phys, 2005, 123: 1 247-1 252
[71]Kupplera R J, Timmonsb D J, Fang Q R,etal. Potential applications of metal-organic frameworks[J]. Coord Chem Rev, 2009, 253(23/24): 3 042-3 066
[72]Yaghi O M, Park K S, Ni Z,etal. Exceptional chemical and thermal stability of zeolitic imidazolate frameworks[J]. Proc Natl Acad Sci USA, 2006, 103: 10 186-10 191
[73]Mueller U, Schubert M, Teich F,etal. Metal-Organic frameworks-prospective industrial applications[J]. J Mater Chem, 2006, 16: 626-636
[74]Xu H, Su Z, Shao K,etal. A novel strong fluorescent three-dimensional supramolecular coordination polymer based on bridging terephthalate[J]. Inorg Chem Commun, 2004, 7: 260-263
[75]Loiseau T, Ludovic L L, Volkringer C,etal. MIL-96, a porous aluminum trimesate 3D structure on structed from a hexagonal network of 18-membered rings and trinuclearunits[J]. J Am Chem Soc, 2006, 128: 10 223-10 230
[76]Vaidhyanathan R, Natarajan S, Cheetham A K,etal. New open-framework zinc oxalates synthesized in the presence of structure-directing organic amines[J]. Chem Mater, 1999, 11: 3 636-3 642
[77]Tian Y, Zhao Y, Chen Z,etal. Design and generation of extended zeolitic metal-organic frameworks (ZMOFs): Synthesis and crystal structures of zinc(II) imidazolate polymers with zeolitic topologies[J]. Chem Eur J, 2007, 13: 4 146-4 154
[78]Wang X, Ma S, Sun D,etal. A mesoporous metal-organic framework with permanent porosity[J]. J Am Chem Soc, 2006, 128: 16 474-16 475
[79]Wang Z, Tanabe K K, Cohen S M. Accessing postsynthetic modification in a series of metal-organic frameworks and the influence of framework topology on Reactivity[J]. Inorg Chem, 2009, 48: 295-301
[80]Zhang J, Wu T, Chen S,etal. Versatile structure-directing roles of deep-eutectic solvents and their implication in the generation of porosity and open metal sites for gas storage[J]. Angew Chem Int Ed, 2009, 48: 3 486-3 490
[81]Lin Z, Slawin A M Z, Morris R E. Chiral induction in the ionothermal synthesis of a 3-D coordination polymer[J]. J Am Chem Soc, 2007, 129(16): 4 880-4 881
[82]Kim S H, Yang S, Kim J,etal. Sonochemical synthesis of Cu-3(BTC)(2) in a deep eutectic mixture of choline chloride/dimethylurea[J]. Bull Korean Chem Soc, 2011, 32: 2 783-2 786
[83]Biemmi E, Christian S, Stock N,etal. High-Throughput screening of synthesis parameters in the formation of the metal-organic frameworks MOF-5 and HKUST-l[J]. Micropor Meospor Mater, 2009, 117: 11l-117
[84]Li Z, Qin L, Xu T,etal. Ultrasonic synthesis of the microporous metal-organic framework Cu3(BTC)2at ambient temperature and pressure: An efficient and environmentally friendly method[J]. Mater Lett, 2009, 63: 78-80
[85]Yang G, Hou L, Ma L. Investigation on the prime factors influencing the formation of entangled metal-organic frameworks[J]. Cryst Eng Comm, 2013, 14: 2 561-2 578
[86]Chen B, Ma S, Zapata F,etal. Hydrogen adsorption in an interpenetrated dynamic metal-organic framework[J]. Inorg Chem, 2006, 45: 5 718-5 723
[87]Gerardin C, In M, Allouche L,etal. In situ pH probing of hydrothermal solutions by NMR[J]. Chem Mater, 1999, 11: 1 285-1 292
[88]孙茜. 金属-有机骨架材料(MIL-101)对典型挥发性有机物(VOCs)的吸附性能及机理[D]. 杭州: 浙江大学, 2013
[89]Forster P M, Burbank A R, Livage C,etal. The role of temperature in the synthesis of hybrid inorganic-organic materials: The example of cobalt succinates[J]. Chem Commun, 2004: 368-369
[90]Forster P M, Stoek N, Cheetham A K. A high-throughput investigation of the role of pH, temperature, eoneentration, and time on the synthesis of hybrid inorganie-organic materials[J]. Angew Chem Int Edit, 2005, 44(46): 7 608-7 611
[91]Livage C, Egger C, Ferey G. Hybrid open frameworks (MIL-n). Part 5-Synthesis and crystal structure of MIL-9: A new three-dimensional ferrimagnetic cobalt (II) carboxylate with a two-dimensional array of edge-sharing Co octahedra with 12-membered rings[J]. J Mater Chem, 1998, 8: 2 743-2 747
[92]Livage C, Egger C, Ferey G. Hybrid open networks (MIL-16): Synthesis, crystal structure, and ferrimagnetism of Co4(OH)2(H2O)2(C4H4O4)3·2H2O, a new layered cobalt (II) carboxylate with 14-membered ring channels[J]. Chem Mater, 1999, 11: 1 546-1 550
[93]Serre C, Millange F, Ferey G,etal. A route to the synthesis of trivalent transition-metal porous carboxylates with trimeric secondary building units[J]. Angew Chem Int Edit, 2004, 43: 6 286-6 289
[94]Li Z, Qiu L, Wang W,etal. Fabrication of nanosheets of a fluorescent metal-organic framework [Zn(BDC)(H2O)]n(BDC=1, 4-benzene dicarboxylate): Ultrasonic synthesis and sensing of ethylamine[J]. Inorg Chem Commun, 2008, 11: 1 375-1 377
[95]Stock N, Biswas S. Synthesis of metal-organic frameworks(MOFs): Routes to various MOF topologies, morphologies, and composites[J]. Chem Rev, 2012, 112: 933-969
[96]杨志. 新型金属-有机骨架化合物的合成、结构及其性能表征[D]. 长春: 吉林大学,2012
[97]Huang L, Wang H, Chen J,etal. Synthesis, morphology control, and properties of porous metal-organic coordination polymers[J]. Micropor Mesopor Mat, 2003, 58: 105-114
[98]Hunt D J, Yaghi O M. Room temperature synthesis of metal-organic frameworks: MOF-5, MOF-74, MOF-177, MOF-199, and IRMOF-0[J]. Tetrahedron, 2008, 64: 8 553-8 557
[99]Cravillon J, Muenzer S, Lohmeier S J,etal. Rapid room-temperature synthesis and characterization of nanocrystals of a prototypical zeolitic imidazolate framework[J]. Chem Mater, 2009, 21: 1 410-1 412
[100]Lee Y R, Kim J, Ahn W S. Synthesis of metal-organic frameworks: A mini review[J]. Korean J Chem Eng, 2013, 30(9): 1 667-1 680
[101]Kaye S S, Dailly A, Yaghi O M,etal. Impact of preparation and handling on the hydrogen storage properties of Zn4O(1,4-benzenedicarboxylate)(3)(MOF-5) [J]. J Am Chem Soc, 2007, 129(46): 14 176-14 177
[102]Jhung S H, Lee J H, Yoon J W,etal. Microwave synthesis of chromium terephthalate MIL-101 and its benzene sorption ability[J]. Adv Mater, 2007, 19: 121-124
[103]El-Shalawy I I, Uddin K, Miyazaki T,etal. Adsorption of ethanol onto phenol resin based adsorbents for developing next generation cooling systems[J]. Int J Heat Mass Tran, 2015, 81: 171-178
[104]Suslick K S. The sonochemical hot spot[J]. Acoust Soc Am,1991, 89 (4B): 1 885-1 886
[105]巴斯福股份公司. 结晶多孔金属有机骨架材料的电化学生产方法: 中国, 200480034679.0[P].2014-11-22
[106]Pichon A, Lazuen-Garay A, James S L. Solvent-Free synthesis of a microporous metal-organic framework[J]. Cryst Eng Comm, 2006, 8: 211-214
[107]Pichon A, James S L. An array-based study of reactivity under solvent-free mechanochemical conditions-insights and trends[J]. Cryst Eng Comm, 2008, 10: 1 839-1 847
[108]Shi Q, Chen Z, Song Z,etal. Synthesis of ZIF-8 and ZIF-67 by steam-assisted conversion and an investigation of their tribologicalbehaviors[J]. Angew Chem Int Ed, 2011, 50: 672-675
[109]Ahmed I, Jeon J, Khan N A,etal. Synthesis of a metal-organic framework, iron-benezenetricarboxylate, from dry gels in the absence of acid and salt[J]. Cryst Growth Des, 2012, 12: 5 878-5 881
[110]Zhang Z, Atkinson J D, Jiang B,etal. NO oxidation by microporous zeolites: Isolating the impact of pore structure to predict NO conversion[J]. Appl Catal B-Environ, 2015, 163: 573-583
[111]Liu X, Zhang C, Geng Z,etal. High-Pressure hydrogen storage and optimizing fabrication of corncob-derived activated carbon[J]. Micropor Mesopor Mat, 2014, 194: 60-65
[112]Britt D, Tranchemontagne D, Yaghi O M. Metal-Organic frameworks with high capacity and selectivity for harmful gases[J]. P Natl Acad Sci USA, 2008, 105: 11 623-11 627
[113]Yang K, Sun Q, Xue F,etal. Adsorption of volite organic compounds by metal-organic frameworks MIL-101: Influnce of molecular size and shape[J]. J Hazard Mater, 2011, 195: 124-131
[114]Stallmach F, Groger S, Yaghi O M,etal. NMR studies on the diffusion of hydrocarbons on the metal-organic framework material MOF-5[J]. Angew Chem Int Ed, 2006, 45: 2 123-2 126
[115]Trens P, Tanchoux N, Papineschi P M,etal. Confinements effects in MCM-41-type materials: Comparison of the energetics ofn-hexane and 1-hexene adsorption[J]. Micropor Mesopor Mat, 2005, 86: 354-363
[116]黄思思. 金属-有机骨架材料——MOF-5和MIL-101的合成及其对VOCs的吸附/脱附性能[D]. 广州:华南理工大学, 2010
[117]Chen B, Eddaoudi M, Yaghi O M,etal. Cu2(ATC)·6H2O: Design of open metal sites in porous metal-organic crystals (ATC:1,3,5,7-adamantane tetracarboxylate) [J]. J Am Chem Soc, 2000, 122: 11 559-11 560
[118]Yang K, Xue F, Sun Q,etal. Adsorption of volatile organic compounds by metal-organic frameworks MOF-177[J]. J Environ Chem Eng, 2013, 1(1): 713-718
[119]Trung T K, Ramsahye N A, Ferey G,etal. Adsorption of C5-C9 hydrocarbons in microporous MOFs MIL-100(Cr) and MIL-101(Cr): A manometricstudy[J]. Micropor Mesopor Mat, 2010, 134: 134-140
[120]Zhao Z, Wang S, Yang Y,etal. Competitive adsorption and selectivity of benzene and water vapor on the microporous metal organic frameworks (HKUST-1) [J]. J Chem Eng, 2015, 259: 79-89
[121]Xian S, Yu Y, Xiao J,etal. Competitive adsorption of water vapor with VOCs dichloroethane, ethyl acetate and benzene on MIL-101(Cr) in humid atmosphere[J]. RSC Adv, 2015, 5: 1 827-1 834
[122]Nicolau M P M, Barcia P S, Gallegos J M,etal. Single-and multicomponent vapor-phase adsorption of xylene isomers and ethylbenzene in a microporous metal-organic framework[J]. J Phys Chem C, 2009, 113: 13 173-13 179
[123]Gu Z, Yan X. Metal-Organic framework MIL-101 for high-resolution gas-chromatographic separation of xylene isomers and ethylbenzene[J]. Angew Chem Int Edit, 2010, 49: 1 477-1 480
[124]Bradley R H, Smith M W, Andreu A,etal. Surface studies of novel hydrophobic active carbons[J]. Appl Surf Sci, 2011, 257: 2 912-2 919
[125]Xiao Y, Yang Q, Liu D,etal. Computational design of metal-organic frameworks for aniline recovery from aqueous solution[J]. Cryst Eng Comm, 2013, 15: 9 588-9 595
[126]Huo S, Yan X. Facile magnetization of metal-organic framework MIL-101 for magnetic solid-phase extraction of polycyclic aromatic hydrocarbons in environmental water samples[J]. Analyst, 2012, 137: 3 445-3 451

