高含硫气藏元素硫溶解度预测新模型
李 洪,李治平,赖枫鹏,王 才,韦 青,张 航
(中国地质大学(北京) 能源学院,北京 100083)
高含硫气藏元素硫溶解度预测新模型
李 洪,李治平,赖枫鹏,王 才,韦 青,张 航
(中国地质大学(北京) 能源学院,北京 100083)
为了提高硫溶解度的预测精度,利用Brunner和Woll实验测得的86个硫溶解度数据,选取组分密度、硫化氢含量和油藏温度3个因素,运用统计学和多元回归理论,在Chrastll模型的基础上建立了3个参数的硫溶解度预测模型。并将该模型和已有的3个模型预测的86个硫溶解度实验数据进行了对比,结果表明本文模型的预测精度大幅度提高。利用该模型对乔海波实验条件下的硫溶解度进行预测,并与实验结果进行对比,进一步验证了该模型的可靠性。
高含硫气藏;硫溶解度;预测模型;酸性气体
高含硫气藏除了H2S具有的高腐蚀性和剧毒性以外,与常规气藏最大的差异在于硫的沉积。该类气藏在开采过程中,随着温度压力的降低,硫微粒在气相中的溶解度逐渐减小,在达到临界饱和态后将从气相中析出。地层中硫颗粒形成后,一部分随气流在多孔介质中运移,另一部分吸附沉积在孔喉表面,堵塞孔道,降低地层的孔隙度和渗透率[1]。因此,准确地预测硫溶解度的变化并及时根据实际情况调整开发策略,具有重要意义。
目前,确定元素硫溶解度的方法主要有实验法和计算法。国外早在1960年就开始研究硫的溶解性,主要的研究者有Kennedy和Wielend[2]、Roof[3]、Swift[4]、Brunner E[5-6]、Woll W[7]、P M Davis[8]、Chrastil[9]、Tomxej R A[10]、Roberts B E[11]和Adel M Elsharkawy[12]等。他们通过理论、实验以及对实验数据进行拟合对硫溶解度进行分析。国内从1993年开始研究硫的溶解度,主要研究者有谷明星[13]、钟太贤[14]、曾平[15]、杨学锋[16]、卞小强[17]等。
自从Roberts B E拟合得出了一套系数后,Chrastll模型就被国内外研究者广泛用于预测元素硫在混合酸性气体中的溶解度。然而,Roberts B E在拟合这套系数时并未说明其适用的温度、压力范围及气体组分条件,致使该套系数的应用具有一定的局限性。后来部分学者提出选取适当密度拐点的思想,分段求取不同密度范围内的模型系数值,但该方法也没有考虑到酸性气体H2S的含量,导致该模型求取的元素硫的溶解度与实验结果相差很大。本文利用Brunner和Woll实验测得的86个硫溶解度数据,重新拟合得到了预测元素硫溶解度的新模型,并对该模型的可靠性进行了验证。
1 Roberts模型的局限性
1982年,Josef Chrastil[9]基于气体组分缔合定律和热力学原理推导出了预测固体溶质硫溶解度的公式
(1)
式中:Cr为元素硫的溶解度,g/m3;ρ为酸性气体的密度,kg/m3;T为气藏温度,K;a,b,k为经验常数。
Roberts根据Chrastil提出的溶解度模型,并利用Brunner和Woll[5]的实验数据(见表1),拟合出了一套预测高压下含硫天然气中元素硫溶解度的系数,得到了硫在高压酸性天然气中溶解度经验公式
(2)

表1 Roberts B E拟合用实验体系
由于计算简单,且能连续关联元素硫在高含硫气体中的溶解度,公式(2)一经提出即得到了广泛应用。然而,该模型即使在拟和上述2组实验数据时也存在着较大的误差,并且未考虑组分的影响,即H2S含量对硫溶解度的影响,因此还需要进一步研究元素硫溶解度的计算模型。
2 硫溶解度新模型
国外学者Brunner和Woll在1980年通过实验分别测试了H2S与CH4、CO2及N2以不同比例组成的混合气体在不同温度和压力下的硫溶解度。本文利用其实验测得的86个硫溶解度数据,选取组分密度、硫化氢含量和油藏温度3个因素,运用统计学和多元回归理论,在Chrastll模型的基础上建立了3个参数的硫溶解度预测模型。本模型拟合用实验体系见表2。根据实验数据,在回归的过程中,发现压力为40 MPa时是一个分界点,通过回归得到压力以40 MPa为分界点的溶解度预测方程:
当压力小于40 MPa时
Cr=(x+232.736)5.663ρ2.518exp[-603.282/(1.159T-305.872)-40.654],
(3)
当压力大于或等于40 MPa时
Cr=x0.618ρ3.263exp[-1 001.7/(1.084T-240.61)-14.258]。
(4)
式中:Cr为元素硫的溶解度,g/m3;x为H2S在混合气体中的体积分数,%;ρ为酸性气体的密度,kg/m3;T为气藏温度,K。

表2 本模型拟合用实验体系
3 模型对比分析
3.1 样本数据对比
目前用于预测元素硫溶解度的模型有Brunner(1980)模型、Brunner(1988)模型和Roberts模型,都是在Chrastil提出的模型基础上通过实验数据建立的。为了将本文提出的模型与上述几个模型加以对比,对86个样本数据进行了计算。由于这86个样本数据的温度、压力和组分都各不相同,因此在此选取实验体系BW1中温度为373.15 K时的数据进行计算分析。图1、表3和表4给出了4种模型依据86个样本计算的元素硫溶解度值及其与实验数据的相对误差。从表3中可以看出,元素硫的溶解度预测精度由高到低为: 新模型>Brunner(1980)模型>Brunner(1988)模型>Roberts模型。
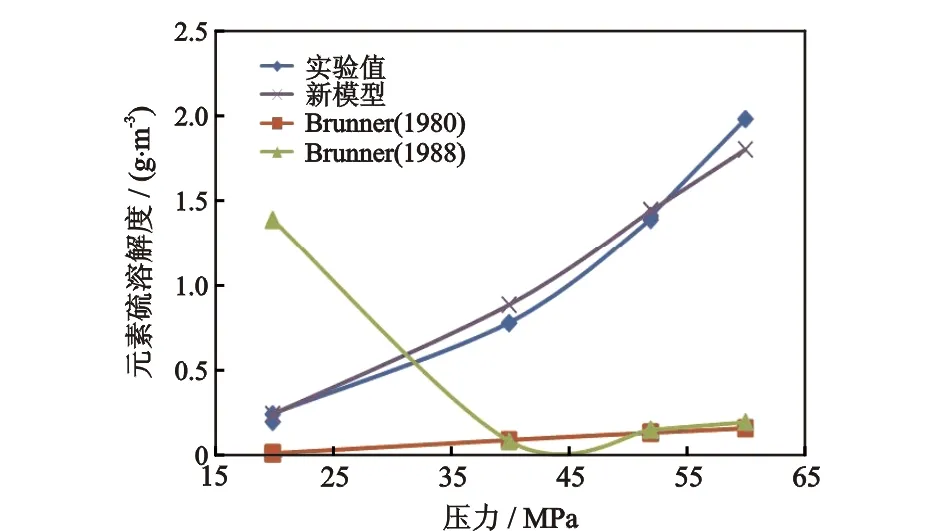
图1 3种模型计算的元素硫溶解度与实验结果对比(温度373.15 K)
表3 不同模型计算的元素硫溶解度对比(温度373.15 K)
Tab.3 Comparison of experimental data with calculation results of four models at 373.15 K
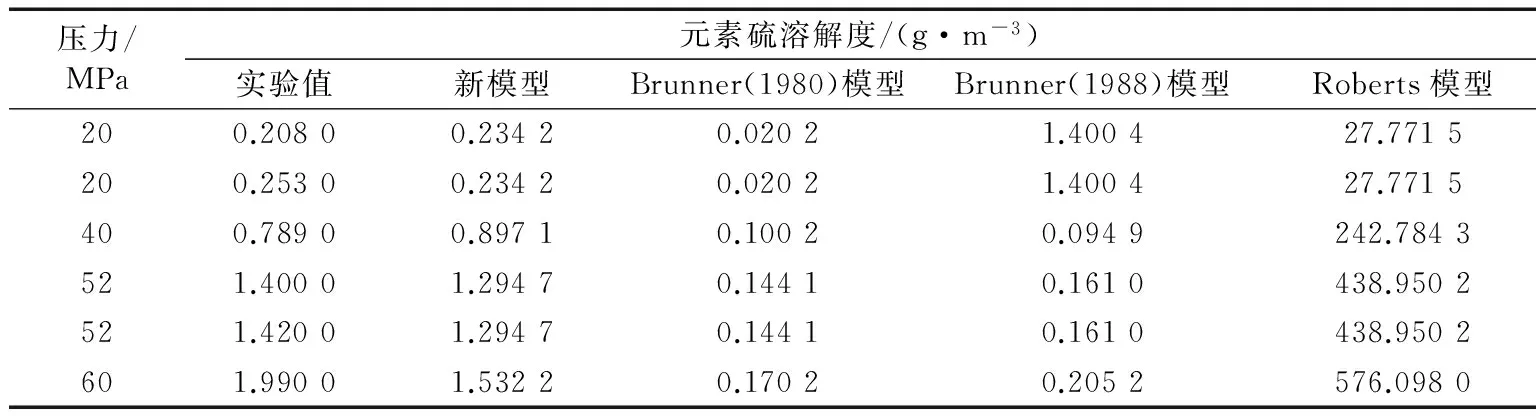
压力/MPa元素硫溶解度/(g·m-3)实验值新模型Brunner(1980)模型Brunner(1988)模型Roberts模型200.20800.23420.02021.400427.7715200.25300.23420.02021.400427.7715400.78900.89710.10020.0949242.7843521.40001.29470.14410.1610438.9502521.42001.29470.14410.1610438.9502601.99001.53220.17020.2052576.0980

表4 不同模型预测的86个样本元素硫溶解度平均相对误差对比
3.2 硫溶解度预测结果对比
为了进一步验证本文半经验公式的适用性,以目前国内外发表的(如谷明星[13]、曾平[15]和杨学锋[16])与实际储层温度压力接近的元素硫在含硫天然气中溶解度实验数据为例,将新模型与Brunner(1980)模型、Brunner(1988)模型和Roberts模型进行了对比分析,结果表明新模型的计算结果较其他3种模型精确。
本文以1993年中国石油大学(北京)谷明星完成的元素硫溶解度实验数据为例,天然气组分见表5。将新模型计算值与上述3种模型计算值同实验测得的元素硫的溶解度进行对比,结果见表6和图2。

表5 天然气的组成
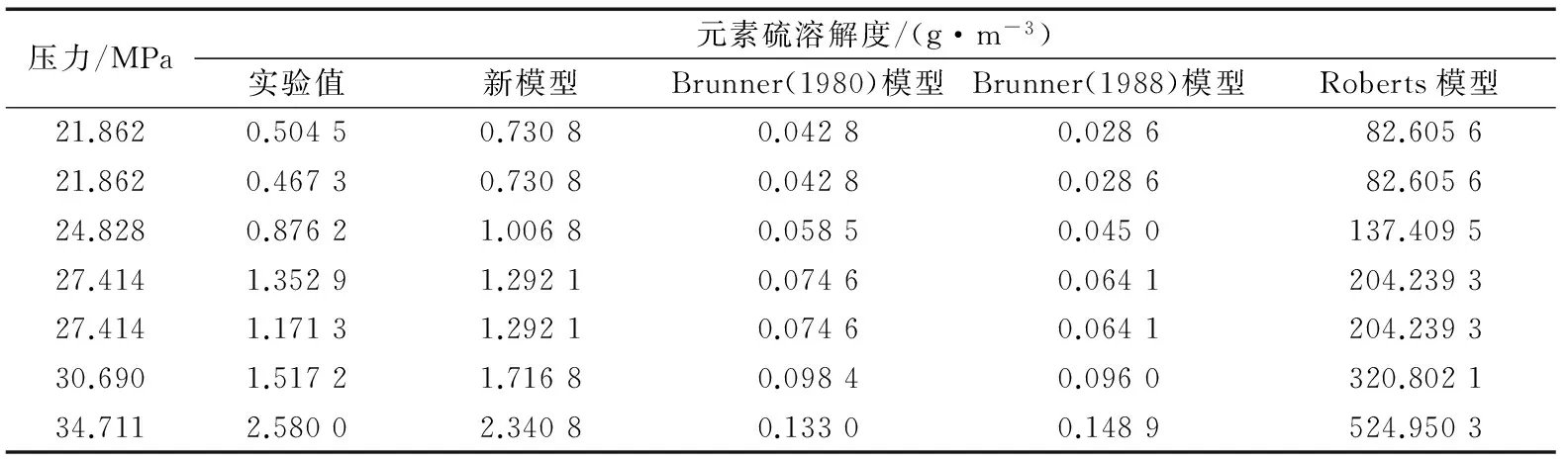
表6 不同模型预测的元素硫溶解度(温度363 K)
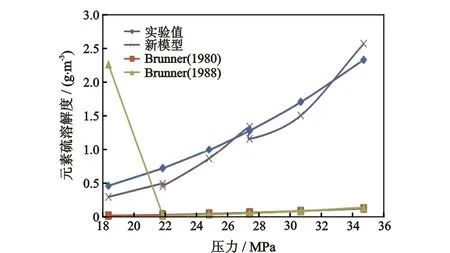
图2 3种模型计算的元素硫溶解度与实验结果对比图(温度363 K)
从表6中可以看出,由式(3)计算的元素硫的溶解度与实验室测得的溶解度比较接近,Roberts模型计算的溶解度与实际值相差很大。在油藏温度和压力条件下,根据Roberts模型计算的溶解度永远也不会有元素硫的析出,从而不会堵塞油藏孔道,对油藏造成伤害。Brunner在1980年和1988年提出密度拐点求元素硫溶解度的思想,据此预测出来的硫溶解度与Roberts模型相比有所改善,但其误差也比较大。从图2中可以看出,本文提出的半经验模型更加接近实验值,求得的元素硫的溶解度更加精确。
4 元素硫溶解度敏感因素分析
从式(3)、(4)中可以看出,元素硫的溶解度与H2S在混合气体中的含量、混合气体组分密度和混合气体温度有关。在不同压力和温度条件下,元素硫溶解度与H2S气体在混合气体中的体积分数的关系见图3和图4。
从图3和图4可以看出,元素硫的溶解度随温度和压力的升高而增大,随H2S体积分数的增加而增加。图3和图4的曲线都可分为2段,前一段硫溶解度随H2S含量直线升高,温度和压力对硫溶解度的影响不太明显;后一段硫溶解度增加速度变快,并且温度和压力对其影响变得十分明显。随着H2S含量的增加,温度对硫溶解度的影响比压力更大。
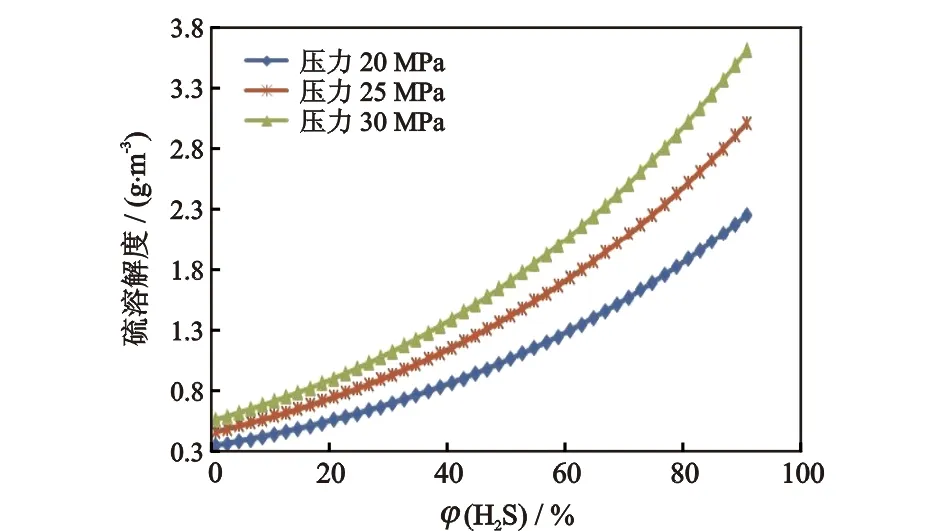
图3 不同压力下元素硫溶解度与H2S气体体积分数的关系
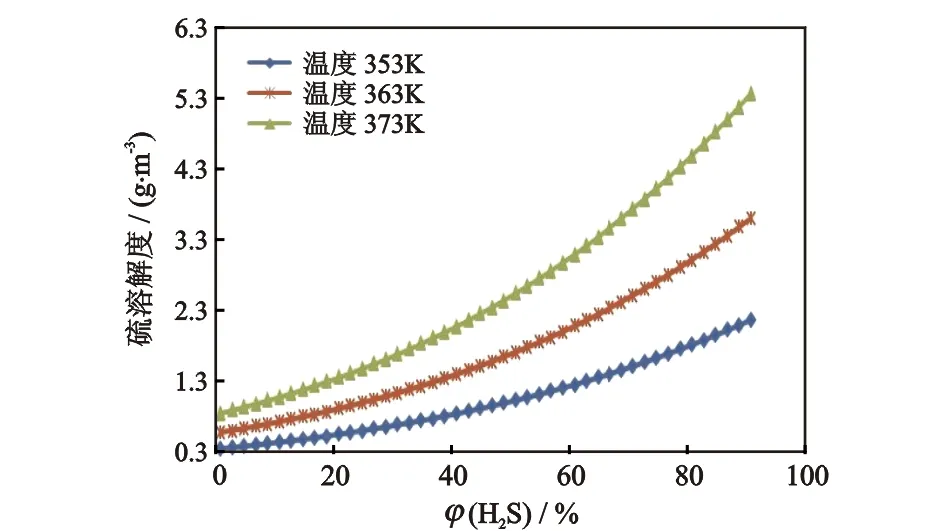
图4 不同温度下元素硫溶解度与H2S气体体积分数的关系
5 结 论
(1)Roberts提出的常系数模型由于只是以特定的流体组分和实验条件为基础回归得到,使用时具有较大的局限性,对不同组分和压力温度条件下元素硫溶解度的计算误差较大。
(2)本文提出的新模型在Josef Chrastil模型的基础上进行了优化,并将混合气体中H2S气体含量考虑在内,拟合的半经验公式计算高含硫气体中元素硫溶解度误差较小,准确性较高。
(3)温度、压力和气体组成是影响硫溶解度的最主要的3个参数。在天然气中,随着温度和压力的升高,硫的溶解度也相应增大,其增加幅度也随之增大。反之,元素硫将从饱和气流中析出。
(4)气体中的H2S对硫的溶解度有着重要的影响。元素硫的溶解度随H2S含量的增加而增加。主要分为2段,前一段硫溶解度随H2S含量直线升高,温度和压力对硫溶解度的影响不太明显;后一段增加速度变快,并且温度和压力对硫溶解度的影响变得十分明显。随着H2S含量的增加,温度对硫溶解度的影响比压力的影响更大。
[1] Abou-Kassem J H.Experimental and numerical modeling of sulfur plugging in carbonate reservoirs[J].Journal of Petroleum Science and Engineering,2000,26(1):91-103.
[2] Kennedy H T,Wieland D R.Equilibrium in the methane-carbon dioxide-hydrogen sulfide-sulfur system[J].Petroleum Transactions,AIME,1960,219:166-169.
[3] Roof J G.Solubility of sulfur in hydrogen sulfide and in carbon disulfide at elevated temperature and pressure[J].Society of Petroleum Engineers Journal,1971,11(3):272-276.
[4] Swift S C,Manning F C , Thompson R E.Sulfur bearing capacity of hydrogen sulfide gas[J].SPE J,1976,16(2):57-64.
[5] Brunner E,Woll W.Solubility of sulfur in hydrogen sulfide and sour gases[J].SPE J,1980,20(5):377-384.
[6] Brunner E,Place Jr M C,Well W H.Sulfur solubility in sour gas[J].Journal of Petroleum Technology,1988,40(12):1587-1592.
[7] Woll W,Brunner E.Solubility of sulphur in hydrogen sulphide and sour gases[C].The 10th World Petroleum Congress,Bucharest,Romania,9-14 September,1979:63-70.
[8] Davis P M,Clark P D.Sulfur deposition in sour gas facilities[J].Alberta Sulfur Research Quarterly Bulletin,1996,111(2):1-40.
[9] Chrastil J.Solubility of solids and liquids in supercritical gases[J].The Journal of Physical Chemistry,1982,86(15):3016-3021.
[10] Tomxej R A,Kalra H,Hunter B E.Prediction of sulfur solubility in sour gas mixtures[C].The 39th Annual Laurance Reid Gas Conditioning Conference,Norman,Oklahoma,06-08 MAR,1989:159-183.
[11] Roberts B E.The effect of sulfur deposition on gas well inflow performance [J].SPE,1997,12(2):118-123.
[12] Elsharkawy A M.Predicting the properties of sour gases and condensates:equations of state and empirical correlations[C].SPE 74369,2002:10-12.
[13] 谷明星,里群,邹向阳,等.固体硫在超临界/近临界酸性流体中的溶解度(Ⅰ)实验研究[J].化工学报,1993(3):315-320. GU Ming-xing,LI Qun,ZOU Xiang-yang,et al.The solid sulfur solubility in supercritical/near critical fluid[J].Journal of Chemical Industry and Engineering,1993(3):315-320.
[14] 钟太贤,袁士义,周龙军,等.含硫天然气相态及渗流[J].石油勘探与开发,2004,31(5):109-111. ZHONG Tai-xian,YUAN Shi-yi,ZHOU Long-jun,et al.Phase behavior and flow of sour gas under reservoir conditions[J].Petroleum Exploration and Development,2004,31(5):109-111.
[15] 曾平,赵金洲,李治平,等.硫在天然气中的溶解度实验研究[J].西南石油学院学报:自然科学版,2005,27(1):67-69. ZENG Ping,ZHAO Jin-zhou,LI Zhi-ping,et al.Study on the mechanism of sulfur solution in nature gas[J].Journal of Southwest Petroleum Institute:Science & Technology Edition,2005,27(1):67-69.
[16] 杨学锋,黄先平,钟兵,等.高含硫气体中元素硫溶解度实验测定及计算方法研究[J].天然气地球科学,2009,20(3):416-419. YANG Xue-feng,HUANG Xian-ping,ZHONG Bing,et al.Experimental test and calculation methods of elemental sulfur solubility in high sulfur content gas[J].Natural Gas Geoscience,2009,20(3):416-419.
[17] 卞小强,杜志敏,郭肖,等.硫在高含H2S天然气中溶解度的实验测定[J].天然气工业,2010,30(12):57-58. BIAN Xiao-qiang,DU Zhi-min,GUO Xiao,et al.Measurement of the solubility of sulfur in natural gas with a high H2S content[J].Natural Gas Industry,2010,30(12):57-58.
责任编辑:董 瑾
2014-09-25
国家自然科学基金项目“CO2驱油对储层的伤害机理研究”(编号:51174178);国家科技重大专项专题 “碎屑岩储层水平井压裂产能预测及压裂效果评价数据支持系统研究”(编号:2011ZX05002-005-008HZ)
李洪(1989-),男,硕士,主要从事油气田动态预测及增产措施研究。 E-mail:lihong19890322@gmail.com
1673-064X(2015)02-0088-05
TE133+.1;P618.13
A

