α-酮戊二酸改性壳聚糖对低浓度U(Ⅵ)的吸附性能
王劲松,邹晓亮,贾 亮,皮艾南,谢 磊,单德才
(1.南华大学城市建设学院,湖南衡阳 421001;2.怀化市规划研究设计院,湖南怀化 418000;3.南华大学化学化工学院,湖南衡阳 421001)
α-酮戊二酸改性壳聚糖对低浓度U(Ⅵ)的吸附性能
王劲松1,邹晓亮2,贾 亮1,皮艾南1,谢 磊1,单德才3
(1.南华大学城市建设学院,湖南衡阳 421001;2.怀化市规划研究设计院,湖南怀化 418000;3.南华大学化学化工学院,湖南衡阳 421001)
通过α-酮戊二酸与壳聚糖反应生成Schiff碱,再用NaBH4还原制备出α-酮戊二酸改性壳聚糖。采用FT-IR、XRD和SEM对其结构进行表征,研究其对水溶液中U(Ⅵ)的吸附行为,考察溶液初始pH值、吸附时间、温度等因素对其吸附水溶液中U(Ⅵ)效果的影响。结果表明,在35℃、pH=4.0、吸附时间为45min的条件下,对U(Ⅵ)浓度为5mg/L的水溶液中铀的去除率在99%以上,U(Ⅵ)的剩余浓度已达到国家排放标准(0.05mg/L)。吸附U(Ⅵ)的α-酮戊二酸改性壳聚糖可用8%的NaOH溶液进行解吸再生,解吸再生后的吸附剂对U(Ⅵ)的吸附效果未明显下降。SEM表明,α-酮戊二酸改性壳聚糖表面粗糙,呈现凹凸不平的多孔结构。FT-IR分析显示,α-酮戊二酸改性壳聚糖表面的—COOH是U(Ⅵ)的主要结合位点。
α-酮戊二酸改性壳聚糖;吸附;解吸;再生;U(Ⅵ)
随着我国核工业的快速发展,对铀的需求量逐年增加,目前国内天然铀的生产能力仅能满足1/3的需求,铀供应面临巨大压力。铀矿冶生产过程中产生大量低浓度含铀放射性废水,对生态环境和人类健康构成严重威胁,如何有效治理和回收废水中的铀已成为亟待解决的问题[1]。目前针对这类废水的处理方法主要有:氧化还原法、絮凝沉淀法、吸附法和离子交换法等[2-4],在这些处理方法中,吸附法以其操作简单、去除率高等优点而备受关注[5-7]。
壳聚糖是自然界中分布仅次于纤维素的天然高分子,分子中含有大量的—OH和—NH2等活性基团,对多种金属离子具有广谱的吸附性能[8-11],且无毒、无害、易降解,是一种理想的吸附剂原料。通常认为,壳聚糖分子中的—NH2是吸附金属离子的主要位点,但—NH2与金属离子的络合作用有限,因此对壳聚糖分子中的—NH2进行改性已成为国内外学者的研究热点,目前已制备出多种壳聚糖吸附剂[12-19]。据报道,在氨基上衍生羧基可提高壳聚糖对铀的吸附性能。经甲基磷酸改性的壳聚糖衍生物对铀的去除率几乎达100%[20],经3,4-二羟基苯甲酸改性的壳聚糖树脂对铀的吸附容量有大幅提升,最大可达330mg/g[21-22],经丝氨酸改性的壳聚糖对铀的富集最高可达到100倍[23]。其他方法去除铀的研究也较多,李小燕等[24]采用纳米零价铁去除溶液中的U(Ⅵ),实验结果表明,对初始浓度为45mg/L的铀溶液,当pH值为5.5、投加量为1.0g/L时,吸附2.5h后,铀的去除率达98.98%,吸附量为27.22mg/g。周泉宇等[25]则利用硫酸盐还原菌与零价铁协同处理含铀废水,铀矿山废水中污染物U(Ⅵ)的去除率达99.4%,同时硫酸根的去除率也可达86.2%,处理后废水的pH值可接近中性。
本研究通过壳聚糖上的—NH2与α-酮戊二酸发生Schiff反应,再用NaBH4还原,将—COOH引入到壳聚糖分子中,并考察这种羧基化壳聚糖衍生物对水溶液中铀的吸附性能,为研发适用于铀矿冶低放废水处理的功能材料及技术奠定基础。
1 实验方法
1.1 仪器与试剂
S-520扫描电镜:日本Hitachi公司;EQUINOX 55傅里叶变换红外光谱仪(FTIR):美国热电尼高力公司;X’Pert Pro XRD:日本理学公司;UV-2000分光光度计:尤尼柯公司;pHS-3C酸度计:上海雷磁仪器厂;JJ-1型定时电动搅拌器:金坛市正基仪器有限公司;QYC-2112大功率恒温摇床,上海福林实验设备有限公司。
壳聚糖:重均相对分子质量(Mw)1.5× 105,脱乙酰度>90%,济南海得贝海洋生物工程有限公司;U3O8(优级纯),α-酮戊二酸、盐酸、氢氧化钠等均为化学纯,国药集团化学试剂有限公司。
1.2 α-酮戊二酸改性壳聚糖制备
α-酮戊二酸改性壳聚糖的合成借鉴文献[26]的方法,合成路线如图1所示,具体步骤如下:准确称取3.125g壳聚糖,用1%的乙酸溶液将其溶解,加入5.0gα-酮戊二酸,用2%的NaOH溶液将pH值调至5.0左右,在37℃下搅拌反应4h后缓慢滴加一定量的NaBH4溶液,滴加完毕后用稀盐酸迅速将溶液调至中性,继续搅拌反应24h后将反应混合物倒入乙醇溶液中,将α-酮戊二酸改性壳聚糖析出,过滤,用无水乙醇和无水乙醚依次洗涤3~4次,将产物转入乙醇索氏提取器中连续提取6h,恒温干燥得白色粉末状的α-酮戊二酸改性壳聚糖。

图1 α-酮戊二酸改性壳聚糖的合成路线Fig.1 Synthetic route ofα-ketoglutaric acid modified chitosan
1.3 吸附实验
铀标准溶液的配制及溶液中铀的浓度测定参照EJ 267.4—1984中的标准方法。用容量瓶移取100mL铀标准溶液到250mL锥形瓶中,用5%的稀HCl和0.3mol/L的NaOH溶液调pH值,然后加入一定量的α-酮戊二酸改性壳聚糖,在220r/min下恒温振荡一定时间,过滤,取滤液测定铀的残余浓度。

图2 壳聚糖和α-酮戊二酸改性壳聚糖的XRD谱Fig.2 XRD spectrum of chitosan and α-ketoglutaric acid modified chitosan

图3 壳聚糖、α-酮戊二酸改性壳聚糖吸附U(Ⅵ)前后的FT-IR谱Fig.3 FT-IR spectra of chitosan,α-ketoglutaric acid modified chitosan before and after adsorption of U(Ⅵ)
2 结果与讨论
2.1 水溶性分析
经羧基改性后,与壳聚糖相比,合成的α-酮戊二酸改性壳聚糖在水中的溶解性稍有提高,表现为一定的溶胀性,这是因为羧基改性壳聚糖在水中溶解度的大小与壳聚糖的相对分子质量、羧基的类型和羧基取代度密切相关,相对分子质量越低,壳聚糖的水溶性越好;羧基取代度越高,水溶性也越好。本文合成的α-酮戊二酸改性壳聚糖相对分子质量较高,且其羧基取代并不完全,只有70%左右,可作吸附剂使用。
2.2 XRD分析
图2为壳聚糖和α-酮戊二酸改性壳聚糖的XRD谱,扫描范围为10°~80°。由图2可见,壳聚糖在2θ为20°、26°和28°处有3个结晶峰,而α-酮戊二酸改性壳聚糖在28°附近的衍射峰几乎消失,且在20°和26°附近的衍射峰明显减弱。这些差别表明,经α-酮戊二酸改性后,分子间的氢键作用削弱,分子结晶度降低[18],说明壳聚糖分子结构已发生变化。
2.3 FT-IR分析
壳聚糖、α-酮戊二酸改性壳聚糖吸附U(Ⅵ)前后的FT-IR谱示于图3。根据文献[27]对图3进行分析,未改性的壳聚糖在3 428cm-1处出现的—NH2和—OH叠加振动吸收峰在α-酮戊二酸改性壳聚糖中发生了微小的偏移,这是由于α-酮戊二酸与壳聚糖反应的过程中不但引入了羧羟基,还消耗了氨基;曲线a中1 596cm-1处的氨基吸收峰在曲线b中消失,同时在1 645cm-1和1 421cm-1处出现了碳氧双键和羧基中—CH2的特征吸收峰,进一步说明壳聚糖分子中的氨基上发生了Schiff碱反应,羧基成功接枝到壳聚糖分子上。
由α-酮戊二酸改性壳聚糖吸附U(Ⅵ)前后的FT-IR谱可看出,吸附前后的特征吸收峰峰型无明显变化,只是发生一定的位移,表明α-酮戊二酸改性壳聚糖在吸附U(Ⅵ)的过程中未改变自身的分子结构,α-酮戊二酸改性壳聚糖与U(Ⅵ)的结合是一个可逆的配位过程。3 428cm-1处—NH2和—OH的伸缩振动叠加峰偏移到3 442cm-1处,这是因为在吸附过程中,部分—OH、—NH2和—COOH结合的H+被UO2+2取代,减弱了O—H、N—H键之间的振动强度。2 879cm-1处为羧基中—OH的特征吸收峰,吸附后偏移到2 923cm-1处,且吸收峰的强度减弱;羧基中的羰基不对称伸缩振动峰在1 645cm-1处变得更加尖锐,羰基对称伸缩振动峰从1 386cm-1处偏移至1 394cm-1处,说明α-酮戊二酸改性壳聚糖分子中的羧基是吸附U(Ⅵ)的重要结合位点。
2.4 SEM分析
壳聚糖、α-酮戊二酸改性壳聚糖吸附U(Ⅵ)前后的SEM图像示于图4。从图4可看出,改性后,壳聚糖的微观形貌并未发生显著变化,但可观察到α-酮戊二酸改性壳聚糖表面粗糙,有明显凹凸不平的多孔结构,且不规则地分布于α-酮戊二酸改性壳聚糖内部及表面,增大了有效比表面积,同时暴露的活性基团数量增加,可利用的吸附位点增加,有利于α-酮戊二酸改性壳聚糖与金属离子的配位;吸附U(Ⅵ)后,α-酮戊二酸改性壳聚糖表面粗糙度明显降低,其孔隙基本被UO2+2占据,展现了改性壳聚糖对铀的良好吸附性能。对图4e中方框内区域进行EDS分析,结果如图5所示。由图5可明显看到吸附后新增了铀元素的能峰,充分说明铀被吸附。

图4 壳聚糖(a),α-酮戊二酸改性壳聚糖吸附U(Ⅵ)前(b,d)、后(c,e)的SEM图像Fig.4 SEM images of chitosan(a),α-ketoglutaric acid modified chitosan before(b,d)and after(c,e)adsorption of U(Ⅵ)
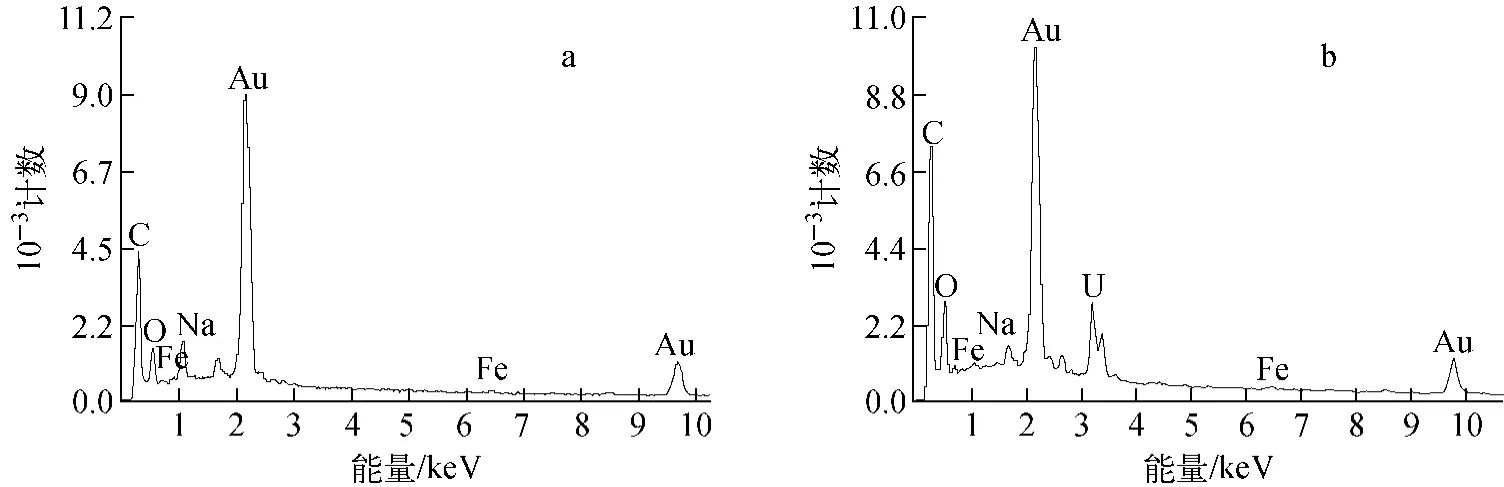
图5 α-酮戊二酸改性壳聚糖吸附U(Ⅵ)前(a)、后(b)的EDS谱Fig.5 EDS spectra ofα-ketoglutaric acid modified chitosan before(a)and after(b)adsorption of U(Ⅵ)
2.5 pH值对吸附效果的影响
称取0.1gα-酮戊二酸改性壳聚糖加入到100mL浓度为5mg/L的含U(Ⅵ)水溶液中,用1mol/L的盐酸或1mol/L的氢氧化钠将吸附液的初始pH值分别调为2.5、3.0、4.0、5.0、6.0、7.0、8.0,30℃恒温振荡30min后过滤,测定滤液中铀的剩余浓度,考察pH值对U(Ⅵ)吸附效果的影响,结果如图6所示。

图6 初始pH值对α-酮戊二酸改性壳聚糖吸附U(Ⅵ)的影响Fig.6 Effect of initial pH on adsorption of U(Ⅵ)onα-ketoglutaric acid modified chitosan
从图6可看出,当溶液初始pH值在2.5~4.0之间变化时,α-酮戊二酸改性壳聚糖对U(Ⅵ)的去除率随pH值的增大而增大,在pH值为4.0左右时,去除率达到最大,随后去除率随pH的增大而减小。这是由于H+与UO2+2
竞争吸附的结果,强酸性下,H+在浓度上占优势,且α-酮戊二酸改性壳聚糖分子中未被取代的—NH2易被质子化(—NH+3)而带正电,与UO2+2产生静电斥力;当pH值升高时,溶液中H+浓度降低,UO2+2在吸附过程中占优势,同时—NH2的质子化程度也会降低,所以U(Ⅵ)的去除率升高;但当pH值过大时,UO2+2会发生水解生成UO2(OH)+、(UO2)2(OH)2+2、(UO2)3(OH)5+、UO2(OH)2等产物[28],不利于α-酮戊二酸改性壳聚糖对UO2+2的吸附。综上所述,将pH值4.0作为后续实验的最佳pH值。
2.6 时间对吸附效果的影响
2.5节中其他条件不变,改变振荡反应时间分别为5、10、15、20、30、45、60、90min,测定滤液中铀的剩余浓度,计算铀的去除率,考察反应时间对吸附效果的影响,结果如图7所示。
从图7可看出,α-酮戊二酸改性壳聚糖对U(Ⅵ)的吸附速率较快,在5min时,U(Ⅵ)的去除率已达84.7%,45min时,去除率大于99%,此时滤液中铀的剩余浓度已低于我国铀的排放标准(0.05mg/L),60min时吸附达到平衡。这主要是由于α-酮戊二酸改性壳聚糖比表面积大,可利用的吸附位点充分暴露于表面,有利于UO2+2与壳聚糖的结合。
为进一步研究α-酮戊二酸改性壳聚糖对U(Ⅵ)的吸附量与时间的关系,本文采用内扩散动力学模型、准一级反应速率模型和准二级反应速率模型方程对实验数据进行拟合。内扩散动力学模型的拟合方程为:y=1.535x+88.14,R2=0.554 9;准一级反应速率模型的拟合方程为:y=0.015 067x+0.698 6,R2=0.987 6;准二级反应速率模型的拟合方程为:y=0.009 935x+0.006 64,R2=0.999 9。可见,α-酮戊二酸改性壳聚糖对U(Ⅵ)的吸附更适合准二级反应速率模型,与文献[29]报道的规律一致。

图7 吸附时间对α-酮戊二酸改性壳聚糖吸附U(Ⅵ)的影响Fig.7 Effect of time on adsorption of U(Ⅵ)onα-ketoglutaric acid modified chitosan
2.7 温度对吸附效果的影响
2.5节中其他条件不变,振荡反应时间设定为45min,改变吸附温度为35、40、45、50、55、60℃,考察温度对吸附效果的影响,结果如图8所示。从图8可看出,在35~60℃范围内,温度对α-酮戊二酸改性壳聚糖吸附水溶液中U(Ⅵ)的影响不太明显,但可看出,随着温度的上升,U(Ⅵ)的去除率略有下降。
2.8 壳聚糖与α-酮戊二酸改性壳聚糖吸附U(Ⅵ)的对比
准确量取100mL浓度为5mg/L的含U(Ⅵ)水溶液,调节其pH值为2.5~8.0,加入0.1g未改性壳聚糖或α-酮戊二酸改性壳聚糖,在30℃下振荡30min后过滤,测定滤液中铀的剩余浓度,对比其对铀的吸附性能,结果如图9所示。由图9可知,两者受pH值影响呈现的规律一致,即pH值为4.0~6.0时,对铀的吸附作用强,这可归因于UO2+2与活性基团形成的配位结构;而在pH<4.0时,对铀的吸附作用弱,则归因于H+与UO2+2存在的竞争吸附关系;pH>6.0时,UO2+2发生水解生成UO2(OH)+、(UO2)2(OH)2+2、(UO2)3(OH)5+、UO2(OH)2等产物,不利于形成配位结构。与壳聚糖相比,α-酮戊二酸改性壳聚糖对U(Ⅵ)的去除率提高了15%左右,这是因为α-酮戊二酸改性壳聚糖上接枝的—COOH与UO2+2形成了多元环的螯合物,增强了壳聚糖与UO2+2
的配位作用,有利于对U(Ⅵ)的吸附。糖用乙醇洗涤干燥后,重复进行吸附实验,测定其对U(Ⅵ)的再生吸附率,结果列于表1。表1数据表明,α-酮戊二酸改性壳聚糖对U(Ⅵ)的一次再生吸附率达98.5%,5次再生后的α-酮戊二酸改性壳聚糖对U(Ⅵ)的吸附去除率基本不变,说明α-酮戊二酸改性壳聚糖具有较好的重复使用性,可用于废水中铀的回收。

图8 反应温度对α-酮戊二酸改性壳聚糖吸附U(Ⅵ)的影响Fig.8 Effect of temperature on adsorption of U(Ⅵ)withα-ketoglutaric acid modified chitosan

图9 壳聚糖与α-酮戊二酸改性壳聚糖吸附U(Ⅵ)的对比Fig.9 Comparison of U(Ⅵ)adsorption on chitosan andα-ketoglutaric acid modified chitosan
2.9 解吸再生
在治理重金属废水的污染过程中,为达到对贵重金属回收和减少处理成本,可通过解吸再生的方法,使重金属离子从吸附材料上分离出来。本实验在pH=4.0的条件下称取0.5g α-酮戊二酸改性壳聚糖加入到100mL浓度为5mg/L的含U(Ⅵ)水溶液中进行吸附,吸附后用8%的NaOH溶液解吸,解吸后的改性壳聚

表1 解吸次数对铀去除率的影响Table 1 Effect of regeneration time on U(Ⅵ)removal rate
3 结论
1)α-酮戊二酸改性壳聚糖上的—COOH能与UO2+2形成稳定的多元环螯合物,增强了壳聚糖与U(Ⅵ)的配位作用,提高了壳聚糖对U(Ⅵ)的吸附能力。与壳聚糖相比,在同样的实验条件下,改性壳聚糖对U(Ⅵ)的吸附去除率提高了15%以上。
2)SEM图像表明,α-酮戊二酸改性壳聚糖呈凹凸不平的多孔结构,使其具有更大的比表面积和更多有效的吸附位点;FT-IR谱分析表明,α-酮戊二酸改性壳聚糖吸附U(Ⅵ)前后特征吸收峰未出现明显变化,但羧基的吸收峰明显减弱,说明—COOH是α-酮戊二酸改性壳聚糖与UO2+2结合的主要位点。
3)α-酮戊二酸改性壳聚糖对水溶液中的微量U(Ⅵ)具有吸附速率快、吸附效果好、可再生利用的特点。在初始pH=4.0、吸附剂投加量0.1g、温度25℃的实验条件下,45min可使初始浓度为5mg/L的含铀水溶液中的铀浓度达到国家排放标准,吸附后的α-酮戊二酸改性壳聚糖可用8%的NaOH溶液解吸,其再生吸附率并未明显下降。
[1] 孙静,丁德馨,胡南,等.诱变绳状青霉吸附铀的行为研究[J].环境科学学报,2012,32(10):2 384-2 393.
SUN Jing,DING Dexin,HU Nan,et al.Characteristics for biosorption of uranium from aqueous solutions by mutated Penicillium funiculosum[J].Acta Scientiae Circumstantiae,2012,32(10):2 384-2 393(in Chinese).
[2] YURLOVA L Y,KRYVORUCHKO A P,ROMANYUKINA I Y,et al.Influence of pH on removal of uranium from aqueous with polyethylenimine,disodium dihydrogen ethylenediaminetetraacetate,and their mixtures[J].Radiochemistry,2010,52(4):418-423.
[3] 任俊树,牟涛,杨胜亚,等.絮凝沉淀处理含盐量较高的铀、钚低放废水[J].核化学与放射化学,2008,30(4):201-205.
REN Junshu,MU Tao,YANG Shengya,et al.Treatment of high salinity low level radioactive wasterwater containing uranium and plutonium by flocculation[J].Journal of Nuclear and Radiochemistry,2008,30(4):201-205(in Chinese).
[4] YURLOVA L Y,KRYVORUVHKO A P.Purification of uranium-containing waters by the ultra-and nanofiltration using modified montmorillonite[J].J Eater Chem Technol,2010,32(6):358-364.
[5] 郑伟娜,夏良树,王晓,等.谷壳对铀(Ⅵ)的吸附性能及机理研究[J].原子能科学技术,2011,45(5):534-540.
ZHENG Weina,XIA Liangshu,WANG Xiao,et al.Adsorption behavior and mechanism of uranium by chaff[J].Atomic Energy Science and Technology,2011,45(5):534-540(in Chinese).
[6] WANG J L,CHEN C.Biosorbents for heavy metals removal and their future[J].Biotechnol Adv,2009,27:195-226.
[7] CHEN C,WANG J L.Removal of Pb2+,Ag+,Cs+,Sr2+from aqueous solution by Brewery’s waste biomass[J].J Hazard Mater,2008,151:65-70.
[8] KRISHNAPRIYA K R,KANANDASWAMY M.Synthesis and characterization of a crosslinked chitosan derivative with a complexing agent and adsorption studies toward metal(Ⅱ)ions[J].Carbohydr Res,2009,344(13):1 632-1 638.
[9] 王洁,黄晓乃,刘迎九,等.壳聚糖吸附铀的机理探讨[J].金属矿山,2009(5):149-153.
WANG Jie,HUANG Xiaonai,LIU Yingjiu,et al.Discussion on the mechanism of chitosan adsorption for uranium[J].Metal Mine,2009(5):149-153(in Chinese).
[10]GAVILAN K C,PESTOV A V,GARCIA H M,et al.Mercury sorption on a thiocarbamoyl derivative of chitosan[J].J Harzard Mater,2009,165:415-426.
[11]KRAMAREVA N V,STAKHEEV A Y,TKAHENKO P.Heterogenized palladium chitosan complexes as potential catalysts in oxidation reactions:Study of the structure[J].J Mol Catal A:Chem,2004,20(1):97-106.
[12]WANG J S,PENG R T,YANG J H,et al.Preparation of ethylenediamaine-modified magnetic chitosan complex for adsorption of uranyl ions[J].Carbohydr Poly,2011,84:1 169-1 175.
[13]WANG G H,LIU J S,WANG X G.Adsorption of uranium(Ⅵ)from aqueous solution onto cross-linked chitosan[J].J Hazard Mater,2009,168(2/3):1 053-1 058.
[14]REPO E,WARCHOL J K,KURNIAWAN T A,et al.Adsorption of Co(Ⅱ)and Ni(Ⅱ)by EDTA-and/or DTPA-modified chitosan:Kinetic and equilibrium modeling[J].Chem Eng J,2010,161:73-82.
[15]VIERA R S,BEPPU M M.Interaction of natural and cross-linked chitosan membranes with Hg(Ⅱ)ions[J].Collodis Surface A,2006,279:768-772.
[16]刘澜,郑怀礼,吴幼权.壳聚糖的改性及应用研究[J].水处理技术,2009,35(11):48-51,56.
LIU Lan,ZHENG Huaili,WU Youquan.Study on modification and application of chitosan,technol[J].Technology of Water Treatment,2009,35(11):48-51,56(in Chinese).
[17]BRITTO D,ASSIS O B G.Synthesis and mechanical properties of quaternary salts of chitosan-based films for food application[J].Int J Biol Macromol,2007,41(2):198-203.
[18]党明岩,张廷安,王娉,等.氯化体系中环硫氯丙烷交联壳聚糖树脂对Au(Ⅲ)的吸附特性[J].化工学报,2007,58(5):1 325-1 330.
DANG Mingyan,ZHANG Tingan,WANG Ping,et al.Adsorption of Au(Ⅲ)on chlorom-ethylthiirane crosslinked chitosan resin in chlorating system[J].Journal of Chemical Industry and Engineering,2007,58(5):1 325-1 330(in Chinese).
[19]黄国林,陈中胜,梁喜珍,等.磁性交联壳聚糖对水溶液中铀(Ⅵ)离子的吸附行为[J].化工学报,2012,63(3):834-840.
HUANG Guolin,CHEN Zhongsheng,LIANG Xizhen,et al.Adsorption behavior of U(Ⅵ)ions from aqueous solution on novel cross-linked magnetic chitosan beads[J].Journal of Chemical Industry and Engineering,2012,63(3):834-840(in Chinese).
[20]YAMAKAWA S,OSHITA K,SABARUDIN A.Synthesis of iminodi(methylphosphonic acid)-type chitosan resin and its adsorption behavior for trace metals[J].Bunseki Kagaku,2004,53(9):1 039-1 043.
[21]SABARUDIN A,NOGUCHI O,OSHIMA M,et al.Application of chitosan functionalized with 3,4-dihydroxy benzoic acid moiety for on-line preconcentration and determination of trace elements in water samples[J].Microchim Acta,2007,159(3-4):341-348.
[22]SABARUDIN A,OSHIMAA M,TAKAYANAGI T,et al.Functionalization of chitosan with 3,4-dihydrox ybenzoic acid for the adsorption/collection of uranium in water samples and its determination by inductively coupled plasmamass spectrometry[J].Analytica Chimica Acta,2007,581(2):214-220.
[23]OSHITA K,OSHIMA M.Synthesis of novel chitosan resin derivatived with serine moiety for the column collection/concentration of uranium and the determination of uranium by ICP-MS[J].Analytica Chimica Acta,2003,480(2):239-249.
[24]李小燕,刘义保,花明,等.纳米零价铁去除溶液中U(Ⅵ)的研究[J].核动力工程,2013,34(2):160-163.
LI Xiaoyan,LIU Yibao,HUA Ming,et al.Removal of U(Ⅵ)from aqueous solution by nanoscale zero-valent iron[J].Nuclear Power Engineering,2013,34(2):160-163(in Chinese).
[25]周泉宇,谭凯旋,曾晟,等.硫酸盐还原菌和零价铁协同处理含铀废水[J].原子能科学技术,2009,43(9):808-812.
ZHOU Quanyu,TAN Kaixuan,ZENG Sheng,et al.Synergetic treatment of uranium-bearing wastewater with sulfate reducing bacteria and zero-valent iron[J].Atomic Energy Science and Technology,2009,43(9):808-812(in Chinese).
[26]丁萍,黄可龙,李桂银,等.壳聚糖衍生物对Zn(Ⅱ)的吸附行为[J].化工学报,2006,57(11):2 652-2 656.
DING Ping,HUANG Kelong,LI Guiyin,et al.Adsorption behavior of Zn(Ⅱ)ion onto chitosan derivatives[J].Journal of Chemical Industry and Engineering,2006,57(11):2 652-2 656(in Chinese).
[27]宁永成.有机波谱学谱图解析[M].北京:科学出版社,2010:109-115.
[28]刘艳,易发成,王哲.膨润土对铀的吸附研究[J].非金属矿,2010,33(1):52-57.
LIU Yan,YI Facheng,WANG Zhe.Study on sorption of bentonite to uranium[J].Non-Metallic Mines,2010,33(1):52-57(in Chinese).
[29]谢志英,肖化云,王光辉.交联壳聚糖对铀的吸附研究[J].环境工程学报,2010,4(8):1 749-1 752.
XIE Zhiying,XIAO Huayun,WANG Guanghui.Study on adsorption of uranium onto cross-linked chitosan[J].Chinese Journal of Environmental Engineering,2010,4(8):1 749-1 752(in Chinese).
Adsorption Performance of Low-strength U(Ⅵ)onα-ketoglutaric Acid Modified Chitosan
WANG Jin-song1,ZOU Xiao-liang2,JIA Liang1,PI Yi-nan1,XIE Lei1,SHAN De-cai3
(1.School of Urban Construction,University of South China,Hengyang421001,China;2.Hunan Huaihua Urban Planning &Design Institute,Huaihua418000,China;3.School of Chemistry and Chemical Engineering,University of South China,Hengyang421001,China)
A kind ofα-ketoglutaric acid modified chitosan(KMCS)was synthesized with the reaction ofα-ketoglutaric acid and chitosan to obtain Schiff base and with the reduction reaction by NaBH4.The structure of KMCS was characterized by FT-IR,XRD and SEM.The effects of initial pH,adsorption time,temperature and other factors on U(Ⅵ)adsorption on KMCS were investigated.The experimental results show that under the condition of 35℃,pH=4.0,adsorption time of 45min,and U(Ⅵ)initial concentration of 5mg/L,the percentage removal of U(Ⅵ)adsorbed by KMCS is higher than 99%,which leads to the U(Ⅵ)concentration in the rest solution lower than the national emission standard(0.05mg/L).The KMCS can be regenerated with the solution of 8%NaOH,and there is no obvious decline after regeneration.The SEM images of the samples show that the KMCS has a rough surface and an uneven porous structure.FT-IR analysis demonstrates that—COOH groups of KMCS are the main binding sites of U(Ⅵ).
α-ketoglutaric acid modified chitosan;adsorption;desorption;regeneration;U(Ⅵ)
X591;O647.3
:A
:1000-6931(2015)02-0255-08
10.7538/yzk.2015.49.02.0255
2013-11-26;
2014-09-06
国家自然科学基金资助项目(21177053,11275095);南华大学科研创新团队项目资助(NHCXTD07)
王劲松(1972—),男,湖南衡阳人,教授,博士,环境工程专业

