生物可降解聚乳酸材料封端剂残留量的研究
刘阳,马丽霞,王勤 ,王传栋△,冯圣玉
(1.山东大学化学与化工学院,济南 250100; 2.山东省药学科学院,山东省生物医用高分子材料重点实验室,济南 250101)
1 引 言
聚乳酸(PLA)是一种生物可完全降解的脂肪族聚酯类高分子材料,具有良好的热塑性,优良的生物相容性和生物可降解性,在体内完全代谢无蓄积,最终的降解产物是二氧化碳和水,对人体无毒、无刺激。已经获得美国食品药品管理局(FAD)批准认可,成为一种备受关注的可生物降解的医用高分子材料[1-3],被广泛应用于食品包装、生物工程和生物医学材料等诸多领域[4-7]。
目前,聚乳酸的合成方法主要有两种,一种是直接缩聚法,另一种是开环聚合法。直接缩聚方法简单,一般只能得到低聚物;开环聚合法工艺较繁琐,成本较高,可以得到高分子量的聚乳酸[8-10]。开环聚合法制备聚乳酸,是以丙交酯为原料,辛酸亚锡为催化剂,十二醇为分子量调节剂进行的聚合反应,本研究主要对聚乳酸材料中十二醇残留量的检测方法进行研究。
十二醇又称月桂醇,常用作制造表面活性剂、香精、洗涤剂、化妆品、纺织助剂等[11],在聚乳酸合成中常作为封端剂,对聚乳酸分子量进行调节。有研究[12]表明醇对聚乳酸的热稳定性有一定的影响,醇会促进聚乳酸的降解,降低聚乳酸的热稳定性,且醇的添加量越大,对聚乳酸热稳定性的影响越大,因此,为控制聚乳酸原料的产品质量,提高聚乳酸的热稳定性,对十二醇的残留量的控制是非常重要的,建立十二醇残留量的检测方法也是非常必要的。十二醇含量的测试方法已有相关文献报道[13-14],但测定聚乳酸中微量十二醇残留的检测方法尚未见文献报道,本研究建立了聚乳酸中十二醇残留的气相色谱测定方法。
2 材料与方法
2.1 仪器与试剂
安捷伦6890N气相色谱仪、配FID检测器(美国,Agilent公司);Sartorius型电子分析天平(感量:0.0001 g,德国Sartoirus公司);KQ5200B型超声清洗器(昆山市超声仪器有限公司),TDL80-2B离心机(上海安亭科学仪器厂)。
聚乳酸原料(自制),十二醇(国药集团化学试剂有限公司,分析纯)、甲醇(天津赛孚瑞科技有限公司,色谱纯)、氯仿(Honeywell Burdick & Jackson,色谱纯)。
2.2 色谱条件
采用DB-624 毛细管色谱柱(30 m×0.530 mm×3.0 μm),程序升温(60℃,保持3 min;30℃/min,升温至250℃,保持10 min),进样口温度250℃,检测器温度260℃,分流比:10∶1,进样量:2 μL,流速:3.0 mL/min。
2.3 标准液的制备
精密称取十二醇0.2521 g,置25 ml量瓶中,甲醇溶解并定容,作为标准储备液。取5 ml标准储备液于50 ml量瓶中,甲醇定容,得1.01 mg/mL标准溶液。各取5 ml浓度为1.01 mg/mL的标准溶液分别于50 ml和10 ml量瓶中,甲醇定容,得0.10 mg/mL和 0.50 mg/mL的标准溶液。取1、2、5和7 ml浓度为0.10 mg/mL的标准溶液分别于10 ml量瓶中,甲醇定容,得0.01 mg/mL、0.02 mg/mL、0.05 mg/mL和0.07 mg/mL的标准溶液。
2.4 样品处理
精密称取聚乳酸1.0 g,置25 ml容量瓶中,加适量氯仿溶解后,缓慢滴加甲醇使聚乳酸沉淀,并用甲醇定容,冰水浴中超声设定时间,取适量上述溶液于离心管中,3000 rpm离心20 min备用。
3 结果
3.1 专属性
分别精密量取空白溶剂A(纯甲醇),空白溶剂B(氯仿与甲醇混合液,V氯仿∶V甲醇=1∶4),十二醇标准溶液C,各2 μL,按照2.2项下的色谱条件进样分析,记录色谱图,见图1。从图1中可以看出,在此条件下,各溶剂对十二醇测定无干扰,十二醇的专属性良好。
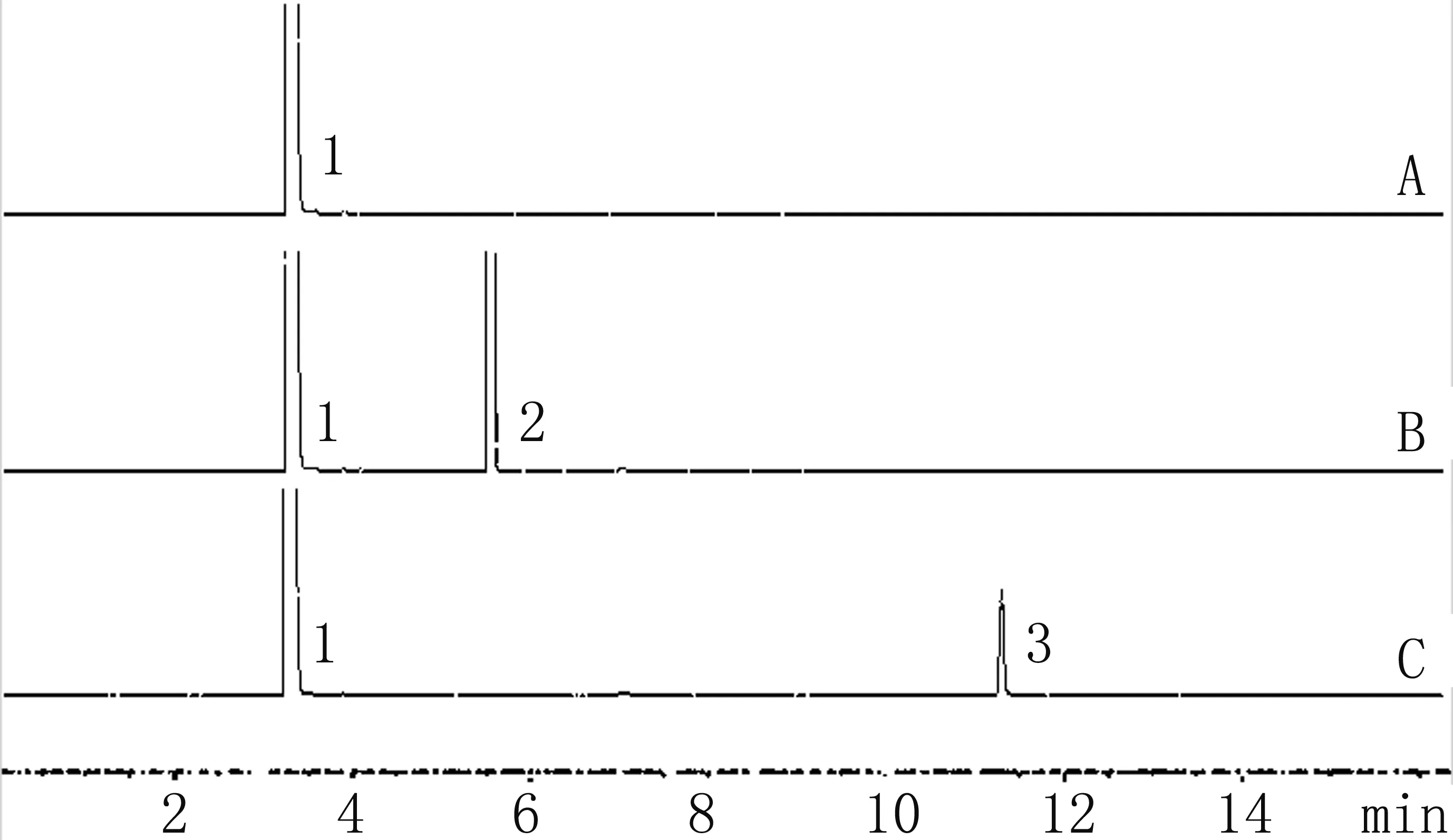
图1空白溶剂A、空白溶剂B和十二醇标准溶液C的GC色谱图
1. 甲醇( methyl alcohol ),2. 氯仿 ( chloroform ), 3. 十二醇 ( lauryl alcohol )
Fig1GCchromatogramsofblanksolvent(A),blanksolvent(B)andsample(C)
3.2 线性关系
取2.3项下的系列标准溶液各2 μL,注入气相色谱仪,照2.2项下的色谱条件测定,以峰面积A对质量浓度C作线性回归,十二醇的线性方程为:A=2717.3C-11.646,γ=0.9998,线性范围为0.01~1.01mg/mL。
3.3 精密度
取浓度为0.10 mg/mL的十二醇标准溶液,照2.2项下的色谱条件,连续进样6次。结果十二醇峰面积均值为272 mAU.s,RSD为3.16%。
3.4 重复性
取同一批号样品,平行制备6份样品溶液,按2.2项下的色谱条件进样测定。十二醇含量均值为0.0837%,RSD为3.49%。
3.5 回收率
为了避免聚乳酸原料中残留十二醇的干扰,我们采用羧基封端的聚乳酸作为回收率试验的基质,精密称取羧基封端的聚乳酸样品9份,置于9个25 ml量瓶中,加入不同量的十二醇标准溶液,制备低、中、高3个水平浓度的回收率试验用供试液,按上述色谱条件测定方法的回收率。结果见表1。从表1中可以看出,十二醇平均回收率为99.21%,RSD值为1.55%。

表1 十二醇加样回收率结果
3.6 检测限和定量限
取0.01 mg/mL标准溶液适量,用甲醇逐级稀释,照2.2项下的色谱条件进样分析,记录色谱图。以信噪比为10∶1时作为十二醇的检测限,以信噪比为3∶1时作为十二醇的定量限。测试结果显示,十二醇检测限浓度为0.0005 mg/mL,定量限浓度为0.001 mg/mL。
3.7 样品处理条件的选择
3.7.1溶剂用量的选择 根据聚乳酸及十二醇的溶解性,选择氯仿做溶剂,甲醇做沉淀剂,对聚乳酸原料中的十二醇进行提取。分别对1 g聚乳酸样品选取2、5和10 ml氯仿作为溶剂,先将聚乳酸溶解,再缓慢滴加甲醇使聚乳酸沉淀下来,十二醇溶解在氯仿和甲醇的混合溶剂中,并用甲醇最终定容至25 ml。图2为氯仿用量对聚乳酸中残留十二醇提取的影响曲线。
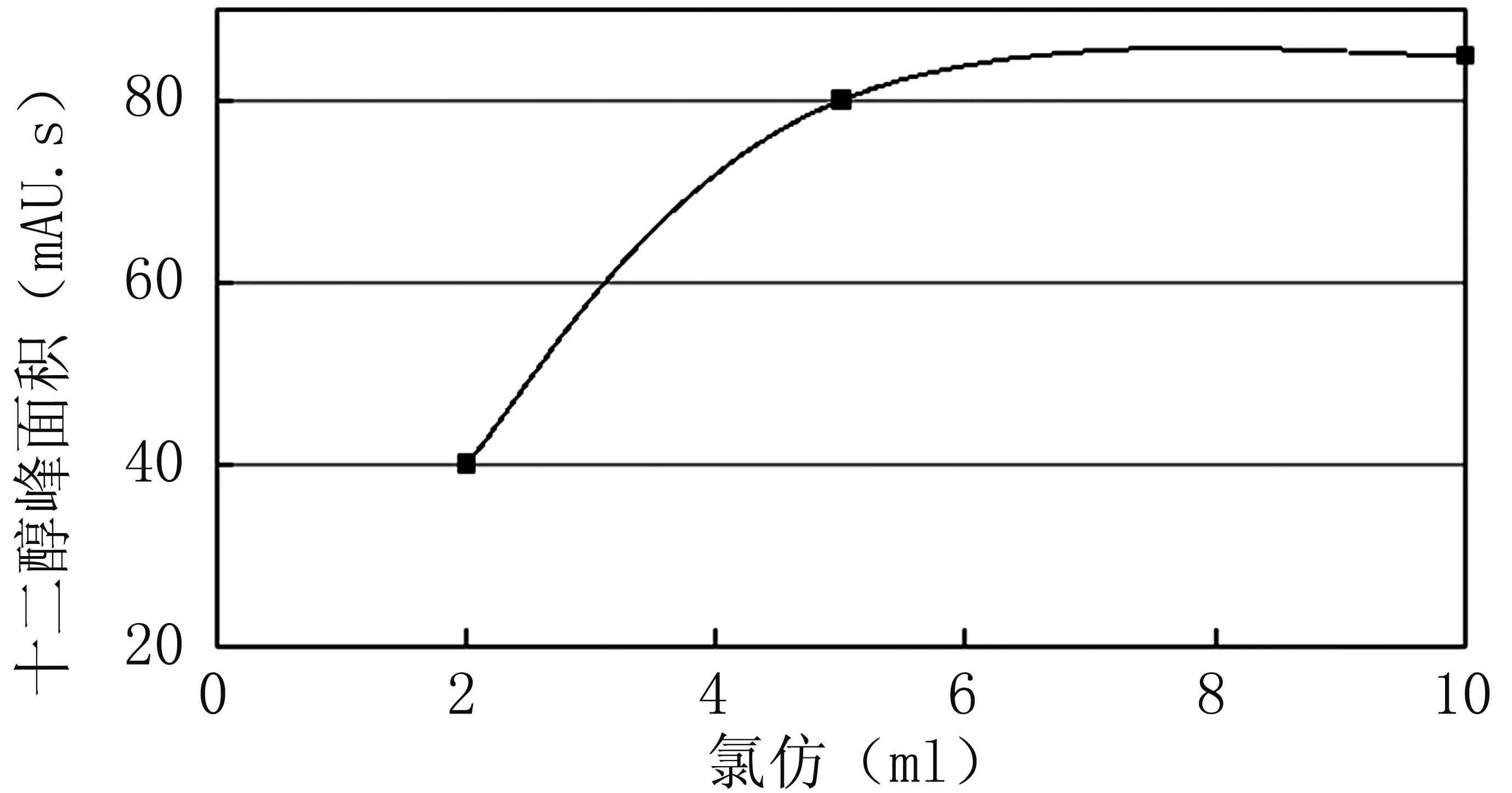
图2 氯仿用量对聚乳酸中残留十二醇提取的影响曲线
从图2中可以看出,1 g聚乳酸原料加5 ml氯仿溶解,待聚乳酸完全溶解后,缓慢滴加甲醇使聚乳酸沉淀下来,并用甲醇定容至25 ml,聚乳酸中残留的十二醇提取趋于完全。氯仿用量达10 ml时,提取完全,但试验发现,此时,聚乳酸溶解在混合溶剂中,无法达到沉淀分离的目的,直接进样测试,由于聚乳酸的不易挥发性,容易对测试系统造成污染。因此,样品处理选择1 g聚乳酸加5 ml氯仿溶解,待聚乳酸完全溶解后,缓慢滴加甲醇使聚乳酸沉淀下来,并用甲醇定容至25 ml的处理方法。
3.7.2超声时间的选择 称取1.0 g聚乳酸原料于25 ml量瓶中,加入5ml氯仿,待聚乳酸完全溶解,缓慢滴加甲醇使聚乳酸沉淀,并用甲醇定容。将上述溶液置于超声清洗器中进行超声处理,分别超声0、10和30 min。图3为超声时间对聚乳酸原料中残留十二醇提取的影响曲线。

图3超声时间对聚乳酸中残留十二醇提取的影响曲线
Fig3Thecurveofultrasonictimeeffectonresiduallaurylalcoholextract
从图3中可以看出,超声处理10、30 min后,测试谱图显示,十二醇的峰面积未见随超声时间的增加而显著增加,这说明超声处理对聚乳酸中残留十二醇提取影响不大,考虑工作效率,采用对样品溶液不经超声,直接3000 rpm离心20 min的处理方法。
3.8 样品测定
选取合成工艺中低、中、高三种比率十二醇封端剂的聚乳酸原料进行测定。精密量称取不同批次下的聚乳酸原料1.0 g于25 ml量瓶中,按最佳样品处理方法对样品进行处理测定,按外标法以峰面积计算聚乳酸原料中十二醇的残留量。结果见表2。
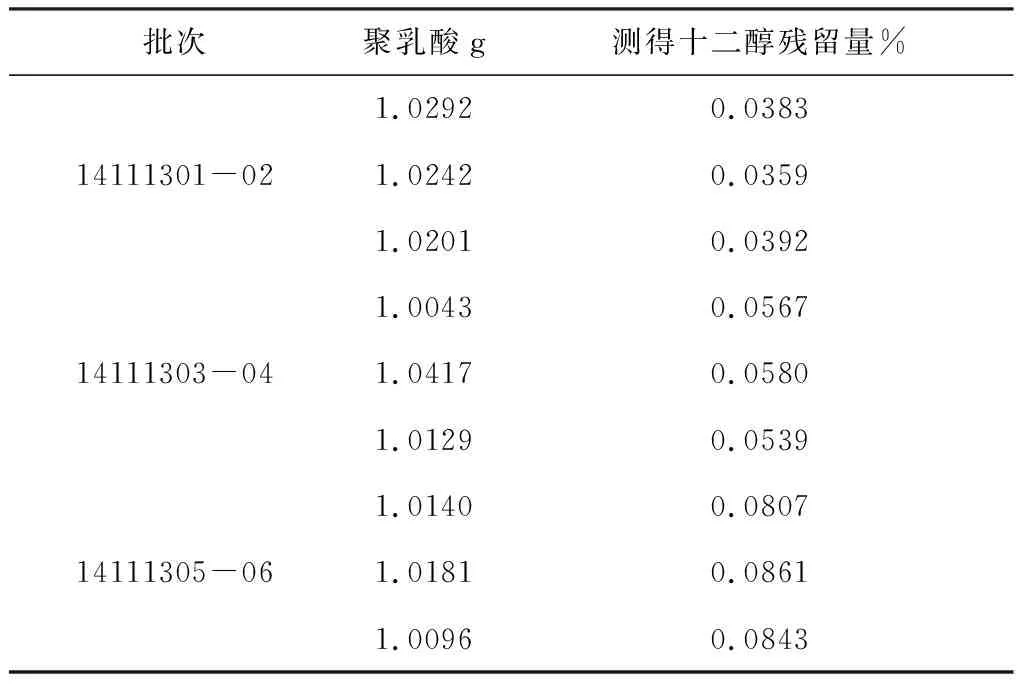
表2 样品测定结果
4 讨论
研究结果表明,采用气相色谱法测定聚乳酸原料中封端剂十二醇的残留量,十二醇的专属性良好,加样回收率平均值达99.21%,RSD值为1.55%。对样品处理方法研究表明,将1 g样品溶于5 ml氯仿中,然后缓慢滴加甲醇,使聚乳酸沉淀,并用甲醇最终定容至25 ml,3 000 rpm离心20 min,对样品中残留的十二醇的提取较为完全。因此,该方法能达到定量检测的目的,将该方法应用于聚乳酸原料中十二醇残留量的测定,结果可靠。
目前,只有欧洲药典中聚桂醇400(lauromacrogol 400)质量标准对十二醇的残留量进行了规定[15],限度为小于2.0%。聚乳酸原料测试结果显示,封端剂十二醇残留量随合成过程中加入量的增加而增加,但十二醇残留量均小于0.1%。根据测试结果,参照欧洲药典,拟定以十二醇为分子量调节剂合成的聚乳酸中十二醇的残留量限度为小于2.0%。

