硫化镍钴矿微生物浸出液萃取除杂过程中界面乳化物的形成
李晓晖,周桂英,黄松涛,温建康,丁建南
(1.北京有色金属研究总院 生物冶金国家工程实验室,北京 100088;2.江西省科学院 生物资源研究所,南昌 330096)
工业上应用生物浸出-溶剂萃取分离矿石中的铜、钴、镍等有价金属离子,取得了很好的浸出和分离效果。但在萃取分离过程中,经常产生界面乳化物,很多生产厂家受乳化影响不能正常生产,比如德兴铜
矿自1997年投产以来遇到严重的界面乳化问题,整个工艺曾多次不能正常运行[1-2]。并且萃取过程中界面乳化物随时间的延长逐渐增多,抽取萃取过程中界面和底部产生的乳化物装入絮凝物槽,经过添加酸化水、过滤等处理,将有机相返回萃取流程继续使用[3-4]。但界面乳化物产生仍会造成有机相大量流失、分相时间延长、萃取效率低等问题,解决微生物浸出液萃取过程中界面乳化问题已成为人们关注的焦点。很多学者已经对萃取过程中乳化物的形成原因进行了研究。MILLER[5]认为造成乳化产生的物质主要有悬浮固体颗粒、金属离子和生物质,其中生物质属于两亲性物质。BEDNARSKI等[6]研究发现铜微生物浸出液中锰离子对萃取过程中的有机相有很强的氧化作用,使有机相氧化降解,造成界面乳化物的形成。刘晓荣等[7-8]取德兴铜矿堆浸厂萃取铜生产过程中的乳化物,分析其形成原因,认为界面乳化物的产生是浸出液中微细固体颗粒和萃取剂降解产物的共同作用。界面乳化物的产生除受固体颗粒、胶体和杂质离子影响外,浸矿细菌也是重要影响因素之一,但目前缺乏关于浸矿细菌对界面乳化产生形成影响的研究。细菌表面双电层结构特征[9]以及胞外聚合物的表面负电荷性、吸附性、絮凝性和亲疏水性等性质[10-13],可能对界面乳化物的形成产生影响。因此,本文作者结合浸矿细菌特征,研究硫化镍钴矿微生物浸出液萃取过程中界面乳化情况,为解决镍钴微生物浸出液萃取过程中界面乳化问题提供理论依据。
1 实验
1.1 实验材料
实验中采用中科院有机化学研究所合成的P204(D2EHPA),主要成分为二(2-乙基己基)磷酸,稀释剂为260号磺化煤油。实验中所采用的硫酸盐均为分析纯。所采用的微生物浸出液取自白山硫化镍钴矿微生物堆浸试验厂。
1.2 实验方法
1.2.1 模拟溶液配制
根据除铁后白山硫化镍钴矿微生物浸出液成分含量以及细菌浓度配制模拟溶液。表1所列为白山硫化镍钴矿微生物浸出液除铁后成分含量,细菌浓度为9×106个/mL。
1.2.2 萃取除杂实验
将有机相(10%P204和90%磺化煤油(体积分数)组成)与浸出液以体积比为1:2加入到分液漏斗中,置于萃取振荡器上振荡,振荡强度为225 r/min,10 min后静止分层,然后将第一次萃取分相后有机相用100 g/L H2SO4反萃、洗涤,有机相经皂化后与新鲜浸出液混合。与上述相同的实验条件下,进行萃取实验,以此循环萃取,每次萃取分相实验结束后,将液体迅速转移到量筒中,记录分相时间及界面乳化物体积,按照式(1)计算界面乳化物生成率Yc,并绘制澄清曲线。

表1 白山硫化镍钴矿微生物浸出液除铁后成分含量Table1 Chemical composition of nickel and cobalt sulfide ore bioleaching from Baishan after removing iron

式中:Yc为界面乳化物生成率;Ve为生成界面乳化物的体积;V为水相和有机相的总体积。
1.3 测试手段
采用日产Nikon 50i相差显微镜和NikonDS-V1数码相机对乳化液显微组织进行观察,放大倍数为1000;采用血球计数板在相差显微镜下进行细菌计数;采用紫外-可见光分光光度计在360~700 nm测试有机相吸收曲线;采用上海中晨数字技术设备有限公司生产的JK-99B型全自动张力仪测试水相表面张力和水油界面张力;采用内径为0.5~0.6 mm的乌氏黏度计测试溶液黏度;采用测量范围为1.0~1.1和1.1~1.2 g/cm3密度计测试溶液密度;采用美国Nicolet Nexus 670型傅立叶变换红外显微光谱仪测定有机相组成结构;采用日本Mac M21X型X射线衍射分析仪测试界面乳化物中固体物质成分。
2 结果与讨论
2.1 硫化镍钴矿微生物浸出液分析
对模拟溶液与实际浸出液分别进行萃取除杂实验,对比二者萃取过程中分相速度,实验结果如图1所示。从图1中看出,模拟溶液在静置90 s后,水相和有机相分相完全,而实际浸出液分相时间为800 s,分相时间明显延长,不易于分相,说明实际浸出液中有阻碍水相和有机相分相的物质存在。另外,发现实际浸出液萃取分相过程中聚结液面上升速度较慢,说明分相速度由水相中液滴的聚结过程控制,分相性能可能受液滴粒径、两相密度差和连续相黏度等因素影响[14]。对实际浸出液和模拟溶液的一些物理参数进行测定,其结果如表2所列。从表2中看出,模拟溶液与实际浸出液的密度和表面张力接近,但实际浸出液中存在某些增大黏度,降低水相透光度的物质,这些物质的存在延长了萃取分相时间。
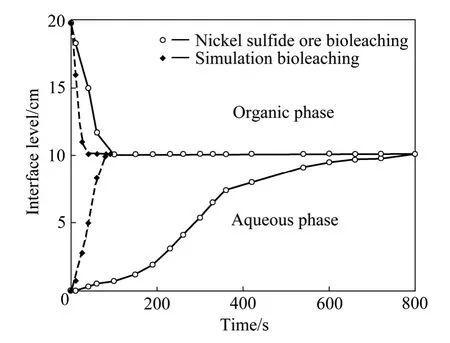
图1 白山硫化镍钴矿微生物浸出液与模拟溶液萃取澄清曲线Fig.1 Clarify curves of nickel and cobalt sulfide ore bioleaching and simulation bioleaching
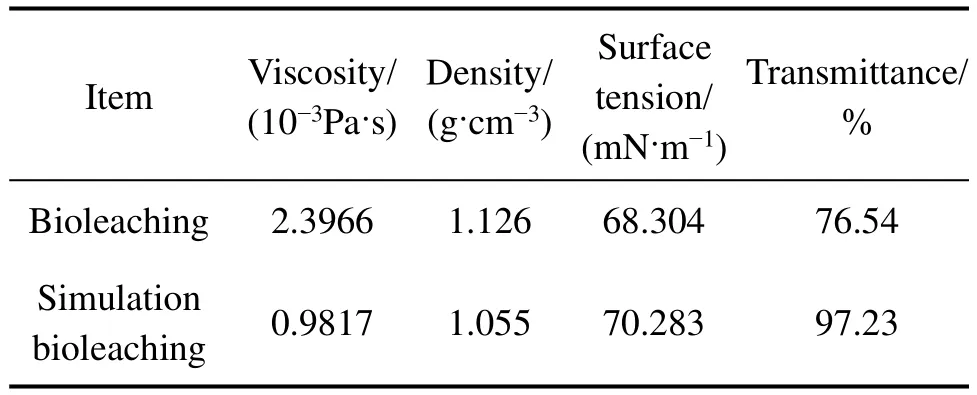
表2 硫化镍钴矿微生物浸出液与模拟溶液物理参数Table2 Physical parameters of nickel and cobalt sulfide ore bioleaching and simulation bioleaching
2.2 硫化镍钴微生物浸出液萃取过程界面乳化情况
图2所示为不同静置时间下界面乳化物生成率变化曲线。从图2中可以看出,随着萃取次数的增加,界面乳化物生成率逐渐增加。萃取5次和萃取50次的溶液静置10 min后,界面乳化物生成率由16%增加到29%,这是由于萃取过程中浸出液杂质累积造成了界面乳化物生成率增加。利用血球计数板记录每次萃取前后萃余液中的细菌数目,并计算细菌吸附率,其结果如图3所示。从图3中可以看出,每次萃取均有60%~80%的细菌被吸附到界面乳化层中。细菌存在于浸出液中会增大浸出液的黏度、密度,并且在萃取过程中细菌易于吸附在水油界面上增大水油分相难度[15]。
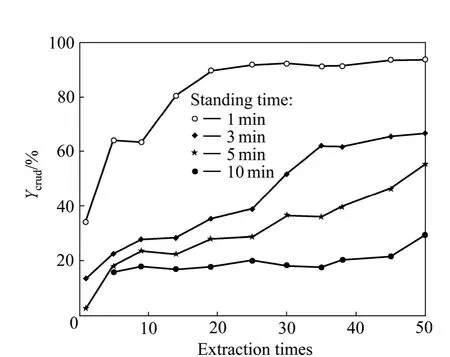
图2 萃取过程中不同静置时间下界面乳化物生成率和萃取次数的关系Fig.2 Relationship between production rate of interfacial crud and extraction times at different standing times during extraction process

图3 萃取过程中细菌吸附率和萃取次数的关系Fig.3 Relationship between bacteria adsorption and extraction times during extraction process
萃取50次后取界面乳化物置于玻璃皿中自然晾干后,对其进行XRD分析,其结果如图4所示。经分析界面乳化层累积的固体物质主要为黄钾铁矾和二氧化硅。黄钾铁矾来源于除铁过程中一些难以聚沉的细小黄钾铁矾颗粒,二氧化硅主要来源于浸矿过程中不能被溶解的细小脉石微粒。
取萃取后稳定的界面乳化物进行显微观察,放大倍数为1000倍,如图5所示。从图5(a)中可以看出,萃取10次后,界面层中有成片堆积的残留界面膜。由于萃取过程中浸出液中的细小颗粒和胶体物质会紧密吸附在界面上,很难脱附。随静置时间的延长,液滴开口排液,界面膜并未消失,会收缩起皱或变厚。图5(b)所示为萃取50次后界面乳化物显微组织。与图5(a)不同,界面上不是完全聚结后残留的界面膜,仍有一些细小液滴吸附在界面膜上未发生聚结、排液,说明随着萃取次数的增加,液滴间聚结难度增加,生成界面乳化物稳定性增强。
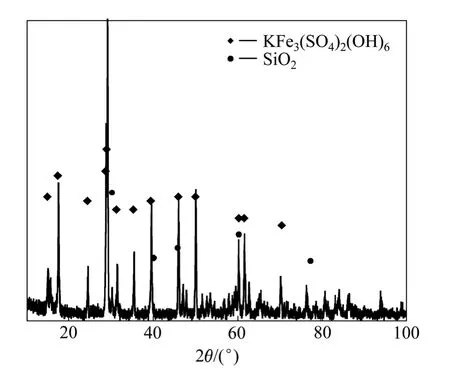
图4 界面乳化层的XRD谱Fig.4 XRD patterns of interfacial crud

图5 萃取过程中不同萃取次数的界面乳化物显微组织Fig.5 Microstructures of interfacial crud in extraction process with different extraction times:(a)10;(b)50
2.3 萃取过程中有机相组成结构变化
图6所示为260号煤油和10%P204(体积分数)的红外光谱。从图6可以看出,煤油的C—H键特征峰在2974.68 cm-1位置,1466.61和1377.92 cm-1处分别为C—H变形振动峰。P204的特征峰有P=O、P—O—H和P—O—C,它们分别对应的特征峰为1231.67、1685.63和1032.36 cm-1[15]。图7所示为经过多次萃取后有机相红外光谱。从图7可以看出,随着萃取次数的增加,有机相在1032.36 cm-1处吸收峰强度明显降低,1685.63 cm-1处吸收峰消失。结果表明,萃取过程中P—O—H键可能与溶液中金属离子相结合形成配合物或发生断裂。

图6 煤油与10%P204的红外光谱Fig.6 Infrared spectra of kerosene and 10%P204

图7 不同萃取次数下有机相红外光谱Fig.7 Infrared spectra of organic phase with different cycle times
图8所示为不同萃取次数有机相的吸收曲线。从图8看出,随着萃取次数的增加,有机相吸收曲线的吸收强度逐渐增加,萃取50次后,在370 nm处出现了吸收峰。除铁后浸出液中含有Co2+、Ni2+、Ca2+、Mg2+和Fe3+(见表1),其中Ca2+和Mg2+易于使界面乳化现象加重,经P204萃取后进入有机相中,但对有机相性质影响很小。当溶液中单独存在Ca2+和Mg2+时,有机相吸收曲线并无变化[16]。Co2+和Ni2+需要在除杂后进行萃取分离,几乎不进入有机相。浸出液中的Fe3+容易与P204形成络合物,有机相吸收曲线的变化可能与Fe3+反萃不完全并不断在有机相中累积有关,有研究发现溶液中单一组分的Fe3+达到一定浓度时就会产生界面乳化物[17]。

图8 萃取过程中不同萃取次数下有机相吸收曲线Fig.8 Absorption curves of organic phase with different extraction times during extraction process
2.4 Fe3+对有机相组成结构的影响
配制不同浓度仅含硫酸铁的溶液,调节硫酸铁溶液pH=1.8,将硫酸铁溶液与10%P204以体积比为1:1混合,振荡强度为225 r/min,振荡5 min后取有机相进行吸收曲线及红外光谱分析。图9所示为不同Fe3+浓度下有机相的吸收曲线。从图9看出,随着有机相负载Fe3+浓度的增加,有机相吸收峰强度及吸收峰位置发生变化。Fe3+浓度为3 g/L时,只存在420 nm的吸收峰。随着Fe3+浓度的升高,在370 nm处出现吸收峰,峰强度逐渐增强。
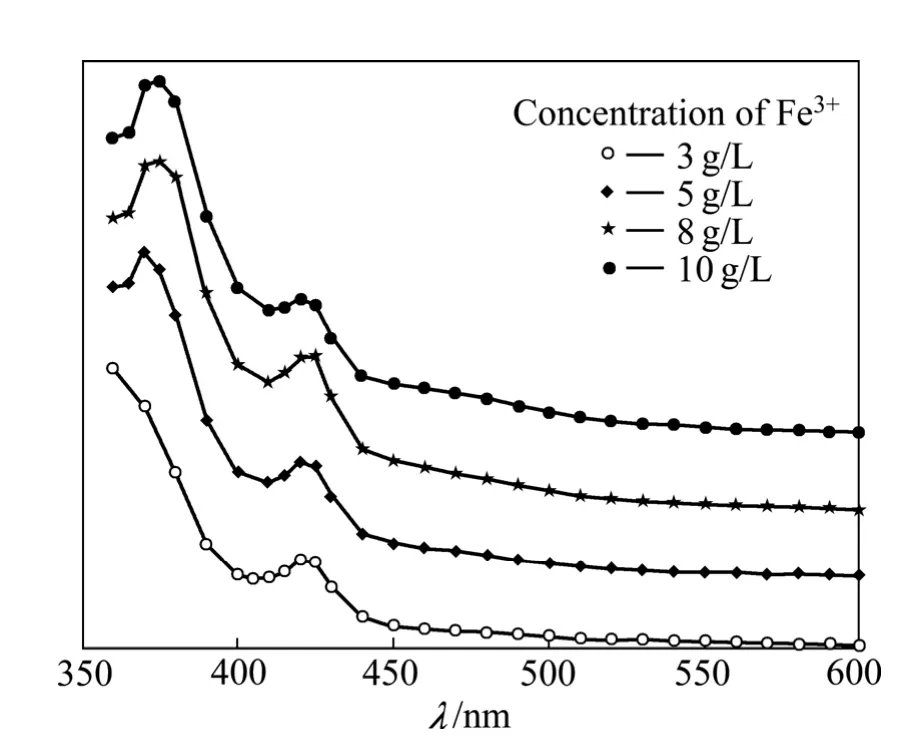
图9 不同Fe3+浓度下有机相吸收曲线Fig.9 Absorption curves of organic phase with different concentrations of Fe3+
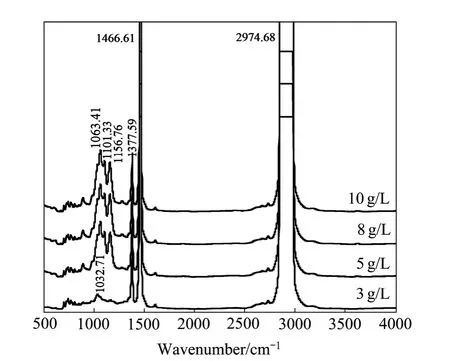
图10 不同Fe3+浓度下萃取后的有机相红外光谱Fig.10 Infrared spectrums of organic phase with different concentration of Fe3+after extraction
图10所示为不同Fe3+浓度下有机相红外光谱,分析结果发现,3 g/L Fe3+溶液与有机相接触后,有机相中P204特征峰P—O—C峰消失,而后随着Fe3+浓度的增加,分别在1063.41、1156.76 cm-1处出现了吸收峰,并且1063.41 cm-1处出现肩峰,吸收峰的变化表明有机相P204与铁离子形成了配合物,结构发生改变。由于P204的酸性较强,P204主要与溶液中非水解Fe3+按阳离子交换机理结合。随着Fe3+浓度的增加,P204首先萃取非水解Fe3+,此时,分子内碳-磷键数目增多,酸性减弱,萃取非水解Fe3+能力减弱,而萃取羟基铁离子的能力增强[18]。对不同Fe3+浓度下萃后水相-有机相界面张力进行测试,测试结果如图11所示。从图11可以看出,随着Fe3+浓度的升高,萃后水油界面张力明显降低,由3 mN/m下降到0.6 mN/m,界面张力降低不利于水相和有机相分相,容易形成界面乳化物。

图11 不同Fe3+浓度下水相-有机相界面张力变化曲线Fig.11 Variation curves of interface tension between aqueous phase and organic phase at different concentrations of Fe3+
3 结论
1) 萃取过程中界面乳化物生成率逐渐增加,在萃取50次静置10 min后,界面乳化物生成率由16%增加到29%,主要原因与浸出液中黄钾铁矾、二氧化硅和细菌的累积有关。
2) 萃取过程中萃取剂结构发生明显变化。红外光谱结果表明1032.36 cm-1处吸收峰强度明显降低,1685.63 cm-1处吸收峰消失。吸收曲线测试发现,萃取50次后370 nm处出现了吸收峰。
3) 通过浸出液成分分析和Fe3+对有机相结构影响实验可知,萃取剂结构变化由于P204与Fe3+形成了配合物,配合物的形成降低了水相-有机相界面张力,增大了水油分相难度。
[1]刘晓荣,邱冠周,胡岳华,柳建设.BL-SX-EW工艺中萃取界面乳化现象成因研究[J].矿冶工程,2000,20(4):38-41.LIU Xiao-rong,QIU Guan-zhou,HU Yue-hua,LIU Jian-she.Interfacial emulsifying phenomenon in BL-SX-EW process-A cause[J].Mining and Metallurgical Engineering,2000,20(4):38-41.
[2]李 玲,阮仁满,温建康,周桂英.铜萃取过程中固体微粒对第三相形成的作用分析[J].稀有金属,2008,32(6):748-753.LI Lin,RUAN Ren-man,WEN Jian-kang,ZHOU Gui-ying.Effect of solid particles on formation of the third phase in solvent extraction of copper[J].The Chinese Journal of Rare Metals,2008,32(6):748-753.
[3]意特冶金技术开发有限责任公司.ACORGA OPT萃取剂对醛肟:酮肟萃取剂的比较研究[C]//湿法冶金技术研讨会文集.北京:意特格冶金技术开发有限责任公司,2012:9-24.Italian Grass Metallurgical Technology Development Co.,Ltd.Comparative study of ACORGA OPT extraction agent and aldoxime:ketoxime extractant[C]//Hydrometallurgy Technology Seminar Corpus.Beijing:Italian Grass Metallurgical Technology Development Co.,Ltd.,2012:9-24.
[4]LAITALA H,LAMPI M,OYI O.Assarel medet JSC Cu SX-TFEW project inbulgaria[C]//Nickel/Cobalt/Copper Conference.Australia:ALTAMetallurgical Services,2011:312.
[5]MILLER G.Contamination management in solvent extraction plants.Nickel/Cobalt/CopperConference.Australia:ALTA Metallurgical Services,2011:1-12.
[6]BEDNARSKI T,SODERSTROM M,WIGGETT S.Oxidation in copper SX processes[C]//Nickel/Cobalt/Copper Conference.Australia:ALTAMetallurgical Services,2011:1-9.
[7]刘晓荣.铜溶剂萃取界面乳化机理及防治研究[D].长沙:中南工业大学,2001:53-68.LIU Xiao-rong.Research on mechanism and prevention of interfacial emulsion formation in copper solvent extraction process[D].Changsha:Central South University,2001:53-68.
[8]刘晓荣,邱冠周,胡岳华,杨俊和.萃取界面乳液的固体微粒稳定机理[J].中南大学学报:自然科学版,2004,35(1):6-10.LIU Xiao-rong,QIU Guan-zhou,HU Yue-hua,YANG Jun-he.Solid particles stabilizing interfacial emulsion in copper-SX[J].Journal of Central South University:Natural Science,2004,35(1):6-10.
[9]王兆慧,谢学辉,柳建设.嗜酸氧化亚铁硫杆菌表面双电层电势分布模拟[J].中国有色金属学报,2011,21(6):1485-1490.WANG Zhao-hui,XIE Xue-hui,LIU Jian-she.Numerical modeling of potential profiles in electrical double layer ofAcidithiobacillusferrooxidanscellsurface[J].TheChinese Journal of Nonferrous Metals,2011,21(6):1485-1490.
[10]倪丙杰,徐得浅,刘绍根.污泥性质的重要影响物质-胞外聚合物(EPS)[J].环境科学与技术,2006,29(3):108-110.NI Bing-jie,XU De-qian,LIU Shao-gen.Extracellular polymeric substance(EPS)and its influence on properties of activated sludge[J].Environmental Science and Technology,2006,29(3):108-110.
[11]MORGAN J M,FORSTER C F,EVISON L A.Comparative study of the nature of biopolymers extracted from anaerobic and activated sludges[J].Water Research,1990,24(6):743-750.
[12]BROWN J M,LESTER J N.Metal removal in activated sludge:The role of bacterial extracellular polymers[J].Water Research,1979,13(9):817-837.
[13]蒲晓芬,胡 涛,周学东.生物膜胞外聚合物的研究[J].国外医学:口腔医学分册,2005,32(5):339-342.PU Xiao-fen,HU Tao,ZHOU Xue-dong.Study of biofilm extracellular polymeric[J].Foreign Medical:Oral Medicine Volume,2005,32(5):339-342.
[14]WOLFGANG R,WALTER M,ECKHART B.Hydrodynamic modeling of droplet coalescence at liquid-liquid interfaces[J].Separation Science and Technology,1992,27(2):129-134.
[15]DARVISHI D,HAGHSHENASD F,ALAMDARI E K,SADRNEZHAAD S K,HALALI M.Synergistic effect of Cyanex 272 and Cyanex 302 on separation of cobalt and nickel by D2EHPA[J].Hydrometallurgy,2005,77:227-238.
[16]李晓晖.钴镍矿微生物浸出液萃取除杂过程乳化物形成机制研究[D].北京:北京有色金属研究总院,2014:29-32,103-110.LI Xiao-hui.Study on the formation mechanism of emulsion in impurity extraction process of cobalt and nickel sulfide ore bioleaching[D]. Beijing: General Research Institute for Nonferrous Metals,2014:29-32,103-110.
[17]RITCEY G M,聂国林.阳离子对铀萃取回路中界面污物生成的影响[J].湿法冶金,1986(4):65-69.RITCEY G M,NIE Guo-lin.Effect of cationic on the formation of crud in the extraction loop of uranium[J].Hydrometallurgy,1986(4):65-69.
[18]陈家镛,于淑秋,伍志春.湿法冶金中铁的分离与应用[M].北京:冶金工业出版社,1991:5-21.CHEN Jia-yong,YU Shu-qiu,WU Zhi-chun.Separation and utilization of ferric from hydrometallurgy[M]. Beijing:Metallurgical Industry Press,1991:5-21.

