PET/CT及其数学预测模型对孤立性肺结节诊断价值的对比研究
林洁,唐坤,殷薇薇,郑祥武,陈杨宗,林信实,戴云飞
(温州医科大学附属第一医院 放射影像中心PET/CT室,浙江 温州 325015)
·论 著·
PET/CT及其数学预测模型对孤立性肺结节诊断价值的对比研究
林洁,唐坤,殷薇薇,郑祥武,陈杨宗,林信实,戴云飞
(温州医科大学附属第一医院 放射影像中心PET/CT室,浙江 温州 325015)
目的:通过受试者工作特征曲线(R0C曲线)分析比较PET/CT及其数学预测模型对孤立性肺结节 (SPN)的诊断价值。方法:对186例行PET/CT检查的SPN患者进行回顾性分析。PET/CT图像分析采用目视法或半定量法对结节的代谢及CT形态学特征进行综合分析判断,判断结果分为良性、良性可能大、良性可能、恶性可能、恶性可能大、恶性,并依次以0、1、2、3、4、5分进行记录。以病灶良恶性结果为应变量,对影响 病灶结果的参数进行单因素和多因素分析,建立诊断SPN良、恶性的回归数学模型。分别计算PET/CT及数学预测模型诊断SPN的灵敏度、特异度、准确度、阳性预测值、阴性预测值,绘制相应R0C曲线并比较两者曲线下面积大小的差异性。结果:PET/CT诊断SPN的灵敏度、特异度、准确度、阳性预测值及阴性预测值分别为97.6%、79.4%、91.4%、90.2%及94.3%。经二元logistic回归分析建立18F-FDG PET/CT诊断SPN良、恶性的数学模型如下:p=ex/(1+ex),x=-8.111+0.091×年龄+1.351×分叶+3.565×血管集束+2.153×胸膜牵 拉+0.447×SUVmax。以数学模型对SPN良恶性进行预测,其诊断SPN的灵敏度、特异度、准确度、阳性预测值及阴性预测值分别为87.8%、81.0%、85.5%、90.0%及77.3%。PET/CT及数学预测模型诊断SPN的R0C曲线下面积分别为0.951±0.015及0.927±0.019,两者间差异无统计学意义(P>0.05)。结论:数学模型作为一 种实验医学其诊断SPN的效能与PET/CT相仿,且不受人为因素干扰,其优势与PET/CT互补,因此可以联合运用、相互佐证,以提高SPN诊断的准确率。
孤立性肺结节;体层摄影术,X线计算机;脱氧葡萄糖;体层摄影术,发射型计算机;二元logistic回归
孤立性肺结节(solitary pulmonary nodule,SPN)是指发生于肺部直径等于或小于3 cm的单发病灶,周边围绕正常肺组织,无与之相关的卫星灶、肺不张及肺炎,亦无肺门及纵隔淋巴结肿大[1]。据报道称,SPN中原发恶性肿瘤约占35%[2],但由于多数SPN病灶体积较小,且良恶性病灶间缺乏特异的影像学特征,故对其进行正确诊断历来是临床面临的重要任务及难点之一。
正电子发射型计算机断层/CT(positron emission tomography,PET/CT)作为一种新型的影像设备,不仅能显示病灶的CT形态学特征,还能从分子水平提供病灶代谢信息,真正实现解剖与功能的完美结合。18氟-脱氧葡萄糖(18F-FDG)PET/CT联合诊断SPN的价值已得到临床的广泛认可。但是,PET/CT 诊断受阅片者的主观因素及临床经验影响较大,其诊断结果的可重复性较低,而数学模型是以统计学为基础的一种客观评价方法,能避免人为因素干扰,其诊断结果可重复性较高,有望为SPN诊断提供一种 可靠、准确的方法。故本研究旨在通过大样本量数据分析,利用受试者工作特征(receive operating characteristics,ROC)曲线比较PET/CT及其数学预测模型对SPN的诊断价值,评价其诊断效率及临床应用价值。
1 资料和方法
1.1 一般资料 回顾性分析2011年9月至2013年6月我院因诊断为SPN而行PET/CT检查的230例患者并进行纳入筛选。入选条件为:①所有患者经影像 学检查均证实为SPN;②所有恶性结节均得到病理学明确诊断,包括手术、穿刺或支气管镜检查;而所有良性结节均经病理或临床随访证实,临床随访包括病灶经抗炎或抗结核治疗后明显缩小或完全消失,或病灶未经治疗,但随访半年以上无明显变化;③所有结节最长径≥6 mm。排除条件为:①有肺部或其他部位原发肿瘤或相关手术病史;②发现远处转移的患者。共纳入研究对象186例,其中男100例,女86例,年龄为26~85岁,平均(61.09±10.98)岁。所有患者检查前均签署知情同意书。
186例中,结节最大径范围为6~30 mm,平均为(18.89±7.02)mm。其中,经病理明确证实的恶性结节共123例:腺癌50例,鳞癌16例,腺鳞癌5例,黏液腺癌2例,细支气管肺泡癌18例,含腺癌成分细支气管肺泡癌4例,含细支气管肺泡癌成分腺癌3例,肉瘤样癌1例,神经内分泌癌2例,不明确病理类型22例;经病理或临床随访证实的良性结节共63例:结核7例,间质性肺炎4例,炎性假瘤2例,错构瘤8例,腺瘤样不典型增生2例,巨淋巴结增生1例,机化性肺炎2例,良性肿瘤性病变9例,肺隐球菌2例,支气管囊肿1例,其他非特异性炎症25例。
1.2 PET/CT检查图像采集 显像仪器为Philips GEMINI TF TOF 64排PET/CT。显像剂为18F-FDG,放化纯度>95%。检查前患者至少禁食6 h,空腹状态下静脉注射显像剂18F-FDG,注射剂量为3.7 MBq/kg。注射后安静休息,60 min后行PET/CT显像。体部采用3D TOF采集模式,共6~7个床位,每个床位1.5 min。CT扫描参数:管电压120 kV,管电流300 mA, 矩阵512×512,准直64×0.625,螺距0.829,旋转时间0.5,CT重建层厚5 mm,层间隔5 mm。以CT数据对PET行进衰减校正,并以有序子集最大期望值迭代(OSEM)进行PET图像重建,PET重建层厚5 mm,层间隔5 mm。重建后CT、PET图像传输至Philips EBW3.0后处理工作站,并分别得到横断位、冠状位、矢状位PET、CT及PET/CT融合图像。
1.3 图像分析
1.3.1 CT图像分析:在不知道病理结果及病灶代谢情况的前提下由两名有经验的放射科医师对结 节的CT影像特征进行独立盲法分析,当两者结果不一致时则由另一位资深放射科医师对图像进行判定并相互协商取得一致。CT图像分析的指标共12项,内容包括:结节大小、密度、部位、边界、磨玻璃密度、分叶、血管集束、胸膜牵拉、毛刺、钙化、空泡、空洞。其中结节大小为测量其最大径,单位mm;密度为结节的平均CT值,单位HU;部位分为右 上、右中、右下及左上、左下;余9项CT征象的有无分别以“1”和“0”的方法表示。
1.3.2 PET图像分析:采用半定量法对病灶代谢的标准摄取值(standard uptake value,SUV)进行测 定。以病灶最大SUV的40%为边界勾画阈值,自动勾 画病灶的感兴趣区(region of interest,ROI),软 件根据患者的体质量、注射剂量及时间自动计算SPN 病灶的最大SUV(SUVmax);当SPN的摄取较低或无摄取以致无法自动勾画ROI时,则以同期CT横断位图像为参照,在PET图像上手动勾画病灶各个层面的ROI,选取各层面中最大SUV为该病灶的SUVmax。
1.3.3 PET/CT联合诊断:由两名同时具有数年CT 及PET诊断经验的医师结合SPN的CT形态特点和PET代谢情况对SPN的良恶性进行主观判断,当两者诊断结果不一致时则由另一位资深PET/CT医师对图像进一步分析并相互协商取得一致。判断结果分为良性、良性可能大、良性可能、恶性可能、恶性可能大、恶性,并依次以0、1、2、3、4、5分进行记录。以≥3分为阳性结果标准,计算PET/CT联合诊断SPN的灵敏度、特异度、准确度、阳性预测值、阴性预测值,绘制相应ROC曲线并计算曲线下面积。
1.3.4 PET/CT数学模型建立及ROC曲线分析:以病灶良恶性结果为应变量,对PET/CT所得独立参数,如患者的性别、年龄及病灶的大小、部位、CT值、边界、磨玻璃成分、分叶、血管集束、胸膜牵拉、毛刺、钙化、空泡、空洞、SUVmax进行单因素和多因素logistic回归分析,并建立诊断SPN良、恶性的回归数学模型。以数学模型对SPN良恶性进行预测,计算模型诊断SPN的灵敏度、特异度、准确性、阳性预测值、阴性预测值,绘制相应ROC曲线并计算曲线下面积。
1.4 统计学处理方法 采用SPSS 17.0统计软件对所有数据进行统计分析。以良恶性结果为应变量,对影响病灶结果的参数进行单因素分析,其中计量资料采用组成t检验,计数或行列表资料采用x2检验;纳入单因素分析有意义的自变量行多因素logistic回归分析并建立诊断SPN良、恶性的回归数学模型。分别绘制PET/CT及数学模型诊断SPN的ROC曲线,并计算曲线下面积,以Z检验分析比较两者曲线下面积大小的差异性。以P<0.05为差异有统计学意义。
2 结果
2.1 PET/CT诊断SPN的结果 PET/CT联合诊断SPN的结果分为良性、良性可能大、良性可能、恶性可能、恶性可能大、恶性,并依次以0、1、2、3、4、5分进行记录,其结果见表1。以≥3分为阳性结果标准,PET/CT诊断SPN的灵敏度、特异度、准确度、阳性预测值及阴性预测值分别为97.6%、79.4%、91.4%、90.2%及94.3%。
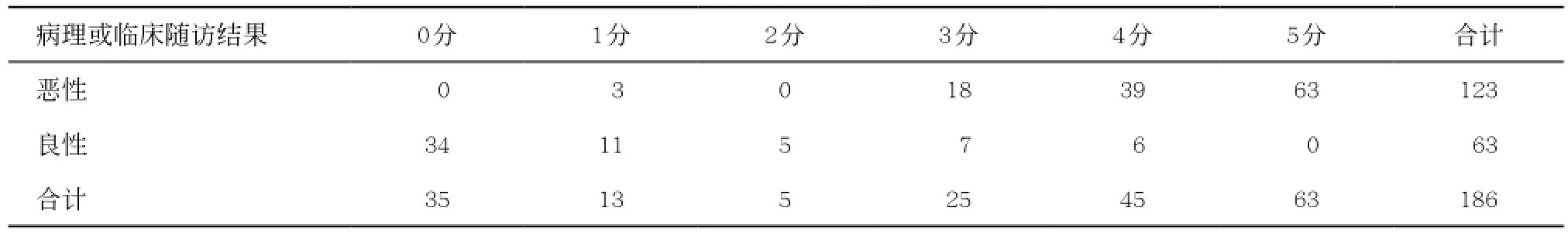
表1 PET/CT诊断SPN结果(例)
2.2 单因素及logistic回归分析结果 将患者的性别、年龄及病灶的大小、部位、CT值、边界、磨玻璃成分、分叶、血管集束、胸膜牵拉、毛刺、钙化、空泡、空洞、SUVmax行单因素分析,结果显示,患者年龄、结节大小、CT值、分叶、胸膜牵拉、血管集束、毛刺、空泡及SUVmax值良、恶性结节间差异具有统计学意义(P<0.01)。
将单因素分析有意义的参数作为自变量行二元logistic回归分析。结果显示,患者年龄、分叶、胸膜牵拉、血管集束及SUVmax为有统计学意义的自变量,见表2。经二元logistic回归分析建立18F-FDG PET/CT诊断SPN良、恶性的数学模型如下:p=ex/ (1+ex),x=-8.111+0.091×年龄+1.351×分叶+3.565 ×血管集束+2.153×胸膜牵拉+0.447×SUVmax。其中e为自然对数;年龄单位为年;分叶:有记为1,无为0;血管集束:有记为1,无记为0;胸膜牵拉:有记为1,无记为0;SUVmax为比值无单位。以数学模型对SPN良恶性进行预测,其诊断SPN的灵敏度、特异度、准确度、阳性预测值及阴性预测值分别为87.8%、81.0%、85.5%、90.0%及77.3%。

表2 logistic回归分析结果
2.3 R0C曲线分析结果 分别绘制PET/CT及数学预测模型诊断SPN的ROC曲线,并计算曲线下面积分别为0.951±0.015及0.927±0.019,见图1-2。经Z检 验,两者曲线下面积差异无统计学意义(P>0.05)。

图1 PET/CT诊断SPN的ROC曲线

图2 数学预测模型诊断SPN的ROC曲线
3 讨论
近来,随着X线及胸部低剂量CT筛查的日益普及,SPN的检出率出现逐年增加的趋势。据报道[3]称,美国每年通过X线或CT体检发现SPN的患者超过150 000 例。虽然SPN大部分为良性病变,但仍有约35%的原发恶性肿瘤[2],其TNM分期多为IA期,且5年生存率可达61%~75%[4]。由于SPN定性困难,约半数肺癌患 者错过手术治疗的最佳时期,从而致5年生存率下降至10%~15%[5]。因此,采取何种有效的检查方法以 提高SPN诊断的准确性,对患者的治疗抉择及其预后都显得甚为重要。
PET/CT作为一种分子影像学检查方法,结合了CT解剖、形态学特征及PET代谢信息对SPN综合诊断,其诊断效能较单纯CT或单纯PET大大提高。Gould 等[6]曾对40项孤立性肺结节的PET/CT研究进行Meta 分析,得出PET/CT对SPN良恶性鉴别的灵敏度和特异度分别达到了96.8%和77.8%。本研究186个SPN中,PET/CT诊断的灵敏度、特异度、准确度、阳性预测值及阴性预测值分别为97.6%、79.4%、91.4%、90.2%及94.3%,这与文献报道相符。但是,PET/CT诊断SPN仍具有局限性,一些良性结节不仅具有恶性灶的CT征象,如分叶、毛刺等,且其SUV代谢值亦与恶性结节重叠[7],这给临床诊断的正确性带来极大困惑。本研究PET/CT诊断SPN假阳性共13例,其中绝大多数为结核、炎性假瘤、隐球菌等形态及代谢特征易与恶性结节混淆的病灶。所以,临床上PET/CT诊断SPN的准确性一定程度上取决于诊断医师的阅片经验,受主观因素的影响较大,不同医师,不同医院或不同地区的PET/CT诊断效能可能不尽相同,尤其对于新起步的PET/CT中心其诊断价值受限较明显。
数学诊断模型是在经验医学基础上的实验医学,是医学研究的高级形式,能很大程度上减低人为主观因素的干扰。国外不少研究[8-9]采用一些定量模型来评估SPN的良恶性程度,并得到业界的认可,如Mayo模型及VA模型。国内杨德松等[10]在此基础上,建立了适合国人SPN良恶性诊断的logistic 回归模型,其预测SPN良恶性的灵敏度为94.9%,特异度为66.0%,阳性预测值为85.3%,阴性预测值为86.1%。虽然上述模型的诊断效能较高,但均建立在CT形态学基础上,并未将PET代谢因素纳为模型自变量分析。
本研究以PET/CT所产生的独立诊断因子作为自变量,将包括SUVmax在内的15项独立因子纳入自变量进行单因素及logistic多因素分析并建立回归方程,结果显示患者年龄、分叶、胸膜牵拉、血管集束及SUVmax为有统计学意义的自变量。分析模型中各风险因子,血管集束征的诊断优势比最高,表明该征象诊断的特异性较高。文献报道,周围型肺癌的血管集束征发生率为37%~83%,显著高于良性结节[11]。这是因为恶性肿瘤细胞可产生肿瘤血管生成因子诱发形成新生血管,其血供异常丰富,造成血管向结节内大量供血。此外,年龄、分叶、胸膜牵拉等风险因子既往文献[9,12]均有报道,但亦有研究[13]认为肿瘤大小为判断肿瘤良恶性的独立影响因素。而本研究单因素分析结果表明结节大小于良恶性两组间差异具有统计学意义,但纳入多因素分析后,由于其权重比过低故未列为独立的风险因子。在本研究中SUVmax虽为判断SPN良恶性的独立影响因素,但是其诊断优势比仅为0.447,究其原因可能在于:①病例纳入时存在选择偏倚,因为大部分良性结节经其他常规检查诊断后未再行PET/CT检查,从而导致入选病例恶性结节比例过高;②与本研究入选结节的病理类型相关,本研究中支气管肺泡癌及含该成分的肺癌比重较大,该类结节FDG摄取值较低;而良性结节中FDG高摄取的病灶较多,如结核、炎性假瘤、肺隐球菌等,从而导致良恶性结节间SUVmax值存在较大比例的重叠,这也是单纯PET诊断SPN效能较低的原因之一。
以所得数学模型对SPN良恶性进行预测,其诊断的灵敏度、特异度、准确度、阳性预测值及阴性预测值分别为87.8%、81.0%、85.5%、90.0%及77.3%。经ROC曲线分析,PET/CT及数学预测模型诊断SPN的ROC曲线下面积均大于0.9,且两者间差异无统计学意义,说明两者诊断SPN的效能相仿。但是,本中心数据模型的建立是基于回顾性研究,样本量仍较小,且在因素分析中,模型不够简化,尚不能完全取代医师的经验判断,今后尚需更大样本量的补充以对模型进行校验。
综上所述,PET/CT诊断SPN的价值虽然较高,但易受诊断的主观因素及临床经验影响,诊断可重复性较低,而数学模型作为一种实验医学其诊断SPN的效能与PET/CT相仿,且不受人为因素干扰,因此其优势与PET/CT互补,两者可联合运用,相互佐证,以提高SPN诊断的准确率。
[1] Tsushina Y,Tateishi U,Uno H,et al.Diagnostic perfor-mance of PET/CT in differentiation of malignant and benign non-solid solitary pulmonary noules[J] .Ann Nucl Med,2008,22(7): 571-577.
[2] Jemal A,Thomas A,Murray T,et al.Cancer statistics,2002 [J] .CA Cancer J Clin,2002,52(1): 23-47.
[3] Tan BB,Flaherty KR,Kazerooni EA,et al.The solitary pul-monary nodule[J] .Chest,2003,123(1 suppl): 89-96.
[4] Mountain CF.Revisions in the international system for stag-ing lung cancer[J] .Chest,1997,111(6): 1710-1717.
[5] Yankelevitz DF,Henschke CI.Small solitary pulmonary nodules[J] .Radiol Clin North Am,2000,38(3): 471-478.
[6] Gould MK,Maclean CC,Kuschner WG,et al.Accuracy of positron emission tomography for diagnosis of pulmonary nodules and mass lesions:a meta analysis[J] .JAMA,2001,285(7): 914-924.
[7] 林洁,唐坤,殷薇薇,等.双时相PET/CT显像对低代谢孤立性肺结节的诊断价值[J] .温州医科大学学报,2014,44 (9): 688-691.
[8] Swensen SJ,Silverstein MD,Iistrup DM,et a1.The proba-bility of malignancy in solitary pulmonary nodules: applica-tion to small radiologically indeterminate nodules[J] .Arch Intern Med,1997,157(8): 849-855.
[9] Gould MK,Ananth L,Bamett PG.A clinical model to esti-mate the pretest probability of lung cancer in patients with solitary pulmonary nodules[J] .Chest,2007,131(2): 383-388.
[10] 杨德松,李运,姜冠潮,等.孤立性肺结节良恶性判断数学预测模型的临床验证及应用[J] .中华胸心血管外科杂志,2012,2(28): 82-85.
[11] 韩玉成,郎志谨,张连君,等.高分辨率CT对周围型小肺癌的诊断价值[J] .中华放射学杂志,1994,28: 737-740.
[12] Tian R,Su MG,Tian Y,et al.Development of a predicting model to estimate the probability of malignancy of solitary pulmonary nodules[J] .Sichuan Da Xue Xue Bao Yi Xue Ban,2012,43 (3): 404-408.
[13] Seemann MD,Seemann O,Luboldt W,et al.Differentiation of malignant from benign solitary pulmonary lesions using chest radiography,spiral CT and HRCT[J] .Lung Cancer,2000,29(2): 105-124.
(本文编辑:丁敏娇)
The comparative study of18F-FDG PET/CT and mathematical prediction model in diagnosis of solitary pulmonary nodule
LIN Jie,TANG Kun,YIN Weiwei,ZHENG Xiangwu,CHEN Yangzong,LIN Xinshi,DAI Yunfei.
Department of PET/CT,Raiology Imaging Center,the First Affiliated Hospital of Wenzhou Medical University,Wenzhou,325015
Objective:To compare and analyze the value of18F-FDG PET/CT and the mathematical prediction model in diagnosis of solitary pulmonary nodule (SPN),using receiver operating characteristic (ROC) curves analysis.Methods: All of 186 patients confirmed with SPN and performed with PET/CT were retrospectively analyzed in this study.For PET/CT integrated images,the morphology and metabolism of lesions were semiquantitatively or visual analysed by observers.A 5-score system was used to classify the diagnostic results of PET/CT integrated images: 0,definitely benign; 1,benign more likely; 2,probably benign; 3,probably malignant; 4,malignant more likely; and 5,definitely malignant.The logistic mathematical model was established with univariate analysis and multivariate analysis.The sensitivity,specificity,accuracy,positive predictive value and negative predictive value of PET/CT and the mathematical model in diagnosis of SPN were calculated respectively.The difference of the areas under the ROC curves (AUC) between PET/CT and the mathematical model was compared.Results:The sensitivity,specificity,accuracy,positive predictive value and negative predictive value of PET/CT were 97.6%,79.4%,91.4%,90.2% and 94.3%,respectively.The mathematical model established by logistic regression analysis was: p=ex/(1+ex),x=-8.111+0.091×age+1.351×lobulation+3.565×vascular convergence+2.153×retraction of pleural+0.447×SUVmax.The sensitivity,specificity,accuracy,positive predictive value and negative predictive value of the model for prediction of SPN were 87.8%,81.0%,85.5%,90.0%and 77.3% respectively.The AUCs of PET/CT and mathematical model were 0.951±0.015 and 0.927±0.019.There was no statistically significant in difference of AUC between PET/CT and mathematical model (P>0.05).Conclusion:The value of mathematical prediction model in diagnosis of SPN is similar to PET/CT and not affected by subjective factors.Therefore,it should be used in clinical practice combined with PET/CT for improving diagnostic accuracy.
solitary pulmonary nodule; tomography,X-ray computed; deoxyglucose; tomography,emissioncomputed; binary logistic
R81
A
10.3969/j.issn.2095-9400.2015.05.009
2014-07-05
林洁(1982-),女,浙江温州人,主治医师。
郑祥武,主任医师,Email:zxw111@sina.com。

