吉西他滨或多西他赛联合卡铂治疗60岁以下晚期肺鳞癌疗效及预后追踪分析
卞晓山,王秀问,魏长宏,王作志
(1.武警山东省总队医院肿瘤科;2.山东大学齐鲁医院化疗科,山东 济南 250014)
吉西他滨或多西他赛联合卡铂治疗60岁以下晚期肺鳞癌疗效及预后追踪分析
卞晓山1,王秀问2,魏长宏1,王作志1
(1.武警山东省总队医院肿瘤科;2.山东大学齐鲁医院化疗科,山东 济南250014)
摘要:目的探讨吉西他滨或多西他赛联合卡铂治疗60岁以下晚期肺鳞癌疗效,以及对预后的影响。方法91例60岁以下初治晚期肺鳞癌患者随机分为吉西他滨联合卡铂组(GC组,n=44)和多西他赛联合卡铂组(DC组,n=47),GC组患者第1天和第8天分别给予1 000 mg·m-2吉西他滨静脉滴注,第1天卡铂AUC=5剂量静脉滴注;DC组患者第1d给予75 mg·m-2多西他赛静脉滴注,第1d卡铂AUC=5剂量静脉滴注。记录两组患者临床疗效、毒副反应及生存质量情况,利用Kaplan-Meier法对患者生存时间进行分析。结果GC组患者总有效率38.6%,DC组总有效率40.0%,两组相比差异无统计学意义(P>0.05);两组患者恶心呕吐、肝功能异常发生率差异无统计学意义(P>0.05),两组患者贫血发生率差异无统计学意义(P>0.05),GC组血小板减少发生率和粒细胞减少发生率均高于DC组,差异均有统计学意义(P<0.05),但GC组Ⅲ~Ⅳ级粒细胞减少发生率15.9%,与DC组的8.5%,差异无统计学意义(P>0.05);两组患者治疗后生存质量各项得分均较治疗前得分提高,尤其是咳嗽、疼痛得分显著提高;GC组患者中位生存时间14.5个月,1年生存率52.7%,2年生存率19.6%;DC组患者中位生存时间11.2个月,1年生存率44.6%,2年生存率11.9%,经Log-rank检验,两组患者生存时间差异有统计学意义(χ2=4.634,P<0.05)。结论 吉西他滨或多西他赛联合卡铂用于60岁以下晚期肺鳞癌患者,总体临床疗效及在改善患者生存质量方面相当,但吉西他滨联合卡铂更有利于延长患者生存时间。
关键词:肺鳞癌;吉西他滨;多西他赛;预后
Efficacy of gemcitabine or docetaxel combined with carboplatin
非小细胞肺癌(NSCLC)是肺癌的主要类型,而其中肺鳞癌的发病约占了NSCLC的25%[1],由于肺鳞癌早期病情较为隐匿,确诊时已进展到晚期,错过手术治疗的最佳时机,化疗成为晚期肺鳞癌治疗的主要手段[2]。常采用吉西他滨、紫杉类药物与铂类联合的化疗方案用于晚期肺癌患者,且临床效果已得到研究证实[3],然而,不同化疗方案是否对60岁以下晚期肺鳞癌更为有效,以及何种化疗方案更有助于改善60岁以下晚期肺鳞癌患者预后鲜有报道。本研究分别将吉西他滨或多西他赛联合卡铂应用于60岁以下晚期肺鳞癌患者,追踪观察其临床效果、毒副反应及对患者生存时间的影响,以期为60岁以下晚期肺鳞癌患者化疗方案的确定提供参考。
1资料与方法
1.1一般资料选取2008年1月至2012年1月在我院肿瘤内科接受化疗治疗的晚期肺鳞癌患者91例,病例入选标准:年龄<60岁,且经组织病理学或细胞学检查确诊;根据AJCC分期标准Ⅲb期或Ⅳ期;首次治疗,Karnofsky评分>60分,PS评分:0~2分,且预计生存时间超过3个月;骨髓造血功能正常,心电图检查正常,且肝肾等重要脏器功能基本正常。其中,男性62例,女性29例,年龄23~59岁,平均年龄(42.7±10.4)岁,利用随机数字表随机分为吉西他滨联合卡铂组(GC组)和多西他赛联合卡铂组(DC组),其中,GC组44例,男性29例,女性15例,平均年龄(43.1±11.3)岁,Ⅲb期14例,Ⅳ期30例,PS平均得分(0.7±0.4)分;DC组47例,男性33例,女性14例,平均年龄(42.4±9.7)岁,Ⅲb期17例,Ⅳ期30例,PS平均得分(0.8±0.4)分,两组患者一般情况指标差异均无统计学意义(P>0.05),均衡可比。本研究经过医院伦理委员会批准。
1.2方法
1.2.1治疗方案GC组:第1天和第8天分别将1 000 mg·m-2吉西他滨静脉滴注,联合第1天卡铂曲线下面积(AUC)=5剂量静脉滴注,治疗21 d为1个周期。DC组:第1天将75 mg·m-2多西他赛静脉滴注,联合第1天卡铂AUC=5剂量静脉滴注,治疗21 d 为1个周期。两组患者均于化疗前给予止吐药以预防性止吐,化疗期间监测血常规,给予对症支持治疗,两组患者均行至少2个周期化疗,且不超过4个周期。
1.2.2评价指标两组患者均每治疗2个周期对治疗效果及毒副反应进行评估[4],根据实体瘤评价标准对治疗客观疗效进行评价:完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),总有效= CR+ PR;根据国际肿瘤通用毒性评价标准对毒力效应进行分级:0~Ⅳ级;两组患者分别于化疗前和末次化疗后21d利用肺癌症状评分量表(LCSS)对患者生活质量进行评估[5]:从呼吸障碍、食欲减退、乏力、咯血、咳嗽、疼痛6个方面进行评分,严重0分,明显25分,中度50分,轻度75分,无100分。两组患者治疗后均每3个月随访1次,随访截止2014年12月,未出现失访病例。

2结果
2.1两组患者化疗周期及临床治疗效果情况两组患者化疗周期分布差异无统计学意义(P>0.05),详见表1;GC组患者总有效率38.6%,DC组总有效率40.0%,两组相比差异无统计学意义(P>0.05),见表2。

表1 两组患者化疗周期分布情况/n,%
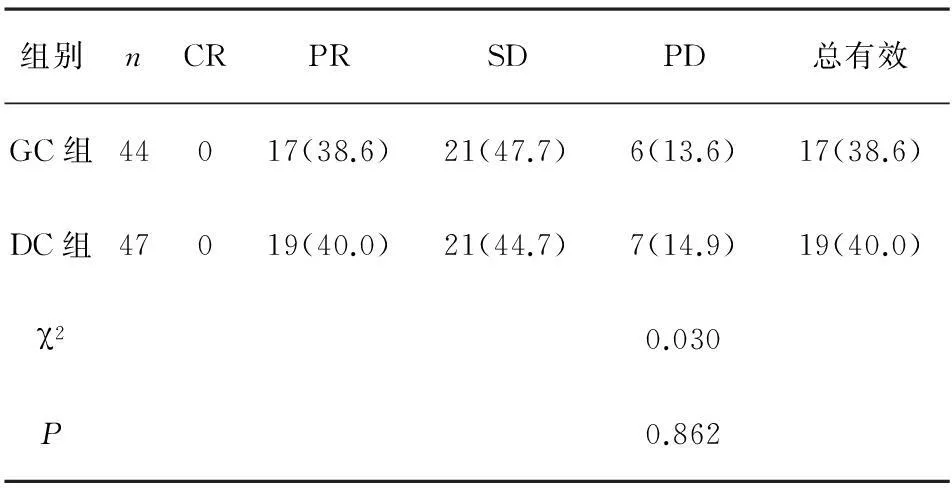
表2 两组患者临床治疗效果情况/n,%
2.2两组患者治疗过程中毒副反应发生情况两组患者均未出现因化疗治疗相关的死亡,毒副反应主要表现在消化道和血液学方面,两组患者恶心呕吐、肝功能异常发生率差异无统计学意义(P>0.05),两组患者贫血发生率差异无统计学意义(P>0.05),GC组血小板减少发生率和粒细胞减少发生率均高于DC组,差异均有统计学意义(P<0.05),但GC组Ⅲ~Ⅳ级粒细胞减少发生率15.9%,与DC组的8.5%,差异无统计学意义(P>0.05),见表3。

表3 两组患者治疗过程中毒副反应发生情况(n,%)
注:与DC组相比,*P<0.05。
2.3两组患者治疗前后生存质量评分两组患者治疗前生存质量各项得分差异均无统计学意义(P>0.05),两组患者治疗后生存质量各项得分差异均无统计学意义(P>0.05),但均较治疗前得分提高,尤其是咳嗽、疼痛得分显著提高,差异均有统计学意义(P<0.05),见表4。
2.4两组患者随访情况GC组患者中位生存时间14.5个月,1年生存率52.7%,2年生存率19.6%;DC组患者中位生存时间11.2个月,1年生存率44.6%,2年生存率11.9%,经Log-rank检验,两组患者生存时间差异有统计学意义(χ2=4.634,P<0.05),见图1。

±s,分)
注:与治疗前相比,aP<0.05;与DC组同一时间相比,bP<0.05。

图1 两组患者治疗后Kaplan-Meier生存曲线
3讨论
肺鳞癌作为NSCLC重要类型,在60岁以下人群中有一定的发病比例,由于年轻人群对疾病具有较强的抵抗能力,加之肺鳞癌早期症状较为隐匿,致使患者发现时已进展为晚期[6]。对于晚期肺鳞癌患者,目前临床上主要以化疗治疗为主,吉西他滨作为第三代化疗药,是细胞周期特异性抗代谢类药物,可促使肿瘤细胞凋亡,与铂类联用方案是目前治疗晚期NSCLC一线选择[7],多西他赛作为紫杉类药物,可阻断M期肿瘤细胞,对增殖期细胞作用强,已被作为NSCLC治疗的一线和二线化疗药[8],卡铂作为第二代广谱抗肿瘤药物,与顺铂临床疗效相当,且胃肠道反应、肾脏及耳毒性均低于顺铂,患者有很好的耐受性[9]。本研究分别将吉西他滨或多西他赛联合卡铂应用于60岁以下晚期肺鳞癌患者,取得了一定临床效果。
本研究显示,GC组患者总有效率38.6%,DC组总有效率40.0%,两组相比差异无统计学意义(P>0.05),说明GC方案和DC方案应用于60岁以下初治肺鳞癌患者,临床疗效相当。本研究显示,两组患者化疗后消化道不良反应发生率无差异,GC组患者虽贫血发生率与DC组无差异,但血小板减少发生率和粒细胞减少发生率均高于DC组,但GC组Ⅲ~Ⅳ级粒细胞减少发生率15.9%与DC组的8.5%无差异,说明GC方案治疗后会出现骨髓抑制,与张贝贝等[10]报道相同,但60岁以下患者并未出现相关出血事件,临床可控,可能与年轻患者总体身体素质相对较好有关[11]。本研究显示,GC和DC治疗方案均可改善患者生存质量各项症状评分,尤其是咳嗽、疼痛得分显著提高,说明两种方案可改善患者生活质量。本研究显示,在对两组患者预后随访中,GC组患者中位生存时间14.5个月,1年生存率52.7%,2年生存率19.6%;DC组患者中位生存时间11.2个月,1年生存率44.6%,2年生存率11.9%,说明GC治疗方案更有利于延长60岁以下肺鳞癌患者生存时间,在改善患者预后方面更有优势,与Wu等[12]研究结论相同。
综上所述,吉西他滨联合卡铂与多西他赛联合卡铂用于60岁以下晚期肺鳞癌患者治疗,总体临床疗效及在改善患者生存质量方面相当,吉西他滨联合卡铂治疗后血液学不良反应发生率较高,但患者可耐受,且更有利于延长患者生存时间,因此,吉西他滨联合卡铂可能更适应于60岁以下晚期肺鳞癌患者治疗。
参考文献:
[1]Okamoto T,Suzuki Y, Fujishita T, et al. The prognostic impact of the amount of tobacco smoking in non-small cell lung cancer -differences between adenocarcinoma and squamous cell carcinoma[J]. Lung Cancer, 2014, 85(2):125-130.
[2]Liao BC, Shao YY, Chen HM, et al. Comparative effectiveness of first-line platinum-based chemotherapy regimens for advanced lung squamous cell carcinoma[J]. Clin Lung Cancer, 2015, 16(2):137-143.
[3]Horita N,Woo T,Miyazawa N,et al. Pre-operative chemotherapy for non-small cell lung carcinoma[J]. Transl Lung Cancer Res, 2015, 4(1):8-14.
[4]施勋,余新民,张沂平,等. 培美曲塞或吉西他滨联合卡铂一线治疗老年晚期非小细胞肺癌的疗效和安全性[J].中华肿瘤杂志, 2013, 35(3):221-224.
[5]朱彦博,王振欣,熊峰,等.培美曲塞与吉西他滨分别联合卡铂对老年晚期NSCLC的疗效对比及安全性评价[J].中国生化药物杂志, 2014, 34(4):145-147.
[6]Deesomchok A, Dechayonbancha N, Thongprasert S. Lung cancer in Maharaj Nakorn Chiang Mai Hospital: comparison of the clinical manifestations between the young and old age groups[J]. J Med Assoc Thai, 2005, 88(9):1236-1241.
[7]Shelley MD, Jones G, Cleves A, et al. Intravesical gemcitabine therapy for non-muscle invasive bladder cancer (NMIBC): a systematic review[J]. BJU Int, 2012,109(4):496-505.
[8]Perletti G, Monti E, Marras E, et al. Efficacy and safety of second-line agents for treatment of metastatic castration-resistant prostate cancer progressing after docetaxel. A systematic review and meta-analysis[J]. Arch Ital Urol Androl, 2015, 87(2):121-129.
[9]Lorusso D, Petrelli F, Coinu A, et al. A systematic review comparing cisplatin and carboplatin plus paclitaxel-based chemotherapy for recurrent or metastatic cervical cancer[J]. Gynecol Oncol, 2014, 133(1):117-123.
[10] 张贝贝, 宋正波, 何春晓, 等. 不同剂量吉西他滨联合卡铂一线治疗晚期非小细胞肺癌的临床疗效[J]. 肿瘤学杂志, 2013, 19(12):977-980.
[11] 王永,唐鹏飞,杨玉蓉.青年肺癌与老年肺癌临床特点研究[J]. 中国全科医学, 2012, 15(23):2674-2676.
[12] Wu ZY, Guan HH, Lin ZX, et al. Combination of low-dose gemcitabine in 6-hour infusion and carboplatin is a favorable option for patients in poor performance status with advanced non-small cell lung cancer[J]. J Chemother, 2014, 26(5):306-311.
in treatment of advanced lung squamous cell carcinoma patients
under 60 years old and prognosis trace analysis
BIAN Xiao-shan, WANG Xiu-wen, WEI Chang-hong, et al
(DepartmentofOncology,ShandongProvincialCorpsHospital,ChinesePeople's
ArmedPoliceForce,Jinan,Shandong250014,China)
Abstract:ObjectiveTo explore the efficacy of gemcitabine or docetaxel combined with carboplatin in treatment of advanced lung squamous cell carcinoma patients under 60 years old and the impact on prognosis.MethodsA total of 91 cases of advanced lung squamous cell carcinoma patients under 60 years old previously untreated were randomized into gemcitabine combined with carboplatin group (GC group,n=44) and docetaxel combined with carboplatin group (DC group,n=47). Patients in GC group were given 1 000 mg·m-2gemcitabine intravenous infusion at 1 d and 8 d, and carboplatin AUC=5 dose intravenous infusion. Patients in DC group were given 75 mg·m-2docetaxel intravenously at 1d, and carboplatin AUC=5 dose intravenous infusion. The clinical efficacy, toxicity and quality of life of the two groups were recorded. The survival spans of patients were analyzed by using Kaplan-Meier method. Results The total efficiency rates of GC group and the DC group were 38.6% and 40.0%, with no significant difference (P>0.05). The differences in incidences of nausea and vomiting and abnormal liver function between the two groups were no significant (P>0.05). The differences of incidences of anemia between the two groups were no significant (P>0.05). The incidences of thrombocytopenia and neutropenia in GC group were higher than the DC group with significant differences(P<0.05). But the incidence of Ⅲ~Ⅳ grade neutropenia in GC group was 15.9% with no significant difference from the DC group (8.5%,P>0.05). The scores of quality of life after treatment in the two groups were higher than before treatment, of which the scores of cough and pain improved significantly. In GC group, the median survival time was 14.5 months, 1-year survival rate 52.7% and 2-year survival rate 19.6%. In DC group, the median survival time was 11.2 months, 1-year survival rate 44.6% and 2-year survival rate 11.9%. By Log-rank test, the differences in survival time between the two groups were statistically significant (χ2=4.634,P<0.05). Conclusion As for gemcitabine or docetaxel combined with carboplatin in treatment of advanced lung squamous cell carcinoma patients under 60-year-old, the overall clinical efficacy and the improved quality of life were similar. But gemcitabine combined with carboplatin was more conducive to prolong the survival time of patients.
Key words:squamous cell lung carcinoma; gemcitabine; docetaxel; prognosis
收稿日期:(2015-09-09,修回日期:2015-11-07)
doi:10.3969/j.issn.1009-6469.2016.01.055
通信作者:王秀问,男,主任医师,研究方向:肿瘤诊断和综合治疗,E-mail:2019945399@qq.com

