微波助离子液体中Y掺杂TiO2光催化剂制备及微波强化光催化活性
李曼弯,张 美,毕先均
(云南师范大学 化学化工学院,云南 昆明 650500)
微波助离子液体中Y掺杂TiO2光催化剂制备及微波强化光催化活性
李曼弯,张美,毕先均*
(云南师范大学 化学化工学院,云南 昆明 650500)
摘要:在微波助离子液体介质中制备稀土元素Y掺杂改性TiO2光催化剂,以提高催化剂的光催化降解活性,用XRD、SEM和BET等测试手段对催化剂结构进行表征;以甲基橙溶液和苯酚溶液为模拟污染物,分别在紫外光照(UV)和微波辐射-紫外光照(MW-UV)条件下考察TiO2-Y催化剂的光催化活性;以对苯二甲酸作为荧光探针利用荧光技术检测TiO2-Y催化剂表面所产生的羟基自由基,并对光催化降解反应进行动力学分析,探索了光催化降解反应机理. 实验结果表明,通过优化反应条件后制得的TiO2-Y催化剂具有较高光催化活性和热稳定性,在UV和UV-MW条件下降解甲基橙和苯酚溶液1.5 h后,甲基橙降解率分别为98.3%和99.5%,苯酚降解率分别为97.5%和98.2%. 荧光光谱分析表明,TiO2-Y在MW-UV条件下产生的羟基自由基比UV条件下要多,因而微波辐照具有强化TiO2-Y降解模拟污染物的作用;反应动力学数据分析表明,TiO2-Y光催化降解甲基橙溶液反应呈现一级反应动力学规律,其表观速率常数K最大值为0.051 9 min(-1).
关键词:离子液体;钇掺杂;TiO2光催化剂;微波强化;光催化活性
高效、低成本二氧化钛因其具有良好的光化学性质而备受关注,但是TiO2禁带宽度较大,致使其光谱响应范围小,因此减小禁带宽度,拓宽其光谱响应范围成为改善TiO2光催化活性的有效方法. 在众多改性研究中,元素掺杂被认为是一种有效的改进途径,如金属元素、非金属元素或者稀土金属元素等单元素掺杂可以阻止TiO2晶粒增大,从而增大其比表面积;此外还可以增强对可见光的吸收,进一步提高光催化活性. 但是,金属元素掺杂的TiO2具有热不稳定性,载流子复合速率增加,使其在紫外区的光催化性能下降;相比较而言,非金属掺杂不影响其在紫外光区的活性,但是对TiO2的改性不明显[1-2].
本课题组曾在微波助离子液体条件下,制备了金属元素Fe、Zn、Cu及稀土元素钕、铈等掺杂的TiO2光催化剂,并利用微波辐射对模拟污染物甲基橙进行了降解测试. 实验结果表明,在微波(MW)、紫外(UV)、微波-紫外(MW-UV) 3种降解条件下,催化剂对甲基橙降解率始终是MW-UV照射条件下要高于UV照射,而 UV照射条件下高于MW辐照,这表明微波-紫外光照具有强化催化剂降解甲基橙的效果. 催化剂的结构分析测试结果表明,催化剂大体上为球形,其结晶度及分散性较好,且表面含有较多的羟基,从而使其具有较高的光催化活性[3-8]. 鉴于元素周期表中稀土元素钇与元素钛处于对角线位置,具有相似的化学性质,两者离子半径差值也较小(分别为0.089 nm和0.068 nm),因而Y3+有可能进入TiO2晶格间隙,分布于TiO2晶格中;并且从能级上来看,Y3+能级靠近TiO2导带,这可能抑制电子-空穴对发生复合,从而提高催化剂的光催化活性[9]. 本文中,本课题组继续在微波助离子液体条件下,制备钇元素掺杂改性TiO2光催化剂,分别在紫外和微波-紫外照射条件下测试其对甲基橙及苯酚溶液的降解率,以考察稀土元素钇掺杂改性制备掺杂型TiO2催化剂的光催化活性,旨在进一步提高掺杂改性TiO2催化剂的光催化活性.
1实验部分
1.1实验试剂与仪器
实验主要试剂:硝酸钇、钛酸丁酯、1-甲基咪唑、溴代正丁烷、对苯二甲酸等均为分析纯. 主要仪器:XH-300UL电脑微波超声波紫外光组合催化合成仪和XH-200A电脑微波固液相合成/萃取仪均购自北京祥鹄科技发展有限公司,美国康塔公司NOVE2000-e型表面分析仪,日本日立高技术公司HITACHI(日立)F-4600型荧光光谱仪等.
1.2TiO2-Y催化剂的制备
TiO2-Y光催化剂的制备采用溶胶-凝胶法. 量取3.4 mL钛酸丁酯与一定量的[Bmim]PF6离子液体,逐滴加入含17.5 mL无水乙醇的烧杯中,搅拌形成溶液A;称取硝酸钇与钛酸正丁酯(n(Y3+)/n(Ti4+)之比依次为0、0.5%、0.6%、0.7%、0.8%、0.9%)分别溶于18 mL二次蒸馏水中得到溶液B;再将溶液B缓慢滴入溶液A中,搅拌1 h,洗涤并真空抽滤,将样品置于微波炉中干燥,研磨,放入高温箱式电阻炉中高温煅烧,得到TiO2-Y光催化剂. 实验过程中,离子液体的制备,催化剂的制备过程中离子液体的用量、微波干燥功率和时间、煅烧温度和时间等条件的确定,催化剂的结构测试和表征方法等详见参考文献[3-8].
1.3光催化活性测试
光催化降解反应分别在自制高压汞灯紫外光降解装置与XH-300UL电脑微波超声波组合催化合成仪中进行,模拟污染物为甲基橙与苯酚溶液. 光催化降解过程XH-300UL电脑微波超声波组合催化合成仪有3种光源: 微波(500 W)、紫外(250 W高压汞灯)、微波(500 W)-紫外(250 W高压汞灯). 高压汞灯自制装置的实验条件为:室温298 K、300 W高压汞灯,反应器距紫外光源15 cm.
光催化降解模拟污染物测试操作如下:称取50 mg TiO2-Y光催化剂加入盛有50 mL 10 mg/L模拟污染物的烧杯中,然后放置于催化合成仪中进行降解反应. 反应结束后取适量降解液放入离心机以4 000 r/min离心20 min,取上层清液在722N型可见分光光度计中,在最大吸收波长(464 nm) 处测定吸光度A,采用公式η1= (At-A0)/At×100% (A0为初始溶液吸光度;At为t时刻吸光度)计算甲基橙降解率η1. 空白实验表明,在没有TiO2-Y催化剂只有紫外光照的情况下,甲基橙和苯酚溶液的浓度基本不变;在有TiO2-Y存在而无紫外光照时,室温下放置相同时间后甲基橙和苯酚溶液的浓度也无明显变化.
苯酚溶液吸光度测定:采用4-氨基安替比林分光光度法[10],即酚类化合物与显色剂(pH=10±0.2)作用后会生成橙红色的安替比林染料. 实验选取K2S2O8与4-氨基安替比林作为显色剂,NH4Cl-NH3作为缓冲溶液. 具体操作如下:量取0.5 mL NH4Cl-NH3缓冲溶液加入盛有10 mL上层清液的比色管中,摇匀,再分别加入1 mL K2S2O8(C=30 g/L)溶液与1 mL 4-氨基安替比林溶液(C=20 g/L),摇匀,静置10 min,于510 nm处测其吸光度,同样利用公式η2= (At-A0)/At×100%计算苯酚降解率η2.
1.4光催化降解反应中羟基自由基测定
TiO2-Y催化过程中以对苯二甲酸作为荧光探针可测定生成羟基自由基,这是因为其可与·OH快速反应生成具有特征荧光的2-羟基对苯二甲酸,故此可通过测定荧光光谱强度确定光催化剂与水界面生成·OH自由基的量[11-12]. 实验分别测定了UV(P=250 W)、MW(P=500 W)、MW-UV 3种条件下产生的羟基自由基. 室温298 K,微波辐照时间分别设为0、5、10、15和20 min.
测定·OH操作的具体过程为:取50 mg TiO2-Y光催化剂加入盛有25 mL一定浓度的对苯二甲酸与氢氧化钠的混合液中,分别测定UV、MW、MW-UV条件下·OH浓度. 实验结束后离心混合物,取上层清液,用Hitachi F-4600型荧光光谱仪分别测定邻羟基对苯二甲酸产生的荧光光谱强度,激发波长为312 nm.
1.5光催化降解反应动力学数据测试
甲基橙是一种化学性质稳定的含氮染料,可通过光催化降解甲基橙溶液来检测不同样品的光催化活性. 称取50 mg TiO2-Y加入50 mL甲基橙溶液(C=10 mg/L)中进行降解反应,降解前将催化剂与甲基橙溶液混合物置于黑暗中避光搅拌,使二者达到吸附平衡. 待光催化降解完成后离心分离,取上层清液,用722N型可见分光光度计测定甲基橙溶液的吸光度,利用公式η= (At-A)/At×100 % 计算甲基橙降解率. 根据一级反应动力学方程Ln(A/At) = - kt(A为初始溶液吸光度;At为t时刻吸光度)线性回归后得到表观速率常数.
2结果与讨论
2.1钇掺杂量对TiO2-Y光催化活性的影响
在TiO2-Y催化剂制备过程中,固定离子液体体积为3.0 mL、微波干燥功率210 W、微波干燥时间20 min、煅烧温度650 ℃、煅烧时间3 h,通过改变硝酸钇加入量[n(Y3+)/n(Ti4+)=0.5%、0.6%、0.7%、0.8%、0.9%]制得不同钇掺杂量的催化剂,再以甲基橙溶液为模拟降解物,固定紫外光照时间为1.5 h,考察了钇掺杂量对TiO2-Y光催化降解活性的影响,结果如图1所示. 从图1可知,当钇加入量n(Y3+)/n(Ti4+) < 0.7%时,TiO2-Y催化剂对甲基橙溶液降解率随硝酸钇加入量增加而升高;当n(Y3+)/n(Ti4+) > 0.7%时,催化活性反而随着硝酸钇加入量增加而降低;而当n(Y3+)/n(Ti4+)=0.7%时,TiO2-Y催化剂对甲基橙降解率达到极大值98.3%,表明催化剂具有较高光催化活性. 其原因可能是由于稀土元素钇的f轨道与降解物相互配位,从而使TiO2掺杂稀土钇元素后其催化活性得以提高. 然而,如果硝酸钇掺杂量过大,过多钇会沉积在TiO2表面,使电子-空穴向催化剂表面传递受阻,同时稀土元素钇会形成电荷载流子复合中心,从而降低光催化活性[13-14]. 因此,硝酸钇最佳掺杂量为n(Y3+)/n(Ti4+)=0.7%.

图1 钇掺杂量对TiO2-Y降解甲基橙降解率的影响Fig.1 Influence of Y-doped amount for TiO2-Y on the degradation rate of methyl orange
2.2微波-紫外辅助强化TiO2-Y光催化活性
取最佳制备条件(离子液体体积3.0 mL、钇加入量0.7%、微波干燥功率210 W、微波干燥时间20 min、煅烧温度650 ℃和煅烧时间3 h)制得的TiO2-Y催化剂,分别于UV和MW-UV两种降解条件下,考察其对模拟污染物的降解情况,结果如图2所示. 从图2可知,模拟污染物降解率随着降解时间的延长而逐渐升高,当降解时间为1.5 h时,UV和MW-UV两种照射条件下甲基橙降解率分别为98.3%和99.5%,苯酚降解率分别为97.5%和98.2%;当降解时间达到2 h后,两种模拟污染物几乎达到完全降解;并且在整个降解反应过程中,TiO2-Y催化剂对模拟污染物降解率始终为MW-UV照射条件下要高于UV照射,这表明微波辐射-紫外光照具有强化TiO2-Y降解模拟污染物的作用. 在298 K恒温条件下,仅用微波辐射降解模拟污染物时只能生成中间产物,模拟污染物降解率极低,表明只有极少部分模拟污染物发生降解;但在紫外光照的条件下,使用微波辐射能够显著提高模拟污染物降解率,说明微波辐射-紫外光照下的降解率均比紫外光照或微波辐射下的要高. 微波辐射能够增加催化剂催化活性,可能原因是在微波场的作用下,TiO2-Y催化剂表面能够产生更多的·OH自由基,这有利于降解和矿化模拟污染物,同时能够抑制光生电子-空穴复合,从而提高其光催化降解活性. 这表明微波辐射加热除有利于掺杂型TiO2-Y催化剂的合成外,还具有强化掺杂型TiO2-Y催化剂光催化降解模拟污染物的作用.

图2 UV和UV-MW条件下TiO2-Y催化剂对甲基橙和苯酚的降解率Fig.2 Degradation rate of methyl orange and solution for TiO2-Y catalyst under UV and MW-UV
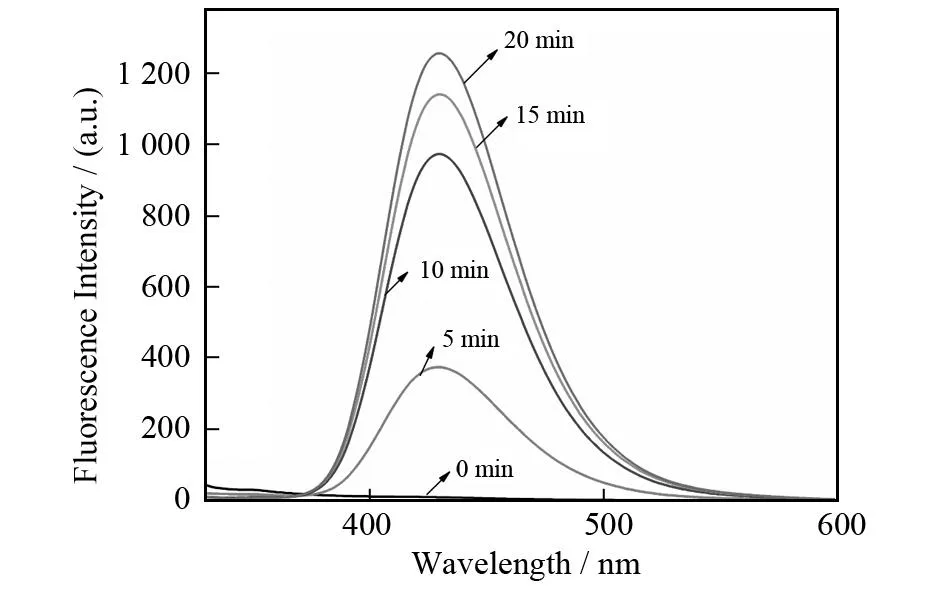
图3 UV照射下TiO2-Y催化剂的荧光光谱图Fig.3 Fluorescence spectra of TiO2-Y catalyst under UV
TiO2-Y催化剂在UV和MW-UV条件下的荧光光谱图分别如图3和图4所示. 从图3和图4可以看出,在每间隔5 min所给出的荧光光谱变化图中,大约在波长429 nm处,荧光强度随光照时间延长而有所增强;但是无TiO2-Y光催化剂或者无紫外光照射时都没有荧光信号,这表明荧光来自于由光催化降解反应生成的·OH与对苯二甲酸反应生成的邻羟基对苯二甲酸. ISHIBASHI等[12]在使用荧光法测定TiO2表面氧化物种时指出,H·和HO2·等自由基诱导产生荧光影响不及·OH起的作用. 因此,荧光强度逐渐增强更进一步说明了光催化降解体系中生成的·OH有所增加,而这些·OH活性基团参与了光催化反应过程,使得模拟污染物发生降解和矿化. 同时,从图3和图4还可以看出,UV和MW-UV条件下·OH活性基团生成量随降解时间的延长而增多;并且当降解时间相同,MW-UV条件下产生的·OH活性基团要多于UV条件下的活性基团. 这表明微波辐射可促进光催化体系生成更多·OH活性基团,更有利于光催化活性的提高,这进一步说明微波辐射具有强化TiO2-Y催化剂降解模拟污染物的作用.

图4 MW-UV照射下TiO2-Y催化剂的荧光光谱图Fig.4 Fluorescence spectra of TiO2-Y catalyst under MW-UV
2.3TiO2-Y催化剂XRD、SEM及BET分析
TiO2-Y催化剂的XRD图谱如图5所示. 可以看出,微波助离子液体介质中制得的未掺杂纯TiO2及掺杂型TiO2-Y催化剂在衍射角2θ=25.26°((101)晶面)、37.86°((004)晶面)、48.02°((200)晶面)附近都有明显主衍射峰出现,这表明纯TiO2和掺杂型TiO2-Y均主要以锐钛矿相存在. 采用Jade软件分析XRD数据,并依据Shceller公式可得到25.26°处TiO2和TiO2-Y催化剂平均粒径分别为15.30 nm和11.34 nm,结合图6的BET数据分析结果可得到TiO2-Y比表面积为 55.616 m2/g,说明TiO2-Y催化剂粒径较小,比表面积较大,因而与模拟污染物接触更充分,表现出较高的光催化降解活性.
图5还表明,稀土离子Y3+掺入TiO2,在一定程度上造成晶体表面发生微小畸变但未改变其晶型结构,仍为锐钛矿相,这说明少量Y3+的存在造成TiO2粒子生长较慢,晶粒扩散势垒升高使TiO2粒子表面结构改变使其无法正常生长. 依据布拉格公式2dsinθ=λ和面间距公式l/d=(h+k)/(a+l2/c),并结合Jade软件对XRD数据分析可知,掺入Y3+后TiO2的体积没有发生膨胀或缩小情况,掺入前后晶胞参数无显著变化,仍然是:a=b=3.783,c=9.497. 这表明Y3+因其离子半径与钛离子半径相差不大取代Ti4+在晶格里面的位置引起晶格畸变,同时,也可能在TiO2禁带中引起杂质能级来俘获TiO2受激发形成的光生载流子. 由于捕获载流子的捕获位间距离变小,掺杂离子会成为电子和空穴的复合中心[14-18]. 而存在晶体间隙处或者TiO2表面的Y3+由于价态低于Ti4+将捕获空穴,减少电子-空穴对在表面的复合,从而增强TiO2-Y催化剂光催化活性.
掺杂型TiO2-Y催化剂的BET吸附曲线和SEM分别如图6和图7所示. 从图6的BET曲线分析可知,TiO2-Y催化剂的比表面积为55.616 m2/g,孔容积为0.171 4 cc/g,平均孔径为6.259 5 nm,较高的孔容、孔径能够增加降解物的吸附量,且其较高的比表面积可增大与降解底物的接触面积,从而提高其光催化降解活性. 从图7可以看出,经微波处理过的TiO2-Y催化剂其颗粒大小及分布也比较均匀,催化剂结晶及分散性较好,颗粒形貌大体上为球形,有利于TiO2-Y催化剂光催化降解活性的提高.

A: TiO2;B: TiO2-Y. 图5 TiO2和TiO2-Y催化剂的XRD图Fig.5 XRD spectra of TiO2 and TiO2-Y catalyst

图6 TiO2-Y催化剂的BET曲线Fig.6 BET analysis of TiO2-Y catalyst

图7 TiO2-Y催化剂的SEM图Fig.7 SEM image of TiO2-Y catalyst
2.4TiO2-Y光催化降解反应动力学数据分析

图8 不同钇掺杂量TiO2-Y催化剂降解甲基橙溶液的光催化活性Fig.8 Photo-catalytic activity of TiO2-Y at the different Y-doped amount for methyl orange degradation
TiO2-Y催化剂对甲基橙溶液光催化降解反应的反应动力学表达式: -dc/dt=kr[kac/(1+kac)],由于甲基橙浓度较小,则表征速率常数Ka可忽略不计,简化后呈现一级反应动力学规律. 图8为不同钇掺杂量TiO2-Y催化剂降解甲基橙溶液的光催化活性线性回归图,而表1为TiO2-Y催化剂降解甲基橙溶液的动力学参数.

表1 不同钇掺杂量 TiO2-Y催化剂
由表1可知,当n(Y3+)/n(Ti4+)=0、0.6%、0.7%和0.8%时,TiO2-Y催化剂降解甲基橙溶液的表观速率常数K值分别为0.026 9、0.033 6、0.051 9和0.040 6 min-1. 结合图8可以看出,稀土元素钇掺杂制得的TiO2-Y催化剂,其光催化降解活性明显高于无掺杂TiO2光催化剂,并且当钇掺杂量为0.7%时,TiO2-Y催化剂表现出较高的光催化活性,其表观速率常数K为最大值0.051 9 min-1;而当钇掺杂量低于或者高于0.7%时,其表观速率常数K小于0.051 9 min-1. 随着K值增加,催化剂光催化活性则越强,这进一步表明稀土元素钇掺杂能够显著提高TiO2催化剂的光催化活性,钇掺杂量0.7%为最佳掺杂量. 从表1还可看出,在有光照但无TiO2-Y催化剂存在,或者有TiO2-Y催化剂存在但无光照的情况下,甲基橙溶液均几乎不发生降解,这表明甲基橙溶液发生降解是由TiO2-Y催化剂的光催化作用所致.
2.5TiO2-Y催化剂光催化稳定性测试
取最佳制备条件下制得的TiO2-Y催化剂,在紫外光照条件下降解模拟污染物1.5 h后,将降解液静置1 d,除去上层清液,使用二次蒸馏水清洗催化剂并进行烘干,在100 ℃下真空干燥30 min,然后重复实验测试催化剂的热稳定性,共计重复前面的步骤5次,所得结果如表2所示. 表2结果表明,TiO2-Y催化剂重复使用5次后,对模拟污染物仍具有较高的降解率,甲基橙和苯酚降解率分别在98.0%和97.6%以上,这表明微波助离子液体介质中制得的掺杂型TiO2-Y催化剂具有较好的热稳定性.

表2 TiO2-Y催化剂降解甲基橙和苯酚溶液
3结论
1) 在微波助离子液体介质中,在最佳条件下制得的TiO2-Y催化剂具有较高的光催化降解活性和较好的热稳定性,在UV和UV-MW条件下降解甲基橙和苯酚溶液,1.5 h后甲基橙降解率分别为98.3%和99.5%,苯酚降解率分别为97.5%和98.2%;
2)羟基自由基检测的荧光光谱结果表明,微波辐射一定程度上促使TiO2-Y催化剂表面生成更多的·OH,·OH活性基团有利于催化剂光催化活性的提高,因而微波辐射具有强化TiO2-Y降解模拟污染物的作用效果;
3) TiO2-Y催化剂的结构分析表明,稀土元素钇掺杂TiO2因其离子半径与钛离子半径相差不大而取代Ti4+在晶格中的位置. 同时,也可能在TiO2禁带中引起杂质能级俘获TiO2受激发形成的光生载流子;
4)光催化反应动力学数据分析表明,TiO2-Y催化剂对甲基橙溶液的光催化降解反应呈现一级反应动力学规律,当钇掺杂量为n(Y3+)/n(Ti4+)=0.7%时,其表观速率常数K具有最大值0.051 9 min-1,催化剂表现出较高的光催化活性.
参考文献:
[1] 程萍, 顾明元, 金燕苹. TiO2光催化剂可见光化研究进展[J]. 化学进展, 2005, 17(1): 8-14.
[2] 王勇, 张艳, 赵亚伟等. 纳米TiO2的制备及其改性和应用研究进展[J]. 化学研究, 2010, (02): 94-99.
[3] 张桂琴, 毕先钧. 离子液体介质中微波助制备铁掺杂纳米TiO2及光催化活性[J]. 分子催化, 2010, 24(6): 17-28.
[4] 张桂琴, 毕先钧. 离子液体介质中微波助锌掺杂纳米TiO2及光催化活性[J]. 工业催化, 2014, 4(2): 17-28.
[5] 孙婧, 蒋文建, 张桂琴等. 微波助离子液体中锌掺杂纳米TiO2的制备及微波强化光催化氧化活性[J]. 工业催化, 2013, 3(21): 27-33.
[6] 王雷清, 施忠芬, 毕先钧. 微波助离子液体中铜掺杂TiO2光催化剂的制备及微波强化光催化活性[J]. 应用化工, 2014, 43(2): 215-221.
[7] 蒋文建, 孙婧, 毕先钧. 微波助离子液体中Nd掺杂纳米TiO2催化剂的制备及其微波强化光催化活性[J]. 化学工程与技术, 2013, 3(9): 161-168.
[8] 王雷清, 李曼弯, 毕先钧. 微波助离子液体中铈掺杂TiO2光催化剂的制备及微波强化光催化活性[J]. 工业催化, 2014, 22(4): 277-283.
[9] 晏爽, 蔡盛臻, 吉钰纯. 钇掺杂改性纳米二氧化钛及其光催化性[J]. 武汉工程大学学报, 2010, 32(12): 65-67.
[10] 杨佳艳. 4-氨基安替比林直接分光光度法测定废水中挥发酚方法改进[J]. 环境科学与管理, 2011, 36(8): 143-146.

[12] ISHIBASHI K, FUJISHIMA A, WATANABE T, et al. Detection of active oxidative species in TiO2photo-catalysis using the fluorescence technique [J]. Electrochem Commun, 2000, 2: 207-210.
[13] 刘艳, 张健杰, 刘自力. 钇掺杂ZnO光催化剂的制备及其光催化性能的研究[J]. 工业催化, 2010, 18(增刊): 241-243.
[14] 曾人杰, 庞起, 林仲华等. 钇离子掺杂对二氧化钛纳米薄膜光诱导超亲水性能的影响及其机理[J]. 无机化学学报, 2003, 19(7): 678-682.
[15] 杜红莉, 张兆志, 李艳等. 金属掺杂二氧化钛纳米管催化性能的研究进展[J]. 材料导报A, 2011, 25(7): 23-25.
[16] 邓谦, 李明, 蔡晴等. 稀土/二氧化钛催化剂的制备和光催化消除气体污染物[J]. 中国稀土学报, 2011, 29(2): 170-176.
[17] 翟春阳, 周卫强, 徐景坤等. 活性炭负载TiO2-Fe3O4磁性光催化剂的制备及性能[J]. 化学研究, 2009, (02): 83-86.
[18] 李玉, 韩兆让, 翟永爱等. TiO2/SiO2复合材料的制备与表征[J]. 化学研究, 2007, (01): 19-22.
[责任编辑:毛立群]
Preparation of Y-doped TiO2photo-catalysts with microwave irradiation in ionic liquid and microwave enhanced photo-catalytic activity
LI Manwan, ZHANG Mei, BI Xianjun*
(InstituteofChemistryandChemicalEngineering,YunnanNormalUniversity,Kunming650500,Yunnan,China)
Abstract:Y-doped TiO2 photo-catalysts were synthesized by a microwave aided sol-gel method using ionic liquid as a reaction medium. The purpose of the experiment was improvement for the photo-catalytic activity and accelerate the degradation of pollutants. The structure and morphology of Y-doped TiO2 were characterized using XRD, BET and SEM. The photo-catalytic activity was respectively investigated by ultraviolet irradiation(UV) and microwave irradiation with ultraviolet irradiation (MW-UV) using the photo-catalytic degradation of methyl orange and phenol solution as simulated pollutants. With terephthalic acid as the fluorescence probing, the influence of hydroxyl radical on the surface of TiO2-Y on the photo-catalytic activity was investigated by the fluorescence technology. To understand the reaction mechanism, the photo-catalytic degradation kinetics was determined. The results showed that the TiO2-Y catalysts prepared at the optimum condition had higher photo-catalytic activity and heat stability, the degradation rate of methyl orange and phenol solution reaching 98.3% and 99.5%, 97.5% and 98.2%, respectively, under UV and MW-UV for 1.5 h. The fluorescence spectra also indicated that the UV combining with MW technology could effectively improve the catalytic efficiency of TiO2-Y catalyst, for the amount of hydroxyl radicals under MW-UV irradiation were more than that under UV. The reaction kinetics data indicated the first order model for the photo-
catalytic degradation reaction of methyl orange, and that the maximum apparent rate constant K was 0.051 9 min-1.
Keywords:ionic liquid; Y-doped; TiO2 photo-catalysts; microwave enhancing effect; photo-catalytic activity
文章编号:1008-1011(2016)02-0234-07
中图分类号:O649
文献标志码:A
作者简介:李曼弯(1988-),女,硕士生,研究方向为催化化学. *通讯联系人,E-mail:bixj159@aliyun.com.
基金项目:国家自然科学基金资助项目(20663007).
收稿日期:2015-08-23.

