不同分子靶向药物给药方案治疗转移性结直肠癌患者生存对比研究
王程,王莉,王会峰
(宁夏医科大学总医院肿瘤医院 肿瘤内科,宁夏 银川 750004)
不同分子靶向药物给药方案治疗转移性结直肠癌患者生存对比研究
王程Δ,王莉,王会峰
(宁夏医科大学总医院肿瘤医院 肿瘤内科,宁夏 银川 750004)
目的 对比研究贝伐珠单抗联合不同化疗药物治疗方案治疗转移性结直肠癌患者生存情况,以期筛选贝伐单抗治疗转移性结直肠癌的优化方案,提高转移性结直肠癌患者生存期及生存质量。方法 选取2013年1月~2013年6月在宁夏医科大学总医院肿瘤医院接受治疗的128例晚期转移性结直肠癌患者作为研究对象,将其随机分为A、B、C、D 4组,每组32例,分别采用贝伐珠单抗(5 mg/kg)联合FOLFIRI、贝伐珠单抗(10 mg/kg)联合FOLFIRI、贝伐珠单抗(5 mg/kg)联合FOLFOX、贝伐珠单抗(10 mg/kg)联合FOLFIRI方案进行治疗,4组患者均行6周期治疗。比较4组患者近期临床疗效、无进展生存期(progression-free survival,PFS)、三年生存率、总生存期(overall survival,OS)。结果 4组患者性别、年龄、疾病分期、治疗前ECOG评分、原发肿瘤部位、肿瘤转移部位、转移肿瘤直径等比较,差异均无统计学意义;4组患者治疗过程中均出现程度不同的毒副反应,但患者均耐受并完成既定化疗方案。A、B、C、D组总有效率分别为:56.25%、59.38%、46.88%、50.00%,3年生存率分别为:25.00%、18.75%、28.13%、18.75%,PFS分别为:(9.5±1.1)月、(9.6±1.1)月、(9.2±1.0)月、(9.3±0.9)月,总生存期分别为:(30.23±2.26)月、(29.83±2.24)月、(26.94±2.08)月、(27.19±2.11)月。A、B组患者在临床总有效率、三年生存率高于C、D两组,但组间比较差异均无统计学意义;A、B组患者在DFS和TTP均明显高于C、D两组,且组间比较差异均有统计学意义(P<0.05),A、B两组组间比较差异无统计学意义,C、D两组组间比较差异也无统计学意义,A、B组患者在OS明显高于C、D两组,且组间比较差异均有统计学意义(P<0.05),A、B两组组间比较差异无统计学意义,C、D两组组间比较差异也无统计学意义。结论 贝伐珠单抗按照5~10 mg/kg/m2联合FOLFIRI方案治疗转移性结直肠癌,能有效提升患者无进展生存期,对促进转移性结直肠癌患者的临床总体生存期具有较高的临床价值。
靶向药物;转移性结直肠癌;贝伐珠单抗;给药方案;生存期
结直肠癌是消化道常见的恶性肿瘤,发达国家结直肠癌的发病率较高,结直肠癌发病率居恶性肿瘤的第三位,近年来,结直肠癌发病率有增加的趋势[1]。手术是治疗结直肠癌的有效方式。但临床约30~40%的结直肠癌手术患者术后复发并最终导致肿瘤转移而死亡[2]。目前转移性结直肠癌患者的5年生存率仅为13%[3],如何提高转移性结直肠癌患者的生存时间及生存质量是结直肠癌患者治疗的重要课题。自20世纪50年代后期将5-氟尿嘧啶用于治疗大肠癌以来,化疗对于提高晚期结直肠癌患者的生活质量及生存期起到了巨大的作用[4]。随着临床药物及技术的发展,分子靶向药物为转移性结直肠癌患者的治疗提供了更优的化疗选择。临床数据显示,分子靶向药物联合化疗对于转移性结直肠癌患者的总生存期可达到30个月。贝伐珠单抗是2004年FDA批准的第一个抑制肿瘤血管生成的药物,成为临床治疗转移性结直肠癌的第一个分子靶向药物。自投放临床使用以来,如何优化贝伐珠单抗治疗转移性结直肠癌的方案,取得更好的临床疗效,一直是临床关注的热点问题。本文采用贝伐珠单抗不同剂量与临床常用的转移性结直肠癌一线化疗方案进行组合,对比不同方案患者经治疗后的近期疗效及生存情况,以期寻找治疗转移性结直肠癌的合理方案,现将结果报道如下。
1 资料与方法
1.1 一般资料 选择2013年1月~2013年6月在宁夏医科大学总医院肿瘤医院接受治疗的128例晚期转移性结直肠癌患者作为研究对象,将其随机分为A、B、C、D 4组,每组32例。A组男性患者18例,女性14例,年龄范围32~60岁,平均年龄(54.0±2.2)岁,B组男性患者17例,女性15例,年龄范围34~60岁,平均年龄(54.9±2.0)岁,C组男性患者17例,女性15例,年龄范围33~60岁,平均年龄(54.5±2.1)岁,D组男性患者18例,女性14例,年龄范围35~60岁,平均年龄(54.6±2.3)岁,4组患者性别、年龄比较差异无统计学意义。
纳入、排除标准[5]:纳入标准:①年龄在18~60岁;②符合2013年《中国结直肠癌诊疗指南2013》中关于转移性结直肠的诊断标准;③有手术治疗禁忌症(a或b或c或合并a、b、c两项以上者):a患者全身状态及脏器耐受能力不符合手术指征,或者麻醉不耐受,b广泛远处转移或(和)外侵,转移灶不能完全切除,c Ⅳ期无梗阻、穿孔、大出血等严重并发症者;④转移部位为肺、肝转移;⑤预估生存期>6个月;⑥ECOG评分≤1分,⑦转移部位≤3个,⑧患者及家属充分了解参加此次研究利弊,愿意配合此次研究各项工作,并签署知情同意书。本方案经医院伦理委员会审核批实施。
排除标准:①妊娠或哺乳期女性;②合并有心、肝、肾、造血系统等严重原发性疾病者;③手术切除后转移患者;④预估生存期≤6个月;⑤未签署知情同意书者。
1.2 方法
1.2.1 治疗方案:A、B、C、D4组患者分别采用贝伐珠单抗(5 mg/kg)联合FOLFIRI、贝伐珠单抗(10 mg/kg)联合FOLFIRI、贝伐珠单抗(5 mg/kg)联合FOLFOX、贝伐珠单抗(10 mg/kg)联合FOLFOX方案进行治疗,4组患者均行6w治疗。
1.2.2 FOLFIRI方案:①5 mg注射用地塞米松磷酸酯钠(马鞍山丰原制药有限公司,国药准字H20051748)溶解于100 mL 0.9%NaCl溶液中,静注1 d,0.4 g西咪替丁(山西普德药业有限公司,国药准字H20051567)溶解于100 mL 0.9% NaCl溶液中静滴1~2 d,0.5 mg阿托品(成都市海通药业有限公司,国药准字H51021302)肌肉注射1 d,按照80 mg/m2剂量伊立替康溶解于500 mL葡萄糖注射液中静滴1 d,200 mg亚叶酸钙溶解于250 mL中静滴1~2 d, 按照400 mg/m2剂量取5-氟尿嘧啶(天津金耀药业有限公司,国药准字H12020959)溶解于500 mL 0.9%NaCl溶液中,静脉滴1~2 d,连续2次,按照600 mg/m2剂量取5-氟尿嘧啶溶解于250 mL 0.9%NaCl溶液中,静脉滴注1~5 d,10 mg胃复安片(上海复旦复华药业有限公司,国药准字H31021209)口服。 2 w 为一化疗周期,连续6个化疗周期。
1.2.3 FOLFOX方案:5 mg注射用地塞米松磷酸酯钠溶解于100 mL生理盐水中,静滴1~2 d,0.4 g西咪替丁溶解于 100 mL 0.9%NaCl溶液中静注1~2 d,奥沙利铂(四川美大康佳乐药业有限公司,国药准字H20050141)85~100 mg/(kg·m2)溶解于500 mL葡萄糖注射液中,静滴1 d,200 mg亚叶酸钙溶解于250 mL 0.9%NaCl溶液中静滴1~2 d,按照600 mg/m2剂量取5-氟尿嘧啶溶解于500 mL 0.9%NaCl溶液中,静滴1~2 d,10 mg胃复安肌肉注射1~2 d,8 mg昂丹司琼溶解于100 mL 0.9%NaCl溶液中,静滴1~2 d,每2 w为一化疗周期,连续治疗6个周期。
1.2.4 贝伐珠单抗用药方案:5 mg注射用地塞米松磷酸酯钠溶解于100 mL 0.9%NaCl溶液中,静注第1 d,按照5 mg或10 mg/kg贝伐珠单抗[Roche Pharma (Schweiz) Ltd,注册证号:S20120069]溶解于100 mL 0.9%NaCl溶液中,静注第1 d,输注时间第一次以90 min为宜,若患者耐受第二次可在60 min内输注完成,根据患者耐受情况,可调整至30 min内输注完成。2w一次为一疗程,连续治疗6个疗程。接受贝伐单抗治疗期间,每2~3周检测一次血压及尿液蛋白检查,防止出现诱发或者加重蛋白尿。
1.2.5 随访:所有患者完成6个化疗周期后,每个月电话随访一次,了解患者临床症状改善情况及毒副作用,每两个月回院随访一次,对患者进行实验室指标、影像学及体格检查,项目包括:肿瘤标志物CEA、CA19-9监测,肝脏B超及胸腹盆增强CT检查,确定肿瘤直径大小,或是否有新增病灶。半年后,3个月随访1次,检查项目同上,连续随访2年后,每6个月随访1次,共3年。根据随访结果对患者的无进展生存期、3年生存率、总生存期及近期疗效进行判定。随访3年后仍生存的患者继续每6个月随访1次,至5年;5年后每1年复查1次,根据患者情况予以观察或针对性治疗。
1.2.6 观察指标:患者治疗后比较4组患者近期临床疗效、无进展生存期(progression-free survival,PFS)、总生存期(overall survival,OS)三年生存率。
1.2.7 近期临床疗效判断标准:按照实体瘤临床近期疗效判断标准对患者临床疗效进行判定:完全缓解(CR):经I治疗后所有病灶及临床表现完全消失且至少保持1个月;部分缓解(PR):可测量的肿瘤垂直两直径的和较基线缩小50%并持续至少1个月;进展(PD):病灶垂直两直径的和较最低值增加25%,或出现新的肿瘤或可评价的疾病。完全缓解率+部分缓解率=总有效率。
① 无进展生存期:入组后至第一次发生疾病进展或任何原因死亡的时间。
② 三年生存率:经治疗后生存时间≥3年以上的比例。
③ 总生存期:从入组开始至因任何原因引起死亡或者末次随访的时间。
1.3 统计学方法 采用SPSS 13.00进行分析,计数资料采用χ2检验,等级资料采用秩和检验,多组计量资料采用方差分析,两两比较采用LSD-t检验,以P<0.05为差异具有统计学意义。
2 结果
2.1 4组患者临床特征比较 4组患者在疾病分期、治疗前体力状况ECOG评分、原发肿瘤部位、肿瘤转移部位、转移肿瘤直径等比较,差异均无统计学意义。见表1。

表1 4组患者临床特征比较Tab.1 Comparison of Clinical features between four groups
2.2 4组患者近期临床疗效 4组患者治疗过程中均出现程度不同的毒副反应,但患者均耐受并完成既定化疗方案。A、B组患者在临床总有效率高于C、D 2组,但组间比较差异均无统计学意义,见表2。
2.3 4组患者三年生存率比较 A、B组患者三年生存率高于C、D 2组,但组间比较差异均无统计学意义,见表3。
2.4 4组患者PFS比较 A、B组患者在PFS明显高于C、D2组,且组间比较差异均有统计学意义(P<0.05),A、B 2组组间比较差异无统计学意义,C、D 2组组间比较差异也无统计学意义。详见表4。
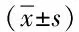
表4 4组患者PFS比较Tab.4 Comparison of PFS between four groups (±s)
*P<0.05,与C组比较,comparedwithCgroup;#P<0.05,与D组比较,comparedwithDgroup
2.5 4组患者OS比较A、B组患者在OS明显高于C、D2组,且组间比较差异均有统计学意义(P<0.05),A、B2组组间比较差异无统计学意义,C、D2组组间比较差异也无统计学意义,见表5。
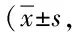
表5 4组患者OS比较月)Tab.5 Comparison of OS between four groups (±s,month)
*P<0.05,与C组比较,comparedwithCgroup;#P<0.05,与D组比较,comparedwithDgroup
3 讨论
自上世纪末期靶向治疗的出现,拓展了恶性肿瘤临床治疗的广阔的前景,是真正意义上的精准治疗[6]。靶向治疗的核心是在明确致癌位点与正常细胞分子生物学(基因、酶、信号转导)上存在的差异,针对性的设计出可以特异地选择致癌位点的药物进入体内与之发生结合,抑制肿瘤细胞的生长增殖而导致肿瘤细胞特异性死亡,这种结合具有高度的选择性,对肿瘤组织周围正常的细胞不会产生任何不利的作用,被称为肿瘤细胞的“生物导弹”[7-8]。分子靶向药物自1997年FDA批准第一个治疗非霍奇金淋巴瘤的靶向药物利妥昔单抗以来,随着药物筛选技术的发展,至目前FDA批准上市的靶向药物已达45个[9]。
转移性结直肠癌的转移部位常集中在肝脏和肺脏,目前临床对于转移性结直肠癌的治疗手段有限,其预后较差转。随着临床化疗药物和化疗方案的不断调整,转移性结直肠癌的总生存期不断延长[10]。分子靶向药物参与到转移性结直肠癌患者的治疗中起到了重要的作用。目前已批准用于转移性结直肠癌治疗的靶向药物有两种类型[11]:①以血管内皮生长因子及其受体为靶点的药物。②以表皮生长因子受体为靶点的单克隆抗体[12]。血管内皮生长因子是肿瘤血管生成的关键驱动因素,且血管生成是肿瘤发生和维持的基本过程。通过对血管内皮生长因子转导通路进行抑制的分子靶向药物能有效抑制肿瘤新生血管,使肿瘤血管正常化[13]。贝伐珠单抗即为临床广泛应用的血管再生抑制剂。于2004被FDA批准用于治疗转移性结直肠癌。贝伐珠单抗是一种重组人单克隆IgG1抗体,可特异性结合并阻断血管内皮生长因子,通过抑制肿瘤血管生成发挥作用[14]。目前贝伐珠单抗在临床上已广泛应用[15]。临床研究显示,贝伐珠单抗单用治疗转移性结直肠癌因临床疗效差而中途放弃研究,因此贝伐珠单抗联合其他化疗药物治疗转移性结直肠癌成为临床共识。但目前尚无临床指南对贝伐珠单抗联合化疗药物治疗转移性结直肠癌予以循证总结,临床也一直在进行多种研究,以期取得较好的治疗效果。
本文采用贝伐珠单抗联合其他化疗药物治疗转移性结直肠癌患者的化疗方案对转移性结直肠癌患者进行治疗,结果显示,贝伐珠单抗(5mg/kg)联合FOLFIRI、贝伐珠单抗(10mg/kg)联合FOLFIRI两种治疗方案较贝伐珠单抗(5mg/kg)联合FOLFOX、贝伐珠单抗(10mg/kg)联合FOLFOX方案对患者的无进展生存期及OS有提升作用,且差异有统计学意义(P<0.05)。说明贝伐珠单抗按照5~10mg/(kg·m2)联合FOLFIRI方案治疗转移性结直肠癌,能有效提升患者PFS,对促进转移性结直肠癌患者的临床OS具有较高的临床价值。
[1] 李珊珊,王岩,葛飞娇,等.分子靶向药物给药模式对转移性结直肠癌患者生存的影响[J].临床肿瘤学杂志,2014,(9):814-818.
[2] 刘佳,李文忠,夏秀娟,等.转移性结直肠癌维持治疗的进展[J].肿瘤学杂志,2016,22(5):344-348.
[3]FialaO,BuchlerT,Mohelnikova-DuchonovaB,etal.G12VandG12AKRASmutationsareassociatedwithpooroutcomeinpatientswithmetastaticcolorectalcancertreatedwithbevacizumab[J].TumourBiol,2016,37(5):6823-6830.
[4] 朱德祥,任黎,许剑民,等.中国《结直肠癌肝转移诊断和综合治疗指南》(V2013)解析[J].中华胃肠外科杂志,2014,(6):525-529.
[5] 解晓霞.转移性结直肠癌联合分子靶向药物的疗效观察[J].大家健康(下旬版),2015,(4):110-111.
[6]BaiL,WangF,ZhangDS,etal.Aplasmacytokineandangiogenicfactor(CAF)analysisforselectionofbevacizumabtherapyinpatientswithmetastaticcolorectalcancer[J].SciRep, 2015,5:17717.
[7] 夏秀娟,李粉婷,刘佳,等.转移性结直肠癌抗血管生成靶向治疗的研究进展[J].现代生物医学进展,2016,16(1):187-191.
[8] 蒙燕,杨建伟.转移性结直肠癌的维持治疗[J].国际病理科学与临床杂志,2013,33(5):412-415.
[9]ChenH,ZhangJ,CaoG,etal.Targethepaticarteryregionalchemotherapyandbevacizumabperfusioninlivermetastaticcolorectalcancerafterfailureoffirst-lineorsecond-linesystemicchemotherapy[J].AnticancerDrugs, 2016,27(2):118-126.
[10] 李健,沈琳.分子靶向药物在胃肠道肿瘤综合治疗中的应用[J].中华胃肠外科杂志,2014,17(11):1062-1067.
[11]GrapsaD,SyrigosK,SaifMW.Bevacizumabincombinationwithfluoropyrimidine-irinotecan-orfluoropyrimidine-oxaliplatin-basedch-emotherapyforfirstl-ineandmaintenancetreatmentofmetastaticcolorectalcancer[J].ExpertRevAnticancerTher,2015,15(11):1267-1281.
[12] 李珊珊.贝伐珠单抗对比抗EGFR单抗治疗转移性结直肠癌患者疗效及不良反应的分析[D].北京:中国人民解放军军事医学科学院,2014.
[13]DosSantosRF,CoutinhoMB,HaasL.Panitumumab+Mfolfox6VersusBevacizumab+Mfolfox6AsFirst-LineTreatmentofWild-TypeRasMetastaticColorectalCancer:ACost-EffectivenessAnalysisfromtheBrazilianPrivateHealthcareSystemPerspective.ValueHealth. 2015,18(7):A821.
[14] 郭晓静,曹妮达,陶丽,等.结直肠癌肝转移的治疗进展[J].国际肿瘤学杂志,2015,(3):228-231.
[15] 谭招丽,王友亮,徐建明,等.EGFR单克隆抗体治疗转移性结直肠癌的耐药分子机制[J].临床肿瘤学杂志,2014,(9):854-858.
(编校:师维康)
Comparative study on survival of patients with metastatic colorectal cancer treated with different molecular targeted drug delivery
WANG ChengΔ,WANG Li,WANG Hui-feng
(Department of Internal Medicine, General Hospital of Medical University, Yinchuan 750004, China)
ObjectiveTo study bevacizumab combined with chemotherapy regimen in treatment of different metastasis survival in patients with colorectal cancer, in order to optimize the scheme selection of bevacizumab for metastatic colorectal cancer metastasis, improve survival and quality of life of patients with rectal cancer.Methods128 cases of late January 2013~2013 year in June in general hospital of medical university for treatment of metastatic colorectal cancer patients as the research object, which were randomLy divided into A, B, C, D 4 groups, 32 cases in each group, respectively with bevacizumab (5 mg/kg) combined with FOLFIRI and bevacizumab (10 mg/kg) combined with FOLFIRI and bevacizumab (5 mg/kg) combined with FOLFOX and bevacizumab (10 mg/kg) therapy combined with FOLFIRI regimen, four patients underwent 6 cycles of treatment. Comparison of four groups of patients with recent clinical efficacy, progression free survival (survival progression-free, PFS), three years survival rate, overall survival (overall survival, OS).ResultsFour groups of patients with gender, age, stage of disease, ECOG score before treatment, primary tumor site, tumor metastasis, metastasis tumor diameter, there were no significant differences. Toxicity of different degrees occurred in the four groups during treatment, but the patients tolerated and complete the established chemotherapy. A, B, C, D group total effective rate were 56.25%, 59.38%, 46.88%, 50%, 3 years survival rates were 25%, 18.75%, 28.13%, 18.75%, PFS respectively: (9.5±1.1), (9.6±1.1), (9.2±1), (9.3±0.9) months, overall survival were: (30.23±2.26), (29.83±2.24), (26.94±2.08), (27.19±2.11) months. A, B group of patients in the clinical total effective rate, three years survival rate were higher than that of C and D two groups, but there were no statistically significant difference between the two groups. A, DFS and TTP in B group were significantly higher than that of C and D two groups, and there were significant differences among the groups (Pall<0.05), the difference between the two groups was no statistically significant, C, D between the two groups there was no significant difference, A, B groups were significantly higher than that of C, OS in D two group, and the difference between the two groups were statistically the significance (P<0.05), A, B between the two groups, but no significant difference, C, D between the two groups there was no significant difference.Conclusionaccording to the 5-10 mg/kg/m2of bevacizumab combined with FOLFIRI regimen in the treatment of metastatic colorectal cancer, can effectively improve progression free survival in patients with a high clinical value to promote the transfer of clinical overall survival of patients with colorectal cancer.
drug targeting; metastatic colorectal cancer; bevacizumab; regimen; survival
10.3969/j.issn.1005-1678.2016.12.046
王程,通信作者,男,本科,副主任医师,研究方向:消化道肿瘤,E-mail:wezhexh@163.com。
R979.1+9;R735.3
A

