两种不同试剂盒检测手段对肝移植患者他克莫司血液浓度的影响
周台玲,张浩,张朝锋
(舟山医院 检验中心,浙江 舟山 316000)
两种不同试剂盒检测手段对肝移植患者他克莫司血液浓度的影响
周台玲Δ,张浩,张朝锋
(舟山医院 检验中心,浙江 舟山 316000)
目的 探讨两种不同试剂盒检测手段对肝移植他克莫司血液浓度的影响。方法 选取2013年2月~2016年8月在舟山医院肝病科接受他克莫司检测的肝移植患者81例,用药后12采集患者空腹上肢静脉血,分别采用酶联免疫吸附法(ELISA)检测试剂盒和酶增强免疫法(EMIT)检测试剂盒对全血样本他克莫司血液浓度进行检测,观察、比较2种检测手段的测定结果及相关性。结果 ELISA法具有较好的日内及日间精密度和准确度,RSD均<5%,其中在低浓度区间时检测的精密度稍差;EMIT法具有较好的日内及日间精密度和准确度,RSD均<5%,其中在低浓度区间检测的精密度稍差;采用ELISA检测试剂盒测得的他克莫司血药浓度(5.19±0.73)μg/L明显低于采用EMIT试剂盒测得的结果(8.29±1.14)μg/L,差异具有统计学意义(P<0.05);2种试剂盒检测结果的相关系数r=0.9176,检测结果呈正相关关系;他克莫司血药浓度<2.0 μg/L时,ELISA试剂盒的测定结果(1.116±0.125)μg/L明显低于EMIT试剂盒的测定结果(1.507±0.201)μg/L,具有统计学意义(P<0.05)。结论 ELISA检测试剂盒和EMIT检测试剂盒均可用于肝移植患者他克莫司血液浓度的监测,且相关性较好,但二者测定的他克莫司血液浓度差异显著,需各自建立治疗窗范围进行判断,检测结果不可相互替换。
他克莫司血药浓度;肝移植;酶联免疫吸附法;酶增强免疫法
肝移植后的1年生存率高达85%,是治疗终末期肝病的主要外科手段[1]。虽然肝脏受到免疫系统攻击的概率相对较小,但术后仍需长期服用免疫抑制剂来防止免疫排斥并发症。他克莫司(又名FK506)是从链霉菌属大环内酯类抗生素,能够通过抑制白细胞介素-2(Interleukin-2,IL-2)的释放来抑制T淋巴细胞的功能,发挥强力的免疫制作用[2],是防治肝移植后排斥反应的一线药物[3]。但是由于治疗窗狭窄、稳态谷浓度(C0)水平与毒性反应、排斥反应具有相关性、药物动力学具有较大的个体差异[4]等原因,导致FK506使用中剂量较低容易出现排斥反应,剂量稍高容易产生毒性,因此,对FK506的血药浓度进行监测使其处于安全有效的治疗范围尤为重要[5]。目前,临床上FK506的血药浓度监测方法主要有酶联免疫吸附法(enzyme-linked immunosorbent assay,ELISA)、酶增强免疫法(enzyme-multipliedimmuno assay technique,EMIT)、微粒子酶免疫法(microparticle enzyme immunoassay assay,MEIA)、化学发光微粒子免疫分析法(chemiluminescence microparticle immunoassay assay,CMIA)等免疫学手段以及高效液相色谱-质谱联用法(high performance liquid chromatography-mass spectrometry,HPLC-MS)[6]等,各种监测手段有其自身的优势和特点,临床使用时应注意选择。本次主要探讨ELISA法和EMIT法两种不同试剂盒检测手段对肝移植FK506血液浓度的影响,现报告如下。
1 资料与方法
1.1 一般资料 选取自2013年2月~2016年8月来舟山医院进行FK506检测的肝移植患者81例作为研究对象,其中男性44例,女性37例,年龄20~69岁,平均年龄(44.32±6.12)岁,体质量为51~77 kg,平均体质量(66.36±9.43)kg,服药时间为3~120月。本试验经患者知情同意,并获得医院伦理委员会批准。
纳入标准[7]:①器官移植、接受FK506治疗时间>3个月;②服药剂量为0.1~0.2 mg/(kg·d),分为2次/d,每隔12h口服一次;③肝肾功能无异常。
排除标准:①年龄<18岁的患者;②肝脏移植时间<3个月的患者;③服用其他免疫抑制剂或其FK506血药浓度有影响药物的患者;④未规律服用药物的患者。
1.2 方法
1.2.1 仪器与试剂:SYVA Viva-E临床化学分析仪,西门子医疗诊断公司产品;Synergy H1全功能酶标仪,美国伯腾仪器有限公司(BioTek)产品;MM-1(MM-2)-微量振荡器,江苏省金坛市友联仪器研究所产品;5417C小型台式高速离心机,德国艾本德股份公司产品;Emit® 2000FK506检测试剂盒,西门子医疗诊断公司产品;人FK506ELISA检测试剂盒,上海乔羽生物科技有限公司产品;FK506(标准品)(爱尔兰Astellas Pharma Co. Limited,国药准字H20090691)。
1.2.2 血液样本采集:所有患者于用药后12 h的次日清晨,采集空腹上肢静脉血5 mL,将血液平均分为2份置于含有乙二胺四乙酸二钾(EDTA-2K)的抗凝管中备用。
1.2.3 定标和质控:酶联免疫吸附法(ELISA)根据0、0.3、1.0、3.0、10、30.0 μg/L 6个浓度的FK506标准液绘制标准曲线,随行低(2.0 μg/L)、中(5.0 μg/L)、高(15.0 μg/L)三个浓度的FK506质控样品进行控制;酶增强免疫法(EMIT)根据0、2.5、5.0、10.0、20.0 30.0 μg/L 6个浓度的FK506标准液绘制标准曲线,随行低(5.0 μg/L)、中(9.8 μg/L)、高(19.0 μg/L)3个浓度的FK506质控样品进行控制。
1.2.4 样本药物浓度测定:①ELISA法:按照ELISA试剂盒说明书的步骤处理样本并进行检测,吸取各浓度FK506标准液+各浓度FK506质控样品+25 μL血液样本,置于离心管中,滴加150 μL消化液混匀,分别在室温及75 ℃水浴箱内进行孵育15 min后离心,取上清液置于酶标微孔板内;分别滴加50 μLFK506单克隆抗体,孵育30 min,加入50 μL酶标试剂,孵育60 min,洗板,加入50 μL显色剂,避光显色10 min,加入终止液终止反应,立即采用酶标仪在450/630 nm双波长下测定各孔吸光度,绘制标准曲线,计算样本浓度值。②EMIT法:将200 μL甲醇+50 μL预处理液+各浓度FK506标准液+各浓度的FK506质控样品+200 μL样本,依次置于离心管中,混匀,静置沉淀,离心,取上清液采用临床化学分析仪检测样本浓度。
1.2.5 精密度(CV)及回收率测定:同日内,采用ELISA法测定低(2.0 μg/L)、中(5.0 μg/L)、高(15.0 μg/L)3个浓度的质控样品各5份,采用EMIT法测定低(5.0 μg/L)、中(9.8 μg/L)、高(19.0 μg/L)3个浓度的质控样品各5份,计算日内CV平均值、相对标准偏差(RSD)以及回收率;连续5 d,不同日间,分别采用ELISA法和EMIT法测定相应质控样品,计算日间CV平均值、RSD以及回收率。
1.2.6 2种方法测定FK506血药浓度相关性比较:分别计算2种方法测定的血液FK506血药浓度,对其进行比较,并观察2种结果的相关性。
1.2.7 不同FK506血药浓度范围内2种方法测量数据比较:将测定的FK506血药浓度分为<0.2、2.0~8.0、8.0~14.0、14.0~20.0、>20.0 μg/L 5个水平,观察比较在各个血药浓度水平上2种检测方法的检测结果。
2 结果
2.1 ELISA法检测FK506的CV及回收率试验 结果显示,ELISA法具有较好的日内及日间精密度和准确度,RSD均<5%,其中在低浓度区间时检测的精密度稍差,见表1。
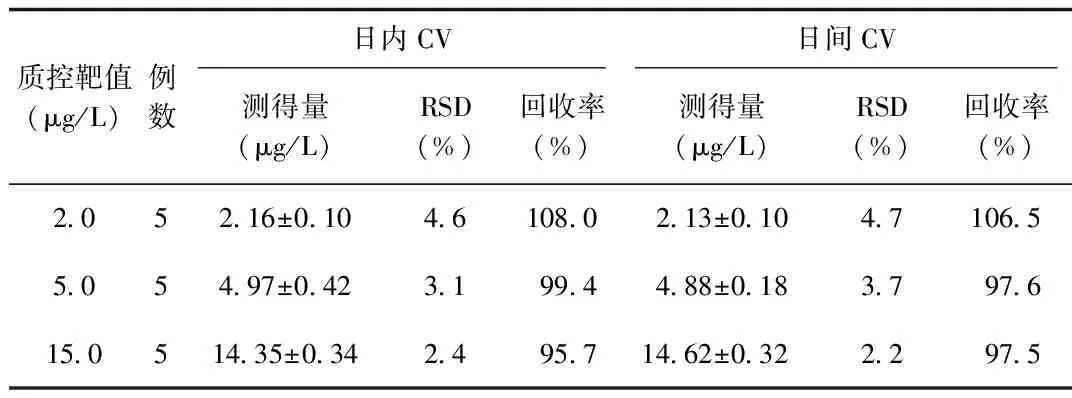
表1 ELISA法检测FK506的CV及回收率试验结果Tab.1 CV and recovery of tacrolimus tested by ELISA
2.2 EMIT法检测FK506的CV及回收率试验 结果显示,EMIT法具有较好的日内及日间精密度和准确度,RSD均<5%,其中在低浓度区间时检测的精密度稍差,见表2。
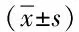
表2 EMIT法检测FK506的CV及回收率试验结果Tab.2 CV and recovery of tacrolimus tested by EMIT (±s)
2.3 2种方法检测FK506血药浓度差异性分析 通过ELISA法测得的FK506血药浓度为(5.19±0.73)μg/L,通过EMIT法测得的FK506血药浓度为(8.29±1.14)μg/L,EMIT法测定值明显高于ELISA法,差异具有统计学意义(P<0.05)。见表3。
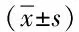
表3 2种方法检测FK506血药浓度差异性分析结果Tab.3 Results of two methods used to analyze FK506 plasma concentration (±s)
*P<0.05,与ELISA法比较comparedwithELISA。
2.4 2种方法检测FK506血药浓度相关性分析结果 对每一个血液样本,以ELISA法测定值为X轴,以EMIT法测定值为Y轴,据此绘制散点图,见图1,得到的线性回归方程为:Y=1.1578X+2.3691,相关系数r=0.9176,表明2种检测方法的检测结果呈正相关关系。
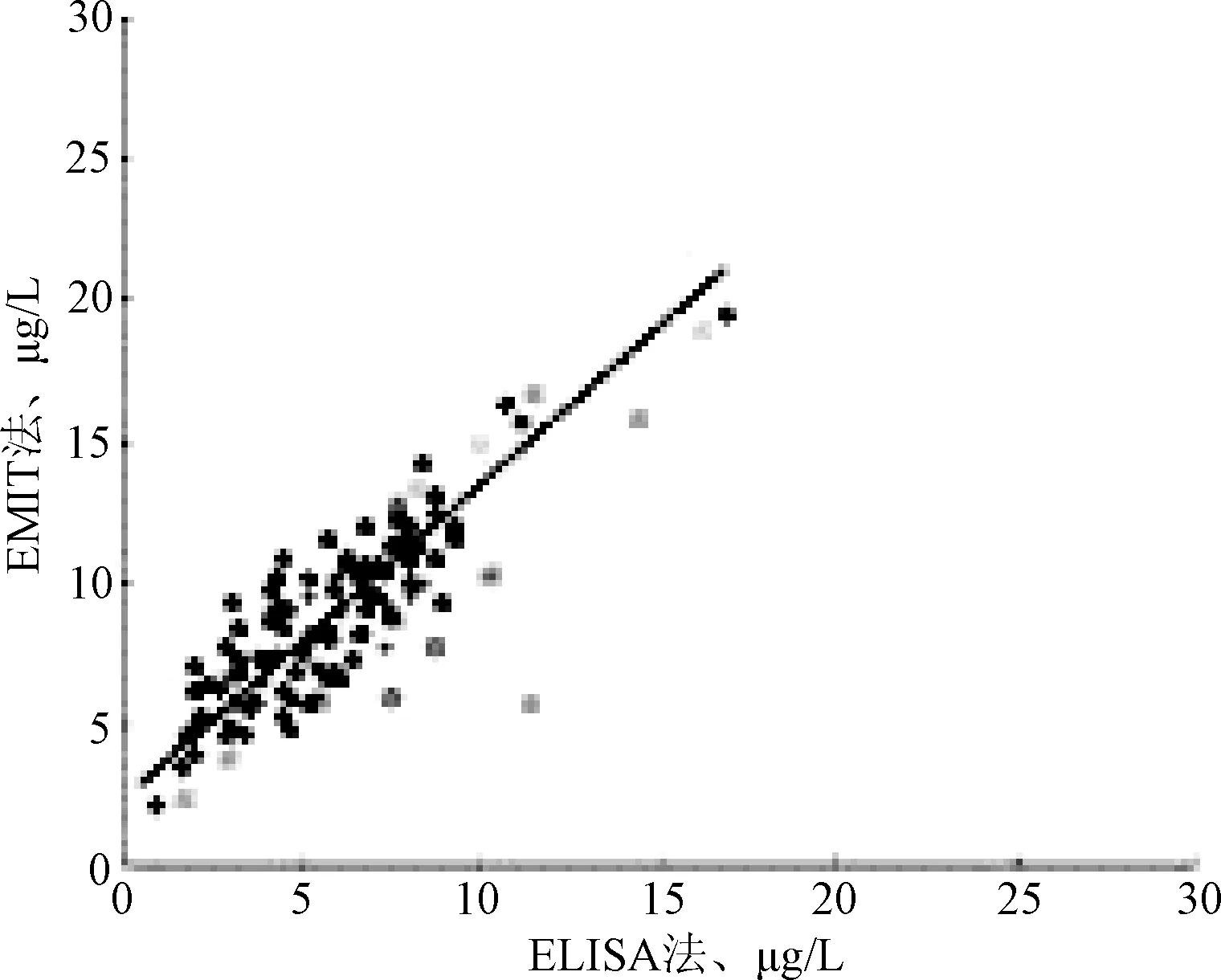
图1 ELISA与EMIT法相关性(n=81)Fig.1 Correlation between ELISA and EMIT (n=81)
2.5 不同FK506血药浓度范围内2种方法测量数据比较FK506血药浓度<2.0μg/L时,ELISA法的测定结果明显低于EMIT法的测定结果,差异具有统计学意义(P<0.05);FK506血药浓度为2.0~14.0μg/L时,ELISA法的测定结果稍低于EMIT法的测定结果,差异无统计学差异;FK506血药浓度为>20μg/L时,ELISA法的测定结果稍高于EMIT法的测定结果,差异无统计学差异,见表4。
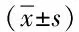
表4 不同FK506血药浓度范围内2种方法测量数据比较Tab.4 Comparison of measurement data of two methods in FK506 plasma concentration range (±s)
*P<0.05,与ELISA法比较comparedwithELISA
3 讨论
近年来,随着器官移植技术的发展,FK506在临床上的应用越来越广泛。FK506是新型的强效免疫抑制剂,能够与细胞性蛋白质FKBP12结合形成复合物,抑制钙调神经磷酸酶,阻断T细胞中钙离子依赖型信息传导通路,从而抑制T细胞活化和B细胞增殖,防止移植排斥相关的淋巴细胞产生,发挥防治排斥反应的作用。监测FK506血药浓度、制订个体化用药方案对于减小其毒副作用,获得最佳免疫抑制效果具有重要意义[8-9]。ELISA法和EMIT法是常用的免疫学检测方法。ELISA法属于竞争性的酶联免疫测定法,FK506自血浆蛋白中游离出来,与抗体结合形成复合物,之后加入的过氧化物酶(HRP)-FK506能竞争性与抗体结合,置换出血样中游离的FK506,再经过显色,使用酶标仪即可测出血样中FK506浓度。该法具有准确性好、迅速、灵敏度高、特异性强等特点[10],但是需全程手工操作,过程较为复杂,易受环境影响[11]。EMIT法也称为酶放大免疫法,原理为抗体结合位点竞争性抑制,试剂中用葡萄糖-6-磷酸脱氢酶(G6PDH)标记的FK506竞争性的与抗体结合,使抗体失活,无法与血液中FK506形成复合物,未结合的G6PDH可以促进抗体试剂中的烟酰胺腺嘌呤二核苷酸还原,从而被SYVAViva-E临床化学分析仪检测到,反映出血样中FK506浓度[12-13],具有预处理步骤简单、快速、自动化程度高的特点[14]。
本研究选取81例接受FK506治疗的肝移植患者,分别采用ELISA和EMIT试剂盒对静脉血样本中FK506血液浓度进行检测,结果显示,ELISA法和EMIT法检测均具有较好的日内及日间精密度和准确度,RSD均<5%,在低浓度区间时检测的精密度稍差,2种方法的监测结果均复合《中国药典》生物标本分析方法RSD<15%的要求[15],表明ELISA检测试剂盒和EMIT检测试剂盒均可用于肝移植患者FK506血液浓度的监测。
2种方法测得的FK506血药浓度平均值符合正态分布,采用配对样本t检验对检测结果差异性分析结果显示,EMIT法测定的FK506血药浓度值明显高于ELISA法(P<0.05),不同FK506血药浓度范围内2种方法测量数据比较结果显示,FK506血药浓度<2.0 μg/L时,ELISA法的测定结果明显低于EMIT法的测定结果(P<0.05),2种检测方法的原理不同,样本提取过程、代谢产物识别过程、人工操作过程、样本内源性物质较差反应等均可以对检测结果造成影响,形成偏差,导致2种检测方法对相同样本的检测结果存在差异,尤其是血药浓度处于<2.0 μg/L水平时,差异较为明显。以ELISA法测定值为X轴,以EMIT法测定值为Y轴,绘制散点图,采用线性回归对2种方法检测FK506血药浓度的相关性进行分析,结果显示,2种检测结果的相关系数r为0.9176,表明2种检测方法的相关性以及一致性较好,但是由于2种检测方法的测定结果存在差异,故在临床使用时应各自建立治疗窗范围,结合各自特点相对固定的采用一种方式进行检测,不适合频繁交叉检测。
综上所述,ELISA检测试剂盒和EMIT检测试剂盒均可用于肝移植患者FK506血液浓度的监测,且相关性较好,但二者测定的FK506血液浓度差异显著,需各自建立治疗窗范围进行判断,检测结果不可相互替换。
[1] 杨扬,张英才.肝移植术后免疫抑制剂撤退的研究进展[J].器官移植,2013,4(6):320-324.
[2] 潘习彰,郑娟.他克莫司在肾小球疾病的应用[J].临床荟萃,2012,27(20):1827-1829.
[3] 张丽华,高柏青,刘宝琴,等.肝移植术后监测他克莫司血药浓度的临床意义[J].中国冶金工业医学杂志,2012,29(6):666-667.
[4] Naik P,Madhavarapu M,Mayur P,et al.Pharmacokinetics of tacrolimus in adult renal transplant recipients.[J].Drug Metabolism and Personalized Therapy,2013,27(3):151-5.
[5] Gérard C,Stocco J,Hulin A,et al.Determination of the most influential sources of variability in tacrolimus trough blood concentrations in adult liver transplant recipients: a bottom-up approach.[J].The AAPS Journal,2014,16(3):379-391.
[6] Donaldson K J,Shaw L M.Quantitation of tacrolimus in whole blood using high performance liquid chromatography-tandem mass spectrometry (HPLC-MS-MS).[J].Methods in Molecular Biology,2010,603:479-487.
[7] 周霞,张敏.成人肝移植评估:美国肝脏疾病和移植协会2013实践指南[J].中华肝脏杂志,2014,22(8):567-569.
[8] 潘习彰,郑娟.他克莫司在肾小球疾病的应用[J].临床荟萃,2012,27(20):1827-1829.
[9] 刘丽娟,赖雁威,李慧云,等.肝移植患者他克莫司谷血药浓度监测意义和临床个体化用药调节[J].现代生物医学进展,2015,15(12):2281-2285.
[10] 吴锦,胡立芬,李嘉嘉,等.酶联免疫吸附法测定他克莫司血药浓度的质量控制[J].安徽医药,2013,17(7):1114-1116.
[11] 李想,颜鸣,史国兵,等.2种免疫法联合肾功能指标测定他克莫司血药浓度的比较[J].中国组织工程研究,2014,18(5):736-741.
[12] 卢蕾,杨欣.酶放大免疫检测技术在监测他克莫司血药浓度中的应用[J].中国免疫学杂志,2014,30(9):1294-1296.
[13] Beck O,Rausberg L,Al-Saffar Y,et al. Detectability of new psychoactive substances,‘legal highs’,in CEDIA,EMIT,and KIMS immunochemical screening assays for drugs of abuse.[J]. Drug Test Anal,2014,6(5):492-499.
[14] 王春燕,纪松岗,陆世宇,等.酶放大免疫法与酶联免疫吸附法测定他克莫司血药浓度的对比研究[J].中国药房,2014,25(30):2816-2818.
[15] 张丽萍,刘元明,张金红,等.自制他克莫司室内质控品的制备及临床应用研究[J].检验医学,2013,28(11):1021-1025.
(编校:师维康)
Effect of two different kits on blood concentration of tacrolimus in liver transplantation
ZHOU Tai-lingΔ, ZHANG Hao, ZHANG Zhao-feng
(Inspection Center, Zhoushan Hospital, Zhoushan 316000, China)
ObjectiveTo investigate the effect of two different detection methods of reagent kits on blood concentration of Tacrolimus in liver transplantation.Methods81 cases of liver transplantation patients
Tacrolimus testing in Zhoushan Hospital from February 2013 to August 2016 were selected, fasting venous blood of upper limb were collected 12h after treatment, blood concentrations of Tacrolimus in whole blood samples were detected by Enzyme linked immunosorbent assay(ELISA)kit and Enzyme enhanced immunoassay(EMIT)kit respectively, the results of the two methods were observed and compared.ResultsThe intra day and inter day precision and accuracy of ELISA method were good, RSD<5%, in the low concentration range, the precision of detection was slightly worse; the intraday and inter day precision and accuracy of ELISA method were good, RSD<5%, in the low concentration range, the precision of detection was slightly worse; the Tacrolimus blood concentration measured by ELISA (5.19±0.73) μg/L test kit was significantly lower than that measured by EMIT kit (8.29±1.14) μg/L, the difference was statistically significant (P<0.05); correlation coefficient of the detection results of two kinds of reagent kit was r = 0.9176, the detection results were positively related; the determination results of ELISA kit (1.116±0.125) μg/L were obviously lower than that of EMIT kit (1.507±0.201) μg/L when Tacrolimus blood concentration <2g/L, with significant difference (P<0.05).ConclusionELISA detection kit and EMIT kit can be used to monitor the blood concentration of Tacrolimus in liver transplantation patients, and the correlation was good, but the blood concentrations of Tacrolimus were significantly different between the two kits, need to establish their own of therapeutic window to judge,the test results can not be replaced with each other.
tacrolimus blood concentration; liver transplantation; enzyme linked immunosorbent assay; enzyme enhanced immunoassay
10.3969/j.issn.1005-1678.2016.12.056
周台玲,通信作者,女,本科,检验技师,研究方向:临床医学检验,E-mail:17192263362@163.com。
R322.4+7
A

