艾塞那肽对2型糖尿病合并无症状高尿酸血症患者血尿酸水平的影响
姜英松,魏 平,何梦鸽,刘春容,卢 松
(1.重庆市人民医院内分泌肾内科 400014;2.第三军医大学西南医院内分泌科,重庆 400038)
艾塞那肽对2型糖尿病合并无症状高尿酸血症患者血尿酸水平的影响
姜英松1,魏平2,何梦鸽1,刘春容1,卢松1
(1.重庆市人民医院内分泌肾内科400014;2.第三军医大学西南医院内分泌科,重庆 400038)
目的观察艾塞那肽对2型糖尿病合并无症状高尿酸血症患者血尿酸(UA)水平的影响。方法选取2014年2月至2015年2月就诊于重庆市人民医院及第三军医大学西南医院门诊及住院部2型糖尿病合并高尿酸血症的患者58例,受试者分为治疗组30例、对照组28例。在原有的口服降糖药物治疗基础上,治疗组皮下注射艾塞那肽,初始剂量每次5 μg,每天2次,1个月后根据临床效果调整为每次10 μg,均为早、晚饭前60 min内皮下注射;对照组皮下注射双时相门冬胰岛素30,起始剂量为0.2 U/kg,每天2次,根据监测血糖水平调整胰岛素使用剂量,同时给予别嘌醇降尿酸。检测两组患者的脂联素(APN)、空腹血糖(FPG)、UA、胰岛素抵抗指数(HOMA-IR)、糖化血红蛋白(HbA1c)、体质量指数(BMI)水平并进行对比。结果治疗12周后,治疗组患者FPG、HbA1c及HOMA-IR较治疗前明显下降,APN水平较治疗前明显升高;治疗24周后,FPG、UA、HOMA-IR、BMI及HbA1c较治疗前明显下降,APN水平较治疗前明显升高。对照组治疗12周后,FPG、HbA1c较治疗前明显下降,但UA及HOMA-IR较治疗前无显著改变,APN水平较治疗前略有下降;治疗24周后,FPG、HbA1c、UA水平较治疗前明显下降,HOMA-IR及APN水平仍无明显变化,而BMI较治疗前略有增加。治疗24周后,治疗组APN较对照组明显升高,而BMI和HOMA-IR较对照组明显下降。结论艾塞那肽在降糖的同时,可有效降低UA水平,其降尿酸机制可能与其升高APN水平、增强胰岛素敏感性、减轻胰岛素抵抗、降低体质量有关。
脂联素;艾塞那肽;无症状高尿酸血症;胰岛素抵抗
2型糖尿病是临床常见、多发的内分泌代谢疾病,除表现为明显糖、脂代谢异常外,还常伴有血尿酸(UA)代谢异常。在合并高尿酸血症的2型糖尿病的患者中,冠心病、急性脑血管病意外、糖尿病肾病等并发症的发生率显著高于不伴高尿酸血症者。高尿酸血症作为糖尿病的慢性并发症状的危险因素和预告因子已引起临床的高度重视[1]。高尿酸血症是发生胰岛素抵抗的独立危险因素,肾小管重吸收功能受到高胰岛素血症的影响,导致血清尿酸清除率随着胰岛素介导的葡萄糖清除率的下降而降低,同时胰岛素抵抗增加了脂肪酸的代谢与糖酵解过程中UA的生成[2]。脂联素(APN)水平低下是高尿酸血症的保护因子[3]。新型降糖药物艾塞那肽是首个获批准的胰高血糖素样肽-1(GLP-1)受体激动剂,除了降低食欲、减轻体质量、改善胰岛素抵抗外,还具有增加APN水平,纠正血脂代谢紊乱及氧化应激等独立于降血糖外的降低心血管疾病高危因素的生理效应[4]。本研究旨在观察GLP-1受体激动剂艾塞那肽在2型糖尿病合并高尿酸血症的患者中对UA水平的疗效分析并探讨其作用机制。
1 资料与方法
1.1一般资料选取2014年2月至2015年2月就诊于重庆市人民医院及第三军医大学西南医院门诊及住院部自愿参加本试验的58例2型糖尿病合并高尿酸血症患者为研究对象。纳入标准:(1)1999年WHO 2型糖尿病诊断标准,经饮食、运动、二甲双胍或其他降糖药物治疗3个月以上血糖控制不达标,空腹血糖(FPG)7~11 mmol/L,餐后2 h血糖(2hPG)10~21 mmol/L;(2)男性UA>420 mmol/L,女性UA>360 mmol/L,均无痛风发作史;(3)常规肝肾功能检查未见异常;(4)血压均小于或等于140/90 mm Hg。排除标准:(1) 1型糖尿病和其他特殊类型糖尿病;(2)存在无症状低血糖症;(3)既往6个月反复发重大低血糖事件;(4)既往3个月内服用降尿酸药物或影响尿酸代谢药物;(5)存在严重心脏病、血液或任何可能影响试验结果的疾病或药物;(6)严重感染或近期慢性疾病活动期患者。采取随机数字表法将58例患者分为2组,艾塞那肽组(治疗组)30例,男18例,女12例,年龄33~67岁,平均(50.70±9.41)岁,病程6~12年,平均(10.78±3.98)年。门冬胰岛素30+别嘌呤醇治疗组(对照组)28例,男18例,女10例,年龄41~69岁,平均(51.20±8.13)岁,病程7~22年,平均(11.02±5.17)年。两组患者年龄、性别、糖尿病病程、APN、空腹血糖(FPG)、UA、糖化血红蛋白(HbA1c)、空腹胰岛素(FINS)水平差异均无统计学意义(P>0.05)。研究方案获得重庆市人民医院及第三军医大学西南医院伦理委员会批准,遵循赫尔辛基宣言和药物临床试验质量管理规范(GCP),试验开始前征得受试者同意并签署知情同意书。
1.2方法在原先的饮食、运动、口服降血糖药物治疗基础上,治疗组加用GLP-1受体激动剂艾塞那肽(美国礼来公司,生产批号141030),初始剂量每次5 μg,每天2次,1个月后根据临床效果调整为每次10 μg,均为早、晚饭前60 min内皮下注射;对照组采用胰岛素联合别嘌醇降尿酸治疗,患者于早、晚餐前5 min皮下注射双时相门冬胰岛素30[诺和诺德(中国)制药有限公司,生产批号S20040059],起始剂量为0.2 U/kg,每天2次,根据监测血糖水平调整胰岛素使用剂量,加用别嘌醇片(重庆青阳药业有限公司,生产批号141214),口服剂量 0.1 g,每天2次。因别嘌醇具有骨髓抑制及肝肾毒性,需每2周复查血、尿、便常规及肝、肾功能。两组患者均连续治疗24周,治疗期间继续原有的降脂方案,均予以清淡、低嘌呤饮食,避免进食海鲜。所有受试者入组时均脱鞋免冠后测量身高及体质量计算体质量指数(BMI),晚餐后8 h空腹至次晨采集静脉血,测定APN、FPG、UA、HbA1c、FINS水平。FPG及UA采用HITACHI7600全自动生物化学分析仪测定,HbA1c测定采用亲和色谱法,酶联免疫吸附试验用以检测APN水平,FINS采用化学发光法。采用稳态模型法计算胰岛素抵抗指数(HOMA-IR),HOMA-IR=(FINS×FPG)/22.5。观察两组患者治疗前,治疗12周、24周上述各项指标。
2 结 果
2.1一般情况治疗组仅1例因不能耐受严重腹胀、恶心等胃肠道反应退出;对照组6例失访,其中2例分别于第4周、6周肾功异常退出(血肌酐大于150 μmol/L),1例第8周肝功异常退出(肝脏丙氨酸氨基转移酶在正常上限的2.5倍以上),1例自服外购中药退出,2例出现严重皮疹退出。最后共有51例患者完成研究,其中治疗组29例(男21例,女8例),对照组22例(男16例,女6例)。
2.2两组各项指数比较治疗组:治疗12周后,患者FPG、HbA1c及HOMA-IR较治疗前明显下降,APN水平较治疗前明显升高,差异有统计学意义(P<0.05);UA水平下降不明显,与治疗前比较差异无统计学意义(P>0.05)。治疗24周后FPG、UA、HOMA-IR、BMI及HbA1c较治疗前明显下降,APN水平较治疗前明显升高,差异均有统计学意义(P<0.05)。对照组:治疗12周后FPG、HbA1c较治疗前明显下降,差异有统计学意义(P<0.05);UA及HOMA-IR较治疗前无显著改变,APN水平较治疗前略有下降,差异均无统计学意义(P>0.05)。治疗24周后FPG、HbA1c、UA水平较治疗前明显下降,差异有统计学意义(P<0.05);HOMA-IR及APN水平仍无明显变化,BMI较治疗前略有增加,差异均无统计学意义(P>0.05)。治疗24周后,治疗组APN较对照组明显升高,而BMI和HOMA-IR明显下降,差异均有统计学意义(P<0.05)。见表1。
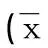
表1 两组患者治疗前后各项指标比较±s)
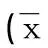
续表1 两组患者治疗前后各项指标比较±s)
3 讨 论
高糖代谢导致尿酸增多主要与肾小管重吸收功能减退有关;同时UA升高严重影响血糖代谢,其相关机制包括氧化应激、炎性反应、下调APN水平等方面。传统的降糖方案无论是胰岛素还是口服降糖药大多数只是针对性的降低血糖水平,而对胰岛β细胞功能、低血糖、血脂、体质量及UA水平等没用明显的改善功能。传统降糖药在有效降低血糖的同时,往往会增加体质量,甚至出现低血糖,从而增加代谢综合征和心脑血管事件的发生概率[5]。有些降糖药物影响尿酸的生成和排泄,UA会呈现继发性的升高,甚至诱发痛风急性发作、泌尿性结石、尿酸性肾病而加重病情。对于合并高尿酸血症的2型糖尿病患者,使用降糖药物的同时,联合应用降尿酸药物不仅增加经济负担,且药物种类多,易发生药物相互作用,引起不良反应[6-7]。在2型糖尿病合并高尿酸血症的患者中常伴有胰岛素抵抗,单纯口服降尿酸药物控制UA水平却无法逆转胰岛素抵抗及胰岛β细胞功能[8],与本研究结果一致。噻唑烷二酮类口服降糖药物罗格列酮为高选择性过氧化物酶体增殖激活受体(peroxisome proliferator-activated receptors,PPARs)的激动剂,降糖的同时虽可以通过上调肾小管上皮细胞人尿酸盐转运子(hUAT)基因和人尿酸盐阴离子转换器1(hURAT1)基因。增加肾脏对尿酸盐排泄,起到降尿酸作用,但是因水钠潴留、体质量增加等不良反应易诱发充血性心力衰竭。对于合并高尿酸血症的2型糖尿病患者,选择一种既能降糖、调脂、改善胰岛素抵抗,又有降尿酸等作用的药物,可获得一举两得的效果。
新型降糖药物艾塞那肽是一种人GLP-1类似物,GLP-1主要是在糖类的作用下释放入血的,能促进胰岛β细胞增殖分化,促进胰岛素的合成与分泌,同时抑制食欲、延缓胃排空、减轻体质量等[9]。APN是新近发现的脂肪组织特异分泌的一种细胞因子,具有调节糖脂代谢、改善胰岛素抵抗、抗炎及抗动脉粥样硬化等作用,在延缓2型糖尿病及其慢性并发症的发生、发展中起重要作用[10]。APN水平低下是高尿酸血症的保护因子[11]。本研究证实艾塞那肽在治疗12周后可明显升高APN水平,24周后可显著降低UA水平。目前研究尚未明确艾塞那肽降尿酸的机制是源于降糖的直接获益还是APN水平升高的结果,抑或仅为伴随现象,或为降糖、APN水平升高及改善胰岛素抵抗、增加胰岛素敏感性等综合因素所致,有待进一步证实。也有研究证实,GLP-1类药物能减轻肾小球系膜增生,从而减少肾小球基底膜厚度,起到保护肾小球滤过膜的电荷和分子屏障的作用,从形态学上解释了艾塞那肽降低UA的原因。本研究中还发现,对照组口服别嘌醇降尿酸过程中诱发痛风3例,治疗组中未出现痛风,考虑与其升高APN水平,抑制单核-巨噬细胞合成白细胞介素6(IL-6)、肿瘤坏死因子α(TNF-α),降低其诱导产生基质金属蛋白酶3(MMP-3)有关。
综上所述,对血糖升高且合并高尿酸血症的患者应用艾塞那肽治疗能够达到与别嘌呤醇相同的降尿酸效果。另外,艾塞那肽治疗组在恢复胰岛功能、心血管危险及降低体质量方面明显优于对照组,可显著减低2型糖尿病患者的空腹、餐后血糖及HbA1c,且不增加低血糖的风险,不影响肝、肾功能。同时通过减轻体质量、升高APN水平,降低尿酸、避免痛风发作,全面调节患者的代谢指标,达到2型糖尿病患者的综合治疗指标,值得临床积极推广。
[1]Yang T,Chu CH,Bai CH,et al.Uric acid level as a risk marker for metabolic syndrome:a Chinese cohort study[J].Atherosclerosis,2012,220(2):525-531.
[2]金明姬,刘冠贤,石咏军.高尿酸血症与胰岛素抵抗关系的研究进展[J].中国全科医学,2012,15(3):233-236,248.
[3] Goodarzynejad H,Boroum AMA.Hyperuricemia and the presence and severity of coronary artery disease[J].Lab Med,2010,41(1):40-45.
[4]刘璠,张趁儒,周慧敏,等.人GLP-1类似物对2型糖尿病患者血清IL-6、TNF-α、CRP及脂联素的影响[J].中国现代医学杂志,2014,24(33):27-30.
[5]Sherifali D,Nerenberg K,Pullenayegum E,et al.The effect of oral antidiabetic agents on A1C levels:a systematic review and meta-analysis[J].Diabetes Care,2010,33(8):1859-1864.
[6]彭波,侯静,刘琦.别嘌呤醇对慢性肾衰竭患者肾脏保护作用及机制[J].临床肾脏病杂志,2011,11(1):20-22.
[7]朱娅梅,董砚虎.高尿酸血症合并高血糖患者的合理用药分析[J].药品评价,2015,12(7):32-35,49.
[8]丁立新,贺娓利,吉漩.降低血尿酸治疗对高尿酸血症患者胰岛素抵抗及胰岛β细胞功能的影响[J].中国糖尿病杂志,2012,20(7):496-498.
[9]Apovian CM,Bergenstal RM,Cuddihy RM,et al.Effects of exenatide combined with lifestyle modification in patients with type 2 diabetes[J].Am J Med,2010,123(5):468.
[10]Lau CH,Muniandy S.Novel adiponectin-resistin (AR) and insulin resistance (IRAR) indexes are useful integrated diagnostic biomarkers for insulin resistance,type 2 diabetes and metabolic syndrome:a case control study[J].Card Diabetol,2011,10(4):8.
[11]杨晓瑜,魏巍,陈捷,等.2型糖尿病合并痛风患者血清内脂素、脂联素和C反应蛋白变化及其临床意义[J].现代实用医学,2013,25(8):854-855,858.
The influence of exenatide in blood uric acid levels of type 2 diabetes patients with asymptomatic hyperuricaemia
Jiang Yingsong1,Wei Ping2,He Mengge1,Liu Chunrong1,Lu Shong1
(1.Department of Internal Medicine,Chongqing People′s Hospital,Chongqing 400014,China;2.Department of Endocrinology,Southwest Hospital,Third Military Medical University,Chongqing 400038,China)
ObjectiveTo observe the influence of exenatide in blood uric acid(UA) levels of type 2 diabetes patients with asymptomatic hyperuricaemia.MethodsTotally 58 voluntary outpatients and inpatients with type 2 diabetes and asymptomatic hyperuricemia in the department of endocrinology in Chongqing Municipal People′s Hospital and Southwest Hospital from February 2014 to February 2015 were selected.Subjects were randomly divided into two groups:30 cases in the observed group (exenatide treatment group),28 cases in the control group (insulin + allopurinol treatment group).In addition to the original oral hypoglycemic medication treatment,exenatide was applied to the treatment group by a subcutaneous injection of 5 μg twice a day for a month,then it was adjusted,according to the clinical effect,to 10 μg twice a day,within 60 minutes before breakfast and supper.The control group was subcutaneously injected with dual-phase insulin aspart 30.The initial dose was 0.2 U/kg,twice a day,and insulin dose was adjusted according to the monitored blood glucose levels.Allopurinol was also provided to control uric acid level.All patients were in light diet and were asked to avoid eating seafood three days before the examination.All patients were clinically observed for a period of 12 weeks and 24 weeks.Blood UA levels,adiponectin (APN),fasting plasma glucose (FPG),body mass index (BMI),insulin resistance index (HOMA-IR),hemoglobin A1c(HbA1c) levels were tested and compared between groups.ResultsIn treatment group,after 12 weeks of treatment,FPG,HbA1c and HOMA-IR levels decreased significantly than before,and serum APN level increased significantly than before.After 24 weeks of treatment,FPG,UA,HOMA-IR,BMI and HbA1c levels decreased significantly than before.Serum APN levels increased significantly than before.In control group,after 12 weeks of treatment,FPG,HbA1c decreased significantly than before.But UA and HOMA-IR did not change significantly than before.Serum APN levels decreased slightly than before.After 24 weeks of treatment,FPG、HbA1c、UA decreased significantly than before.HOMA-IR and serum APN levels did not change significantly than before.And BMI levels increased slightly than before.Comparing the two groups,after 24 weeks of treatment,serum APN levels increased significantly in treatment group than in control group.BMI and HOMA-IR levels decreased significantly in treatment group than in control group.ConclusionExenatide can not only control blood glucose,but also reduce the blood uric acid level effectively.And the mechanism of its reduction of uric acid may be related to elevating serum adiponectin levels,enhancing insulin sensitivity,reducing insulin resistance,and reducing weight.
adiponectin;exenatide;asymptomatic hyperuricemia;insulin resistance
姜英松(1979-),主治医师,博士,主要从事肾内科工作。
论著·临床研究10.3969/j.issn.1671-8348.2016.22.015
R589.7
A
1671-8348(2016)22-3066-03
2016-02-23
2016-04-11)

