日灼胁迫对枇杷果皮蛋白质组的影响
潘德灼,邓朝军,吕晓杰,宋晓敏,邱智敏,龚慧文,蒋际谋,陈 伟*
(1 福建农林大学 生命科学学院,福州 350002;2 福建省农业科学院果树研究所,福州 350013;3 福建农林大学 林学院,福州 350002)
日灼胁迫对枇杷果皮蛋白质组的影响
潘德灼1,邓朝军2,吕晓杰1,宋晓敏1,邱智敏3,龚慧文1,蒋际谋2,陈伟1*
(1 福建农林大学 生命科学学院,福州 350002;2 福建省农业科学院果树研究所,福州 350013;3 福建农林大学 林学院,福州 350002)
为了探讨枇杷果皮响应日灼胁迫的差异表达蛋白的变化,以日灼抗性弱的‘金钟’枇杷和日灼抗性较强的‘红猴本’枇杷为研究对象,将处于转色期的枇杷果实在40 ℃下日灼处理90 min,果皮蛋白采用双向电泳分离和MALDI-TOF/TOF-MS进行鉴定。结果显示:(1)日灼后枇杷果皮中有64个表达丰度在2倍以上的差异蛋白,其中56个蛋白被成功鉴定,且38个在‘金钟’中表达,23个在‘红猴本’中表达。(2)这些蛋白质参与胁迫响应和防御(30.3%)、光合作用(14.3%)、呼吸作用(25.0%)、蛋白质代谢(14.3%)等生理过程。(3)相对于‘红猴本’枇杷,‘金钟’枇杷果皮细胞中多种热激蛋白(HSP)的含量上升,参与呼吸作用的蛋白含量增加以产生更多的能量,但是大部分与光合作用相关的蛋白含量下降,清除活性氧(ROS)酶如抗坏血酸过氧化物酶(APX)和多酚氧化酶(PPO)含量降低,同时PPO酶活性下降。研究表明,要提高枇杷果皮抗日灼性可能需要提高清除ROS酶的含量和活性,需要一定量的HSP,以及保持正常的呼吸作用和光合作用。
枇杷;果皮;日灼;差异蛋白
枇杷(Eriobotryajaponica(Thunb.) Lindl.)是原产于中国南方的蔷薇科枇杷属的亚热带果树,果实成熟于春末夏初,果肉柔软多汁,富含蛋白质、氨基酸和维生素等营养物质,经济价值高,同时果实还可入药,具有润肺止咳等功效,药用价值高[1]。2006年,中国枇杷的栽培面积达到了12万公顷,产量高达45.4万吨,约占世界总产量的67%[2]。福建是中国枇杷的主产地之一,高居中国枇杷总产量前列[3]。
果实日灼是一种由高温强光胁迫引起的果实生理病害现象。“温室效应”的增强造成全球气温的升高,而高温下的强光对许多园艺作物的生产栽培造成了很大的威胁,尤其是果实外观会出现不同程度的日灼病斑[4-6]。高温强光胁迫会引起果实果皮的抗氧化能力发生变化。有研究发现,日灼的石榴(PunicagranatumL.)果实无法抵抗氧化胁迫从而造成可见的果皮病斑[6]。苹果(Malus×domesticaBorkh)果皮受高温强光胁迫引起活性氧含量的上升,同时抗氧化酶的活性也增强,但是不足以防御光氧化胁迫带来的损伤,最终导致苹果果皮日灼病斑的出现[7]。在一定高温胁迫范围内,苹果果皮中抗坏血酸过氧化物酶(APX)活性随日灼程度的增强而上升,但超过一定限度,其活性明显下降,这意味着过度的高温强光会破坏APX的活性从而加大日灼伤害[8]。日灼的柑橘(Citrusreticulata)表皮细胞内活性氧含量剧增,抗氧化系统清除活性氧的能力明显降低[9]。喷施外源抗氧化剂能显著提高红地球葡萄(Vitisviniferacv. Red Globe)果皮过氧化氢酶(CAT)、APX和SOD的活性,增强果皮的抗热性[10]。此外,高温强光胁迫还会引起细胞中蛋白质种类和表达量发生变化[11-12],尤其可诱导产生大量热激蛋白[4]。
枇杷以鲜销为主,枇杷果皮的日灼极大地影响其果实品质、产量和经济效益,造成极大的损失,直接制约了枇杷在国际鲜果市场上的占有量[13-14],研究枇杷果实日灼发生的生理分子机制具有重要的意义。目前,学者已明确了枇杷果实日灼发生的敏感时期[15],解析了枇杷果皮日灼发生的生理生化的原因[14],探讨了果皮日灼发生时蛋白质表达的变化[11-12],同时提出预防枇杷果皮日灼的套袋等方法[16]。但是对于枇杷果皮日灼发生的分子机制还不清楚。因此,本研究采用双向电泳(Two-dimentional electrophoresis,2-DE)和MALDI-TOF/TOF-MS技术,以日灼抗性弱的‘金钟’和日灼抗性较强的‘红猴本’枇杷品种为研究对象,比较分析这2种枇杷果皮中差异表达的蛋白功能,以揭示调控果皮抗高温强光胁迫的分子机理,为选育抗日灼枇杷品种提供理论依据,也为防治枇杷日灼提供参考。
1 材料和方法
1.1试验材料供试枇杷品种为日灼抗性弱的‘金钟’(JZH)和日灼抗性较强的‘红猴本’(HHB),均采自福建省农业科学院果树研究所国家果树种质福州龙眼枇杷圃。在晴天(光照强度 ≥ 1 100 μmol·m-2·s-1),选择位于7年树龄的枇杷树的树冠外围中上部相同方位、结果性状基本一致、果实大小均一、果皮无损伤、处于转色期的果穗10穗,使用果实日灼诱导仪进行诱导处理(图1),诱导温度40 ℃,诱导时间90 min,以未诱导处理的枇杷为对照组,削取向阳面的果皮,液氮速冻后储藏于-80 ℃冰箱中备用。
1.2蛋白质的分离与鉴定
1.2.1蛋白质的提取蛋白质的提取采用酚抽提法[17]。取3 g样品于预冷的陶瓷研钵中,加入少量的石英砂,加入液氮充分研磨至细粉末状,加入12 mL的蛋白酚抽提取液[100 mmol·L-1Tris-HCl (pH 8.0),50 mmol·L-1抗坏血酸,50 mmol·L-1硼砂,100 mmol·L-1KCl,1% (v/v) Triton-100,2% (v/v) β-巯基乙醇]和12 mL Tris-饱和酚(pH 8.0),混匀后4 ℃、5 500 ×g离心10 min,吸取酚层,加入6倍体积预冷的0.1 mol·L-1乙酸铵甲醇溶液,-20 ℃过夜沉淀蛋白后4 ℃、20 000 ×g离心20 min,弃上清液,沉淀的蛋白先用预冷的甲醇溶液清洗1次,再用预冷的含有0.07% (v/v) β-巯基乙醇的丙酮溶液清洗2次,均置于-20 ℃下静置1 h;4 ℃、20 000 ×g离心20 min,再用含有0.07%β-巯基乙醇的丙酮溶液清洗1次,均置于-20 ℃下静置1 h后再以4 ℃、20 000 ×g离心20 min,最后将沉淀的蛋白悬浮于预冷的丙酮中,4 ℃、20 000 ×g离心20 min后所得蛋白沉淀,冷冻干燥后-80 ℃保存备用。

图1 枇杷果皮的日灼诱导处理Fig. 1 Treatment induced by sunburn on loquat pericarp
1.2.2蛋白质的2-DE分离取3 mg蛋白质干粉溶解于300 μL蛋白裂解液[2% (v/v) Ampholyte pH 4~7,7 mol·L-1尿素,40 mmol·L-1DTT,2 mol·L-1硫脲,40 g·L-1CHAPS]中,37 ℃恒温水浴2.5 h后20 000 ×g室温离心15 min,取上清液采用Bradford法[18]测定蛋白质含量,以牛血清蛋白(BSA)为标准品。2-DE参考You等[17]方法,第一向固相pH梯度等电聚焦(IEF)采用Amersham Ettan IPGphor Ⅲ系统(GE Healthcare Amersham Biosciences),上样量为1.3 mg,IPG胶条为24 cm、pH 4~7的线性胶条,IEF参数的设定为:30 V(12 h)、200 V(1 h)、500 V(1 h)、1 000 V(1 h)、1 000~8 000 V Gradient(30 min)、8 000 V(6 h)、1 000 V(1 h),运行温度20 ℃,最大电流50 μA。第二向凝胶电泳采用EttanTMDALT Ⅱ垂直板电泳系统(GE Healthcare Amersham Biosciences),凝胶浓度为11%,先设恒定电流15 mA电泳30 min后增大至30 mA,直至溴酚蓝迁移至胶底0.5 cm处结束。采用考马斯亮蓝G250染色并脱色后经EPSON PERFECTION 2480 PHOTO仪器扫描,应用ImageMaster 2D platinum 5.0 软件分析胶图并找出差异表达2倍以上并且重复性好(P≤ 0.5)的蛋白点。
1.2.3蛋白质的质谱鉴定差异表达的蛋白经trypsin酶解后进行MALDI-TOF/TOF-MS质谱鉴定[19]。质谱所用仪器为5800串联飞行时间质谱仪(Applied Biosysterms SCIEX,USA),质谱数据通过GPS Explorer 3.6 (Applied Biosysterms SCIEX,USA) 和 MASCOT 软件(Version 2.1,Matrix Science,London,UK)检索:数据库为NCBInr(发布日期:2010.07.01),检索方式为Combined,最大允许胰蛋白酶漏切位点为1,质谱误差设置为100 ppm,MS/MS误差设置为0.6 Da。
1.3果皮膜透性和丙二醛(MDA)含量的的测定
枇杷果皮膜透性的测定参考商宏莉等[20]方法,略作修改。称取2 g枇杷果皮,剪成长约1 cm小段放入小烧杯中,加入20 mL蒸馏水后,用抽气机抽气10 min,室温静置20 min后用电导仪测定烧杯中溶液的电导率B;最后将烧杯置于沸水中水浴处理10 min,取出烧杯并室温静置20 min后测定枇杷果皮煮沸后的电导率C。另外设空白组,测定蒸馏水的电导率A。根据公式:伤害率(%)=(B-A)/(C-A)×100%,求得伤害率。
MDA含量的测定采用硫代巴比妥酸(TBA)法[21]。称取1 g枇杷果皮,用液氮磨成粉末,加入8 mL 50 g·L-1三氯乙酸,4 ℃、3 000 ×g离心10 min。取2 mL上清液加入2 mL 6.7 g·L-1TBA,振荡混匀,沸水浴30 min,迅速冷却后,3 000 ×g离心10 min,上清液分别在450 nm、532 nm和600 nm下测得OD值,计算单位鲜重叶片组织中MDA的含量,单位表示为μmol·g-1。
1.4多酚氧化酶(PPO)活性的测定
PPO活性的测定采用邻苯二酚法[22]。称取0.8 g 枇杷果皮,用液氮磨成粉末,加入4 mL 0.1 mol·L-1(pH 6.5)磷酸缓冲液,4 ℃、8 000 ×g离心15 min,上清液即为待测酶液。常温条件下,取0.2 mol·L-1邻苯二酚2.5 mL、0.1 mol·L-1(pH 6.5)磷酸缓冲液4 mL,加入1 mL待测酶液启动反应,同时以缓冲液(不加酶液)作空白对照,37 ℃保温3 min后,于410 nm下测定OD值。以每毫升每分钟吸光度变化0.01为一个酶活力单位(U),酶活性单位表示为U·g-1。
1.5Western blotting验证分析
枇杷果皮蛋白的免疫印迹分析参考Wang等[19]方法,略作修改。上样量为50 μg的果皮蛋白经12% SDS-PAGE电泳分离后,采用CDY40C半干转移系统(北京六一仪器厂)转移至硝酸纤维膜上,50 g·L-1脱脂奶粉封闭2 h,用TBST缓冲液(0.01 mol·L-1Tris-HCl缓冲盐溶液,0.1% (v/v) Tween-20,pH 7.6)漂洗后加入按照比例(1∶3 000)稀释的兔抗HSP 70或cAPX多克隆抗体液体室温孵育1 h,用TBST缓冲液漂洗后再加入按照比例(1∶1 000)稀释的HRP偶联的羊抗兔二抗液体继续室温孵育1 h,用TBST缓冲液漂洗后加入DAB(Boster,中国武汉)显色。免疫印迹相对强度用Quantity软件(Bio-Rad,USA)分析。
1.6数据分析
所有实验数据均以平均值±标准差表示,每个实验均进行3 次生物学重复,采用SPSS 13.0统计软件进行方差分析,显著差异为P≤ 0.05,极显著差异为P≤ 0.01 。
2 结果与分析
2.1日灼枇杷果皮差异蛋白的分离与鉴定
果皮是果实中最先遭受高温强光胁迫影响的结构组织。枇杷果实在40 ℃下日灼诱导处理90 min,本实验分别选取处于转色期的JZH和HHB两品种枇杷果实的果皮进行2-DE分离,获得分辨率较高和重复性较好的2-DE图谱(图2)。同时,经过ImageMaster软件对2-DE凝胶图谱的分析,本实验于2个品种的枇杷果皮中共得到64个丰度差异变化在2倍以上的蛋白点(图2)。
通过对64个差异蛋白点的MALDI-TOF/TOF-MS分析,本实验成功鉴定出56个蛋白,但有8个蛋白未能得到可信的匹配,鉴定成功率为87.5%;同时,对鉴定出的56个蛋白进行功能注释和分类(表1)。表1显示,这些蛋白主要分为:(1)胁迫响应与防御蛋白,共有17蛋白点,占所鉴定出的总蛋白的30.3%;(2)光合作用蛋白,共有8个,占14.3%;(3)呼吸作用相关的蛋白,共有14个,占25.0%;(4)与蛋白质代谢相关的蛋白,共有8个,占14.3%;(5)其他蛋白,共有9个,占16.1%。
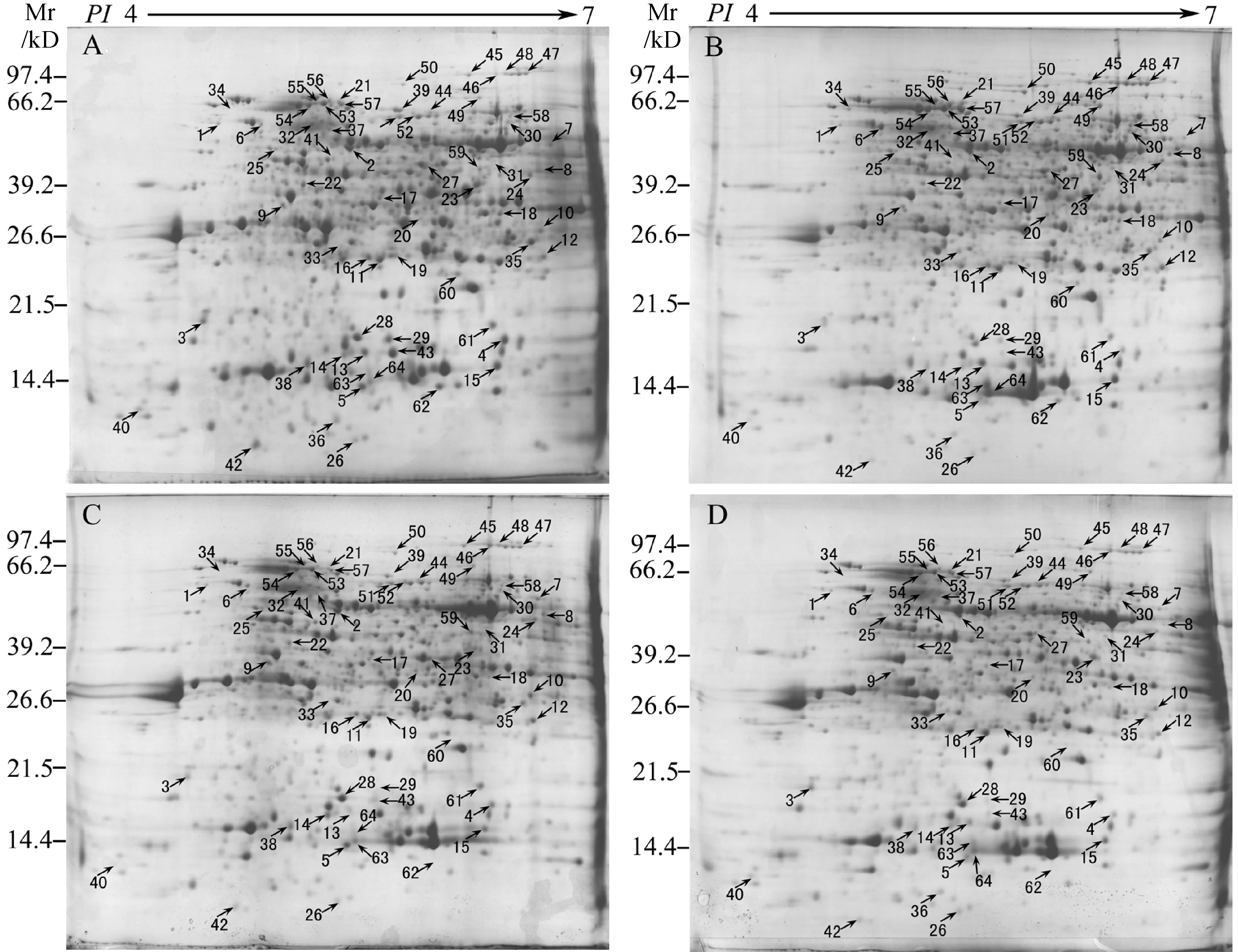
A.‘金钟’对照组;B.‘金钟’日灼处理组;C.‘红猴本’对照组;D.‘红猴本’日灼处理组图2 枇杷果皮日灼诱导的蛋白质2-DE图谱A. Control of JZH; B. Sunburn of JZH; C. Control of HHB; D. Sunburn of HHBFig. 2 2-DE maps of loquat pericarp proteins under sunburn stress
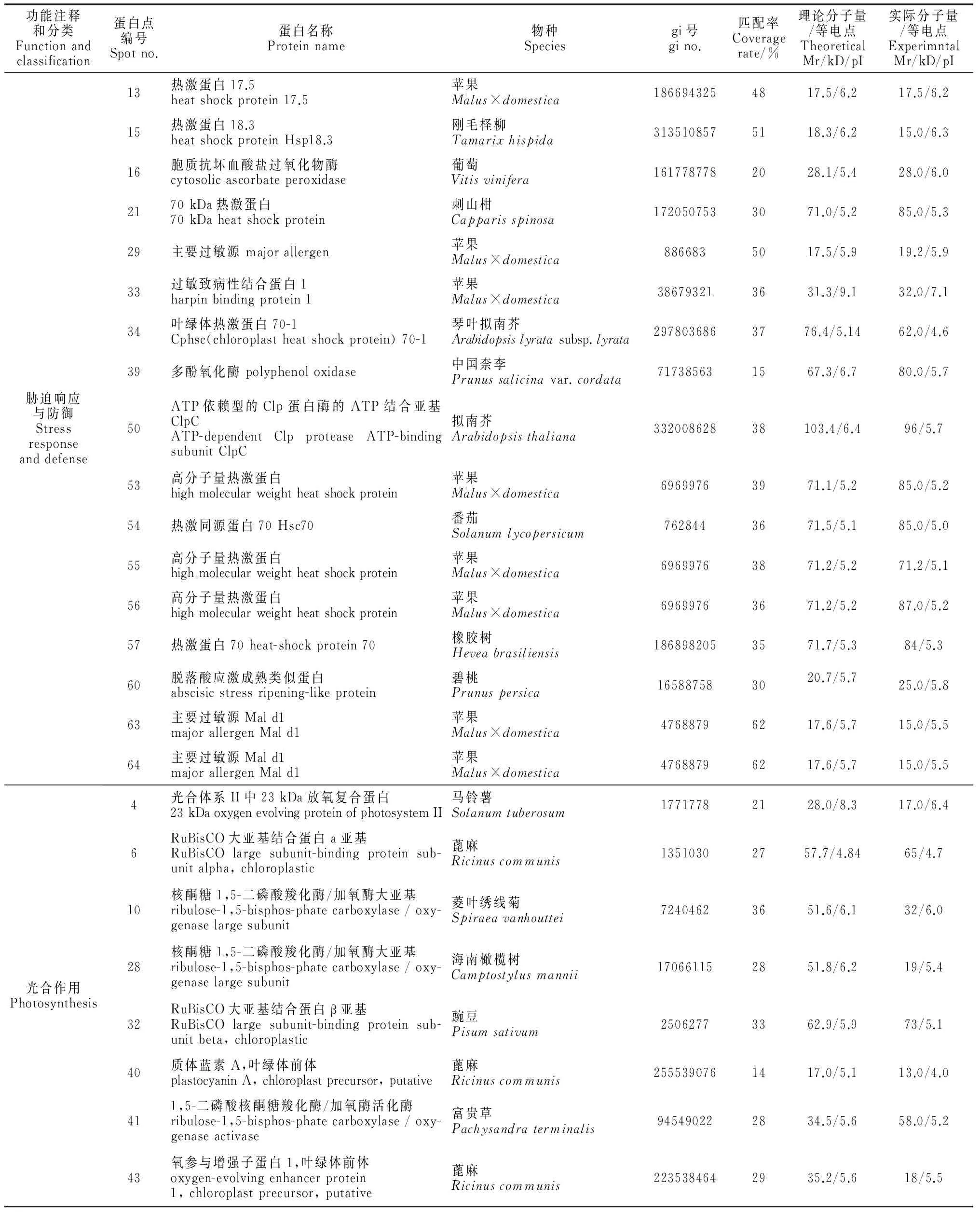
表1 日灼胁迫下两品种枇杷果皮差异蛋白的MALDI-TOF/TOF-MS鉴定结果Table 1 Identification of differentially expressed proteins in loquat fruits pericarps under sunburn by MALDI-TOF/TOF-MS
续表1Continued Table 1
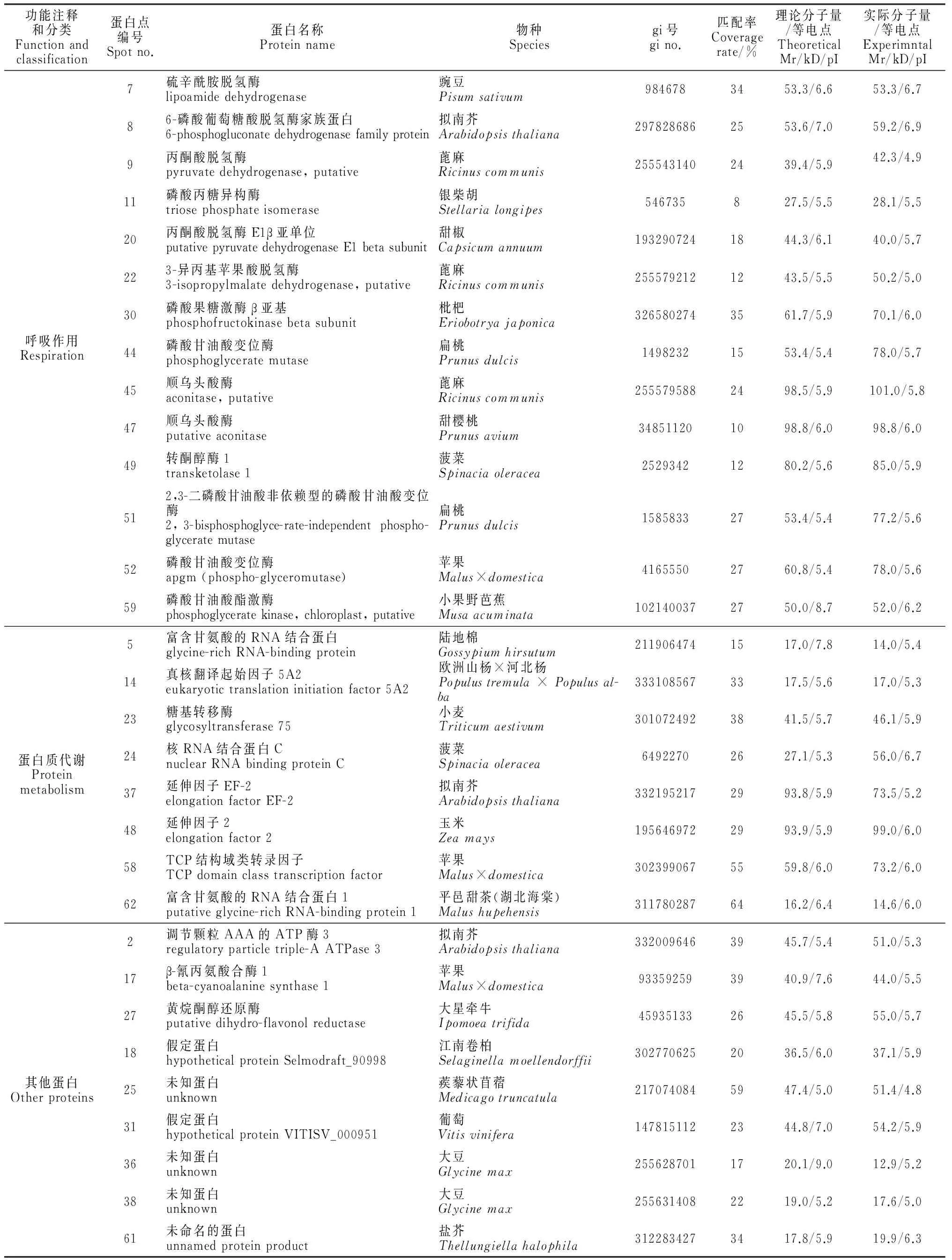
功能注释和分类Functionandclassification蛋白点编号Spotno.蛋白名称Proteinname物种Speciesgi号gino.匹配率Coveragerate/%理论分子量/等电点TheoreticalMr/kD/pI实际分子量/等电点ExperimntalMr/kD/pI呼吸作用Respiration7硫辛酰胺脱氢酶lipoamidedehydrogenase豌豆Pisumsativum9846783453.3/6.653.3/6.786-磷酸葡萄糖酸脱氢酶家族蛋白6-phosphogluconatedehydrogenasefamilyprotein拟南芥Arabidopsisthaliana2978286862553.6/7.059.2/6.99丙酮酸脱氢酶pyruvatedehydrogenase,putative蓖麻Ricinuscommunis2555431402439.4/5.942.3/4.911磷酸丙糖异构酶triosephosphateisomerase银柴胡Stellarialongipes546735827.5/5.528.1/5.520丙酮酸脱氢酶E1β亚单位putativepyruvatedehydrogenaseE1betasubunit甜椒Capsicumannuum1932907241844.3/6.140.0/5.7223-异丙基苹果酸脱氢酶3-isopropylmalatedehydrogenase,putative蓖麻Ricinuscommunis2555792121243.5/5.550.2/5.030磷酸果糖激酶β亚基phosphofructokinasebetasubunit枇杷Eriobotryajaponica3265802743561.7/5.970.1/6.044磷酸甘油酸变位酶phosphoglyceratemutase扁桃Prunusdulcis14982321553.4/5.478.0/5.745顺乌头酸酶aconitase,putative蓖麻Ricinuscommunis2555795882498.5/5.9101.0/5.847顺乌头酸酶putativeaconitase甜樱桃Prunusavium348511201098.8/6.098.8/6.049转酮醇酶1transketolase1菠菜Spinaciaoleracea25293421280.2/5.685.0/5.9512,3-二磷酸甘油酸非依赖型的磷酸甘油酸变位酶2,3-bisphosphoglyce-rate-independentphospho-glyceratemutase扁桃Prunusdulcis15858332753.4/5.477.2/5.652磷酸甘油酸变位酶apgm(phospho-glyceromutase)苹果Malus×domestica41655502760.8/5.478.0/5.659磷酸甘油酸酯激酶phosphoglyceratekinase,chloroplast,putative小果野芭蕉Musaacuminata1021400372750.0/8.752.0/6.2蛋白质代谢Proteinmetabolism5富含甘氨酸的RNA结合蛋白glycine-richRNA-bindingprotein陆地棉Gossypiumhirsutum2119064741517.0/7.814.0/5.414真核翻译起始因子5A2eukaryotictranslationinitiationfactor5A2欧洲山杨×河北杨Populustremula×Populusal-ba3331085673317.5/5.617.0/5.323糖基转移酶glycosyltransferase75小麦Triticumaestivum3010724923841.5/5.746.1/5.924核RNA结合蛋白CnuclearRNAbindingproteinC菠菜Spinaciaoleracea64922702627.1/5.356.0/6.737延伸因子EF-2elongationfactorEF-2拟南芥Arabidopsisthaliana3321952172993.8/5.973.5/5.248延伸因子2elongationfactor2玉米Zeamays1956469722993.9/5.999.0/6.058TCP结构域类转录因子TCPdomainclasstranscriptionfactor苹果Malus×domestica3023990675559.8/6.073.2/6.062富含甘氨酸的RNA结合蛋白1putativeglycine-richRNA-bindingprotein1平邑甜茶(湖北海棠)Malushupehensis3117802876416.2/6.414.6/6.0其他蛋白Otherproteins2调节颗粒AAA的ATP酶3regulatoryparticletriple-AATPase3拟南芥Arabidopsisthaliana3320096463945.7/5.451.0/5.317β-氰丙氨酸合酶1beta-cyanoalaninesynthase1苹果Malus×domestica933592593940.9/7.644.0/5.527黄烷酮醇还原酶putativedihydro-flavonolreductase大星牵牛Ipomoeatrifida459351332645.5/5.855.0/5.718假定蛋白hypotheticalproteinSelmodraft_90998江南卷柏Selaginellamoellendorffii3027706252036.5/6.037.1/5.925未知蛋白unknown蒺藜状苜蓿Medicagotruncatula2170740845947.4/5.051.4/4.831假定蛋白hypotheticalproteinVITISV_000951葡萄Vitisvinifera1478151122344.8/7.054.2/5.936未知蛋白unknown大豆Glycinemax2556287011720.1/9.012.9/5.238未知蛋白unknown大豆Glycinemax2556314082219.0/5.217.6/5.061未命名的蛋白unnamedproteinproduct盐芥Thellungiellahalophila3122834273417.8/5.919.9/6.3
注:表中蛋白点序号与图2中2-DE凝胶上的蛋白点序号一致
Note: Spot No. in the table corresponds to the 2-DE gel in Figure 2
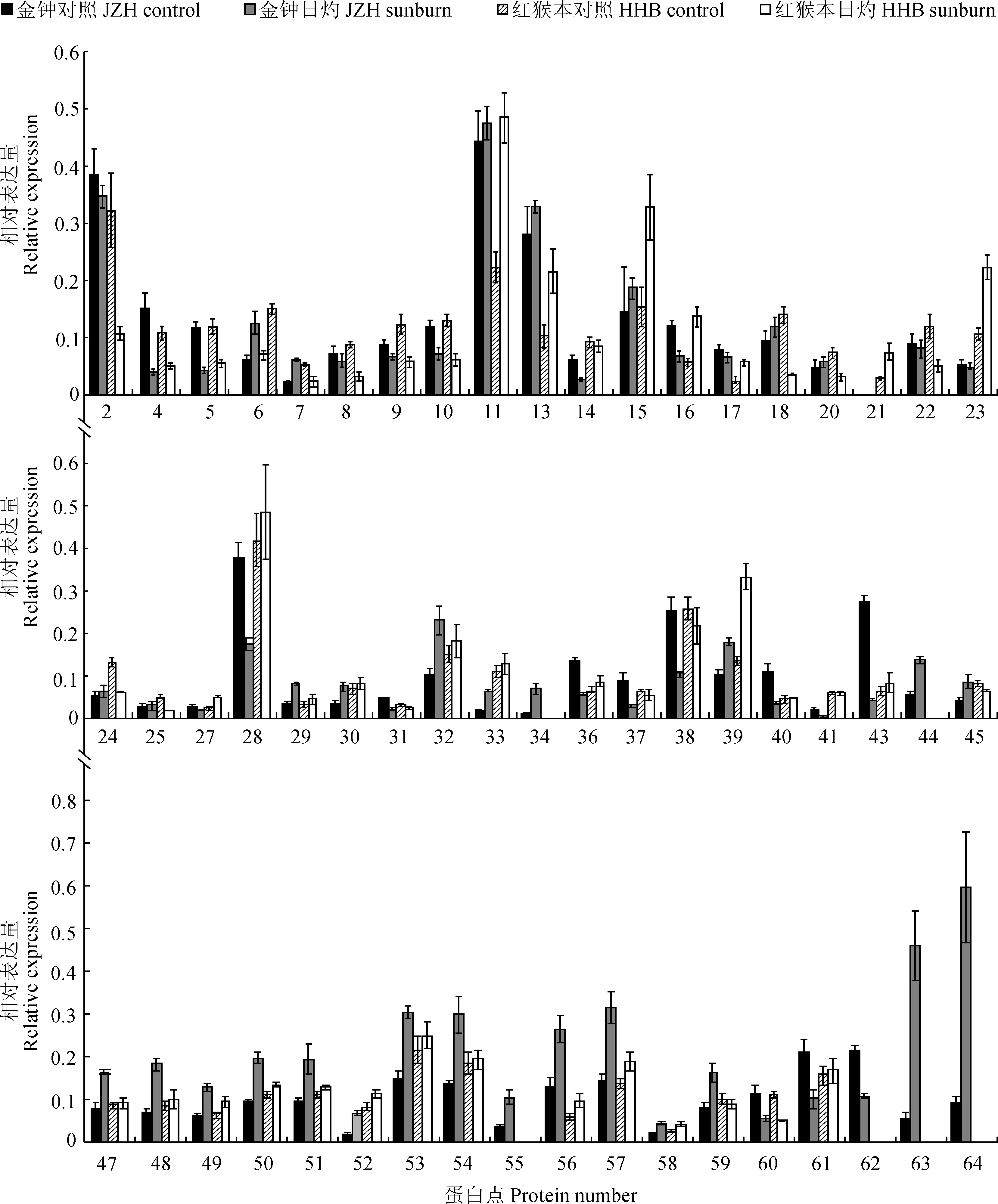
图中蛋白点序号与图2中2-DE凝胶上的蛋白点序号一致图3 枇杷果皮56个差异蛋白相对表达量的变化Spot No. in this figure corresponds to the 2-DE gel in Figure 2Fig. 3 Relative expression quantities of 56 differential expressed proteins in loquat pericarp
同时,这56个差异表达蛋白在JZH和HHB枇杷果皮中的表达模式是不同的(图3)。其中,5个蛋白在2种枇杷中表达均差异显著,蛋白点4、5和60在2种枇杷中均下调表达,蛋白点6在2种枇杷中上调表达,而蛋白点7在JZH枇杷中上调表达,在HHB枇杷中下调表达;33个蛋白只在JZH枇杷果皮中的表达差异显著,有11个蛋白下调表达,22个蛋白上调表达;另外18个蛋白只在HHB枇杷果皮中的表达差异显著,有9个蛋白下调表达,9个蛋白上调表达。在所有鉴定出的蛋白中,还有6个蛋白未知其功能。
2.2日灼枇杷果皮细胞膜透性以及MDA含量的变化
植物在逆境环境下会发生膜脂过氧化作用,MDA是其产物之一,因此,MDA的含量可以反映出膜质的过氧化程度和植物对逆境反应的强弱。当植物受到逆境胁迫时,细胞膜受到破坏,膜透性会增大。图4,A显示,经过90 min日灼诱导处理后,JZH枇杷果皮的膜透性显著增大,而HHB枇杷果皮的膜透性略微增大。同时,与对照组相比,经过90 min日灼诱导处理后,JZH和HHB枇杷果皮的MDA含量分别增加了2.0倍和0.9倍,差异均达到极显著水平(图4,B)。由此可知,日灼胁迫对枇杷果皮细胞膜的损害较大,而且抗日灼能力弱的JZH枇杷的膜伤害程度明显大于抗性强的HHB。
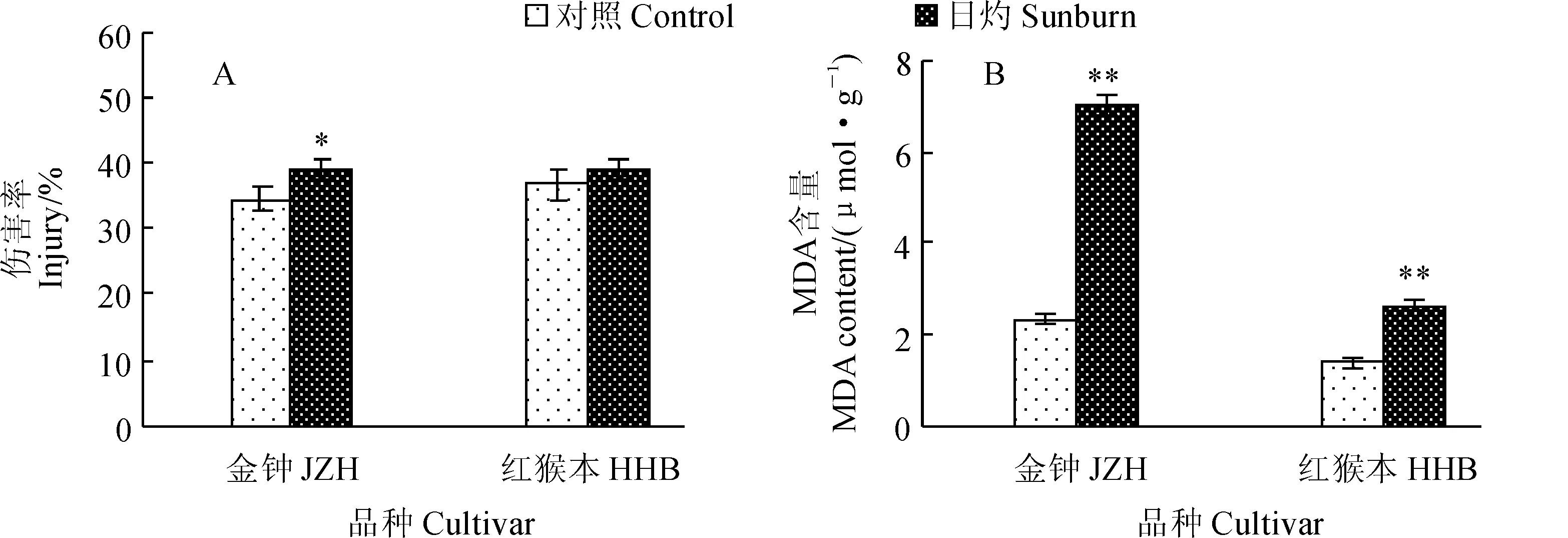
*和**分别表示日灼处理与对照之间在0.05和0.01水平存在显著性差异;下同图4 日灼枇杷果皮的细胞膜伤害率(A)和MDA含量(B)*and ** above the bars indicate a significant difference between the sunburn and control at 0.05,and 0.01 level,respectively;The same as belowFig. 4 Membrane injury (A) and MDA content (B) in sunburn loquat pericarp
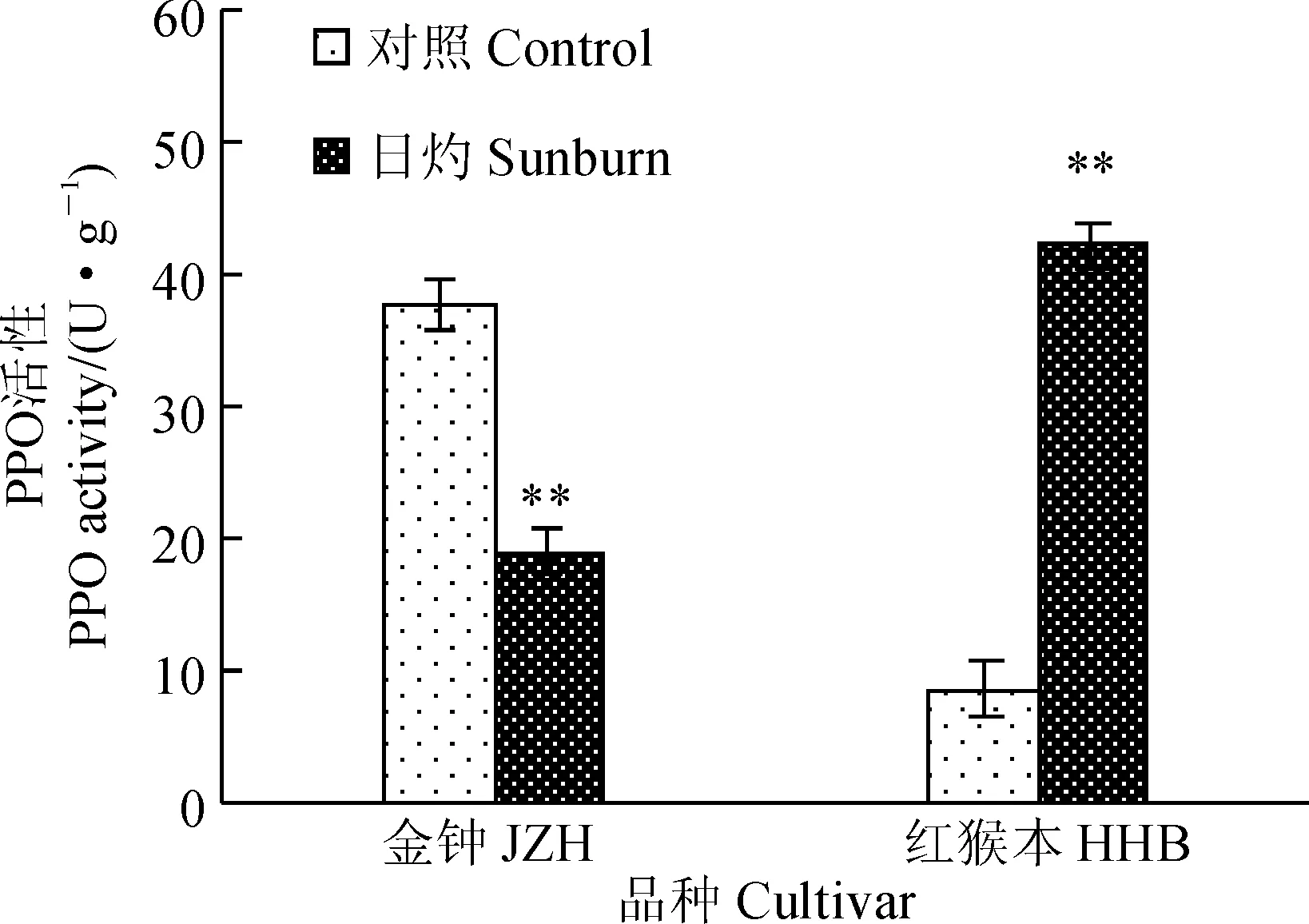
图5 日灼枇杷果皮PPO活性Fig. 5 PPO activity in loquat pericarp
2.3日灼枇杷果皮多酚氧化酶活力的变化
植物在逆境条件下,多酚氧化酶(PPO)的活性会发生变化。由图5可知,与对照组相比,经90 min的日灼诱导处理,JZH枇杷果皮细胞中PPO活性降低了50%,而HHB枇杷果皮细胞中PPO活性却提高了4.0倍。由此可见,抗日灼能力不同的2种枇杷在抵御日灼伤害时所表现出来的PPO活力变化情况正好相反,抗性弱的JZH枇杷果皮中PPO活性极显著下降,而抗性强的HHB枇杷却极显著上升。
2.4日灼枇杷果皮HSP 70和cAPX免疫印迹分析
HSP 70是一种非常重要的热激蛋白,在植物响应高温胁迫中起着作用。前面的2-DE结果发现,日灼处理的JZH枇杷果皮的HSP 70含量显著增加,而日灼HHB枇杷果皮的HSP 70含量略微增加;此外,在日灼处理的JZH枇杷果皮中cAPX蛋白显著下降,在日灼HHB枇杷果皮中cAPX蛋白却显著增加。由图6可知,经过HSP 70和cAPX抗体的免疫印迹分析,HSP 70蛋白在2个品种日灼处理枇杷果皮中均显著增加,而cAPX蛋白在JZH枇杷果皮中显著下降,却在HHB枇杷果皮中显著增加,这与2-DE的结果基本一致。
3 讨 论
本实验通过蛋白质组学研究发现在日灼胁迫下JZH枇杷果皮中有38个差异表达蛋白,在HHB枇杷果皮中有23个差异表达蛋白。这些差异蛋白的生物学功能主要涉及到胁迫响应与防御、光合作用、碳水化合物和能量代谢等生理过程。
3.1胁迫响应与防御相关蛋白
高温强光会引起植物体内活性氧(ROS)含量的增加,植物可通过提高抗氧化酶含量或活性来抵御高温强光胁迫[23-25]。苹果、红地球葡萄果皮中APX活性的提高有助于抗高温强光能力的增强[8,10]。胞质APX是植物体内重要的脱氢过氧化物酶,参与活性氧的清除,维持细胞内平衡[26]。此外,PPO可参与植物组织的衰老和氧化褐变,同时PPO活性的提高可加速H2O2的清除进而有利于草莓的保鲜[27],PPO对采后油桃中H2O2清除也有直接作用[28]。本研究发现胞质APX和PPO含量在HHB枇杷中均上调表达,而在JZH枇杷中均下调表达,同时PPO酶活性的变化趋势与此一致。这可能原因是在JZH枇杷受到日灼过程中产生过多的活性氧进而引起细胞膜质过氧化,导致MDA含量增加和膜透性显著增大,导致了酶活力的下降;相反,在HHB枇杷中这两种酶为了更好地清除细胞产生的大量活性氧而提高了自身活力,进而维持细胞内环境的活性氧代谢平衡,因而这是一种应激保护。以上结果表明JZH枇杷果皮细胞的抗氧化能力弱于HHB枇杷。
植物在受到逆境胁迫时,细胞中的错误折叠蛋白或多肽就会增多,因此植物需要产生多种分子伴侣蛋白(如热激蛋白HSP)来指导蛋白或多肽的正确折叠。当植物遭受高温胁迫时,植物细胞就会产生多个高分子量HSP(60~110 kD)和小分子量HSP(15~45 Da)[23, 29]。这些HSP能够聚合胁迫导致的变性蛋白并且使变性蛋白去折叠,从而恢复其天然的生物学功能[30-31]。本研究发现所有检测到的HSP在两种枇杷中均上调表达,其中HHB枇杷中有3个(蛋白点13、15和21),而JZH枇杷中有6个(蛋白点34、53~57),这可能是因为JZH枇杷的抗热性弱,在日灼处理过程中会形成更多的错误蛋白或多肽,因此需要产生更多的HSP来维持细胞蛋白的正常功能从而抵抗热胁迫。然而,HHB枇杷的抗热性强,对高温强光不敏感,在短期日灼处理时未形成过多的错误折叠蛋白,因此不需要太多的HSP来维持正常的功能。在JZH枇杷果皮中除了有HSP参与错误折叠蛋白或多肽的去折叠外,还有ClpC亚基的参与。有研究表明,Clp是一种非常重要的蛋白酶,用于降解错误的蛋白,而ClpC亚基是其主要的调控成分[32]。由此认为,JZH枇杷中ClpC亚基的上调表达可以提高Clp蛋白酶的降解能力,从而加速清除细胞中错误折叠的蛋白,这也说明JZH枇杷比HHB枇杷对日灼更敏感。
3.2光合作用相关蛋白
高温强光胁迫诱导植物的光合作用发生变化。本研究共检测到8个与光合作用相关的差异表达蛋白,其中JZH枇杷果皮中有6个蛋白(蛋白点4、10、28、40、41和43)均下调表达,只有蛋白6和32上调表达,而HHB枇杷果皮中蛋白6也上调表达,蛋白32略微上调,蛋白4和10下调表达。植物中RuBisCO是光合作用碳反应中重要的羧化酶,由RuBisCO大亚基和小亚基组成[33]。RuBisCO大、小亚基组装成全酶需要RuBisCO亚基结合蛋白的参与[34]。RuBisCO大亚基结合蛋白α亚基(蛋白点6)在2种枇杷中均显著上调表达,RuBisCO大亚基结合蛋白β亚基(蛋白点32)在JZH枇杷中显著上调表达,而在HHB枇杷中略微上调。然而,调控RuBisCO酶活性的RuBisCO活化酶(蛋白点41)以及RuBisCO大亚基(蛋白点10和28)在JZH枇杷中的表达量显著下降,而在HHB枇杷中变化不明显。此外,氧参与增强子蛋白1(蛋白点43)是光系统Ⅱ中心的装配及稳定性的一种必需蛋白[35-36]。质体蓝素参与光合过程中电子的传递,可以将电子从水传递给NADP+,最后形成氧分子。这两种蛋白在JZH枇杷中均下调表达,而在HHB枇杷中未发生显著变化。这些表现意味着JZH枇杷对高温日灼更为敏感,光合作用受到的抑制更加严重。
3.3呼吸作用相关蛋白
高温强光胁迫不仅可以使植物中光合作用和细胞膜的稳定性发生改变,还会影响呼吸作用[37]。其中,与糖酵解途径相关的磷酸果糖激酶(蛋白点30)、磷酸丙糖异构酶(蛋白点11)和磷酸甘油酸变位酶(蛋白点44、51和52)在JZH枇杷果皮中均显著上调表达,而在HHB枇杷中只有磷酸丙糖异构酶显著上调表达,另外2种酶均未发生显著变化。此外,丙酮酸脱氢酶E1和硫辛酰胺脱氢酶参与了氧化代谢,可将丙酮酸转化为2个乙酰CoA,其表达量的降低会造成植物三羧酸(TCA)循环障碍[38]。在TCA循环中,顺乌头酸酶能够摧化柠檬酸转化为异柠檬酸,而且3-异丙基苹果酸脱氢酶催化异柠檬酸转化为2-酮戊二酸。本研究发现丙酮酸脱氢酶(蛋白点9)、丙酮酸脱氢酶E1 β亚基(蛋白点20)、3-异丙基苹果酸脱氢酶(蛋白点22)和硫辛酰胺脱氢酶(蛋白点7)在HHB枇杷中均下调表达,而在JZH枇杷中顺乌头酸酶(蛋白点45和47)却上调表达,其他酶无明显变化。此外,转酮醇酶1(蛋白点49)在戊糖磷酸途径中起重要作用,它在JZH枇杷果皮中显著上升,在HHB枇杷中只是略微上调。我们发现在JZH枇杷果皮中与碳水化合物及能量相关的差异蛋白大部分都上调表达,而在HHB枇杷中只有2个差异蛋白(蛋白点11和49)上调表达,其他均下调表达或无明显差异。这表明在日灼胁迫条件下JZH枇杷果皮中糖酵解途径、三羧酸途径和戊糖磷酸途径均表现出上调表达,而在HHB枇杷中还是以下调表达为主,这可能是因为抗热性弱的JZH枇杷需要更多的能量来抵御日灼胁迫。抗性弱的JZH枇杷在呼吸作用上的变化与‘WDYDB’枇杷果皮响应高温强光胁迫的蛋白质变化模式一致[12]。
3.4蛋白质代谢相关蛋白
在8个与蛋白质代谢相关的差异蛋白中,RNA结合蛋白(蛋白点24)和富含甘氨酸的RNA结合蛋白(蛋白点5和62)参与转录后的基因调控,包括前体mRNA的拼接与带帽、mRNA转运及翻译,它们在植物的生长发育以及抗逆境胁迫中具有重要的作用[39]。起始因子5A(蛋白点14)能够通过控制mRNA核输出率而选择性地翻译蛋白质[40]。延伸因子2(蛋白点37和48)参与新生肽链的延伸。糖基转移酶(蛋白点23)能够将糖基转移到蛋白上,对蛋白进行糖基化修饰,进而调节蛋白功能。本研究发现,在JZH枇杷中,这些蛋白的含量总体上呈下降趋势,而在HHB枇杷中总体上没有发生显著变化,这表明抗热性弱的枇杷因日灼伤害造成蛋白质合成量减少,而抗性强的枇杷所受到的影响较小。
综上所述,本研究比较了JZH枇杷(日灼抗性弱)和HHB枇杷(日灼抗性较强)果皮在日灼胁迫下的差异蛋白表达模式。相对于HHB枇杷,对日灼抗性较弱的JZH枇杷果皮细胞中多种HSP含量显著上升,能够减少因高温强光胁迫造成的过多错误折叠的蛋白质;参与呼吸作用的蛋白含量增加,可以产生更多的能量以维持果皮细胞正常的生理活动;但是大部分与光合作用有关的蛋白质含量下降,说明其光合作用受到严重的抑制;清除ROS的酶系统中APX和PPO含量与PPO活性均下降,导致活性氧的增加,脂膜系统受到破坏。根据以上结果我们认为,提高枇杷果皮的抗日灼性,需要较高的清除ROS酶的含量和活性来清除过多的ROS,同时需要一定量的HSP以维持蛋白的正确折叠和正常功能,还需要保持正常的呼吸作用和光合作用以维持细胞物质和能量的正常供应。
[1]余筱洁, 金晓燕, 周存山, 等. 红肉和白肉枇杷果仁营养成分分析[J]. 浙江农林大学学报, 2011, 28(1): 149-152.
YU X J, JIN X Y, ZHOU C S,etal. Nutritional components for kernels of two loquat cultivars[J].JournalofZhejiangA&FUniversity, 2011, 28(1): 149-152.
[2]张婷婷, 令桢民, 赵旺生. 枇杷的研究现状和应用前景[J]. 农产品加工·学刊, 2006, 6(70): 50-52.
ZHANG T T, LING Z M, ZHAO W S. Investigation actuality and foreground of loquat[J].AcademicPeriodicalofFarmProductsProcessing, 2006, 6(70): 50-52.
[3]吴文毅. 福建枇杷产业现状、存在的问题及对策[D], 北京:中国农业大学, 2005.
[4]张建光, 刘玉芳, 孙建设, 等. 嘎拉苹果高温处理与果实日灼的关系[J]. 中国农业科学, 2003, 36(6): 731-734.
ZHANG J G, LIU Y F, SUN J S,etal. Acclimation of fruit to high temperatures in relation to sunburn in gala apples[J].ScientiaAgriculturaSinica, 2003, 36(6): 731-734.
[5]SCHRADER L E, KAHN C, ELFVING D C. Sunburn browning decreases at-harvest internal fruit quality of apples (MalusdomesticaBorkh.)[J].InternationanlJournalofFruitScience, 2009, 9(4): 425-437.
[6]WEERALLPDY P, JOBLING J, INFANTE M M V,etal. The effect of maturity, sunburn and the application of sunscreens on the internal and external qualities of pomegranate fruit grown in Australia[J].ScientiaHorticulturae, 2010, 124(1): 57-61.
[7]CHEN L S, LI P, CHENG L. Effects of high temperature coupled with high light on the balance between photooxidation and photoprotection in the sun-exposed peel of apple[J].Planta, 2008, 228: 745-756.
[8]王静璞, 李英丽, 张建光. 高温、强光胁迫对苹果果皮组织APX活性的影响[J]. 华北农学报, 2008, 23(6): 144-147.
WANG J P, LI Y L, ZHANG J G. Effect of high--temperature and excessive-light stress on APX activity in apple peel[J].ActaAgriculturaeBoreali-Sinica2008, 23(6): 144-147.
[9]万继锋, 李娟, 陈杰忠. 柑橘日灼病果皮抗氧化代谢的变化[J]. 园艺学报, 2012, 39(10): 2 009-2 014.
WAN J F, LI J, CHEN J Z. Changes in antioxidant metabolism in the fruit pericarps of citrus during sunburn development[J].ActaHorticulturaeSinica, 2012, 39(10): 2 009-2 014.
[10]王文举, 王振平. 外源抗氧化剂对高温胁迫下红地球葡萄果皮组织CAT、APX和SOD酶活性的影响[J]. 中外葡萄与葡萄酒, 2013, 3: 8-10.
WANG W J, WANG Z P. Effects of exogenous antioxidants on CAT, APX and SOD activity in Red Globe grape skin under high temperature stress[J].Sino-OverseasGrapevine&Wine, 2013, 3: 8-10.
[11]邓朝军, 蒋际谋, 龚慧文, 等. 2个枇杷品种果皮日灼伤害差异蛋白质组分析[J]. 福建农业学报, 2012, 27(12): 1 313-1 317.
DENG C J, JIANG J M, GONG H W,etal. Proteome analysis of loquat peel under sunburn in two varieties[J].FujianJournalofAgriculturalSciences, 2012, 27(12): 1 313-1 317.
[12]蒋际谋, 邓朝军, 林永祥, 等. 枇杷果皮响应高温强光胁迫的蛋白质组分析[J]. 热带亚热带植物学报, 2014, 22(4): 383-390.
JIANG J M, DENG C J, LIN Y X,etal. Proteomic analysis of loquat peels under high temperature and strong light stre-sses[J].JournalofTropicalandSubtropicalBotany, 2014, 22(4): 383-390.
[13]张志其, 曾小明, 白成刚, 等. 枇杷裂果与萎蔫、日灼的防止技术[J]. 柑桔与亚热带果树信息, 2004, 20(8): 32-34.
ZHANG Z Q, ZENG X M, BAI C G,etal. Control technologies for dehiscent fruit and wilting, sunburning of loquat[J].CitrusandSubtropicalFruitTreeInformation, 2004, 20(8): 32-34.
[14]邓朝军, 许奇志, 蒋际谋, 等. 高温胁迫对枇杷果皮热伤害的抗氧化特性影响[J]. 热带亚热带植物学报, 2012, 20(5): 439-444.
DENG C J, XU Q Z, JIANG J M,etal. Changes in antioxidant properties induced by heat injury in loquat peel under high temperature stressp[J].JournalofTropicalandSubtropicalBotany, 2012, 20(5): 439-444.
[15]邓朝军, 蒋际谋, 张小艳, 等. 枇杷果皮热伤害发生影响因子研究[J]. 福建农业学报, 2012, 27(10): 1 081-1 086.
DENG C J, JIANG J M, ZHANG X Y,etal. Research on influence factors in heat injury of loquat peel[J].FujianJournalofAgriculturalSciences, 2012, 27(10): 1 081-1 086.
[16]吴万兴, 鲁周民, 李文华, 等. 疏花疏果与套袋对枇杷果实生长与品质的影响[J]. 西北农林科技大学学报 (自然科学版), 2001, 32(11): 73-75.
WU W X, LU Z M, LI W H,etal. Effects of eliminating partial flowers and young fruits and bagging on growth and quality of loquat fruit[J].JournalofNorthwestA&FUniversity(Natural Science Edition), 2001, 32(11): 73-75.
[17]YOU X, WANG L, LIANG W,etal. Floral reversion mechanism in longan (DimocarpuslonganLour.) revealed by proteomic and anatomic analyses[J].JournalofProteomics, 2012, 75: 1 099-1 118.
[18]BRADFORD M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J].AnalyticalBiochemistry, 1976, 72: 248-254.
[19]WANG L, LIU X, LIANG M,etal. Proteomic analysis of salt-responsive proteins in the leaves of mangroveKandeliacandelduring short-term stress[J].PLoSOne, 2014, 9: e83141.
[20]商宏莉, 郭启高, 宋明, 等, 生姜四倍体抗热性与抗寒性的初步研究[J]. 西南农业大学学报, 2003, 25(3): 210-211, 233.
SHANG H L, GUO Q G, SONG M,etal. A preliminary study of heat- and cold-resistance of tetraploid ginger (Zingiberofficinale)[J].JournalofSouthwestAgriculturalUniversity, 2003, 25(3): 210-211, 233.
[21]李合生. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2000: 164-169.
[22]王学奎. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2006: 169-173.
[23]IBA K. Acclimative response to temperature stress in higher plants: approaches of gene engineering for temperature tole-rance[J].AnnualReviewofPlantBiology, 2002, 53(1): 225-245.
[24]CUI L, LI J, FAN Y,etal. High temperature effects on photosynthesis, PSII functionality and antioxidant activity of twoFestucaarundinaceacultivars with different heat susceptibility[J].BotanicalStudies, 2006, 47: 61-69.
[25]DAT J F, LOPEZ-DELGADO H, FOYER C H,etal. Para-llel changes in H2O2and catalase during thermotolerance induced by salicylic acid or heat acclimation in mustard seedlings[J].PlantPhysiology, 1998, 116(4): 1 351-1 357.
[26]FAYROBERT M, MIHR C, BERTIN N,etal. Major proteome variations associated with cherry tomato pericarp development and ripening[J].PlantPhysiology, 2007, 143(3): 1 327-1 346.
[27]李健, 张萌, 李丽萍, 等. 热处理对草莓品质与活性氧代谢影响的多变量解析[J]. 食品科学, 2013, 34(16): 306-310.
LI J, ZHANG M, LI L P,etal. Multivariate analysis of the effect of postharvest heat shock treatment on fruit quality and reactive oxygen species of strawberry during cold storage[J].FoodScience, 2013, 34(16): 306-310.
[28]杨宏伟, 陈小燕, 张影, 等. 油桃采后衰老与病害发生中品质与活性氧代谢相关性分析[J]. 食品科学, 2011, 32(20): 244-248.
YANG H W, CHEN X Y, ZHANG Y,etal. Analysis of the relationship between quality and active oxygen species meta-bolism in nectarine during postharvest ripening and pathogenesis[J].FoodScience, 2011, 32(20): 244-248.
[29]SCAFARO A P, HAYNES P A, ATWELL B J. Physiological and molecular changes inOryzameridionalisNg., a heat-tolerant species of wild rice[J].JournalofExperimentalBotany, 2010, 61(1): 191-202.
[30]SUNG D Y, KAPLAN F, GUY C L. Plant Hsp70 molecular chaperones: protein structure, gene family, expression and function[J].PhysiologiaPlantarum, 2001, 113(4): 443-451.
[31]MYOUGA F, MOTOHASHI R, KUROMOMORI T,etal. An Arabidopsis chloroplast-targetedHsp101 homologue,APG6, has an essential role in chloroplast development as well as heat-stress response[J].ThePlantJournal, 2006, 48(2): 249-260.
[32]STANNE T M, POJIDAEVA E, ANDERSSON F I,etal. Distinctive types of ATP-dependent Clp proteases in cyanobacteria[J].JournalofBiologicalChemistry, 2007, 282(19): 14 394-14 402.
[33]PATEL M, BERRY J O. Rubisco gene expression in C4plants[J].JournalofExperimentalBotany, 2008, 59(7): 1 625-1 634.
[34]陈根云, 肖元珍, 李立人. 影响豌豆Rubisco组装的因子及其作用机制[J]. 植物生理学报, 2001, 27(5): 369-374.
CHEN G Y, XIAO Y Z, LI L R. The factors affecting Rubisco assembly and the reaction mechanism in pea[J].ActaPhytophysiologicaSinica, 2001, 27(5): 369-374.
[35]YANG E J, OH Y A, LEE E S,etal. Oxygen-evolving enhancer protein 2 is phosphorylated by glycine-rich protein 3 wall-associated kinase 1 inArabidopsis[J].BiochemicalandBiophysicalResearchCommunications, 2003, 305(4): 862-868.
[36]YI X, MCCHARGUE M, LABORDE S,etal. The manganese-stabilizing protein is required for photosystem II assembly/stability and photoautotrophy in higher plants[J].JournalofBiologicalChemistry, 2005, 280(16): 16 170-16 174.
[37]KUMAR S, KAUR R, KAUR N,etal. Heat-stress induced inhibition in growth and chlorosis in mungbean (PhaseolusaureusRoxb.) is partly mitigated by ascorbic acid application and is related to reduction in oxidative stress[J].ActaPhy-siologiaePlantarum, 2011, 33(6): 2 091-2 101.
[38]刘琳琳, 席景会, 连杰, 等. 拟南芥和甜菜夜蛾相互作用的差异蛋白分析[J]. 高等学校化学学报, 2009, 30(9): 1 767-1 772.
LIU L L, XI J H, LIAN J,etal. Analysis of differential protein expression patterns on interaction betweenArabidopsisthalianaandSpodopteraexigua[J].ChemicalJournalofChineseUniversities, 2009, 30(9): 1 767-1 772.
[39]GLISOVIC T, BACHORIK J L, YONG J,etal. RNA-binding proteins and post-transcriptional gene regulation[J].FEBSLetters, 2008, 582(14): 1 977-1 986.
[40]THOMPSON J E, HOPKINS M T, TAYLOR C,etal. Regulation of senescence by eukaryotic translation initiation factor 5A: implications for plant growth and development[J].TrendsinPlantScience, 2004, 9(4): 174-179.
(编辑:裴阿卫)
Effect of Sunburn Stress on Pericarp Proteomics in Loquat Fruits
PAN Dezhuo1, DENG Chaojun2, LÜ Xiaojie1, SONG Xiaomin1, QIU Zhimin3,GONG Huiwen1, JIANG Jimou2, CHEN Wei1*
(1 College of Life Sciences, Fujian Agriculture and Forestry University, Fuzhou 350002, China; 2 Fruit Research Institute, Fujian Academy of Agricultural Sciences, Fuzhou 350013, China; 3 College of Forestry, Fujian Agriculture and Forestry University, Fuzhou 350002, China)
The objective of this work was to investigate the changes of differential expressed proteins in response to sunburn stress on loquat pericarp. The fruits of loquat cultivar ‘Jinzhong’ and ‘Honghouben’ sunburned for 90 min at 40 ℃ during color changing period were selected as experiment materials, among which the ‘Jinzhong’ loquat is poorer than ‘Honghouben’ at sunburn resistance. Total proteins in pericarp were separated using two-dimensional electrophoresis and differentially expressed proteins were identified using matrix-assisted laser desorption ionization time-of-flight/time-of-flight mass spectrometry (MALDI-TOF/TOF-MS). (1) Total 64 proteins were changed at least 2-fold differences in abundance, among which 56 proteins were successfully identified with 38 in ‘Jinzhong’ and 23 in ‘Honghouben’. (2) These identified proteins were involved in stress response and defense (accounting for 30.3%), photosynthesis(14.3%), respiration (25.0%), protein metabolism(14.3%)and some other physiological processes. (3) Compared to ‘Honghouben’, the abundance of many heat shock protein (HSP) was increased, and the abundance of proteins participating in respiration was also increased in order to generate more energy in ‘Jinzhong’. But the contents of many proteins related to photosynthesis as well as ascorbic acid peroxidase (APX) and polyphenol oxidase (PPO) removing reactive oxygen species (ROS) were all decreased, otherwise the activity of PPO was declined in ‘Jinzhong’. It is suggested that in order to enhance sunburn resistance in loquat, the content and activity of the enzymes removing ROS may be increased, the amount of HSP may need to some extent, and respiration and photosynthesis might be kept at the normal level.
Eriobotryajaponica(Thunb.) Lindl.; pericarp; sunburn; differential expressed proteins
1000-4025(2016)09-1801-12doi:10.7606/j.issn.1000-4025.2016.09.1801
2016-05-05;修改稿收到日期:2016-09-12
福建省自然科学基金(2014J01099);公益性行业(农业)科研专项经费(201003073)
潘德灼(1982-),男,在读博士研究生,主要从事植物生理与分子生物学研究。E-mail: pdz_006@163.com
陈伟,教授,博士生导师,主要从事植物生理与分子生物学研究。E-mail: weichen909@163.com
Q945.78; Q591.2
A

