动态固相微萃取-气相色谱法测定环境空气中挥发性脂肪酸的研究
孟 洁,王 亘,韩 萌,翟增秀,耿 静,鲁富蕾
(1.天津市环境保护科学研究院,国家环境保护恶臭污染控制重点实验室,天津 300191;2.天津迪兰奥特环保科技开发有限公司,天津 300191)
动态固相微萃取-气相色谱法测定环境空气中挥发性脂肪酸的研究
孟 洁1,2,王 亘1*,韩 萌1,翟增秀1,2,耿 静1,鲁富蕾1,2
(1.天津市环境保护科学研究院,国家环境保护恶臭污染控制重点实验室,天津 300191;2.天津迪兰奥特环保科技开发有限公司,天津 300191)
建立了动态固相微萃取-气相色谱(FID)测定环境空气中挥发性脂肪酸(VFAs)的分析方法,选择乙酸(AA)、丙酸(PA)、丁酸(BA)、异丁酸(iso-BA)、戊酸(VA)和异戊酸(iso-VA) 6种代表性VFAs为研究对象,研制了动态萃取装置并建立了动态萃取机制。研究了固相微萃取材料、萃取时间、萃取温度、萃取流速、解析温度及时间对VFAs萃取效率的影响,在此基础上优化了气相色谱法检测条件。在优化条件下,6种脂肪酸的线性范围均达到4个数量级,相关系数均大于0.990。方法的检出限(S/N=3)为1.0~4.7 μg/L,相对标准偏差(RSD,n=3)为1.1%~6.8%。与常规方法相比,该方法大大提高了检测范围和检测灵敏度,并成功用于环境空气中挥发性脂肪酸的分析检测。
挥发性脂肪酸;动态固相微萃取;气相色谱(GC);空气
恶臭污染作为一种扰民污染已成为公众身边比较突出的环境问题[1],引起恶臭污染的物质种类众多,其中对人生活环境影响较大的物质有氨、硫化氢、三甲胺、甲醛、苯乙烯、硫醇类等,其中还有一类重要的恶臭物质,即挥发性脂肪酸(Volatile fatty acids,VFAs)。VFAs是一类低碳数(C1~C5)、易挥发的有机酸,主要包括乙酸、丙酸、丁酸、戊酸及其同分异构体[2],这类物质具有强烈的刺激性气味,且随着分子量的增加,嗅觉阈值不断降低[3]。VFAs广泛存在于畜禽养殖场[4]、污水处理厂[5]、垃圾处理场[6]以及黑臭水体等与人们日常生活密切相关的污染源,虽然VFAs的气味对人体不会产生严重危害,但难闻的味道给人们的生活带来很大困扰。
VFAs的嗅阈值极低,在环境中该物质以很低的浓度存在(甚至达到ppt级)时,人们即可察觉,但在该浓度下,无法直接用仪器检测,需结合样品前处理技术[7-8]。目前我国常用的检测VFAs的前处理方法主要为碱性玻璃微珠富集法和溶液吸收法,即分别以涂覆碱性液体的玻璃微珠或碱性吸收液吸收样品气体后,使用气相色谱仪或离子色谱仪检测。其中碱性玻璃微珠法为日本提出的检测VFAs的标准方法,其检出限可达0.1~1 μg/L,但由于采样管需自制,重复性差[9];而溶液吸收法主要应用于工业废气,方法的检出限较高,无法满足环境中低浓度物质的检测要求[10]。 除上述两种前处理方法,环境中针对痕量VFAs检测的常用前处理方法还包括酯化法[11]、固体吸附剂采样管法[12]以及固相微萃取法[13]。酯化法的原理是将样品气体吸收到醇类物质中,使VFAs衍生为酯类物质,该方法有效增加了仪器的灵敏度,但VFAs无法完全转化成酯类物质,导致样品损失,使检测结果有偏差;采样管法[14]是通过填有多孔材料的吸附管富集样品气体,被分析物在高温条件下热解析后进行检测,该方法操作简便,应用较为广泛,但吸附管的装拆过程易导致仪器漏气,不利于操作;固相微萃取法是将样品气体通过涂覆有高表面积多孔材料的萃取纤维以达到预富集目的[15],将富集有目标分子的萃取纤维在气相色谱仪的进样口处热解析,该方法较碱性玻璃微珠法和采样管法操作更易于掌握,较酯化法可以避免样品流失,因而被国内外广泛应用于脂肪酸的检测,且具有很好的萃取效果和稳定性。然而,固相微萃取法目前主要应用于水中脂肪酸[16]以及大气中长链脂肪酸的检测[17],对环境空气中VFAs的检测研究较少。
本研究选择固相微萃取技术作为前处理方法,设计开发动态气体样品萃取装置,研究固相微萃取材料、萃取时间、萃取温度、萃取流速、解析温度及时间对VFAs萃取效率的影响,并对萃取条件进行优化。在此基础上通过优化气相色谱检测条件,建立了动态固相微萃取-气相色谱检测环境空气中VFAs的分析方法,从而填补了国内检测环境空气中挥发性脂肪酸方法研究的空白,为我国环境恶臭污染分析与评估提供了技术支持。
1 实验部分
1.1 仪器与试剂
7890A气相色谱仪(GC),配FID检测器和色谱柱HP-INNOWAX(30 m×0.25 mm×0.25 μm);固相微萃取装置(CORNING PC-420D),购于安捷伦科技有限公司;固相萃取纤维包括65 μm 聚二甲酯硅氧烷/二乙烯苯(PDMS/DVB)、75 μm碳分子筛/聚二甲基硅氧烷(CAR/PDMS)和85 μm聚丙烯(PA)购于北京康林科技有限责任公司;样品气体袋(规格3 L,大连德霖气体包装有限公司);恒流低流速采样泵(SKC 224-50,北京康林科技有限公司);动态稀释仪(4600A,北京博赛德科技有限公司)。
标准挥发性脂肪酸混合气体(1 μg/mL和20 μg/mL)购于大连大特气体有限公司,包括乙酸、丙酸、异丁酸、丁酸、异戊酸、戊酸和高纯氮气(平衡气);高纯氮气(纯度≥99.999%,空气化工产品(天津)有限公司)。
1.2 GC分析条件
载气为氮气(纯度≥99.999%),载气流速1.5 mL/min,不分流模式;进样口温度为280 ℃,检测器温度300 ℃,柱温使用程序升温,起始柱温为75 ℃,以10 ℃/min程序升温至180 ℃,保持3 min。
1.3 动态固相微萃取富集方法
将装有样品的气袋连接到固相微萃取采集室一端,使用恒流低流速采样泵抽取一定体积的样品气体,同时对萃取采集室加热,待一定的萃取时间后,将萃取纤维取出并转移至进样口处解析,通过气相色谱仪分析得到萃取后的VFAs谱图。
1.4 标准曲线
将标准VFAs气体(1 μg/mL和20 μg/mL)使用动态气体稀释仪按照一定稀释比例,用高纯氮气作为稀释气体,依次稀释得到8个浓度梯度,即0.005,0.010,0.050,0.100,1.000,5.000,10.00,20.00 μg/mL,建立方法标准曲线。
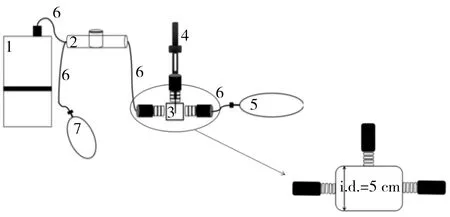
图1 动态固相微萃取装置示意图Fig.1 Sketch map of dynamic solid-phase microextraction device

图2 萃取时间对萃取效果的影响Fig.2 Effect of extraction time on extraction efficiencies of six VFAs
2 结果与讨论
2.1 动态固相微萃取装置
动态萃取实验装置结构如图1所示,该装置由7部分组成,分别为采样泵(1),流速控制器(2),萃取采集室(3),固相微萃取装置(4),采样袋(5),聚四氟乙烯连接管(6)和废气袋(7)。其中萃取采集室是整个实验装置的核心部分,使用玻璃作为采集室的主体材料,采集室形状呈类似T型三通,主体内径为5 cm,接头内径6 mm,左右接头使用连接管分别与流速控制器(2)和采样袋(5)相连,上接头与固相微萃取装置(4)相连。萃取纤维在使用前,需在290 ℃下老化1 h。取装有样品气体的样品袋与萃取采集室连接好,将恒流低速采样泵的流速通过流速控制器调节为100 mL/min,对萃取采集室的加热温度为80 ℃,萃取时间为20 min,将萃取后的萃取纤维转入气相色谱仪(GC)进样口,于280 ℃下解析1 min,萃取后的气体通过流速控制器后使用废弃袋回收。
萃取采集室的材料选择和内径尺寸会影响样品气体的分析结果。将浓度1 μg/mL、萃取体积2 L的标准VFAs混合气体使用内径尺寸相同但材料不同的萃取采集室进行比较,萃取采集室的材料选择常用的聚四氟乙烯材质和玻璃材质两类。结果表明,聚四氟乙烯材料制作的采集室对样品的吸附程度大,特别是异戊酸,使用该材料制作的萃取采集室的检测方法不能反映样品气体的实际含量,检测结果存在误差,因此选择玻璃材质制作萃取采集室,以降低对目标物的吸附作用,减少样品损失,提高检测准确性;以浓度1 μg/mL、萃取体积2 L的VFAs混合气体进行测试,进一步研究了不同内径尺寸(1,5,10 cm)的萃取采集室对萃取效果的影响。结果显示,1 cm和10 cm内径的采集室较5 cm内径的萃取效果较差,这是由于过大的内径不能使萃取纤维接触到所有的样品气体,而过小的内径不利于样品流通[19]。因此选择采集室的内径尺寸为5 cm,以确保目标分子能够被有效萃取。
2.2 萃取时间对萃取效果的影响
萃取时间对萃取效率有很大影响。一般情况下,萃取时间越长,萃取效率越高。为确定最佳的萃取时间,使用75 μm CAR/PDMS萃取纤维,对2 L的1 μg/mL VFAs分别萃取10,20,30,40,50,60 min。结果显示,随着萃取时间的增加,乙酸、丙酸、异丁酸、丁酸、异戊酸和戊酸的吸附峰面积增大(见图2)。其中,萃取纤维对具有支链结构的异丁酸和异戊酸的萃取效果最好,对直链酸的萃取效果较差,这主要是由于异丁酸和异戊酸的分子尺寸和空间位阻较大,较易被CAR/PDMS捕捉且不易穿透[20]。由于SPME技术可以基于平衡、未平衡和渗透[21],只要分析物的灵敏度足够用于定量分析,可以在非平衡状态下萃取,同时考虑样品的通量,因此选择萃取时间为20 min。
2.3 萃取温度对萃取效果的影响
在SPME过程中,通过加温,有利于气体分子扩散到萃取纤维,从而提高萃取效率。将2 L的 1μg/mL VFAs分别在20,40,60,80,100 ℃条件下进行萃取。结果显示,各待测物的萃取效率随着加热萃取采集室温度的升高而增大,其中异丁酸和异戊酸的萃取效果随时间的变化最明显,当萃取温度达到80 ℃后,各物质的萃取效率均较高,且继续升高温度时萃取效率增加不明显,因此选取80 ℃作为萃取温度。
2.4 气体流速对萃取效果的影响
通常情况下,增大气体流速能够提高萃取效率,这是因为萃取流速能够增大样品流通量和扩散速度,而另一方面,流量的增大也促使分析物未能及时富集而流失,不利于对分析物的萃取,并且流速对小分子气体化合物的影响较大[22]。在其他萃取条件一定的情况下,将2 L的 1 μg/mL VFAs分别在20,40,60,80,100,200 mL/min的流速下进行萃取。实验结果显示,当流速增至100 mL/min时,萃取效率达到最高值,因此选择100 mL/min作为后续实验的流速。
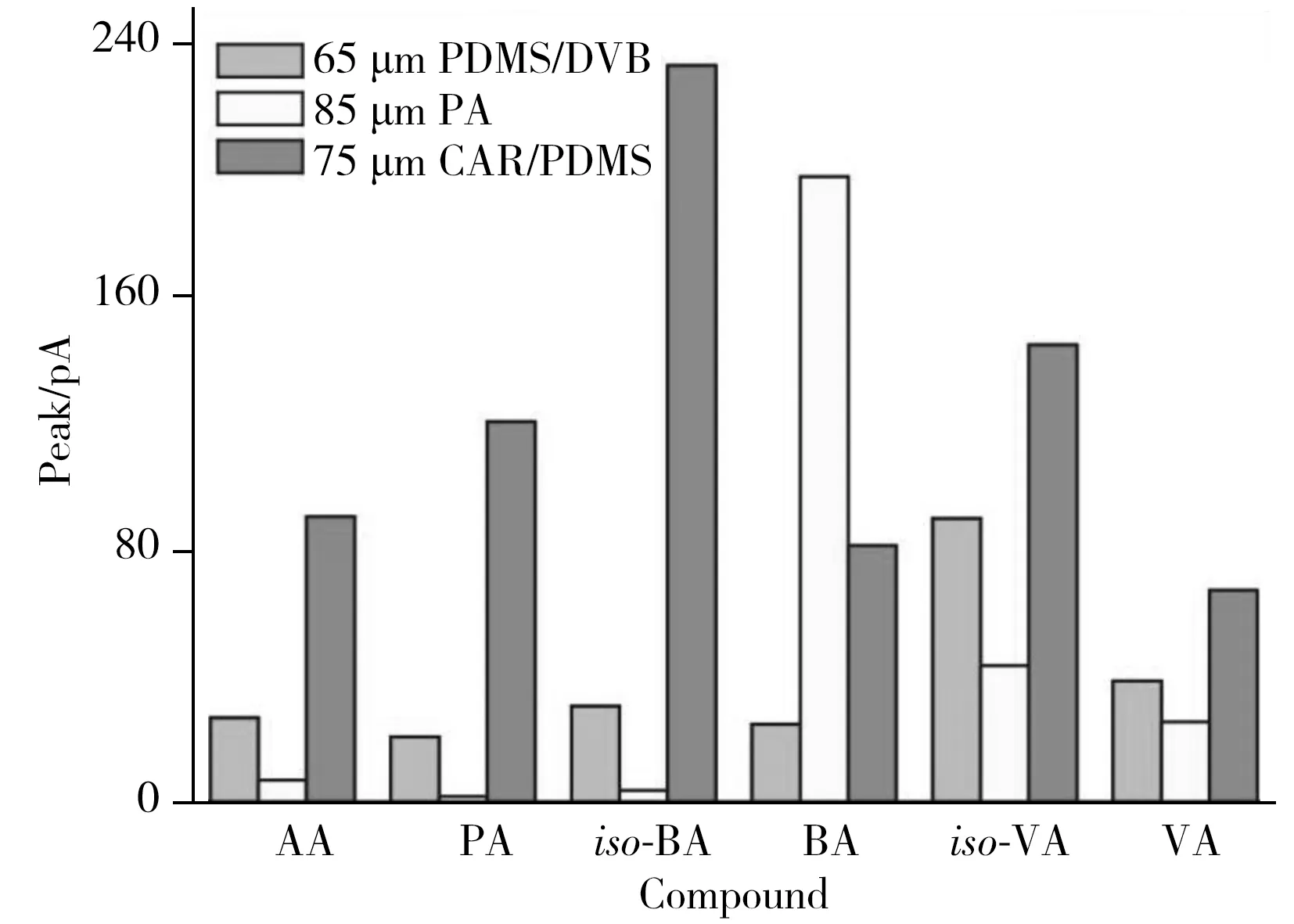
图3 萃取纤维类型对萃取效果的影响Fig.3 Effect of SPME fiber types on extraction efficiencies of six VFAs
2.5 萃取纤维对萃取效果的影响
为了直观说明不同萃取纤维对VFAs的萃取能力,选择适用于低分子量挥发性有机物的65 μm PDMS/DVB,75 μm CAR/PDMS和85 μm PA在相同萃取条件下对2 L的 1 μg/mL VFAs进行萃取,结果如图3所示,75 μm CAR/PDMS从整体上看表现出更强的萃取能力,其更适合萃取气体和小分子化合物[23]。因此,本实验选择75 μm CAR/PDMS作为萃取纤维。
2.6 解析温度与时间的影响
萃取过程完成后在气相色谱进样口进行热解析,因此解析温度和解析时间决定了分析物能否从萃取纤维上完全解析。为了考察解析温度的影响,将萃取后的 2 L 1 μg/mL的VFAs分别在250,280,300 ℃下进行解析。结果表明,在280 ℃下,解析时间1 min时,二次解析不再有分析物出现,说明在该条件下分析物已解析完全。因此,后续实验选择解析温度280 ℃,解析时间1 min。
2.7 分析特征量
在优化条件下,用动态固相微萃取-气相色谱法检测6种VFAs标准气体,分析特征量如表1所示。实验结果表明,75 μm CAR/PDMS萃取纤维对VFAs具有较强的萃取能力,富集倍数从7倍提高到115倍,大大提高了方法检测范围,有利于环境中痕量VFAs的检测。本方法的线性范围跨度4个数量级,检出限为1.0~4.7 μg/L,重复测定3次的相对标准偏差(RSD)为1.1%~6.8%。
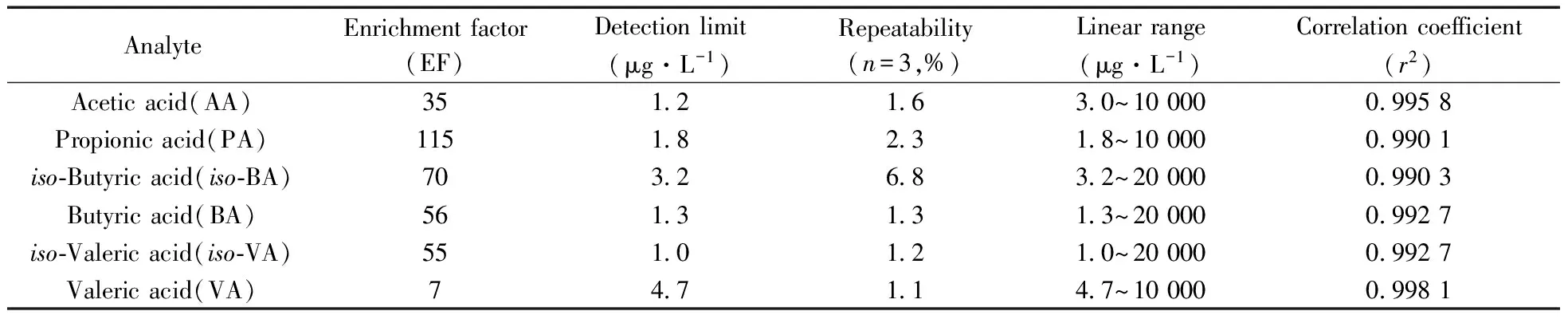
表1 动态固相微萃取-气相色谱法测定低级脂肪酸的分析特征量
2.8 实际样品的测定
选择香河某垃圾填埋场的厂界下风向、厂门口和作业区为采样点,采样点的位置、采样频次、采样器的放置以及采样记录等参照国家标准方法[24-25]的相关规定,采样仪器和采样步骤参照GB/T 14675-93[26]的相关规定。应用本方法对3个点位采集的样品进行测定,平行采集3次,结果如表2所示,表中结果由测定数据和偏差组成。其中作业区的VFAs均被检出,且检出量最高,达到0.056~4.615 μg/mL,感官上味觉比较刺激。厂界下风向和厂门口有5种挥发性脂肪酸被检出,其中厂界下风向值更高,并以异戊酸的浓度最高,可达0.123 μg/mL,其余3种物质的浓度在0.025~0.106 μg/mL之间。
表2 样品的分析结果
Table 2 Analytical result of sampleρ/(μg·mL-1)
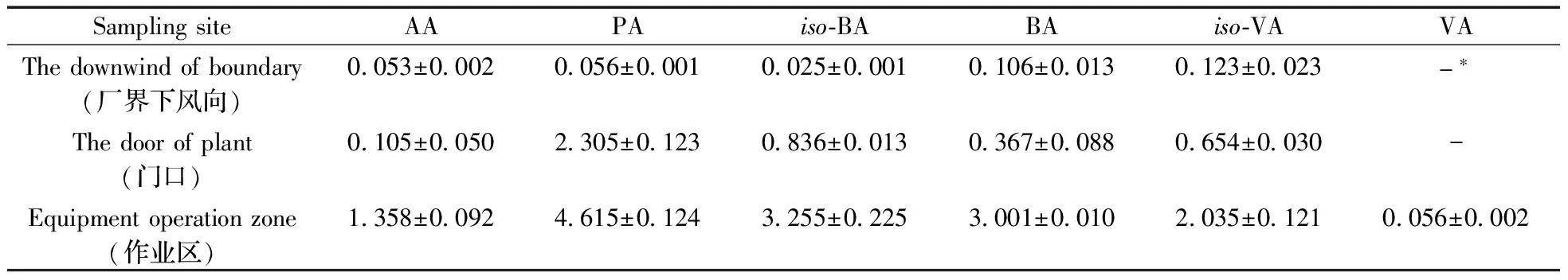
SamplingsiteAAPAiso⁃BABAiso⁃VAVAThedownwindofboundary(厂界下风向)0053±00020056±00010025±00010106±00130123±0023-∗Thedoorofplant(门口)0105±00502305±01230836±00130367±00880654±0030-Equipmentoperationzone(作业区)1358±00924615±01243255±02253001±00102035±01210056±0002
* no detected
3 结 论
本文以6种典型的挥发性脂肪酸为研究对象,研制了动态萃取装置并建立了动态固相微萃取-气相色谱(FID)测定环境空气中挥发性脂肪酸的分析方法,并用于实际样品的检测。该方法的检出限低,重现性好,线性范围可达4个数量级。与常规方法相比,本方法大大提高了检测范围和检测灵敏度,为建立环境空气中挥发性脂肪酸的标准检测方法提供了理论基础,为我国环境恶臭污染分析与评估提供了技术支持。
[1] Li W F.ShanghaiEnviron.Sci.(李伟芳.上海环境科学),2012,31(1):1-4.
[2] Parawira W,Murto M,Read J S,Mattiasson B.J.Chem.Technol.Biotechnol.,2004,79(7):673-677.
[3] Li Y,Mao R Y,Sun R S.TaboccoSci.Technol.(李云,毛若云,孙瑞申.烟草科技),1989,(3):27-30.
[4] Francesco F D,Lazzerini B,Marcelloni F,Pioggia G.Atmos.Environ.,2001,35(7):1225-1234.
[5] Tang X J,Wang B G,Zhao J D,Liu S L,He J,Feng Z C.Chin.Environ.Sci.,2011,31(4):576-583.
[6] Komilis D P,Ham R K,Park J K.WaterRes.,2004,38(7):1707-1714.
[7] Akdeniz N,Koziel J A,Ahn H K,Glanville T D,Crawford B P,Raman D R.J.Agric.FoodChem.,2009,57(13):5658-5664.
[8] Cai J A,Liu Z J,Yuan J W,Pan Y H,Ye Y J.J.Instrum.Anal.(蔡锦安,刘志健,袁嘉伟,潘永红,叶元坚.分析测试学报),2016,35(2):245-248.
[9] Jing Z Y,Yang R C,Han Q L,Zhao H,Yang J.Environ.Protect.Sci.(荆治严,杨瑞城,韩庆莉,赵虹,杨杰.环境保护科学),1987,3:69-74.
[10] Wu H X.NorthernEnviron.(吴红星,北方气体),2013,25(9):126-127.
[11] Metcalfe L D,Schmitz A A.Anal.Chem.,1961,33(3):363-364.
[12] Kim Y H,Kim K H.Anal.Chem.,2012,84(19):4126-4139.
[13] Meng Y J,Pino V,Anderson J L.Anal.Chem.,2009,81(16):7107-7112.
[14] Kim Y H,Kim K H.Anal.Chem.,2013,85(16):7818-7825.
[15] Zhong L L,Hu L,Guo L A,Lei S R,Mao J F,Li X,Ouyang H X.J.Instrum.Anal.(仲伶俐,胡莉,郭灵安,雷绍荣,毛建霏,李曦,欧阳华学.分析测试学报),2016,35(4):466-470.
[16] Feng L.Phys.Chem.Anal.Test:Chem.Anal.(冯琳.理化检验:化学分册),2011,41(1):86-89.
[17] Pinho O,Ferreira I M P L V O,Ferreira M A.Anal.Chem.,2002,74(20):5199-5204.
[18] Cui X Y,Gu Z Y,Jiang D Q,Li Y,Wang H F,Yan X P.Anal.Chem.,2009,81(23):9771-9777.
[19] Haberhauer-Troyer C,Rosenbery E,Grasserbauer M.J.Chromatogr.A,1999,848(1/2):305-315.
[20] Alaerts L,Maes M,Giebeler L,Jacobs P A,Martens J A,Denayer J F M,Kirschhock C E A,De Vos D E.J.Am.Chem.Soc.,2008,130(43):14170-14178.
[21] Pawliszyn J.Anal.Chem.,2003,75(11):2543-2558.
[22] Kim H,Nochetto C,McConnell L L.Anal.Chem.,2002,74(5):1054-1060.
[23] Yang Y C,Hui Y Q,He X B,Deng Y,Liu X H,Lin T.Phys.Chem.Anal.Test:Chem.Anal.(杨宇川,辉永庆,何小波,邓义,刘秀华,林涛.理化检验:化学分册),2008,44(9):904-908.
[24] HJ/T 55-2000.Technical Guidelines for Fugitive Emission Monitoring of Air Pollutants.National Standards of the People's Republic of China(大气污染物无组织排放技术导则.中华人民共和国环境标准).
[25] HJ/T 194-2005.Manual Methods Ambient Air Quality Monitoring.National Standards of the People's Republic of China(环境空气质量手工监测技术规范.中华人民共和国环境标准).
[26] GB/T 14675-93.Air Quality-Determination of Odor-Triangle Odor Bag Method.National Standards of the People's Republic of China(空气质量 恶臭的测定 三点比较式臭袋法.中华人民共和国国家标准).
Analysis of Six Volatile Fatty Acids in Air Using Dynamic Solid-phase Microextration-Gas Chromatography
MENG Jie1,2,WANG Gen1*,HAN Meng1,ZHAI Zeng-xiu1,2,GENG Jing1,LU Fu-lei1,2
(1.State Key Laboratory on Odor Pollution Control,Tianjin Academy of Environmental Sciences,Tianjin 300191,China;2.Environmental Science and Technology Development Co.,Ltd.in Tianjin,Tianjin 300191,China)
An analytical method for the detection of volatile fatty acids(VFAs) was established.Acetic acid(AA),propionic acid(PA),butyric acid(BA),iso-butyric acid(iso-BA),valeric acid(VA) andiso-valeric acid(iso-VA) were chosen as the target,and a dynamic solid-phase microextration(SPME) device was developed.The effects of extraction materials,extraction time,extraction temperature,extraction flow rate,extraction temperature and time of desorption were investigated on the efficiency of SPME extraction,and by which the optimal extraction conditions were determined.Furthermore,test conditions for gas chromatography were optimized,and a new dynamic SPME method was developed for gas chromatography ionization detection(GC-FID) to determine VFAs with the detection limits of 1.0-4.7 μg/L.The RSDs for three replicate extractions ranged from 1.1% to 6.8%,and the calibration curves were linear in the four orders of magnitude, with correlation coefficients(r2) more than 0.990.The developed method was successfully applied in the determination of trace VFAs in the environment.
volatile fatty acids;dynamic solid-phase microextration;gas chromatography(GC);air
2016-05-30;
2016-07-06
国家重大科学仪器设备开发专项(2012YQ060165)
10.3969/j.issn.1004-4957.2016.12.017
657.72;O625.323
A
1004-4957(2016)12-1611-05
*通讯作者:王 亘,硕士,高级工程师,研究方向:环境中恶臭物质分析检测方法的开发,Tel:022-87671322,E-mail:18622034260@163.com

