微粒作用观在有机化学教学中的运用
高修库 何彩霞 王春
摘要:文章阐述了微粒作用观的内涵及其教学价值,以“醇的化学性质”为例,从化学键的极性出发,分析了有机化学教学中如何借助微粒作用观深入分析有机物宏观性质产生的本质特征。
关键词:微粒作用观;键的极性;醇的化学性质
文章编号:1008-0546(2017)01-0008-03 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2017.01.002
对于《有机化学基础》的学习,学生普遍感到比较困难。难在什么地方呢?有机反应纷繁复杂,方程式记不住;虽然知道结构决定性质,但官能团到底如何决定有机物的性质,学生并不理解;认识到某种官能团可能具备这样的性质,但利用已有的共价键的知识从结构解释原因还是难,预测有机物的性质就更加盲目。笔者结合“醇的化学性质”的教学,想就微粒作用观在有机化学教学中的运用和大家讨论如下。
一、微粒作用观的内涵
中学化学教育的一个首要任务就是使学生能够建立物质的微粒性认识,能够从微观(分子、原子层次)的角度认识、理解一些自然现象及其变化的科学本质。物质的微粒性认识和微观角度的核心是理解微粒作用观,其基本要义是:(1)不同层次的微粒本身是有结构的,微粒结构就是内部微粒间作用的结果,如甲烷分子有一个碳原子和四个氢原子构成四面体型分子,中心碳原子通过4个sp3杂化轨道分别与四个氢原子形成极性共价键;(2)微粒之间存在着作用,如果是分子之间的相互作用就是分子间作用力 (包括氢键),如果是原子之间则是共价键;(3)物质变化的自然趋势是“强”作用代替“弱”作用,也就是朝着能量低、稳定性好的方向发展。
二、微粒作用观在有机化学教学中的教学价值
有机物绝大多数是共价化合物,分子间的相互作用为分子间作用力(包括氢键)。有机分子间的作用力实质就是微粒间的电性作用,有机物的分子一般极性较小或者没有极性,这就意味着有机分子间的作用弱,所以有机物的熔点一般较低。如果有机物分子间形成氢键,意味着分子间的作用变强,则沸点会升高,如醇的分子间可以产生氢键,使得醇的沸点比相对分子质量相近的烷烃高。总之,分子间的相互作用会影响有机物的部分物理性质,借助于微粒作用观可以解释有机物物理性质的变化规律。
有机物大多数以共价键结合,可以认为有机化学是研究共价键化合物的化学。有机反应的过程,就是旧共价键断裂、新共价键形成的过程。若有机物分子中某些共价键的键能较小,就是说原子间的作用较弱,那么当它与其他试剂作用时就容易断裂;或者说形成新的作用强,那么它就容易形成;这些都有助于有机反应的发生。
三、“醇的化学性质”对促进“微粒作用观”观念建构的分析
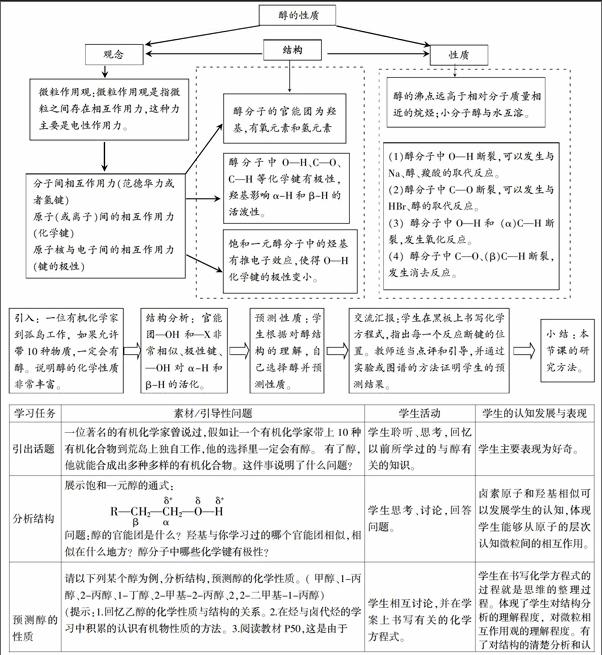
1. “醇的化学性质”所承载的化学观念
和烷烃的结构对比,在醇分子中,由于活泼非金属元素氧的存在,使得某些化学键的极性发生变化。醇分子中氧氢键、碳氧键及α-C上的碳氢键、β-C上的碳氢键均为极性键。在有机反应中,由于微粒之间的相互碰撞,极性键就容易断开。结合醇与活泼金属的置换反应、与氢溴酸的取代反应、浓硫酸存在时的消去反应和与氧气的催化氧化反应,可以很好地印证极性键在有机反应中容易断裂的结论。
2. 教学知识结构图
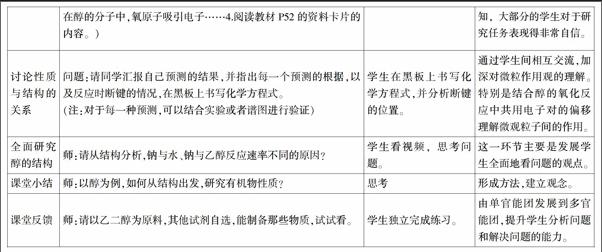
3. 教学实施活动
(1)教学思路及教学结构图
对于醇的化学性质的教学,它的起点是必修2乙醇的部分性质。选修5重点学习醇类物质的性质,或者说是基于官能团的学习。关于有机物化学性质的学习,学生已经积累了一些经验,也形成了一套有效的学习方法。所以本节课设计了开放性问题,让学生自己研究醇的性质,研究的基础是对饱和一元醇的分子结构进行充分的分析,基于极性键在化学反应中容易断裂展开,最后讨论交流,教师展示实验进行验证的教学思路。
(2)主要教学活动设计与实施
(3)醇的化学性质教学效果测查与分析
首先,这种授课的方式——“基于观念建构的化学教学”使学生能够接受,学生愿意学到一种方法而不是某一个具体的知识点。本节课的基本观点是从结构推测性质,学生可以理解。有机化学的核心思想就是结构决定性质,通过本节课的教学,学生普遍感到这一学科思想更加清晰。但是,分析到键断裂时到底发生取代反应还是氧化反应,学生拿不准;发生取代反应时,到底是取代氢原子还是取代羟基,学生也不明白。所以,有机化学的教学,从结构的视角分析问题是可以的,但是老师适当的引导也是必需的,而不能完全放开让学生自学,否则学生还会臆造出“古怪”的化学方程式。
有机化学反应的机理非常复杂,中学教学的一个基本要求就是复杂问题简单化。极性键在有机反应中容易断裂,极性越大越容易断裂,这一点是符合科学实际,也能够为中学生接受。但是,断键之后发生什么类型反应,还要结合反应物、反应条件、生成物等多方面考虑。如乙醇与浓硫酸混合,如果是分子内脱水,形成了不饱和键,则为消去反应;如果分子之间脫水生成乙醚,则为取代反应。还有,乙醇与氢溴酸发生取代反应时,学生容易写出用溴原子取代羟基氢的反应,那就要考虑取代基团之间化合价相等,同时电性也要相同,这样才可以取代的基本原则了。
四、微粒作用观在有机化学教学中运用的几点启示
1. 有机化学中的微粒作用观要特别关注基团间的相互影响
有机化学中微粒作用观的层次有分子间的作用力、原子间的共价键,还有基团(原子团)之间的相互作用。对于中学生来说,基团之间的相互作用是难点。水分子、乙醇分子、苯酚、乙酸分子中均有官能团羟基,但是这四种分子中羟基氢的活泼性却不同。乙醇分子中由于乙基的推电子效应导致—O—H键极性变弱而比水难电离;而苯酚分子中由于p-π共轭效应导致—O—H键极性变强而易于电离显酸性;在乙酸分子中,由于羰基的吸电子效应,使得与羰基相连的—O—H键极性变强,易于电离显酸性。如果学生除了体会到分子间作用力、化学键外,还能体会到基团之间的作用,这样才能说微粒作用观的建构是较为成功的。
2. 在有机教学中引入微粒作用观的时机要符合学生的实际
化学观念的建构不能一蹴而就,不能急于求成。任何一个化学观念都是蕴含于具体的化学知识当中并借助于它们表达出来,学生需要对化学知识的深刻理解和反思应用,才能形成化学观念。在烷烃的取代反应中,其实就是极性键断裂,但是不建议从微粒作用观的角度进行理解。烯烃中碳碳双键的加成反应,也是由于π键的电子云重叠的面积小,作用弱而易于断裂,但是仍然是让学生感受,而到炔烃的性质时,学生有了积累,慢慢就可以悟出其中蕴含的微粒作用观,到了芳香烃的教学中,还可以发展微粒作用观,引出基团间的相互作用。
3. 微粒作用观是有机化学中宏观和微观转化的桥梁
《有机化学基础》的核心内容是组成、结构、性质、制备和应用。组成和结构是基础,是性质和变化的根本原因;性质和变化是表象,是组成和结构的体现;性质还决定了有机物的制备和应用。“结构决定性质”是有机化学的核心思想,掌握通过结构预测性质,通过性质判断结构的方法,对于有机化学的学习至关重要。而要知道结构如何决定性质,就必须理解微粒作用观,要从结构科学地预测性质,减少预测的盲目性也必须用好微粒作用观。透过宏观现象看到的微观本质就是微粒作用观。
致谢:感谢2014年北京市级学科带头人及骨干教师高级研修“化学观念教学研究”工作室全体老师对醇的化学性质教学设计和本文悉心指导。
参考文献
[1] 梁永平.微粒作用观的科学价值及其科学建构[J].化学教育,2003(6)
[2] 何彩霞.关注学生认知发展的化学教学——以“乙醇”为例[J].化学教学,2013(12):29~31
[3] 王笃年,何彩霞.基于实验支持的“有机物分子内基团间作用观”教学研究[J].实验教学研究,2011(12)
[4] 曾国琼,将化学观念的培养融入到《有机化学基础》的教学中[J].中学化学教学参考,2013(10)

