超声波辅助绿茶提取物的制备及多壁碳纳米管/绿茶提取物复合体系分散性能研究
他雪峰,许 军
(中国民航大学理学院 天津 300300)
超声波辅助绿茶提取物的制备及多壁碳纳米管/绿茶提取物复合体系分散性能研究
他雪峰,许 军
(中国民航大学理学院 天津 300300)
以干燥绿茶粉末为原料,食用酒精溶液为萃取液,采用超声波辅助提取制备绿茶提取物。控制萃取液浓度、固/液比及超声萃取时间,研究提取工艺,用紫外可见分光光度计对提取物中的茶多酚含量进行分析。结果表明,食用酒精溶液浓度为70%、固液比为1∶12、45℃下超声萃取60min,提取物产率和茶多酚含量最高,分别达到42.22%和22.49%。将多壁碳纳米管(MWNTs)分散到绿茶提取物水溶液中时,茶多酚的苯环与MWNTs产生π-π共轭效应并吸附在MWNTs表面,茶多酚的羟基伸向水相,使MWNTs均匀分散在水中。
绿茶提取物;超声波;茶多酚;碳纳米管
茶叶提取技术是将茶叶中的有效成分提取出来,茶叶提取物包括茶多酚、茶多糖、咖啡碱、茶黄素、茶氨酸等[1]。茶多酚(Tea Polyphenols,TP)占茶叶干质量的18%~36%,是茶叶中与亚铁离子反应的酚类化合物的总称,它是茶叶中具有活性的多种化合物的混合物,其中儿茶素含量最高占茶多酚的80%左右。儿茶素主要包括表没食子儿茶素没食子酸酯(EGCG)、表没食子儿茶素(EGC)、表儿茶素没食子酸酯(ECG)、表儿茶素(EC)等[2]。茶多酚对机体活性氧自由基和脂类自由基有清除作用,具有抗畸变、抗遗传毒性、降血糖、抑制肿瘤发生和防治神经退行性疾病等功效,广泛应用在油脂、食品、医药、化妆品及饮料等领域[3]。茶叶提取技术和提取物应用研究备受国内外学者关注。茶叶提取方法主要有树脂吸附分离法、有机溶剂萃取法、膜渗透分离法、超临界萃取法、超声波辅助提取法等[4]。其中超声波辅助提取法利用超声波产生空化、振动、加速、乳化、扩散、击碎和搅拌作用增加溶剂穿透能力,加速细胞内物质释放、扩散及溶解,促进提取过程的进行[5],具有提取温度低、氧化损耗小、不改变提取物性状和有效成分结构、提取效率高等特点[6-8]。
碳纳米管(CNTs)是石墨片形成的中空碳笼管,具有独特的导电、导热和电磁特性,具备优异的热稳定性、耐腐蚀性及轻质性。其中多壁碳纳米管(MWNTs)生产成本低,管径和长度可在较宽范围内选择,基于MWNTs的先进复合材料有望满足产业化要求。CNTs具有大比表面积和长径比,表面缺少活性基团,导致CNTs易聚集并相互缠结,当它与其它物质复合时,其优异性能难以发挥[9],对CNTs进行表面修饰使其均匀分散成为研究重点。超声波或高速剪切等机械分散法,操作简单但会使CNTs断裂,长径比下降,进而导致其性能下降[10-11]。共价键化学修饰法把特定官能团或聚合物通过化学反应接枝到CNTs表面,可促进CNTs分散并增强与基体的界面结合,但破坏了CNTs的表面结构也降低了它的性能[12-13]。非共价键化学修饰法是指CNTs侧壁由石墨片层结构组成,其碳原子sp2杂化形成高度离域π电子,这些π电子和含有π电子的其他化合物可通过π-π共轭作用相结合,将化合物以非共价键形式包覆在CNTs表面,这样在既带有活性基团、表面结构又不被破坏的情况下,CNTs可从团簇中分散到溶剂中去[14-15]。
茶多酚中存在邻苯三酚和儿茶酚基团,具有良好的水溶性和还原性。大量苯环结构中的π电子可与CNTs或石墨烯片层的sp2杂化碳原子形成π-π共轭体系,茶叶提取物在CNTs分散及制备水溶性CNTs方面存在潜力。如Nakamura等[16]报道了绿茶水可以将 MWNTs分散溶解在水中。Wang Yan等[17]用茶多酚还原氧化石墨并获得水溶性导电石墨烯。
本研究以干燥绿茶粉末为原料,食用酒精溶液为萃取液,采用超声波辅助提取法制备绿茶提取物。用紫外可见分光光度计对茶多酚含量进行分析,通过改变萃取液浓度、固/液比及超声时间,研究工艺参数对提取物产率和茶多酚含量的影响。采用傅利叶变换红外光谱(FTIR)、扫描电子显微镜(SEM)对MWNTs/绿茶提取物复合体系的结构、形貌进行研究。将MWNTs分散到绿茶提取物水溶液中时,茶多酚的苯环与MWNTs产生π-π共轭效应并吸附在MWNTs表面,使MWNTs均匀分散在水中。
1 实验部分
1.1 超声辅助绿茶提取物的制备及茶多酚含量测定
将市售绿茶于45℃干燥12h后置于F-80高速粉碎机中粉碎至0.175mm。准确称取5.00g干燥绿茶粉末加入100mL圆底烧瓶中,加入食用酒精水溶液后置于KQ3200DB数控超声波清洗器中,在45℃下超声波辅助提取,超声功率150W。提取结束后将提取液置于800离心机中离心5min,转速4000 r·min-1。分离后的上层黄绿色透明溶液为提取物与食用酒精溶液的混合物,下层为绿茶残渣,取清液弃残渣。将提取液中的大部分食用酒精通过减压蒸馏回收,剩余的高浓度提取液倒入表面皿中于80℃真空干燥2h得到绿茶提取物。改变食用酒精浓度、固/液比(即绿茶粉末质量与食用酒精溶液体积之比)和超声萃取时间,得到不同工艺参数条件下的绿茶提取物样品,进行产率计算和茶多酚含量分析。提取物质量占所用干燥绿茶粉末质量的百分比为提取物产率。
茶多酚含量测定根据国标GB/T 8313-2002,采用WGZ-8双光束紫外-可见分光光度计进行测定。将实验制得的各绿茶提取物样品取其质量的1/10,用25mL质量分数为70%的食用酒精溶液溶解制成提取液。称取硫酸亚铁1.000g和酒石酸钾钠5.000g加入1L容量瓶中,用蒸馏水溶解并定容得到酒石酸亚铁溶液。准确称取磷酸氢二钠23.877g和磷酸二氢钾9.078g分别置于1L容量瓶中,用蒸馏水溶解并定容,分别取磷酸氢二钠溶液85mL和磷酸二氢钾溶液15mL置于100mL容量瓶中,混合均匀即得pH=7.5的磷酸盐缓冲液。量取1mL提取液、4mL水、5mL酒石酸铁四水合物溶液和15mL缓冲液混合后倒入25mL容量瓶,以试剂空白溶液作参比,用10mm比色皿于540 nm处测定吸光度,计算茶多酚含量,其计算公式如式(1)所示:
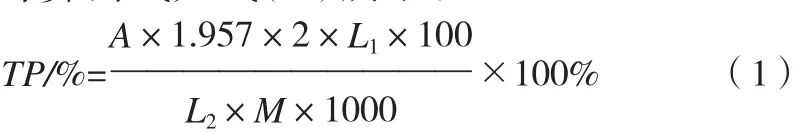
式中,A为试样吸光度;L1为试液量,25mL;L2为测定时用液量,1mL;M为干燥茶叶粉末质量,500 mg;1.957为用10mm比色皿比色时吸光度等于0.50时每mL茶汤中TP含量,mg。
1.2 MWNTs/绿茶提取物复合体系的制备与表征
取10mg绿茶提取物溶解在10mL水中后加入10mg的MWNTs超声分散5min,得到MWNTs/绿茶提取物复合体系悬浮液。取少量MWNTs、绿茶提取物、MWNTs/绿茶提取物复合体系悬浮液真空干燥后经KBr研磨压片,用Nicolet Avata 330傅立叶变换红外光谱仪(FTIR)测量红外光谱。取少量MWNTs和MWNTs/绿茶提取物复合体系悬浮液置于盖玻片上干燥后喷金,用FEI Nano SEM 430场发射扫描电镜(SEM)观察并拍照。
2 结果与讨论
2.1 绿茶提取物的产率与茶多酚含量
干燥的绿茶粉末5g在45℃下制备提取物时,改变食用酒精溶液浓度、固/液比和超声萃取时间得到不同工艺参数条件下的提取物样品,各提取物样品的产率和茶多酚含量如表1和图1所示。
从表1和图1实验数据看出,干燥绿茶粉末5g在45℃下用60mL浓度为70%的食用酒精溶液溶解、固液比为1∶12、超声萃取60min后,绿茶提取物的产率最高,达到42.22%,同时在此工艺条件下茶多酚含量最高,达到22.49%。
2.2 红外光谱分析
MWNTs、绿茶提取物、MWNTs/绿茶提取物复合体系的FTIR光谱如图2所示。从图2看出,在MWNTs的FTIR谱图中,1400cm-1处的峰是声子模式振动引起的,这是MWNTs红外光谱特征峰[18]。在绿茶提取物的FTIR谱图中,3387cm-1处的峰对应提取物中茶多酚的C-OH键伸缩振动,1036cm-1处的峰对应茶多酚的C-O键伸缩振动,1607cm-1处的峰对应茶多酚的C=C键伸缩振动[19]。在MWNTs/绿茶提取物复合体系的FTIR光谱中,1370cm-1和1597cm-1处的峰分别对应MWNTs声子振动和茶多酚C=C键的特征吸收。由于茶多酚的苯环与MWNTs发生了π-π共轭效应共轭,使MWNTs和绿茶提取物的特征峰发生了红移[20]。

表1 不同工艺参数条件下绿茶提取物产率和茶多酚含量Tab. 1 Yield of green tea extract and tea polyphenol content with different process parameters

图1 不同工艺参数条件下绿茶提取物的产率(a)和茶多酚含量(b)Fig. 1 Yield of green tea extract (a) and tea polyphenol content (b) with different process parameters

图2 MWNTs(a)、绿茶提取物(b)和MWNTs/绿茶提取物复合体系(c)的FTIR光谱Fig. 2 FTIR spectra of MWNTs (a), green tea extract (b) and MWNTs/green tea extract composite system (c)
2.3 MWNTs/绿茶提取物复合体系的溶解分散稳定性
MWNTs分散在水中、绿茶提取物水溶液、MWNTs/绿茶提取物复合体系悬浮液常温下静置24h后的数码照片如图3所示。从图3(a)看出,MWNTs分散在水中静置24h后沉淀到底部,说明MWNTs在水中不稳,容易发生沉淀。从图3(b)看出,绿茶提取物溶解在水中静置24h后没有沉淀发生,说明绿茶提取物能在水中溶解并保持稳定。从图3(c)看出,将MWNTs分散在绿茶提取物水溶液中形成MWNTs/绿茶提取物复合体系的悬浮液,静置24h后没有沉淀发生,说明借助与绿茶提取物间的复合效应,MWNTs能均匀地分散在悬浮液中并保持稳定。产生这一现象的原因在于:绿茶提取物中含有茶多酚结构(图4),茶多酚中的苯环与MWNTs形成π-π共轭效应,使其被吸附在MWNTs表面,同时茶多酚的羟基伸向水相,阻止了MWNTs之间的聚集,同时使MWNTs稳定地分散在水中[19]。

图3 MWNTs分散在水中(a)茶叶提取物溶解在水中(b)和MWNTs/绿茶提取物复合体系悬浮液(c)常温下静置24小时后的数码照片Fig. 3 DC photos of MWNTs in water (a), green tea extract dissloved in water (b) and MWNTs/green tea extract composite system suspension (c)

图4 茶多酚的结构图Fig. 4 Chemical structure of tea polyphenol
为进一步说明MWNTs在MWNTs/绿茶提取物复合体系悬浮液中的分散状态,MWNTs和MWNTs/绿茶提取物复合体系悬浮液干燥后的SEM照片如图5所示。从图5(a)看出,原始MWNTs相互缠结并聚集在一起。当MWNT s加入到绿茶提取物的水溶液中后,由于π-π共轭效应,提取物中的茶多酚被吸附在MWNTs表面,从而阻止MWNTs之间的聚集,使MWNTs发生了解缠结并且碳管彼此之间分散开,如图5(b)所示。
3 结论

图5 MWNTs(a)和MWNTs/绿茶提取物复合体系(b)的SEM照片Fig.5 SEM images of MWNTs (a), MWNTs/green tea extract composite system (b)
以干燥绿茶粉末为原料,食用酒精溶液为萃取液,采用超声波辅助提取法制备了绿茶提取物。通过改变食用酒精溶液浓度、固液比及超声萃取时间,研究了绿茶提取工艺,用紫外分光光度法对茶多酚含量进行分析。研究结果表明,食用酒精溶液浓度为70%、固液比为1∶12、45℃下超声萃取60min时,提取物产率和茶多酚含量最高,分别达到42.22%和22.49%。将MWNTs加入到提取物的水溶液中时,茶叶提取物的苯环与MWNTs之间通过π-π共轭效应,吸附在MWNTs表面,提取物的羟基伸向水相,使MWNTS均匀稳定地分散在水中。
[1] 施玲,陈惠衡,李适.不同绿茶原料对茶叶提取物品质的影响[J].湖南农业大学学报(自然科学版),2008,34(2):229-231.
[2] 宋传奎,肖斌,王艳丽,李瑞,宋红霞.超声波辅助提取茶多酚工艺条件的优化[J].西北农林科技大学学报(自然科学版),2011,39(5):133-146.
[3] KHAN N, MUKHTAR H. Tea polyphenols for health promotion[J]. Life Sciences, 2007, 81: 519.
[4] 戴群晶.用茶末及废茶枝叶提取高纯茶多酚的研究[J].现代食品科技,2007,22(1):45-47.
[5] 严伟,李淑芬,田松江.超声波协助提取技术[J].化工进展,2002,21(9):649-651.
[6] 郭树琴,吴胜举,牛春玲,等.超声提取绿茶茶多酚研究[J].陕西师范大学学报(自然科学版),2009,36(1):36-38.
[7] 陆爱霞,姚开,贾冬英,等.超声辅助法提取茶多酚和儿茶素的研究[J].中国油脂,2005,30(5):48-50.
[8] 肖文军,唐和平,龚志华,等.茶叶超声波辅助浸提研究[J].茶叶科学,2006,26(1):54-58.
[9] TASIS D,TAGMATARCHIS N, BIANCO A,et al. Chemistry of carbon nanotubes[J]. Chemical Reviews, 2006, 106: 1105-1136.
[10] PENG B, LOCASCIO M, ZAPOL P, Li S,MIELKE S L,SCHATZ G C, et al. Measurements of near-ultimate strength for multiwalled carbon nanotubes and irradiationinduced crosslinking improvements [J]. Nature Nano technol, 2008(3): 626-631.
[11] YI W, MALKOVSHIY A, CHU Q, SOKOLOV A P, COLON M L, MEADOR M, et al. Wrapping of single-walled carbon nanotubes by a π-controlled size selectivity.[J] Journal of Physical Chemistry B, 2008, 39: 12263-12269.
[12] SINGH P, CAMPIDELLI S, GIORDANI S, BONIFAZI D, BIANCO A, PRATO M. Organic functionalization and characterization of single-walled carbon nanotubes [J]. Chemical Society reviews, 2009, 38: 2214-2230.
[13] ZDENKO S, DIMITRIOS T, KONSTANTINOS P, COSTAS G. Carbon nanotube-polymer composites: chemistry, processing, mechanical and electrical properties[J]. Progress in Polymer Science, 2010, 35: 357-401.
[14] AZMI M, ARGO K A, SURIANI A B, TRETYA A, WAN M W. Z, SOFIAN I, MASANOBU S, PAUL B, JULIAN E. Enhanced dispersion of multiwall carbon nanotubes in natural rubber latex nanocomposites by surfactants bearing phenyl groups [J]. Journal of Colloid and Interface Science, 2015, 455: 179-187.
[15] LINGLING L, WENJUN H, JUN S, JIANJUN W, CHUANXIANG Q, LIXING D. Preparation of poly (vinyl alcohol)fibers strengthened by multi-walled carbon nanotubes functionalized with tea polyphenols [J]. Journal of Materials Science, 2014, 49: 3322-3330.
[16] NAKAMURA G, NARIMATSU K, NIIDOME Y, NAKASHIMA N. Green tea solution individually solubilizes single-walled carbon nanotubes [J].Chemistry Letters, 2007, 36: 1140-1141.
[17] YAN W, ZIXING S, JIE Y. Facile synthesis of soluble graphene via a green reduction of graphene oxide in tea solution and its biocomposites[J]. ACS Applied Materials & Interfaces, 2011(3): 1127-1133.
[18] TUNG T T, YEON J H, et al. Synthesis and characterization of the carbon nanotube-based composite with poly(3,4-ethylenedioxythiophene)[J]. Synthetic Metals, 2010, 160: 1266-1272.
[19] MOHD N M Z, AHMAD B, SALIM N K,MISNI M, RUSHDAN I, AHMAD A, RAD S. Exploration of the environmentally benign and highly effective approach for improving carbon nanotube homogeneity in aqueous system[J]. Journal of Thermal Analysis and Calorimetry, 2016, 124: 815-825.
[20] XU J, LI J G, WU Y, BAI S. Preparation and characterization of water soluble and conducting poly(sodium 4-styrenesulfonate)doped poly(3,4-ethylenedioxythiophene)/multi-walled carbon nanotubes coreshell nanocomposites by in situ polymerization[J]. Journal of Materials Science:Materials in Electronics, 2014, 25(7): 3233-3241.
Preparation of Green Tea Extract Assisted by Ultrasonic Wave and Dispersion of Multi-walled Carbon Nanotubes/Green Tea Extract Composite System
TA Xuefeng, XU Jun
(College of Science, Civil Aviation University of China, Tianjin 300300, China)
Green tea extract was obtained by ultrasonic assisted extraction, in which edible alcohol solution was used as extract liquid and dried green tea powder as raw materials. Extracting process of green tea extract was studied by using different edible alcohol concentration, ratio of solid to liquid and ultrasonic extraction time. Contents of tea polyphenol in the green tea extract were determined by UV-Vis spectrophotometer. The results showed that when temperature was 45℃, concentration of edible alcohol was 70%, ratio of solid to liquid was 1:12 and ultrasonic extraction time was 60min,the most yield of green tea extract and content of tea polyphenol were obtained, and reached 42.22% and 22.49%, respectively. When multi-walled carbon nanotubes (MWNTs) were dispersed in the tea extract water solution, phenylring moieties of tea polyphenol were adsorbed on the surfaces of MWNTs via π-π conjugated interaction and hydroxy groups of tea polyphenol were exposed to water phase. As a result, MWNTs dispersed homogeneously in water.
green tea extract; ultrasonic wave; tea polyphenols; caffeine; multi-walled carbon nanotubes
TB 553;TS 272.5+1
A
1671-9905(2017)02-0009-05
大学生创新创业资助项目(IECAUC2016011)
许军(1972-),男,天津河西人,中国民航大学理学院材料化学专业副教授,博士,主要从事材料化学及纳米复合材料研究
2016-12-20

