砷滤饼的铜砷分离
沈 忱,闵小波, , 3,史美清,周波生,赵宗文,李辕成,张 纯
砷滤饼的铜砷分离
沈 忱1,闵小波1, 2, 3,史美清2,周波生1,赵宗文1,李辕成1,张 纯1
(1. 中南大学冶金与环境学院,长沙410083;2. 中南大学国家重金属污染防治工程技术研究中心,长沙410083;3. 中南大学湖南省战略金属矿产资源清洁高效利用协同创新中心,长沙410083)
采用浸出方法使砷滤饼中的铜砷元素进行分离,铜以硫化铜的形式沉淀,砷以砷酸根离子进入溶液中。考察NaCl浓度、Na2S添加量、液固比、时间及温度等因素对砷滤饼中砷、铜浸出率的影响。得出最优的工艺条件如下:NaCl溶液浓度为20g/L、液固比7:1、Na2S与砷滤饼质量比3:4、浸出时间4 h、温度80 ℃、H2O220 mL。在此最优工艺条件下,砷浸出率高达95.56%,铜浸出率低于0.5%,浸出渣铜含量富集至33.6%。浸出液采用硫酸亚铁沉砷方法,沉砷率可以达到98%,生成的砷酸铁晶体含砷量为32.15%,滤液含砷量为0.23g/L,滤液可以返回浸出过程,实现循环利用。
砷滤饼;铜;砷;分离;浸出;脱砷
砷是一种对人体及其他生物体有毒害作用的致癌物质,砷在有色金属的提取过程中常常以硫化物或盐的状态不同程度地进入烟气、废水和废渣中[1],除个别厂以As2O3的形式回收少量砷外,大部分厂家因找不到合适的处理方法,而将大量的含砷废弃物堆存或以“三废”形式排放[2],这些含砷废弃物构成了我国有色冶金企业最主要的环境污染源,对企业的周边环境造成了很恶劣的影响[3]。
闪速炼铜产生的烟气送入硫酸系统用水吸收其中的砷等有害元素得到污酸原液,经硫化处理产生砷滤饼。经过调研,国内铜冶炼厂的砷滤饼年产量在2000~4000 t,而大部分冶炼企业对砷滤饼采取堆存的方式,对环境造成了极大的威胁。
由于火法处理砷滤饼的方法脱砷不彻底,工艺复杂且易造成砷的二次污染,所以大部分冶炼企业倾向选择湿法浸出的方法处理砷滤饼[4]。以NaOH或Na2S为浸出溶液的砷滤饼碱浸方法很容易将砷从原渣中分离出来[5],其他有价金属如铜、铋等留在渣中,如易宇等[6−7]研究在NaOH-Na2S体系中脱砷的可行性和碱浸液的再生性;李玉虎等[8]采用NaOH-Na2S选择性浸出氧化锌中的砷。但是砷滤饼是污酸硫化处理过程产生的为强酸性渣,用碱浸方法会造成碱液的大量消耗,后续含砷的强碱溶液如何进行再处理也是一个难题。江西铜业公司进行了砷滤饼酸性浸出的试验[9],该工艺使用硫酸作为浸出液,浸出过程中通入空气做氧化剂,提高浸出过程的压力,砷和铜同时从砷滤饼中提出。PADILLA等[10]也同样提出了用H2SO4-O2浸出含砷物料中的砷,砷和铜能同时被浸出,并对浸出过程进行了动力学分析。但是该方法的加压氧化条件对设备要求较高,成本较大,难以大规模应用。水志良等[11]提出了一种硫酸高铁法的改进方法处理砷滤饼,将砷滤饼中的三硫化二砷以亚砷酸或砷酸形式溶出,再用二氧化硫还原得到白砷。该方法虽然降低了设备要求,但是最终得到的白砷产品回收率只达到了85%左右。
本文作者针对现有技术的不足之处,依据砷滤饼的特性,通过湿法浸出方法,在浸出过程中加入NaCl、H2O2、Na2S等化合物[12],使铜以硫化铜形式沉淀,砷以砷酸根离子形式进入溶液,达到铜砷分离的目的。考察了NaCl浓度、Na2S与砷滤饼渣的质量比、液固比、时间及温度等因素对砷滤饼中砷、铜浸出率的影响。浸出液再进行氧化、调节pH,用硫酸亚铁进行沉砷,生成砷酸铁晶体[13−14]。
1 实验
1.1 实验原料
本研究中采用的砷滤饼为国内某大型铜冶炼厂污酸硫化处理过程中所产生,其化学元素成分及矿物学分析分别如表1、表2及图1所示。由表1可以看到,砷滤饼中主要含硫、砷、铜3种元素,其含量分别为31.2%、13.5%和17.6%。由表2可知,砷在渣中的形态主要为氧化砷和硫化砷,铜的存在形态主要为易溶性铜和硫化铜。图1所示为砷滤饼的XRD谱。图1中观察不到硫化砷、硫化铜的峰,这是由于经过硫化过程形成的硫化砷和硫化铜不稳定,晶型欠佳。

表1 砷滤饼主要元素含量

表2 砷滤饼中砷、铜主要物相含量

图1 砷滤饼XRD谱
1.2 实验原理
砷滤饼氧化浸出过程中发生的主要反应:
As2O3+O2+3H2O=2H3AsO4(1)
2As2S3+5O2+6H2O=4H3AsO4+6S (2)
2H++CuS+H2O2+4Cl−=[CuCl4]2−+S+2H2O (3)
CuS+4H2O2+4Cl−=[CuCl4]2−+SO42−+4H2O (4)
后续浸出沉铜过程中发生的主要反应:
3Cu2++4S+4H2O=3CuS+SO42−+8H+(5)
Cu2++S2−=CuS (6)
3Cu2++As2S3+4H2O=3CuS+2HAsO2+6H+(7)
浸出反应的第一步是砷滤饼中砷和铜进入到溶液中的过程。添加双氧水使溶液的氧化还原电位提高,砷滤饼中部分不稳定的As2S3经过氧化溶解生成砷 酸[15]。NaCl溶液能提供大量氯离子,与Cu2+形成[CuCl]2−,降低金属离子Cu2+的浓度,这样可以降低CuS的离子积,此时溶液中CuS离子积<sp,从而使CuS沉淀溶解[15−16]。CuS和As2S3溶度积常 数[17](sp)分别为1.3×10−36和2.1×10−22,由于CuS的溶度积小于As2S3的溶度积,所以在浸出沉铜过程中添加硫化钠会优先和Cu2+反应生成溶度积较低的CuS。并且沉铜的过程除了Cu2+和硫元素结合生成CuS沉淀外,Cu2+还可以和不稳定三硫化二砷中的砷置换,使砷和铜达到最大限度的分离[18−19]。
1.3 实验方法
实验流程图如图2所示。砷滤饼在105 ℃烘干后破碎。称取砷滤饼50 g,加入一定浓度的NaCl溶液和H2O2进行一段浸出反应,反应过程用磁力搅拌器进行搅拌并加热。浸出一定时间后,向浸出体系中按一定比例加入Na2S进行沉铜反应。过滤得到的滤液再经过调节pH,最后添加一定比例的FeSO4,经过一定条件的沉砷反应,得到砷酸铁晶体和上清液。过滤所得到的滤液可返回浸出液继续浸出砷滤饼,循环使 用[20]。

图2 砷滤饼铜砷分离工艺流程图
1.4 分析方法
采用ICP-AES(电感耦合等离子体发射光谱法)仪器对砷滤饼消解液和浸出液中砷、铜含量进行检测。砷、铜浸出率以浸出液计算,公式如下:
式中:1为原料质量;1为元素在原料中质量分数。为浸出液中元素的质量浓度;1为浸出液体积。
2 结果与讨论
2.1 NaCl浓度对砷、铜浸出率的影响
在液固比7:1、Na2S与砷滤饼质量比3:4、反应时间4 h、加入双氧水20 mL及反应温度80 ℃的条件下,考察NaCl浓度对砷、铜浸出率的影响,实验结果如图3所示。由图3可见,当不添加NaCl时,As的浸出率为69.1%,Cu的浸出率为0.24%,这是由于没有添加Cl−时,砷滤饼中铜的浸出不完全,此时与Cu2+作用后剩余的S2−会沉淀部分浸出液中的砷,导致砷浸出率的较低;当溶液中NaCl的浓度由0 g/L升高到 20 g/L时,As的浸出率逐渐上升到95.43%,铜的浸出率略有提高,这是由于铜会优先于砷与S2−反应生成CuS,同时发生反应(7),所以砷的浸出率提高;当NaCl浓度继续升高到25 g/L时,As的浸出率几乎没有变化。铜的浸出率从0.24%升高到0.61%,这个阶段溶液中的S2−已经基本反应完全,砷的浸出率已经达到最大,继续增加NaCl不利于铜和砷的分 离[15]。从As、Cu的浸出率、工艺的经济化等因素综合考虑,确定NaCl最优浓度为20 g/L。

图3 NaCl浓度对砷、铜浸出率的影响
2.2 液固比对砷、铜浸出率的影响
在NaCl浓度为20 g/L、Na2S与砷滤饼质量比3:4、反应时间4 h、反应温度80 ℃的条件下,考察不同液固比对砷、铜浸出率的影响,实验结果如图4所示。由图4可见,随着液固比由4:1增大到7:1,砷的浸出率由55.9%提高到94.8%,当液固比继续增加,砷的浸出率稳定维持在95%左右;当液固比较低时,铜的浸出率维持在1%左右,当液固比大于6:1时,铜浸出率下降到0.4%左右并且稳定维持。当液固比小于6:1时,铜、砷在溶液中的溶解度有限,会影响S2−与Cu2+的沉淀反应,同时也会造成部分砷被沉淀,导致砷的浸出率较低。为了保证砷的高浸出率和铜的较低浸出率,综合考虑最优液固比为7:1。
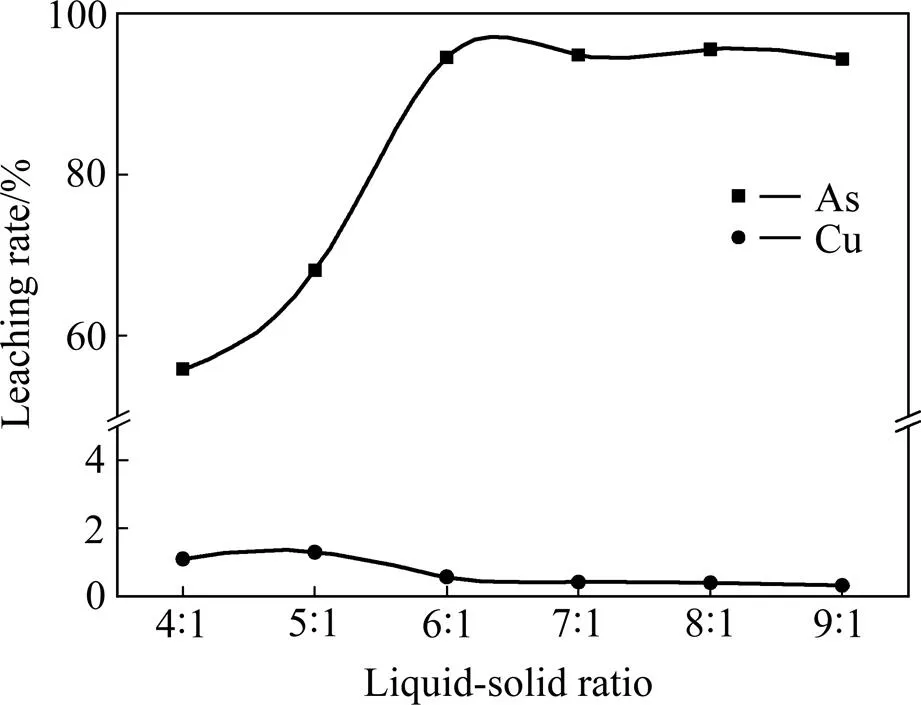
图4 液固比度对砷、铜浸出率的影响
2.3 浸出时间对砷、铜浸出率的影响
在液固比为7:1、NaCl浓度20 g/L、Na2S与砷滤饼质量比3:4、反应温度80 ℃的条件下,考察不同反应时间对砷、铜浸出率的影响,实验结果如图5所示。当反应时间为1 h时,砷的浸出率为50.1%,铜的浸出率为2.34%,此时主要是As2O3和可溶性铜的浸出;随着反应时间的增加,砷的浸出率提高,铜的浸出率降低;当反应4 h后,砷的浸出率达到95.5%,铜的浸出率降低到0.42%,在这个过程中添加的Na2S与Cu2+反应生成沉淀,同时溶液中的Cu2+与As2S3中的砷发生置换生成CuS和AsO2−;此后继续延长反应时间,砷的浸出率波动幅度较小,铜的浸出率都保持在0.5%左右,证明反应进行完全,砷已经达到最大浸出率。从提高作业效率、降低生产成本、增加砷的浸出率等方面综合考虑,确定最佳浸出时间为4 h。
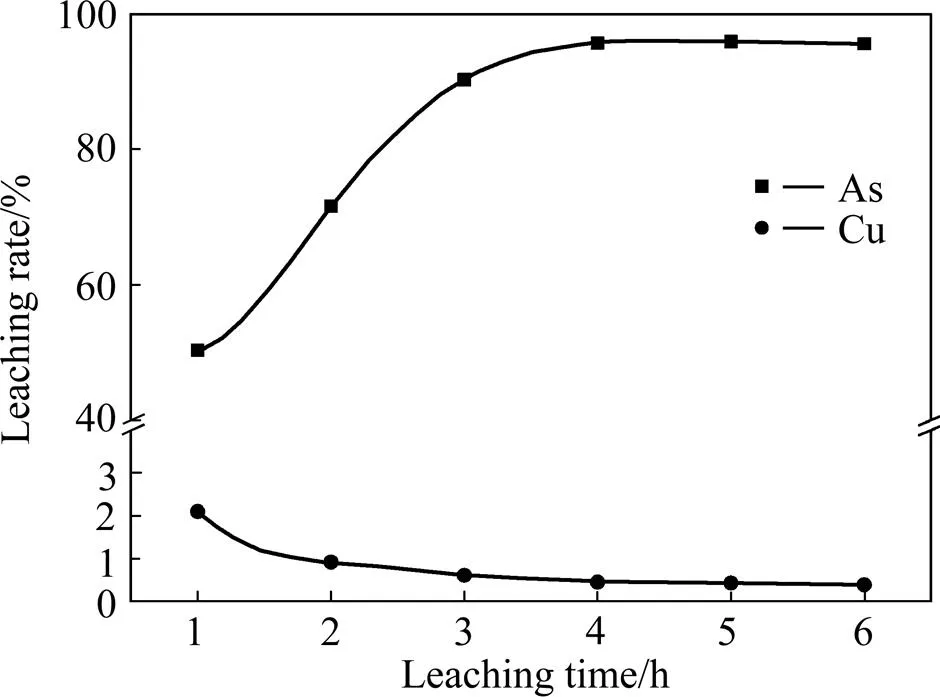
图5 浸出时间对砷、铜浸出率的影响
2.4 浸出温度对砷、铜浸出率的影响
在液固比为7:1、Na2S与砷滤饼质量比3:4、NaCl浓度20 g/L、浸出时间4 h的条件下,考察不同浸出温度对砷、铜浸出率的影响,实验结果如图6所示。由图6可见,当浸出温度由20 ℃提高至80 ℃时,砷的浸出率由27.52%增加至95.37%,由此可知浸出温度的增加有利于砷浸出反应的进行,这是由于一方面As2O3的溶解度随温度的提高而增加[15],另一方面,随着温度升高,浸出到溶液中的铜含量增加,同时促进Cu2+与As2S3反应生成CuS和AsO2−;此后温度对砷浸出率影响不大;在浸出温度小于60 ℃时,铜的浸出率随着温度升高而降低,这是由于温度较低时硫化沉铜反应和铜砷的置换不能完全进行,部分可溶性铜不能转化成CuS,导致铜浸出率的升高。因此,在浸出脱砷沉铜过程中,温度的提高有利于提高砷的浸出率,并且降低铜的浸出率,从能耗和砷、铜浸出率等方面综合考虑,确定最佳浸出温度为80 ℃。
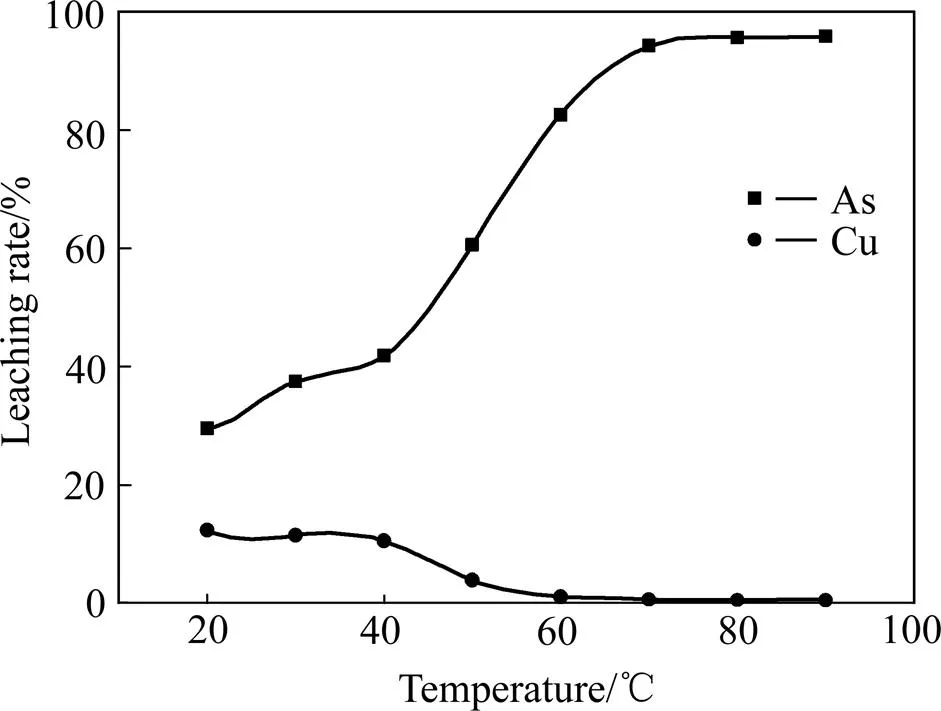
图6 浸出温度对砷、铜浸出率的影响
2.5 Na2S与砷滤饼渣的质量比对砷、铜浸出率的影响
在铜砷分离工艺的前半段,添加H2O2和NaCl使铜和砷大量浸出,之后需要添加一定比例的Na2S来沉淀Cu2+,使铜、砷达到最大限度的分离。在液固比为7:1、氯化钠浓度20 g/L、浸出时间4h及浸出温度80℃的条件下,考察不同Na2S添加量对砷、铜浸出率的影响,研究结果如图7所示。当不添加Na2S时,砷和铜的浸出率分别为96.01%和90.23%,随着Na2S添加量的增大,铜的浸出率迅速降低,证明添加的S2−迅速与Cu2+进行反应。当Na2S与砷滤饼质量比3:4时,铜浸出率为0.47%,继续添加Na2S,铜的浸出率几乎不受影响,而砷浸出率有所降低,这是由于溶液中S2−过量,会与溶液中的砷生成沉淀,降低砷的浸出率。综合考虑,选择最优的Na2S添加量和砷滤饼的质量比为3:4。

图7 Na2S与砷滤饼渣的质量比对砷、铜浸出率的影响
2.6 最优工艺条件试验
在前期单因素浸砷沉铜实验的基础上,选择液固比为7:1、NaCl浓度20 g/L、浸出时间4 h、浸出温度80 ℃、Na2S与砷滤饼质量比3:4以及添加20 mL H2O2的最优条件进行了5组平行实验,实验结果如图8所示。由图8可见,在最优工艺条件下,砷的浸出率稳定维持在95%以上,铜的浸出率稳定在0.5%左右。最优工艺条件实验浸出结果分析如表3所示,浸出液中砷浓度为12.42 g/L,铜浓度仅为0.29 g/L;浸出渣中砷含量为0.6%,铜含量富集到33.12%,达到了铜砷分离的目的。结合XRD谱可以得知,三氧化二砷已被浸出至溶液中,铜生成了CuS。
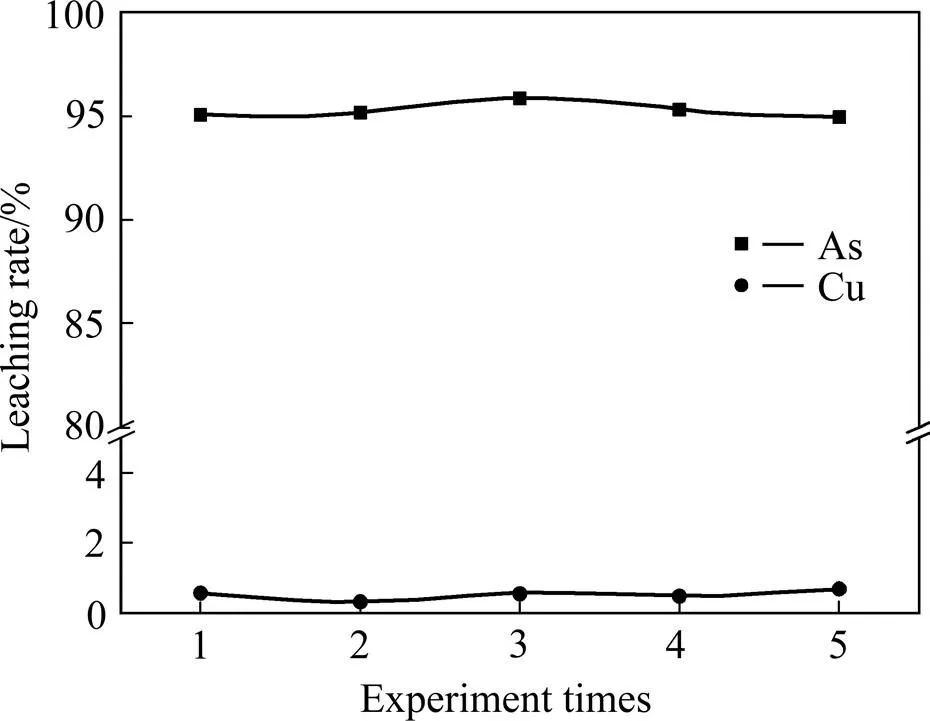
图8 最优工艺条件平行实验结果

表3 最优工艺条件实验结果分析

图9 最优工艺条件下浸出渣的XRD谱
2.7 浸出液的沉砷处理
砷滤饼浸出后所得浸出液中含有大量的砷,直接排放会对环境造成极大的污染,因此,需要对浸出液进行沉砷处理[21]。由于浸出液为强酸性,使用石灰沉砷会造成试剂的大量浪费,并且产生更多的废渣。而亚铁沉砷的条件是酸性,滤液含砷量大约为12 g/L,对于亚铁沉砷是一个适宜的浓度值,因此,本研究中采用FeSO4沉砷的处理工序[21−22]。
由于亚铁沉砷的最佳pH范围为弱酸性[23],滤液加入适量NaOH调节pH为4~5。按(Fe):(As)=2:3加入FeSO4。在90~95 ℃下搅拌反应3~5 h,产生浅灰绿色沉淀,实验结果如表3所示。测得滤液含砷量为0.23 g/L,砷酸铁晶体含砷量为32.15%。沉砷后的上清液可返回氧化浸出过程,实现循环利用[24]。

表4 亚铁沉砷实验结果
由表3可以看出,在pH 4~5、(Fe):(As)=2:3、90~95 ℃搅拌浸出3~5 h条件下沉砷率可达98%以上,故亚铁沉砷的浸出沉砷方案可行。
3 结论
1)在氯化钠氧化浸出−Na2S沉铜体系作用下,实现了砷滤饼中铜砷的有效分离和铜的富集,通过单因素实验确定的最优工艺条件为:液固比7:11、NaCl浓度20 g/L、浸出时间4 h、浸出温度80 ℃、Na2S与砷滤饼质量比3:4以及添加20 mL双氧水。砷滤饼砷浸出率可达95.56%,铜的浸出率仅为0.45%,达到了铜砷分离的要求。
2) 浸出液使用硫酸亚铁沉砷方法,沉砷率可以达到98%,生成的砷酸铁晶体含砷量为32.15%。浸出后的上清液可返回氧化浸出过程,实现浸出液的循环利用。
[1] 何秀梅. 铜冶炼过程中杂质元素走向探析[J].有色金属(冶炼部分), 2013(2): 55−57. HE Xiu-mei. Research on distribution of impurity elements in copper smelting[J]. Nonferrous Metals (Extractive Metallurgy), 2013(2): 55−57.
[2] 崔 洁, 杜亚光, 刘 芫, 曹龙文, 杜冬云. 工业硫化砷渣的性质研究与环境风险分析[J]. 硫酸工业, 2013(2): 41−46. CUI Jie, DU Ya-guang, LIU Yuan, CAO Long-wen, DU Dong-yun. Property research of industrial arsenic sulphide residue and environmental risk analysis[J]. Sulphuric Acid Industry, 2013(2): 41−46.
[3] 肖 愉. 硫化砷渣的无害化处理研究[J].环境科技, 2015, 28(5): 8−11. XIAO Yu. Study on innocent treatment of arsenic sulfide sludge[J]. Environmental Science and Technology, 2015, 28(5): 8−11.
[4] 张焕然, 刘晓英, 衷水平, 伍赠玲, 蓝碧波, 王俊娥. 富铼砷滤饼加压浸出工艺研究[J]. 中国有色冶金, 2015, 10(5): 59−62. ZHANG Huan-ran, LIU Xiao-ying, ZHONG Shui-ping, WU Zeng-ling, LAN Bi-bo, WANG Jun-e. Study on pressure leaching process of arsenic-rhenium filter cake[J]. China Nonferrous Metallurgy, 2015, 10(5): 59−62.
[5] 徐志峰, 聂华平, 李 强, 卢秋虎, 王 巍, 月日辉. 高铜高砷烟灰加压浸出工艺[J]. 中国有色金属学报, 2008, 18(S1): 59−63. XU Zhi-feng, NIE Hua-ping, LI Qiang, LU Qiu-hu, WANG Wei, YUE Ri-hui. Pressure leaching technique of smelter dust with high-copper and high-arsenic[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(S1): 59−63.
[6] 易 宇, 石 靖, 田庆华, 郭学益. 高砷烟尘氢氧化钠−硫化钠碱性浸出脱砷[J]. 中国有色金属学报, 2015, 25(3): 806−814. YI Yu, SHI Jing, TIAN Qing-hua, GUO Xue-yi. Arsenic removal from high-arsenic dust by NaOH-Na2S alkaline leaching[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(3): 806−814.
[7] 易 宇, 石 靖, 田庆华, 郭学益. 高砷烟尘碱浸渣制备焦锑酸钠的新工艺[J]. 中国有色金属学报, 2015, 25(1): 241−249. YI Yu, SHI Jing, TIAN Qing-hua, GUO Xue-yi. Novel technology for preparation of sodium pyroantimonate from alkali leaching residue of high arsenic dust[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(1): 241−249.
[8] LI Yu-hu, LIU Zhi-hong, ZHAO Zhong-wei. Dete.rmination of arsenic speciation in secondary zinc oxide and arsenic leachability[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(5): 1209−1216.
[9] 郑雅杰, 张胜华, 龚 昶. 含砷污酸资源化回收铜和砷的新工艺[J]. 中国有色金属学报, 2013, 23(10): 2985−2992. ZHENG Ya-jie, ZHANG Sheng-hua, GONG Chang. Novel technique for recovery of copper and arsenic from arsenic- containing waste acid[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(10): 2985−2992.
[10] PADILLA R, GIRÓN D, RUIZ M C. Copper and arsenic dissolution from chalcopyrite-enargite concentrate by sulfidation and pressure leaching in H2SO4-O2[J]. Hydrometallurgy, 2010, 100(3/4): 152−156.
[11] 水志良, 靳 珍, 黄卫东. 砷滤饼综合利用方法: CN 851042[P]. 1986−05−10. SHUI Zhi-lian, JIN Zhen, HUANG Wei-dong. Comprehensive utilization method of arsenic filtration cake: CN 851042[P]. 1986−05−10.
[12] 陈 云. 硫化法从砷滤饼中分离砷的试验研究[J]. 湿法冶金, 2010, 28(4): 233−235. CHEN Yun. Test research on removal of arsenic from filtration cake containing arsenic by sulfurization[J]. Hydrometallurgy of China, 2010, 28(4): 233−235.
[13] MIN Xiao-bo, LIAO Ying-ping, CHAI Li-yuan. Removal and stabilization of arsenic from anode slime by forming crystal scorodite[J].Transactions of Nonferrous Metals Society of China, 2015, 25(4): 1298−1306.
[14] LEPPINEN J, RUONALA M, MIETTINEN V.将砷作为臭葱石除去的方法: CN 102307813A[P]. 2012−01−04. LEPPINEN J, RUONALA M, MIETTINEN V. The method for removing arsenic as scorodite: CN 102307813A[P]. 2012−01−04.
[15] 库建刚, 王安理, 乔翠杰, 张文彬. 氯离子对硫化铜精矿浸出的影响[J]. 湿法冶金, 2008, 27(2): 113−116. KU Jian-gang, WANG An-li, QIAO Cui-jie, ZHANG Wen-bin. Influence of chloride ions on leaching of copper sulfide concentrate[J]. Hydrometallurgy of China, 2008, 27(2):113−116.
[16] PADILLA R, GIRÓN D, RUIZ M C. Leaching of enargite in H2SO4-NaCl-O2media[J]. Hydrometallurgy, 2005, 80(4): 272−279.
[17] 迪安. 兰氏化学手册[M]. 科学出版社, 1991. DEAN. Lange's handbook of chemistry[M]. The Science Publishing Company, 1991.
[18] 镫屋三雄, 佐藤祐辅, 见上宽信. 含砷的有色金属冶炼中间产物的处理方法: CN 101784488 A[P]. 2010−07−21. ABUMIYA M, SATO Y, MIKAMI H. The Processing method of intermediate product containing arsenic in nonferrous metallurgy: CN 101784488 A[P]. 2010−07−21.
[19] 郑雅杰, 崔 涛, 彭映林. 二段脱铜液还原结晶法脱砷新工艺[J]. 中国有色金属学报, 2012, 22(7): 2103−2108. ZHENG Ya-jie, CUI Tao, PENG Ying-lin. New process of arsenic removal from second stage decopperizing electrolyte by reduction[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(7): 2103−2108.
[20] 张荣良, 丘克强, 谢永金, 洪育民, 郑春到. 铜冶炼闪速炉烟尘氧化浸出与中和脱砷[J]. 中南大学学报(自然科学版), 2006, 37(1): 73−78. ZHANG Rong-liang, QIU Ke-qiang, XIE Yong-jin, HONG Yu-min, ZHENG Chun-dao. Treatment process of dust from flash smelting furnace at copper smelter by oxidative leaching and dearsenifying process from leaching solution[J]. Journal of Central South University (Science and Technology), 2006, 37(1):73−78.
[21] TONGAMP W, TAKASAKI Y, SHIBAYAMA A. Arsenic removal from copper ores and concentrates through alkaline leaching in NaHS media[J]. Hydrometallurgy, 2009, 98(3/4): 213−218.
[22] 倪 冲, 赵燕鹏, 阮福辉. 氨浸法从含砷石灰铁盐渣中回收铜的动力学[J]. 中国有色金属学报, 2013, 23(6): 1769−1774. NI Chong, ZHAO Yan-peng, RUAN Fu-hui. Kinetics of copper recovery from As-contained solid waste by ammonia leaching method[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(6): 1769−1774.
[23] DAENZER R, XU L, DOERFELT C, JIA Y, DEMOPOULOS C P. Precipitation behaviour of As(Ⅴ) during neutralization of acidic Fe(Ⅱ)-As(Ⅴ) solutions in batch and continuous modes[J]. Hydrometallurgy, 2014, 146(3): 40–47.
[24] 熊 珊. 含砷废液臭葱石沉砷研究[D].长沙: 中南大学, 2012. XIONG Shan. Arsenic precipitation in arsenic-containing wastewater based on scorodite formation[D]. Changsha: Central South University, 2012.
Separation of copper and arsenic in arsenic filtration cake
SHEN Chen1, MIN Xiao-bo1, 2, 3, SHI Mei-qing2, ZHOU Bo-sheng1, ZHAO Zong-wen1, LI Yuan-cheng1, ZHANG Chun1
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;2. Chinese National Engineering Research Center for Control and Treatment of Heavy Metal Pollution, Central South University, Changsha 410083, China;3. Co-Innovation Center for Clean and Efficient Utilization of Strategic Metal Mineral Resources, Central South University, Changsha 410083, China)
Leaching method was used to separate copper and arsenic in the arsenic filtration cake, which was achieved by the formation of CuS in the residue and AsO43−in the solution during the leaching process. The effects of various parameters, such as concentrations of NaCl, mass ratio of Na2S to arsenic filtration cake, liquid-solid ratio, leaching time and temperature, on leaching rate of As and Cu were investigated. On this basis, the optimal conditions are obtained through single factor experiment as follows, 20 g/L NaCl, liquid-solid ratio 7:1, mass ratio of Na2S to arsenic filtration cake 3:4, leaching at 80 ℃ for 4h, with 20 mL H2O2. Under this optimal condition, the leaching rate of As reaches 95.56%, and leaching rate of Cu is less than 0.5%. The copper content in leaching residue is as high as 33.6% (mass fraction). In addition, arsenic-containing leachate can be treated with FeSO4and removal rate of As in leachate exceeds 98%. Arsenic content in the generated crystal is 32.15% (mass fraction), and arsenic concentration in the effluent is 0.23 g/L which can be returned to the leaching process.
arsenic filtration cake; copper; arsenic; separation; leaching; arsenic removal
(编辑 龙怀中)
Project(201509050) supported by Special Program on Environmental Protection for Public Welfare; Project(2015CX001) supported by Innovation-driven Plan in Central South University, China
2016-01-25; Accepted date:2016-06-17
MIN Xiao-bo; Tel: +86-731-88830875; E-mail: mxb@csu.edu.cn
1004-0609(2017)-02-0356-07
TF811
A
国家公益性(环保)行业科研专项(201509050);中南大学创新驱动计划资助项目(2015CX001)
2016-01-25;
2016-06-17
闵小波,教授,博士;电话:0731-88830875;E-mail: mxb@csu.edu.cn
——非均布滤饼的局部比阻与平均比阻的测定与计算方法

