亲水作用色谱—质谱联用法同时测定参附注射液中的14种有机酸
刘瑶+张娜+史社坡+宋青青+李军+宋月林+屠鹏飞

[摘要]有机酸广泛分布在植物及相关产品中,其参与多种代谢途径(如三羧酸循环),并表现出多种药理活性。参附注射液作为广泛使用的中药注射剂,不良反应时有报道。因而,应深入阐明参附注射液的化学组成,并制定严格的质量标准,进而保障其临床使用安全有效。参附注射液由红参及黑顺片经现代工艺提取制备而成,有机酸为其主要成分类别之一。该研究通过建立HTTJTC-LC-MS,同时测定参附注射液中肉桂酸、阿魏酸、4-羟基苯甲酸、乳酸、己二酸、延胡索酸、咖啡酸、琥珀酸、马来酸、丙二酸、苹果酸、莽草酸、酒石酸和金鸡纳酸等14种有机酸成分的含量。14种有机酸类成分在HTTJTC色谱柱上均获得较好的保留和分离。除肉桂酸(231μg·L-1)、乳酸(113μg·L-1)和丙二酸(32.5μg·L-1)外,其余11个化合物的定量限均小于10μg·L-1。定量结果表明,苹果酸、丙二酸、奎尼酸、乳酸和肉桂酸在参附注射液中含量较高(>1.89 mg·L-1),而10批样品中均未检测到咖啡酸和己二酸。该方法适用于参附等中药注射液中多种有机酸含量的同时测定。
[关键词]有机酸;参附注射液;多成分含量测定;亲水作用色谱法;质谱
参附注射液由红参和黑顺片经现代工艺提取制备而成,具回阳救逆、益气固脱之功效,为临床常用中药注射剂。主要用于阳气暴脱的厥脱症(感染性、失血性、失液性休克等)及阳虚(气虚)所致的惊悸、怔忡、喘咳、胃疼、泄泻、痹症等作为广泛使用的中药注射剂。参附注射液的不良反应时有报道。因此,应深入阐明参附注射液的化学组成,并制定严格的质量标准。有机酸作为参附注射液的主要化学成分类别之一,在其药效作用及不良反应中均发挥了重要作用。
有机酸广泛分布于植物的根、叶、果实等部位。常见的植物有机酸,如脂肪族的酒石酸、草酸、苹果酸、枸椽酸、抗坏血酸(维生素C)等和芳香族的水杨酸、咖啡酸等。有机酸常表现出抑菌、消炎、抗病毒、抗突变、抗癌、增强冠状动脉血流量、降低食糜的pH、增加胰液分泌、改变肠道微环境等药理活性。近年来,特别是在短链脂肪酸类化合物(SCFA)被认定为多种肠道及相关疾病的生物标志物(biomark-ers)后,有机酸的定性、定量分析受到了越来越多的关注。除少数芳香族有机酸外,有机酸类化合物仅在紫外检测范围的末端具有较弱的吸收。并且,该类化合物常表现出较强的极性,甚至是离子态,使得在常见的RP-C18色谱柱上很难实现较好的保留。这些因素给有机酸类化合物的准确定量带来了极大的挑战。目前,有机酸类化合物的分析主要采用离子色谱-质谱联用(IC-MS)、液相色谱结合低pH流动相和液质联用配备新型的五氟苯乙基(PFP)色谱柱等。然而,这些方法存在对设备要求高、灵敏度低、操作繁琐等缺点,难以满足复杂样品中各有机酸类化合物快速、灵敏定量分析的需求。虽然亲水作用色谱法(HILIC)已被广泛报道适用于大极性化合物的色谱分析,HILIC用于有机酸的定量分析却鲜有报道。因此,本研究拟充分利用HILIC的优点,建立快速、灵敏的HILIC-LC-MS方法,并将其用于复杂样品的定量分析。
作为本课题组对参附注射液化学物质组系统研究的一部分,在对参附注射液中的氨基酸、核苷、乌头生物碱、人参皂苷等成分进行了定性及定量分析的基础上,本文进一步利用亲水作用色谱法结合质谱(HILIC.LC-MS)同时测定参附注射液中14种有机酸类成分的含量。
1材料
岛津SHIMADZU高效液相色谱系统,配备2个LC-20ADXR泵、SIL-20ACXR自动进样器、CTO-20AC柱温箱、SPD-M20A PDA检测器、DGU-20A3在线脱气机和CBM-20A控制器;ABSciex 5500 Qtrap质谱仪(美国ABSciex公司)配备ESI离子源和Analyst1.6.2软件;Milli-Q超纯水一体机(美国Millipore公司)。
14种有机酸对照品包括乳酸[L·(+)=lacticacid]、丙二酸(malonic acid)、马来酸(maleic acid)、富马酸(fumaric acid)、琥珀酸(succinic acid)、苹果酸(D-malic acid)、己二酸(adipic acid)、莽草酸[(一).shikimic acid]、奎尼酸(quinic acid)、酒石酸(D-tartaric acid)均来自于SUPELC0的有机酸套装(美国Sigma-Aldrich公司);咖啡酸(caffeic acid)和4.羟基苯甲酸(4-hydroxybenzoic acid)购自日本东京化成工业株式会社;阿魏酸(ferulic acid)购自上海阿拉丁生化科技股份公司;肉桂酸(cinnamic acid)購自北京国药集团化学试剂有限公司;内标物为4.氟肉桂酸(IS),购自北京百灵威科技有限公司。乙腈(Optima LC-MS级别,美国Thermo-Fisher公司),甲酸(Optima LC/MS级别,美国Thermo-Fisher公司)。其余试剂均为分析纯。
10批次的参附注射液(SFI1~SFI10)均由华润三九药业有限公司(四川雅安)提供。
2方法与结果
2.1LC-MS条件
色谱柱为Waters XBridge BEH Amide(4.6mmx150mm,3.5μm,美国Waters公司),柱温40℃;0.1%甲酸.水溶液(A)和0.1%甲酸.乙腈(B)作为流动相;梯度洗脱(0~10.0min,98%-55%B;10.0~10.1min,55%~98%B;10.1-15.0min,98%B);流速0.8 mL·min-1;进样体积2.0μL。
质谱检测采用ESI负离子化模式;雾化气N2(GSl)50 psi(1psi=6.89 kPa);辅助气N2(GS2)50psi;气帘气(CUR)35 psi;碰撞气(CAD)high;喷雾电压(IS)-4500V;离子化温度(TEM)550℃;选择离子检测模式(selected ion momtoring,SIM);射入电压(EP)-10V;碰撞室射出电压(CXP)-16V。各有机酸的定量离子对、保留时间及其他质谱参数(脱簇电压DP和碰撞能CE)见表1。典型色谱图见图1。
2.2溶液配制
2.2.1对照品溶液制备取乳酸、丙二酸、琥珀酸、苹果酸、4.羟基苯甲酸、肉桂酸适量,精密称定,分别用DMSO配制成20mmol·L-1的对照品储备液;取马来酸、富马酸、己二酸、莽草酸、奎尼酸、酒石酸、咖啡酸、阿魏酸适量,分别用DMSO配制成10mmol·L-1的对照品储备液,4℃保存,备用。
取内标物4.氟肉桂酸(IS)适量,用DMSO配制成10 mmol·L-1的内标储备液,再用40%乙腈逐步稀释1000倍,配制成10μmol·L2的内标溶液,4℃保存,备用。
2.2.2供试品溶液制备吸取10批次参附注射液样品各200μL,每批抽取3份,分别用40%乙腈稀释5倍后,再吸取100μL再用10μmol·L-1的内标溶液稀释10倍,用0.22μm微孔滤膜过滤,取续滤液,即得供试品溶液。
2.3线性关系考察
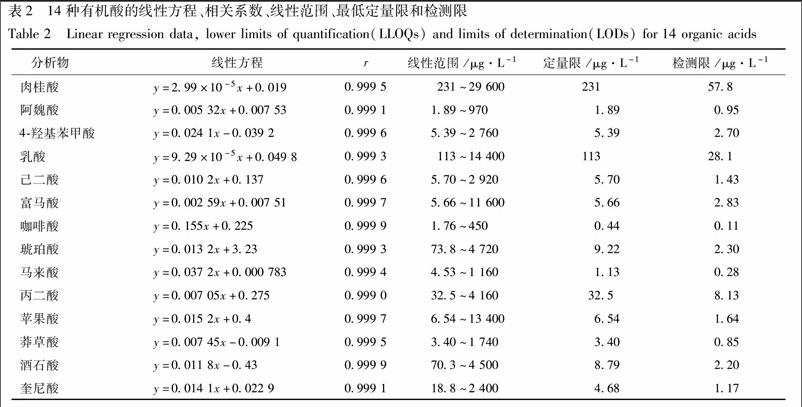
吸取适量各对照品的储备液,混合,并用40%乙腈稀释至1.0mL,配制成乳酸、丙二酸、马来酸、富马酸、琥珀酸、苹果酸、4.羟基苯甲酸、己二酸、肉桂酸、莽草酸、咖啡酸、奎尼酸、阿魏酸、酒石酸质量浓度分别为144,41.6,11.6,116,94.4,268,55.2,29.2,296,34.8,36,192,38.8,45 mg·L-1的混标储备液。用40%乙腈逐步倍半稀释混标储备液,获得系列浓度梯度的混标溶液。分别吸取各浓度混标溶液100μL,用10μmol·L-1。的内标溶液稀释10倍,即得系列浓度梯度的含内标的样品溶液。在优化的实验条件下,对含有相同浓度内标的一系列标准溶液按照2.1项下条件进行检测,重复进样3次。以各有机酸峰面积与内标峰面积的比值作为纵坐标(Y),各有机酸质量浓度(μg·L-1)作为横坐标(X),绘制标准曲线,进行线性回归得标准曲线。对标准溶液进行逐步稀释,分别取信噪比(S/N)约为3和10时各分析物的浓度作为检测限(μg·L-1,LOD)和最低定量限(μg·L-1,LLOQ)。14种待测成分的线性回归方程、线性范围、相关系数(r)、检测限和最低定量限见表2。
2.4精密度试验
分别选择高、中、低浓度标曲样品溶液作为质控样品,具体浓度见表3。取3个浓度的质控样品进行日内(intra-day)和日间(inter-day)精密度考察。按2.1项下LC-MS条件进行样品分析,日内精密度通过每隔2h进样1次,共进样6次考察;日间精密度通过连续3d,1 d3次,采用同法测定考察,计算各有机酸含量的相对标准偏差(RSD)。由表3可见各化合物的日内精密度RSD≤13%,日间精密度RSD≤15%,均符合方法学的要求。
2.5重复性试验
取参附注射液1批次,按2.2.2项下方法平行制备6份,测定峰面积,并计算各待测化合物的含量,RSD为2.1%~8.6%,结果表明该方法的重复性良好。
2.6稳定性试验
取同一份供试品溶液,室温放置,分别于0,2,4,8,12,18,24 h,按2.1项下LC-MS条件进行样品分析,计算各待测化合物含量的相对标准偏差,各RSD为3.7%~10%,表明各待测化合物在室温下24 h之内能够稳定存在。
2.7加样回收率试验
取已测得含量的参附注射液样品,分别精密加入适量体积的高、中、低3个浓度的混标溶液,见表3,按2.2.2项下方法处理后按2.1项下LC-MS条件测定,每一浓度平行测定3次,计算平均回收率。由表3可见,除2种未检测到的有机酸(己二酸和咖啡酸)外,其余12种有机酸的平均加样回收率为86.33%一114.3%(RSD≤14%),表明加入不同浓度的混标溶液后,各分析物的回收率较为稳定,准确度较好。
2.8样品溶液含量测定
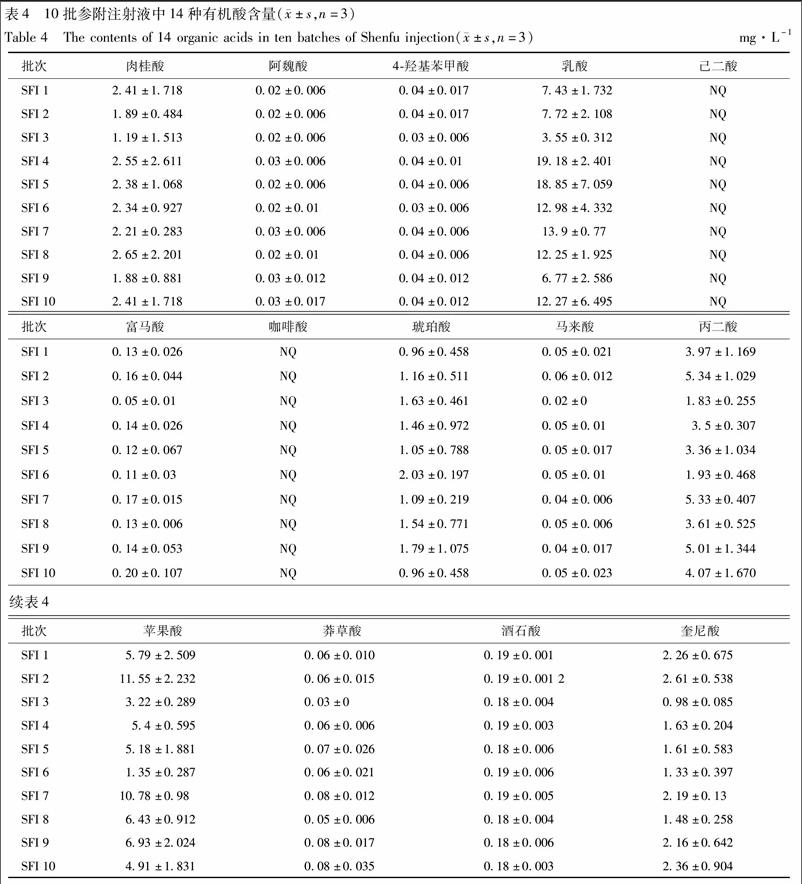
将10批参附注射液按2.2.2项下供试品溶液制备方法制备,依照2.1项下色谱和质谱条件测定,重复3次。将所得峰面积代入标准曲线,计算各批次参附注射液中各有机酸类成分的含量。典型图谱见图1B,测定结果见表4。
3讨论与结论
有机酸广泛分布于中药材及中药复方制剂当中。由于苯环等强发色团的缺失,除少数芳香族有机酸外,该类化合物只具备较弱的紫外吸收。另一方面,由于羧基的存在,有机酸类化合物常表现出较强的极性。因此,常用的HPLC-UV配备RP-C18色谱柱的方法难以实现有机酸的全面准确定量分析。本文采用HILIC色谱柱实现了有机酸类分析物的较好保留,并且采用质谱检测器,利用选择离子监测(SIM)模式对各有机酸类化合物进行灵敏地检测,建立了参附注射液中14个有机酸类分析物同时定量分析的方法。实验过程中筛选了多种HILIC色谱柱,方法学考察和实际样品测定结果表明,使用化学性质稳定的三键键合的酰胺基键合相的Waters XBridge BEH Amide色谱柱对有机酸类化学成分保留能力强、柱流失低,能够实现多种有机酸的快速分离。已有文献报道常通过调低流动相pH(硫酸或磷酸盐缓冲体系,pH<3)流动相,对色谱柱损害较大。并且,由于非挥发性缓冲盐的使用,使得无法采用蒸发光散色检测器及质谱检测器。而本文采用0.1%甲酸作为流动相改性剂,不仅能很好地降低色谱柱的损害,而且能满足质谱检测器的要求。在对待测化合物离子对进行筛选的过程中,发现有机酸类分析物由于结构中存在羧基,响应最好的离子对一般为[M-H]->[M-H-CO2]-,能够很好地与其他类型化合物进行区分。
附子生物碱及人参皂苷类成分通常被认为是参附注射液中的主要活性成分。然而,在系统研究过程中发现参附注射液中大量存在各种大极性成分,主要包括有机酸类、氨基酸类、核苷类等化学类型。本研究在定量分析参附注射液中附子生物碱、人参皂苷、氨基酸及核苷类成分的基础上,进一步建立了一种可快速测定参附注射液中14种有机酸含量的色谱.质谱联用法。在所测的10批参附注射液中,苹果酸、丙二酸、奎尼酸、乳酸和肉桂酸的含量均较大(>1.89mg·L-1),而咖啡酸和己二酸均未检测到。本文的定量分析结果对于参附注射液的系统质量控制及用药安全标准提升具有重要意義。同时,所建立的HILIC-LC-MS方法适用于参附等中药注射剂中多种有机酸含量的同时测定。

