MOR分子筛与水复合环境对赖氨酸手性转变反应的共催化机理*
刘逸轩,王佐成,董丽荣,赵晓波,杨晓翠,佟华
(1.海口经济学院马克思主义学院自然科学教学部,海南 海口 570100; 2.白城师范学院物理学院,吉林 白城 137000; 3.吉林师范大学物理学院,吉林 四平 136000)
MOR分子筛与水复合环境对赖氨酸手性转变反应的共催化机理*
刘逸轩1,王佐成2,董丽荣3,赵晓波2,杨晓翠2,佟华2
(1.海口经济学院马克思主义学院自然科学教学部,海南 海口 570100; 2.白城师范学院物理学院,吉林 白城 137000; 3.吉林师范大学物理学院,吉林 四平 136000)
采用量子力学与分子力学组合的ONIOM方法, 研究了赖氨酸限域在水与MOR分子筛复合环境下的手性转变.结构分析表明:2个水分子比1个水分子助氢迁移反应的过渡态分子氢键键角显著增大。反应通道研究发现:标题反应有a、b和c三个通道,是赖氨酸在MOR分子筛限域环境下,水助质子以氨基、羰基和羟基为桥从手性碳的一侧迁移到另一侧,实现手性转变。势能面计算表明,a是主反应通道,质子从手性碳向氨基的迁移是决速步骤,在2个水分子助决速步时,吉布斯自由能垒被降到最低值101.9 kJ/mol,与裸反应、限域在MOR分子筛和限域在水环境的此通道决速步能垒252.6、229.7和123.9 kJ/mol相比较,均有明显降低。结果表明:水与MOR分子筛复合环境对赖氨酸手性转变具有较好的共催化作用,左旋赖氨酸在生命体内可以缓慢地旋光异构。
MOR分子筛;赖氨酸;手性转变;ONIOM方法;密度泛函;过渡态
赖氨酸(Lys)是一种十分重要的生命体必须氨基酸。根据其旋光性的不同,分为左赖氨酸(S-Lys)和右赖氨酸(R-Lys),S-Lys具有活性,R-Lys基本无活性。S-Lys在合成蛋白质的氨基酸中最为重要,和别的营养成分一起在生命体中形成胶原蛋白。在缔结肌肉和关节软骨等组织过程中也发挥着及其重要的作用。S-Lys对于改善免疫系统、促进吸收钙、降低甘油三酯和抵制单纯疱疹等也有着十分重要的作用,还用作人类食品和动物饲料添加剂。R-Lys则主要用在生物化学的研究领域,另外还有促进细胞吸附性的作用。
由于Lys具有重要的作用,人们对他进行了大量的研究。文献[1]对水溶液中的S-Lys结构进行了研究, 根据“自洽迭代”方法,分离得到了S-Lys中各C原子的接触位移和偶极位移。文献[2]研究了S-Lys与三种还原糖美拉德反应产物的理化特性及抗氧化活性。文献[3]研究了聚-S-Lys的物理化学性质。文献[4]的研究,揭示了在细胞核外不同的细胞通路对Lys乙酰化的调控。文献[5]研究了溶液中的聚S-赖氨酸的构象以及红外和拉曼光谱特性。文献[6-9]研究了裸环境、水环境和MOR分子筛限域环境下Lys的手性转变机制。研究发现,Lys可以在4个通道实现手性转变裸反应,质子H以氨基N为桥从手性碳的一侧迁移到另一侧是主反应通道,其裸反应决速步吉布斯自由能垒为252.6 kJ·mol-1。水分子对Lys的手性转变具有催化作用,使主反应通道裸反应决速步吉布斯自由能垒降为123.9 kJ·mol-1。MOR分子筛12元环孔道对赖氨酸分子的手性转变具有限域催化作用,使主反应通道裸反应决速步吉布斯自由能垒降为229.7 kJ·mol-1。
虽然人们对Lys的手性转变进行了大量的研究,但并没有找到使Lys实现手性转变的理想环境。文献[10-14]研究了α-丙氨酸在几种不同的单壁碳纳米管和单壁硼氮纳米管与水复合环境下的手性转变机制,文献[15]研究了布洛芬在MOR分子筛与水的复合环境下的手性转变机制,研究表明纳米孔材料与水构成的复合环境对丙氨酸和布洛芬等手性分子的旋光异构具有共催化作用。基于文献[9-15]的研究经验,本文研究了MOR分子筛与水的复合环境对Lys手性转变反应的共催化作用。
1 模型的选取与计算研究方法
MOR分子筛由Si、O和H 3种元素构成,含有12元环和8元环两种一维主直孔道,12元环窗口直径为0.65 nm×0.70 nm,八元环窗口直径为0.26 nm×0.57 nm。Lys与2个水分子以氢键形成的水合分子的最大横向线度为0.58 nm×0.51 nm[7],只能进入12元环孔道,因此,将MOR分子筛的12元环孔道作为限域环境。Lys与2个水分子以氢键形成的水合分子的最大纵向线度为1.027 nm,为充分地考虑孔道限域效应,采用周期性模型把含有12元环和部分8元环直孔道分子筛骨架包括进来,用含有240T的簇模型作为限域催化环境(此模型的长度约为3.2 nm),用氢原子饱和模型截断处的硅原子,并把硅氢键长固定为1.46 nm[16],如图1(a)所示。
采用QM/MM组合的ONIOM(our own n-layered integrated molecule orbit and molecule mechanics)方法[17],研究标题反应机制。将分子筛与其内部反应物的水合物等形成的包结物分为两层处理:内层反应底物为QM区,考虑到分子筛与内部反应底物的长程作用,用CAM(coulomb-attenuated hybrid exchange-correlation functional)结合DFT的长程校正泛函CAM-B3LYP[18-19]方法,基组采用6-31G(d, p);外层分子筛为MM区,采用分子力学的UFF(universal force field)力场[20]处理,为不使分子筛骨架形变,把外层固定,全参数优化稳定点和过渡态[21-22]。为计算出相对精确的势能面,QM区采用微扰理论的MP2[23-24]方法,在ONIOM(MP2/6-311++G(2df, pd):UFF)理论水平,计算各包结物的单点能,利用Gtotal=ESP+Gtc(ESP和Gtc分别为高水平的单点能和吉布斯自由能热校正)计算高水平的总吉布斯自由能,绘制反应过程的吉布斯自由能势能面。通过对过渡态进行频率分析和内禀反应坐标(IRC)计算[25],确认过渡态的可靠性。a通道上的产物R-Lys分子与1个水分子以氢键形成的复合分子限域在MOR分子筛内的包结物记为aP_R-Lys·1H2O@MOR, 其它体系的表示类似。文中计算均采用Gaussian 09软件包[26]完成。
2 结果与讨论
在B3LYP/6-31+G(d, p)水平,优化的单体S型和R型Lys的几何构型[6],见图1(b)和图1(c)。
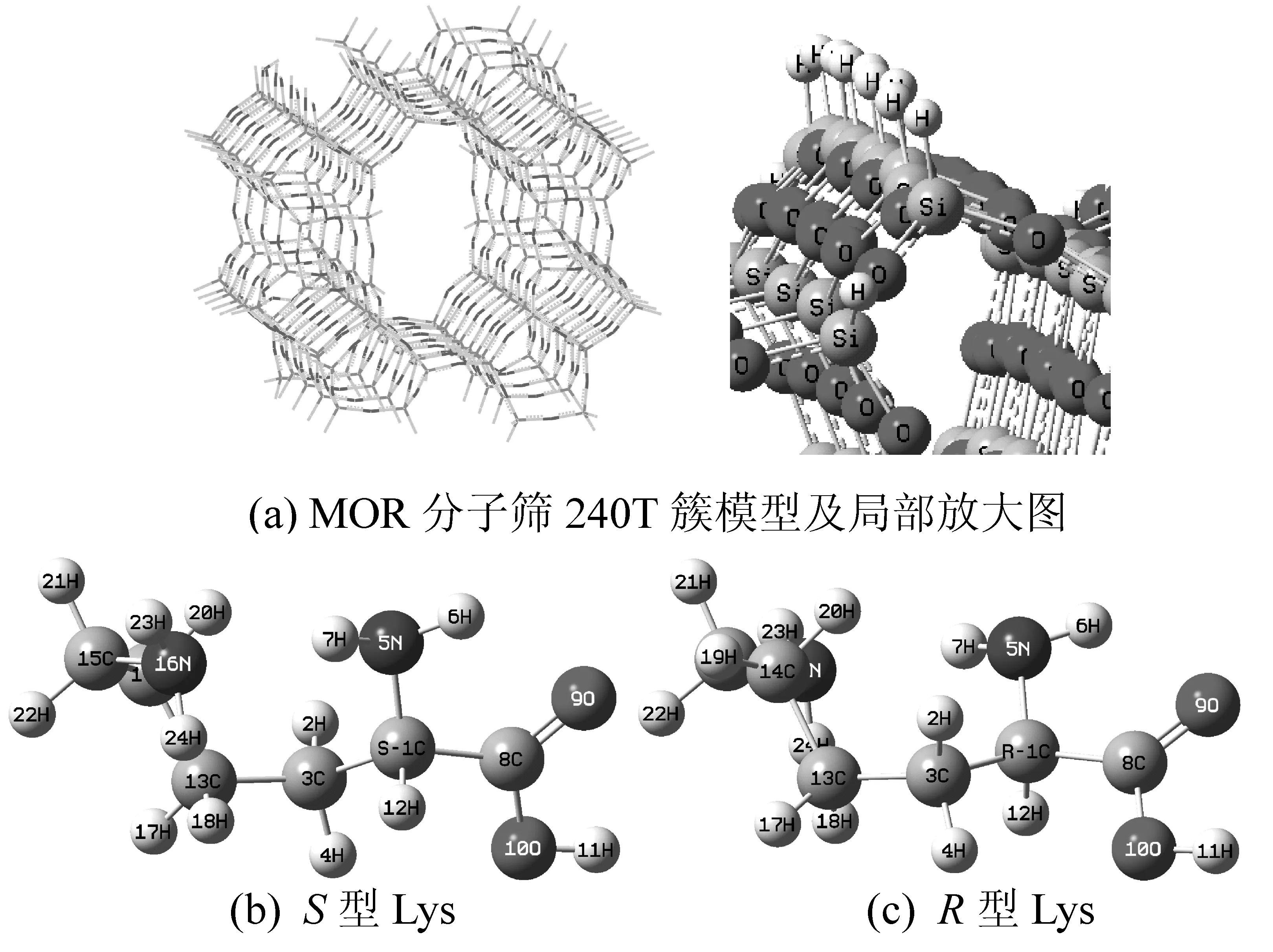
图1 MOR分子筛240T簇模型(a),S型与R型Lys分子的几何结构(b)和 (c)Fig.1 240T cluster model of the MOR zeolite (a),geometries of S and R type Lys molecules(b),(c)
对图1的分析与计算研究发现,限域在MOR分子筛与水复合环境下,S-Lys向R-Lys的异构反应有a、b和c三个通道,分别是水助质子以氨基、羰基和羟基为桥从手性碳的一侧迁移到另一侧。b通道又分为2个路径,一个是质子以水分子为媒介在纸面里直接从羰基迁移到手性碳,另一个是质子以水分子为媒介先从羰基迁移到氨基,然后在以水分子为媒介在纸面里从氨基迁移到手性碳(同于a通道的后半程)。计算表明,在分子筛内3个水分子助质子迁移反应的能垒基本同于甚至低于2个水分子的情形,并且a通道是最具优势反应通道。因此,本工作只讨论1个和2个水分子助质子迁移反应,对a通道进行详细讨论,其他通道只讨论主要的基元反应过程。
2.1 限域在MOR分子筛与水复合环境下S-Lys在a通道的手性转变反应机理
1个水分子助a通道上的手性转变反应历程见图2:X。S-Lys与氨基和手性碳前面的1个水分子以氢键结合的水和分子包结物aS-Lys·1H2O@MOR,经过氨基氮上的714H和715H左右反转的过渡态包结物aSTS1·1H2O@MOR,二面角714H-713N-709C-715H从133.25°变为-123.30°,异构成第1个产物中间体包结物aSINT1·1H2O@MOR。aSINT1·1H2O@MOR的氨基氮713N左侧裸露,负电荷增多(负电荷密度增加),接受正电荷的能力增加。aSINT1·1H2O@MOR经过aTS2·1H2O@MOR实现了手性碳上的质子以1个水分子为媒介向氨基氮713N的迁移,异构成第2个产物中间体包结物aSINT2·1H2O(m)@MOR(水分子可以分别在INT2的左右两侧与INT2以氢键结合,此处m表示水分子在左侧。后面类似的情况不再予以解释),aSINT2·1H2O(m)的氨基是质子化的,其氨基正离子上面的715H向手性碳迁移的趋势较强。此过程过渡态是5元环结构,内含2个氢键,氢键键角709C-733H-735O和735O-720H-713N分别是141.10°和140.19°,相对平角180°差距很大,氢键相对较弱,过渡态不稳定。因此,aTS2·1H2O@MOR会产生较高的能垒。aINT2·1H2O(n)@MOR经过和aTS2·1H2O@MOR类似的过渡态aTS3·1H2O@MOR,实现了715H以水分子为媒介向手性碳的迁移,异构成中间体产物aRINT3·1H2O@MOR,完成手性转变。最后,aRINT3·1H2O@MOR经过和aSTS1·1H2O@MOR类似的过渡态aRTS4·1H2O@MOR,714H和720H翻转到纸面里侧,异构成产物aP_R-Lys·1H2O@MOR。
2个水分子助a通道上的手性转变反应历程见图2Y。反应机理基本雷同于前面1个水分子助反应的情况,这里不再详述。计算表明2个水分子助a通道上的手性转变反应最具优势,决速步能垒显著降低。这里对决速步的过渡态aTS2·2H2O@MOR结构进行详细分析,此过渡态是7元环结构,计算表明,其氢键键角709C-733H-738O、738O-734H-737O和737O-720H-713N分别是164.44°、164.30°和167.54°,接近平角180°,氢键较强,过渡态aTS2·2H2O@MOR要稳定许多,其产生的能垒会低于aTS2·1H2O@MOR的能垒。
在ONIOM(CAM-B3LYP/6-31G(d, p):UFF)理论水平,全参数优化a通道上的各个驻点包结物,在ONIOM(MP2/6-311++G(2df, pd):UFF)理论水平计算单点能。稳定点和过渡态包结物的几何结构以及过渡态在虚频下的振动模式见图2。对诸过渡态进行的频率分析和IRC计算,确认了诸过渡态的可靠性。各驻点包结物的吉布斯自由能热校正和过渡态虚频(Ima)见表1。驻点包结物的单点能,热校正的总吉布斯自由能和相对总吉布斯自由能见表1。
根据表1中的数据,绘制了标题反应在a通道上的吉布斯自由能势能面,见图3。
从图3看出,标题反应在a通道经过4个基元反应实现,第2基元反应为决速步骤。决速步能垒在2个水分子作氢迁移媒介时被降到101.9 kJ/mol,是由2个水分子构成的链作媒介,手性碳上的H向氨基氮713N迁移的过渡态产生的。与裸反应、限域在MOR分子筛和限域在水环境的此通道决速步能垒252.6、229.7和123.9 kJ/mol[6,8-9]相比较,均有不同程度的降低。结果表明:水与MOR分子筛复合环境对Lys分子的手性转变具有明显的共催化作用。从图3还可以看出,第3基元反应的产物中间体,会有一部分以产物存在。原因是第4基元反应的逆反应能垒在30 kJ/mol以下,尤其是1个水分子助反应时,逆反应能垒只有19.9 kJ/mol,这两个能垒很容易越过。对于101.9 kJ/mol的能垒通常情况下在生命体内是难以逾越的,如若考虑到生命体内温度的涨落、分子的频繁碰撞和某种催化酶的作用,此能垒有被逾越的可能。这说明S-Lys在生命体内可以缓慢地异构为R-Lys,人们应该适时地补充S-Lys,以满足生命体的需求。
Table 1 Thermal correction to gibbs free energy, transition state imaginary frequency, single point energies, thermal recalibration free energies, relative total free energies of the each stationary points in channel a of Lys chiral transition confined in water and MOR zeolite combined environment

StructuresGtc/(a.u)Esp/(a.u)Gtotal/(a.u)ΔGtotal/(kJ·mol-1)Ima/cm-1aS-Lys·1H2O@MOR0.17273-557.63865-557.465920.0aSTS1·1H2O@MOR0.17598-557.63817-557.462199.8245.89aSINT1·1H2O@MOR0.17669-557.64479-557.46810-5.7aTS2·1H2O@MOR0.17080-557.57907-557.40827151.41431.62aINT2·1H2O(m)@MOR0.17261-557.59661-557.42400110.1aINT2·1H2O(n)@MOR0.17190-557.59573-557.423830.0aTS3·1H2O@MOR0.16809-557.57742-557.4093338.11451.97aRINT3·1H2O@MOR0.17376-557.64364-557.46988-120.9aRTS4·1H2O@MOR0.16753-557.63349-557.46596-110.6543.90aP_R-Lys·1H2O@MOR0.17136-557.64488-557.47352-130.5aS-Lys·2H2O@MOR0.19537-633.98108-633.785710.0aSTS1·2H2O@MOR0.19230-633.97413-633.7818310.2454.52aSINT1·2H2O@MOR0.19920-633.98421-633.785011.8aTS2·2H2O@MOR0.19281-633.93904-633.74623103.71480.23aINT2·2H2O(m)@MOR0.19398-633.94661-633.7526386.7aINT2·2H2O(n)@MOR0.19571-633.94621-633.750500.0aTS3·2H2O@MOR0.19052-633.93276-633.7422421.71018.92aRINT3·2H2O@MOR0.19394-633.98006-633.78612-93.5aRTS4·2H2O@MOR0.19059-633.97270-633.78211-83.0269.57aP_R-Lys·2H2O@MOR0.19241-633.98495-633.79254-110.4
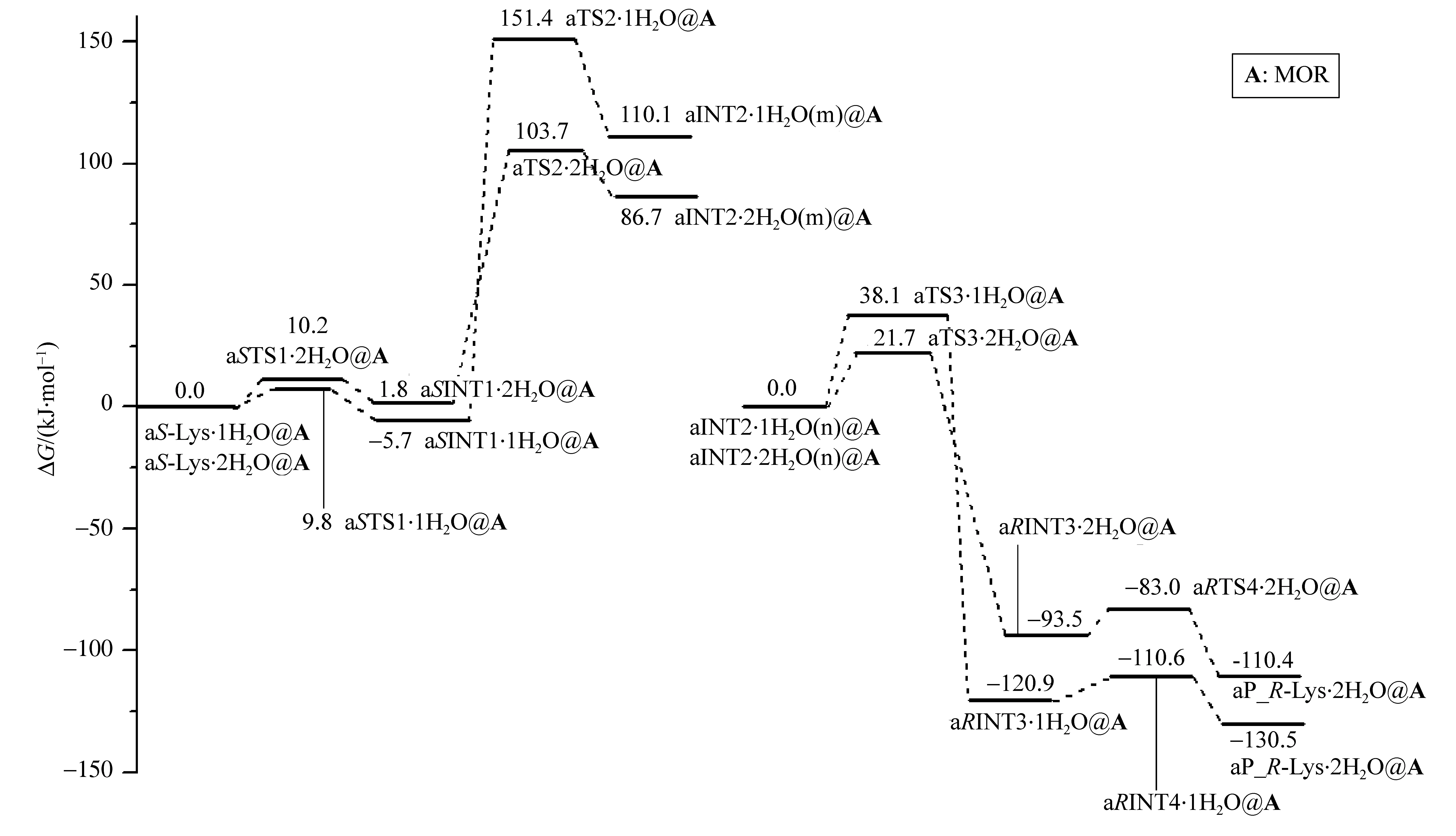
图 3 限域在MOR分子筛与水复合环境,S-Lys在a通道手性转变反应的自由能势能面示意图Fig.3 Gibbs free potential energy surfaces diagram of S-Lys chiral transition in the channel a confined in water and MOR zeolite combined environment
2.2 限域在MOR分子筛与水复合环境下的S-Lys在b和c通道手性转变步骤反应机理
S-Lys在b通道手性转变第1基元反应见图4:A。S-Lys与手性碳上的质子与羰基前面的1个和2个水分子以氢键结合的水和分子的包结物bS-Lys·1H2O@MOR和bS-Lys·2H2O@MOR,分别经过六元环和八元环结构的过渡态bTS1·1H2O@MOR和bTS1·2H2O@MOR异构成产物中间体包结物bINT1·1H2O@MOR和bINT1·2H2O@MOR(图4)。以后的过程分又为2个分路径b1和b2,b1是氨基先旋转异构,形成氨基氮的右侧易于接受质子的中间体b1INT2,然后质子化羧基上面的1个H以水分子为媒介向氨基氮迁移,形成中间体b1INT3的1水合物包结物,此中间体包结物即是a通道第2基元反应的产物中间体aINT2·1H2O@MOR。接下来的过程同aINT2·1H2O(n)@MOR以后的过程。b2是经过质子化羧基异构的过渡态b2TS2@MOR,羧基上的一个质子摆到纸面里,然后这个质子再在以水分子为媒介,经过和第1基元反应类似的过渡态b2TS3·1H2O@MOR和b2TS3·2H2O@MOR在纸面里侧迁移到手性碳,完成手性转变。篇幅所限,不对这两个分路径的反应进行详细讨论。
S-Lys在c通道手性转变的第1和第2基元反应见图4B。首先是S-Lys与羧基右侧的1个和2个水分子以氢键结合的水合分子包结物cS-Lys·1H2O@MOR和cS-Lys·2H2O@MOR,分别经过1个和2个水分子作氢迁移媒介的过渡态cTS1·1H2O@MOR和cTS1·2H2O@MOR,实现羧基内的质子迁移,异构成产物中间体包结物cINT1·1H2O(m)@MOR和cINT1·2H2O(m)@MOR,这时原来的羟基变成新的羰基。然后cINT1与其手性碳上的质子与新羰基前面的1个和2个水分子以氢键结合的水和分子的包结物cINT1·1H2O(n)@MOR和cINT1·2H2O(n)@MOR,分别经过图4所示的1个和2个水分子作质子迁移媒介的六元环和八元环结构的过渡态cTS2·1H2O@MOR和cTS2·2H2O@MOR,实现了质子从手性碳向新羰基的迁移,异构成产物中间体cINT2·1H2O@MOR和cINT2·2H2O@MOR,此时cINT2的羧基已经质子化。以后的过程是cINT2的羧基先异构,其上面的1个质子摆到纸面里,然后这个质子再在纸面里侧以水分子为媒介从质子化羧基迁移到手性碳,完成手性转变过程。篇幅所限,不对这两步反应进行详细讨论。
计算表明:b通道第1基元反应和c通道第2基元反应是对应反应通道的决速步。对决速步过渡态结构进行计算的数据显示:bTS1·1H2O@MOR的氢键键角709C-734H-732O是148.3°,732O-735H-717O是155.3°;bTS1·2H2O@MOR的氢键键角709C-734H-736O是160.9°,732O-735H-717O是171.3°,736O-738H-732O是164.5°,后者明显大于前者,更接近180°。所以bTS1·2H2O@MOR的结构比bTS1·1H2O@MOR稳定,产生的能垒要低些。cTS2·1H2O@MOR的氢键键角分别是151.7°和154.5°,cTS2·2H2O@MOR氢键键角分别是168.7°、170.3°和164.4°,后者明显大于前者,更接近180°。所以cTS2·2H2O@MOR的结构比cTS2·1H2O@MOR稳定,产生的能垒要低些。
在与前面相同的理论水平上,全参数优化b和c通道上1个和2个水分子助主要反应步骤的驻点包结物,进行单点能计算。得到b和c通道主要反应步骤各驻点包结物的几何构型以及过渡态在虚频下的振动模式,见图4的A与B。对诸过渡态的频率分析和IRC计算,确认了各个过渡态的可靠性。各驻点吉布斯自由能热校正和过渡态虚频(Ima)见表2。各个驻点的高水平单点能,热校正的总自由能和相对总自由能亦见表2。
根据表2的数据,绘制了Lys限域在MOR分子筛,在b和c通道水助手性转变主要反应过程的吉布斯自由能势能面示意图,见图5。
从上面的图5可以看出,标题反应在b通道决速步骤的能垒在以2个水分子为质子迁移媒介时被降到169.5 kJ/mol,是由质子H从手性碳向羰基氧迁移的过渡态产生的。比裸反应和只限域在MOR分子筛时此通道的决速步能垒327.1和277.5 kJ/mol[6, 9]均有大幅度的降低。标题反应在c通道的决速步骤能垒在以2个水分子为质子迁移媒介时被降到167.6 kJ/mol,是由质子H从手性碳向新羰基氧迁移的过渡态产生的。比裸反应和只限域在MOR分子筛时此通道的决速步能垒318.9和291.7 kJ/mol[6, 9]也均有大幅度的降低。说明MOR分子筛与水的复合环境对Lys在b和c通道的旋光异构均具有较好的共催化作用。与前面2.1的研究结果共同说明,MOR分子筛与水的复合环境可以作Lys旋光异构的理想纳米反应器。综合图3和5可知,a是主反应通道,第2基元反应是决速步骤,在2个水分子与MOR分子筛共催化作用下,决速步吉布斯自由能垒被降到最低值101.9 kJ/mol。

图4 限域在MOR分子筛的S-Lys,在b和c通道水助手性转变主要步骤Fig.4 The main steps of S-Lys water-assisted chiral transition in channel b and c confined in MOR zeolite
Table 2 Thermal correction to gibbs free energy, transition state imaginary frequency, single point energies, thermal recalibration free energies, relative total free energies of the each stationary points in channel b and c ofS-Lys chiral transition main steps confined in MOR zeolite

StructuresGtc/(a.u)Esp/(a.u)Gtotal/(a.u)ΔGtotal/(kJ·mol-1)Ima/cm-1bS-Lys·1H2O@MOR0.17271-557.63788-557.465170.0bTS1·1H2O@MOR0.16968-557.56225-557.39257190.61875.87bINT1·1H2O@MOR0.17326-557.60034-557.42708100.0bS-Lys·2H2O@MOR0.19830-633.97907-633.780770.0bTS1·2H2O@MOR0.19214-633.90834-633.71620169.51584.73bINT1·2H2O@MOR0.19777-633.94202-633.7442595.9cS-Lys·1H2O@MOR0.17562-557.64484-557.469220.0cSTS1·1H2O@MOR0.17071-557.62534-557.4546338.31429.56cSINT1·1H2O(m)@MOR0.17458-557.64366-557.469080.4cSINT1·1H2O(n)@MOR0.17153-557.63628-557.464750.0cTS2·1H2O@MOR0.16906-557.56169-557.39263189.41860.62cINT2·1H2O@MOR0.17028-557.59919-557.4289194.1cS-Lys·2H2O@MOR0.19762-633.98630-633.788680.0cSTS1·2H2O@MOR0.19075-633.96643-633.7756834.11091.78cSINT1·2H2O(m)@MOR0.19848-633.98689-633.788410.7cSINT1·2H2O(n)@MOR0.19771-633.97584-633.778130.0cTS·2H2O@MOR0.19341-633.90769-633.71428167.61540.90cINT2·2H2O@MOR0.19657-633.94119-633.7446288.0

图5 限域在MOR分子筛的S-Lys,在b通道水助手性转变决速步骤的自由能势能面示意图Fig.5 Gibbs free potential energy surfaces diagram of step-determining processes of S-Lys water-assisted chiral transition in channel b confined in MOR zeolite
3 结 论
结构分析表明:2个水分子比1个水分子助氢迁移反应的过渡态分子氢键键角显著增大,过渡态结构稳定,产生的能垒低。反应通道研究发现:标题反应有a、b和c三个通道,分别是赖氨酸在MOR分子筛限域环境下,水助质子以氨基、羰基和羟基为桥从手性碳的一侧迁移到另一侧,实现手性转变。反应势能面计算表明,a是主反应通道,质子从手性碳向氨基的迁移是决速步骤,在2个水分子助决速步时,吉布斯自由能垒被降到最低值101.9 kJ/mol,与裸反应、限域在MOR分子筛和限域在水环境的此通道决速步能垒252.6、229.7和123.9 kJ/mol相比较,均有明显降低。结果表明:水与MOR分子筛复合环境对赖氨酸手性转变具有较好的共催化作用。说明了S-Lys在生命体内可以缓慢地异构为R-Lys,因此,人们应该适时地补充S-Lys,以满足生命体的需求。实验上可以利用水与MOR分子筛复合环境来实现赖氨酸手性转变,从而可以廉价并环保地获得光学纯的赖氨酸。
[1] 王建军,王晓春,欧阳一山,等.用镧系位移试剂研究L-赖氨酸在水溶液中的结构[J].物理化学学报,1992, 8(5):647-653. WANG Jianjun, WANG Xiaochun, OUYANG Yishan, et al. Research on the structure ofL-lysine in aqueous solution with lanthanide shift reagent [J]. Journal of Physical Chemistry, 1992, 8(5): 647 -653.
[2] 李菁,刘骞,孔保华,等.L-赖氨酸与三种还原糖美拉德反应产物的理化特性及抗氧化活性的研究[J].食品科学, 2013, 34(3): 80-85. LI Jing, LIU Qian, KONG Baohua, et al. Research on the physicochemical properties and antioxidant activity ofL-lysine and three reaction products of sugar Maillard [J]. Food Science, 2013, 34 (3): 80-85.
[4] KIM S C,SPRUNG R, ZHAO Y M. Substrate and functional diversity of lysine acetylation revealed by a proteomics survey[J]. Molecular Cell, 2006, 23(4): 607-618.
[5] PAINTER P C, KOENIG J L. The solution conformation of poly(L-lysine): a Raman and infrared spectroscopic study[J]. Biopolymers, 1976, 15(2): 229-240.
[6] 刘凤阁,辛春雨,闫红彦,等.气相赖氨酸分子手性转变机制的理论研究[J].武汉大学学报(理学版), 2015,61(1): 93-98. LIU Fengge,XIN Chunyu,YAN Hongyan, et al. Theoretical research on chiral change mechanism of gaseous lysine molecules[J].J Wuhan Univ(Nat Sci Ed), 2015,61(1): 93-98.
[7] 刘凤阁,王佐成,梅泽民,等. 水环境下赖氨酸分子的手性转变机理[J].武汉大学学报(理学版), 2015,61(5): 491-496. LIU Fengge,WANG Zuocheng,MEI Zemin, et al. Chiral shift mechanism of lysine molecules under water enviroment [J].J Wuhan Univ(Nat Sci Ed), 2015,61(5):491-496.
[8] 王晓玲,高峰,佟华,等. 基于氨基作为质子转移桥梁的赖氨酸分子手性转变机理[J]. 吉林大学学报(理学版), 2016, 54(5): 1161-1167. WANG Xiaoling, GAO Feng, TONG Hua, et al. Chiral transition mechanism of lysine molecules based on amino as proton transfer bridge [J]. Journal of Jilin University(Science Edition), 2016, 54(5): 1161-1167.
[9] 闫红彦,梅泽民,王佐成,等. MOR分子筛对赖氨酸手性转变反应的限域催化 [J]. 吉林大学学报(理学版), 2016, 54(6): 1437-1444. YAN Hongyan,MEI Zemin,WANG Zuocheng , et al.The confined catalysis of the MOR zeolite on the lysine chiral transition reaction[J]. Journal of Jilin University(Science Edition), 2016, 54(6): 1437-1444.
[10] 王佐成, 梅泽民, 佟华,等. α-Ala限域在扶手椅型SWCNT(9,9)与水复合环境下的手性转变机制[J].复旦学报(自然科学版), 2015,54(1):107-118. WANG Zuocheng , MEI Zemin, TONG Hua, et al. The chiral shift mechanism of α-Ala confined in the complex environment of armchair SWCNT(9,9) and water[J]. Journal of Fudan University(Science Edition), 2015, 54(1): 107-118.
[11] 王佐成,高峰,佟华,等. α-丙氨酸限域在螺旋手性SWCNT(12,6)与水复合环境下的手性转变机理[J].复旦学报(自然科学版),2015,54(3):261-276. WANG Zuocheng, GAO Feng, TONG Hua, et al. The chiral transition mechanism of α-alanine confined in the chiral helicity SWCNT(12,6)/water complex environment [J]. Journal of Fudan University(Science Edition), 2015, 54(3): 261-276.
.[12] 梅泽民, 佟华,夏立利,等. α-丙氨酸限域在扶椅型SWBNNT(9,9)与水复合环境下的手性转变机制[J]. 中山大学学报(自然科学版),2015,54(3): 85-92. MEI Zemin, TONG Hua, XIA Lili, et al. Chiral transition mechanism of α-alanine confined in the armchair SWBNNT(9,9) /water complex environment [J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2015, 54(3): 85-92.
[13] 佟华,杨晓翠,闫红彦,等. α-Ala限域在螺手性SWBNNT(10,6)与水复合环境下的手性转变机理[J]. 复旦学报(自然科学版), 2015,54(4): 529-540. TONG Hua,YANG Xiaocui,YAN Hongyan,et al. Chiral transition mechanism of α-alanine confined in the armchair SWBNNT(10,6) /water complex environment [J]. Journal of Fudan University(Science Edition), 2015, 54(4): 529-540.
[14] 赵衍辉,程彦明,李忠,等. α-Ala限域在螺旋SWBNNT(10,5)与水复合环境的手性转变机理—基于氨基作H迁移桥梁[J].吉林大学学报(理学版), 2015, 53(6):1299-1307. ZHAO Yanhui, CHENG Yanming, LI Zhong, et al. Chiral transition mechanism of α-Ala molecule confined in the complex environment SWBNNT(10,5) and water [J]. Journal of Jilin University(Science Edition), 2015, 53(6):1299-1307.
[15] 孙永清,王佐成,高峰, 等. 水与MOR分子筛复合环境对布洛芬分子手性转变反应共催化的理论研究[J].复旦学报(自然科学版), 2016,55(5):818-828. SUN Yongqing, WANG Zuocheng, GAO Feng,et al.Theoretical research on the co-catalysis of water and MOR zeolite combined environment on the chiral transition of ibuprofen molecules[J]. Journal of Fudan University(Science Edition), 2016, 55(5):818-828.
[16] 李惊鸿,周丹红,任珏. Ga/HZSM-5分子筛上乙烯二聚反应的理论研究[J].物理化学学报,2011, 27(6):1393-1399. LI Jinghong, ZHOU Danhong, REN Jue. Theoretical study of ethylene dimerization on the Ga/HZSM-5 zeolite[J].Acta Phys-Chim Sin, 2011, 27(6):1393-1399.
[17] SVENSSON M, HUMBEL S, FROESE R D J, et al. ONIOM: A multilayered integrated MO + MM method for geometry optimizations and single point energy predictions. A test for Diels-Alder reactions and Pt(P(t-Bu)3)2+ H2oxidtivae addition[J]. Physical Chemistry, 1996, 100(50): 19357-19363.
[18] KOBAYASHI R, AMOS R D.Erratum to The application of CAM-B3LYP to the charge-transfer band problem of the zincbacteriochlorin-bacteriochlorin complex[J]. Chem Phys Letts, 2006, 420:106-109.
[19] YIN S W, DAHLBOM M G, CANFIELD P J, et al.Assignment of the Qy absorption spectrum of photosystem-I from thermosynechococcus elongatus based on CAM-B3LYP calculations at the PW91-optimized protein structure[J]. Phys Chem B, 2007, 111(33) : 9923-9930.
[20] RAPPE A K, CASEWIT C J, COLWELL K S, et al. UFF, a full periodic table force field for molecular mechanics and molecular dynamics simulations[J]. Journal of the American Chemical Society, 1992, 114(25): 10024-10053.
[21] GARRETT B C, TRUHLAR D G. Generalized transition state theory. Classical mechanical theory and applications to collinear reactions of hydrogen molecules[J]. Journal of Physical Chemistry, 1979, 83(8): 1052-1079.
[22] GARRETT B C, TRUHLAR D G. Criterion of minimum state density in the transition state theory of bimolecular reactions[J]. The Journal of Chemical Physics, 1979, 70(4): 1593-1598.
[23] 徐光宪,黎乐民,王德民. 量子化学(中册)[M]. 北京:科学技术出版社,1985: 962-986.
[24] BINKLEY J S, POPLE J A. Moeller-Plesset theory for atomic ground state energies[J]. Int J Quantum Chem, 1975, 9(2):229-236.
[25] ISHIDA K, MOROKUMA K, KOMORNICKI A. The intrinsic reaction coordinate. Anabinitiocalculation for HNC→HCN and H-+ CH4→CH4+ H-* [J]. The Journal of Chemical Physics, 1977, 66(5):2153-2156.
[26] FRISCH M J, TRUCKS G W, SCHLEGEL H B, et al. Gaussian 09. Revision D.01 [CP]. Pittsburgh U S A: Gaussian, Inc, Wallingford CT, 2013.
Theoretical study on the co-catalysis of MOR zeolite and water combined environment on the chiral transition of lysine molecules
LIUYixuan1,WANGZuocheng2,DONGLirong3,ZHAOXiaobo2,YANGXiaocui2,TONGHua2
(1. Haikou College of Economics, College of Marxism, Natural Science Instruction, Haikou 570100, China; 2.College of Physics, Baicheng Normal University, Baicheng 137000, China; 3.College of Physics, Jilin Normal University, Siping 136000, China)
The chiral transition of lysine molecules confined in water and MOR zeolite combined environment was studied in the paper by introducing the ONIOM methods using combination of quantum mechanics and molecular mechanics. The molecular structure researches show that hydrogen bond angle of the transition state molecules in the hydrogen transfer reactions with the help of two water molecules is significantly larger than that with the help of one water molecule. The study of reaction channels shows there are three channels a, b and c in the title reaction where lysine is confined in MOR zeolite, protons transfer with the help of water molecules from one side to the other of the chiral C with amino, carbonyl and hydroxyl as a bridge, and at last the chiral transition is achieved. Calculations of potential energy surface show that channel a is the dominant reaction path and protons transfer the chiral C to amino is the step-determining where gibbs free energy barrier of two water-assisted proton transfers reaction is reduced to the minimum value 101.9 kJ·mol-1, that is significantly lower than the gibbs free energy barrier 252.6, 229.7 and 123.9 kJ·mol-1, respectively corresponding to the bare reaction, confined in MOR zeolite and confined in water environment. The results show that water and MOR zeolite combined environment has a good co-catalysis on the chiral transition of lysine molecules, and S-Lys in vivo can be slowly optical isomerism.
MOR zeolite; lysine; chiral transition; our own n-layered integrated molecule orbit and molecule mechanics methods; density functional; transition state
2016-06-20 基金项目:吉林省科技发展计划资助项目自然科学基金(20160101308JC)
刘逸轩(1983年生),男; 研究方向:原子与分子物理; E-mail:116999592@qq.com
王佐成(1963年生),男;研究方向:原子与分子物理; E-mail:wangzc188@163.com 佟华(1970年生),女;研究方向:原子与分子物理; E-mail:tonghua699@126.com
10.13471/j.cnki.acta.snus.2017.01.003
O641.12
A
0529-6579(2017)01-0014-10

