糖类衍生物催化制备含氧液体燃料和精细化学品
王英雄,侯相林,朱玉雷
中国科学院山西煤炭化学研究所,山西省生物炼制工程技术研究中心,太原 030001
糖类衍生物催化制备含氧液体燃料和精细化学品
王英雄,侯相林,朱玉雷
中国科学院山西煤炭化学研究所,山西省生物炼制工程技术研究中心,太原 030001

朱玉雷,中国科学院山西煤炭化学研究所研究员、博士生导师。从事精细化学品和可再生能源的多相催化反应研究,解决了加氢、脱氢、耦合反应过程中的关键技术问题,相关新型成果成功地应用于企业。作为项目负责人和研究骨干完成了多项国家基金、“863”和“973”项目。获得2004年中国石化协会技术发明一等奖(第二完成人),2005年国家技术发明二等奖(第一完成人),2005年中国科学院杰出科技成就奖(集体),2013年山西省自然科学二等奖(第一完成人)。2006年获国务院特殊专家津贴。以第一作者和通讯作者,在ACS Catal., Chem. Commun., J. Catal., Green Chem.等专业刊物上发表论文100多篇,授权专利20余项。E-mail:zhuyulei@sxicc.ac.cn
通过生物炼制获取液体燃料和化学品是缓解当前能源危机的有效途径。概述了木质纤维素和甲壳素综合利用方面的研究进展。重点介绍了笔者研究团队在平台化合物加氢制液体燃料、甲壳素类生物质制含氮杂环精细化学品方面的研究成果,并展望了该领域未来的发展方向。
生物炼制;木质纤维素;甲壳素;平台化合物;精细化学品;液体燃料
能源、化学品和材料是工业社会的必需物资。当前经济发展对能源需求不断攀升,而生物圈内探明储量的石化资源却日趋减少,能源供给形势严峻。此外,CO2大规模排放引起的“温室效应”已影响到人类赖以生存的环境。研发可再生资源正受到各国政府的普遍关注。鉴于生物质资源的可持续性、使用过程不增加CO2净含量等优点,以其为原料通过生物炼制获取液体燃料和化学品,是当前能源化工领域的研究前沿[1-2]。当前的研究主要集中在木质纤维素类生物质和甲壳素类生物质两方面(图1)。以木质纤维素类生物质为原料可获得5-羟甲基糠醛(HMF)、乙酰丙酸(LA)等平台化合物[3-5]。其中HMF可进一步转化为其他化学中间体和含氧燃料添加剂等[6-10]。LA作为重要的化工原料常用于合成多种精细化学品、液体燃料[11]。甲壳素类生物质是储量仅次于纤维素的第二大类生物质资源,也是自然界中除蛋白质外,数量最大的天然含氮有机化合物[12]。全球渔业产生的甲壳素每年大约可达100亿吨[13]。以甲壳素类生物质为原料转化为高附加值的化学品,对于其资源化利用、缓解日益严峻的环境问题也具有重要意义[14]。本文将论述近年来木质纤维素和甲壳素类生物质转化制备燃料和精细化学品两方面的研究进展,并对其未来发展趋势做前瞻性预测和评述。

图1 纤维素和甲壳素类生物质及其单体化合物的结构
1 木质纤维素类生物质转化
1.1 糖类化合物制备HMF的研究
以非食用的纤维素及其单体葡萄糖和果糖为原料转化HMF,大多使用质子酸或固体酸为催化剂,采用合适的反应介质,最高的HMF收率为80%~90%,反应选择性达到90%以上[3,15-16]。近年来,金属卤化物作为该类转化反应的催化剂,离子液体作溶剂或直接起催化作用的研究也受到越来越多的关注[17]。Zhao等[18]在离子液体中用CrCl2作催化剂,提出了金属离子可以促进葡萄糖异构化为果糖,果糖在酸性条件下就更容易转化为HMF,这一发现为制备HMF开拓了新思路。Hu等[19-20]研究了离子液体对以葡萄糖、果糖、菊糖为原料转化为HMF的影响。研究表明离子液体对该类转化反应都具有较好的促进作用。当以SnCl4为催化剂,1-乙基-3-甲基-咪唑四氟硼酸盐([B MIM]BF4)离子液体为溶剂时,Hu等提出Sn4+与葡萄糖之间形成的五元环络合物对葡萄糖的转化发挥了关键作用,且[BMIM]BF4/SnCl4体系对果糖、蔗糖、菊糖、纤维二糖、淀粉等也有部分相同的催化作用。Deng等[21]也对糖类化合物在ZnCl2的水溶液中转化为HMF进行了研究。实验表明,63%(质量分数)ZnCl2水相体系中Zn2+与糖类化合物的络合有利于它们异构化为果糖,再进一步转化为HMF,提出了水相体系中不完全配位的锌离子是催化葡萄糖等异构化为果糖的催化中心,而且该水相氯化锌反应体系也适用于纤维素和淀粉等糖类大分子水解为低聚合度的糖(图2)。
1.2 糖类化合物制备LA的研究
与HMF制备过程相比,LA的制备过程需要在相对较强的酸性条件下完成,但工艺参数易于控制,在生物质资源制备HMF过程中,通常伴随着HMF经水合反应转化为LA和甲酸的副反应。笔者团队近期开展了利用菊粉类生物质生产HMF或LA的研究,通过加入助催化剂SnCl4,可调控主产物由HMF逐渐转为LA,LA收率可达25.7%,并通过原位核磁共振技术跟踪反应,验证了LA是由HMF进一步水合生成[10]。
1.3 平台化合物HMF和LA转化制含氧液体燃料
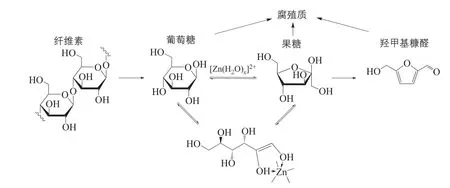
图2 纤维素类生物质转化为HMF路径及Zn2+与糖类化合物的络合作用
平台化合物HMF可催化转化为多种化学品(图3),因此,HMF被称为“沉睡的巨人”[22]。近年来,笔者研究团队构建了高效的非贵金属催化剂体系,实现HMF加氢和氢解过程,揭示了其催化反应的基本规律。研究团队以商用的雷尼金属催化剂(Raney Ni,Raney Co,Raney Cu)催化HMF加氢,研究结果表明非贵金属催化剂在该反应中具有很好的应用前景。其中以Raney Ni为催化剂,100℃条件下,获得收率为96%的2,5-二羟甲基四氢呋喃;180℃条件下,获得收率为88.5%的2,5-二甲基呋喃[23]。为促进C=O/C—O氢解过程,提高Ni基催化剂的性能,研究团队还以类水滑石为催化剂前驱体,构建了高分散的Ni-Al2O3金属-酸双功能体系,通过调变Ni活性位数目改变催化剂酸强度,最终以NiAl-850为催化剂获得了较高的2,5-二甲基呋喃收率(91.5%)。随着反应时间的延长,2,5-二甲基呋喃收率逐渐减少,2,5-二甲基四氢呋喃收率逐渐增加,反应20h,以NiAl-850为催化剂实现了97.4%的2,5-二甲基四氢呋喃收率[24]。另外,还以蒸氨法制备了页硅酸镍材料(NiSi-PS)用于羟甲基糠醛氢解制呋喃燃料,该催化剂可在130~150℃条件下高效催化合成呋喃燃料,收率可达90.2%,这是目前文献报道的非贵金属催化剂催化5-HMF转化的最低反应温度[25]。
笔者团队在LA加氢制备含氧液体燃料γ-戊内酯(GVL)方面也取得了一系列重要进展。团队以Ru为催化活性中心,在水相介质中研究了LA加氢制GVL,收率可达99.9%。较高的产品收率可能源于水能够促进氢溢流的发生,提高催化剂加氢活性。2H同位素标记实验(图4)证明水通过嵌入LA的羰基位置(即图4中GVL的C5位置)参与了反应过程[26]。
图3 平台化合物HMF转化为含氧燃料分子示意图

图4 水促进LA加氢的反应机理研究
针对水相加氢反应中催化剂不稳定的问题,团队设计了稳定性高、低温催化加氢活性高的固载型r-Ru-NH2-γ-Al2O3催化剂,借助有机硅对金属氧化物载体表面进行改性,解决了水相中金属氧化物载体不稳定导致催化剂的失活问题,同时可提高催化剂的低温加氢活性[27]。基于载体与活性 金属的强相互作用以及载体的电子效应显著影响催化剂活性的思路,笔者团队还以富含π电子的石墨烯为载体,通过原位还原法设计制备了新型Ru/石墨烯(RGO)催化剂。反应温度为-10℃,Ru/RGO催化剂可以高效催化LA加氢制GVL,收率高达70.5%,这是多相催化加氢反应中所报道的最低温度[28]。
近期,笔者团队开创性地在水/γ-丁内酯体系中,以磷钨酸和负载型Ru为共催化剂,通过精准调变溶剂碱性,成功将六碳糖(果糖、葡萄糖、蔗糖、菊粉、淀粉、纤维素)经LA转化为GVL,反应温度为130℃,H2压力为4MPa时,GVL的收率可达55.1%[29]。后续研究工作中,团队以Hβ分子筛为催化剂,选择性断裂六碳糖中的C—C键形成五碳糖,进而转变为糠醛。反应温度为150℃,分别以果糖和葡萄糖为原料,糠醛收率分别可达63.5%和56.5%。该研究工作首次实现了由纤维素类六碳糖生物质制五碳平台化合物糠醛。糠醛通常由生物质原料中的半纤维素组分脱水制备。原料中含量更高的纤维素等六碳糖使用现有生产工艺无法转化,被当为固体残留物(糠醛渣)废弃。该研究工作有望克服当前糠醛生产工艺中面临的资源浪费和环境污染问题[30]。
2 甲壳素类生物质转化
2.1 甲壳素类生物质转化制HMF和LA
近年来,利用甲壳素类生物质为原料制平台化合物的研究越来越受到关注。Kerton等[31]报道了水溶液在微波加热的条件下,以Lewis酸SnCl4·5H2O为催化剂,将壳聚糖选择性地转化为高附加值平台化合物HMF和LA。Wang等[7]将67%(质量分数)ZnCl2水溶液作为催化剂和溶剂,研究了甲壳素生物质转化制HMF,当用硼酸做催化剂时,HMF收率较高(21.9%)。Li等[32]研究了以咪唑衍生物类离子液体为催化剂,在水溶液中催化甲壳素生物质转化生成HMF,发现以N-甲基咪唑硫酸氢盐([MIM]HSO4)离子液体催化剂,以壳聚糖为反应原料,反应温度为180℃,得到HMF的收率为30%。
甲壳素生物质还可转化为LA、乙酸等化合物。Szabolcs等[33]发现在微波加热的条件下,盐酸有利于低聚合度的壳聚糖和单体氨基葡萄糖、乙酰氨基葡萄糖(GlcNAc)的水解,而硫酸更有利于甲壳素的降解,通过条件优化,可得到较高收率的LA。Gao等[34]在300℃NaOH溶液中加入氧化铜为催化剂,通入氧气,以甲壳素为原料转化得到乙酸的最高收率为38%,在同样条件下以未处理的虾壳粉末为原料得到的乙酸的收率高达48%,推测虾壳中的蛋白质成分可以促进乙酸的形成。上述研究为甲壳素类生物质的资源化利用提供了一条有效途径。
2.2 甲壳素或壳聚糖水解制氨基糖和氨基糖醚
甲壳素或壳聚糖水解可得到氨基糖[7],例如GlcNAc、氨基葡萄糖(GlcNH2)以及壳寡糖[35]。这些氨糖类化合物被广泛用于食品、生物医学和制药领域[36]。Ajavakom等[37]用微波和超声波来辅助甲壳素水解制备单糖,研究发现微波加热能够将反应效率提高10倍,此外超声波可促进甲壳素的溶解。在另外一项工作中,在1-丁基-3-甲基咪唑氯盐([BMIM]Cl)离子液体溶液中,6%(质量分数)的盐酸,反应温度为100℃,反应时间为7h,壳聚糖解聚制备还原糖的收率为60%[38]。
Fukuoka等[39]报道了结合物理和化学方法可选择性水解甲壳素制单糖GlcNAc。甲壳素首先被浸渍上催化量的硫酸,在无溶剂条件下球磨机转速设定为500r/min,球磨6h后,可获得100%溶解产物,包括单体GlcNAc(4.7%),二聚乙酰氨基葡萄糖[(GlcNAc)2, 7.8%],三聚乙酰氨基葡萄糖[(GlcNAc)3,11%],四聚乙酰氨基葡萄糖[(GlcNAc)4,9.7%],五聚乙酰氨基葡萄糖[(GlcNAc)5,8.6%],以及其他长支链的低聚物。物理机械作用力与化学催化方法产生的协同效应,有助于甲壳素解聚,且分子结构中的乙酰氨基官能团几乎全部保留。考虑到甲壳素或壳聚糖的单体在水溶液中不稳定,Yan等[40]发现可以用醇解甲壳素代替水解,以8%(质量分数)的硫酸为催化剂,得到的主要产品是羟乙基-2-氨基-2-脱氧己吡喃糖苷(HADP)和羟乙基-2-乙酰氨基-2-脱氧己吡喃糖苷(HAADP),两种产物的合计收率为30%左右。最近,该团队又报道通过甲酸液化甲壳素制备氨基糖衍生物[41]。反应温度为100℃,反应时间为12h,可获得收率超过60%的各种甲酸衍生的GlcNAc。
2.3 氨基葡萄糖转化制吡嗪类杂环化合物
甲壳素类生物质可催化转化得到含氮类多羟基烷基吡嗪衍生物(图5):脱氧果糖嗪(deoxyfructosazine,DOF)和果糖嗪(fructosazine,FZ)[42],它们可用作食品工业中的调味剂以及香料潜香物。此外,由于其结构的特殊性, DOF和FZ呈现出较强的生理活性和药用价值。许多研究表明这类化合物能预防和治疗糖尿病及其并发症,DOF具有一定的抗癌活性[43]。
Rohovec等[44]发现,在碱性水溶液中,以苯基硼酸为催化剂,GlcNH2可转化制备DOF,收率高达58%,其中也会产生少量的FZ。从硼谱(11B NMR)和碳谱(13C NMR)推断,硼酸可能会与反应底物GlcNH2形成硼酸酯,推测其主要是与糖环上C3和C4位的羟基及C2位的氨基络合。尽管该研究阐述了体系中存在硼酸络合作用,却没有提供证据证实硼酸络合位点以及络合比等问题。

图5 GlcNH2与GlcNAc转化为各种含氮类化学品结构示意图
Candiano等[45]研究发现GlcNH2与赖氨酸在模拟生理环境的水溶液中,可制备得到以FZ为主的多种化合物。1991年,Sumoto等[46]以28%(质量分数)的氨水溶液为碱性催化剂,催化转化GlcNH2,得到的主要产物为FZ。将1.0g氨基葡萄糖盐酸盐(GlcNH2·HCl)溶解到10mL浓度为28%(质量分数)的氨水溶液中,在室温条件下搅拌反应溶液,经过3周的反应,可制备收率为47%的FZ。

图6 GlcNH2选择性生成DOF和FZ的机理路径
近年来,笔者团队发展了以离子液体为新型绿色催化剂,定向转化GlcN H2制备DOF和FZ的系列工作。2014年,笔者团队首次发现以碱性离子液体氢氧化1-丁基-3-甲基-咪唑([BMIM]OH)为催化剂兼溶剂,GlcNH2可自聚合形成吡嗪类化合物DOF和FZ。通过优化反应工艺参数,发现在120℃,产品总收率最高可达49%[47]。随后,在DMSO体系中,以1-乙基-3-甲基-咪唑乙酸盐([C2C1Im][OAc])为催化剂,利用液体核磁共振技术探讨了离子液体催化剂的微观催化机制。阐明了离子液体[C2C1Im] [OAc]会与底物糖分子GlcNH2上的活泼氢基团发生强的氢键作用并促进GlcNH2构型由α向β转变,转变过程中可能经历的开链结构是GlcNH2制DOF和FZ的糖构型,因此,强的氢键作用是该催化反应能够发生的内在推动力[48]。在此基础上,对该反应的催化反应机理进行了探讨。高温原位核磁共振技术与同位素标记实验相结合,成功地捕获到了反应中间体二氢果糖嗪,并揭示了从中间体出发的两条平行竞争的反应路径。进一步结合量子化学计算,探讨了离子液体[C2C1Im][OAc]的酸碱协同催化作用[49]。基于以上反应机理,通过加入添加剂,可选择性调控反应产物分布。实验发现,加入添加剂B(OH)3,可显著促进脱水过程,从而选择性生成DOF;而以H2O2为添加剂,可明显促进脱氢过程,从而使FZ为反应的主要产物。通过核磁共振实验发现,B(OH)3与GlcNH2会发生分子间络合作用,硼络合物为反应的主要中间产物,并通过质谱结果得出其络合比为1∶1。由DFT理论计算得知中间产物二氢果糖嗪的脱水过程是控制整个反应的关键步骤,硼酸的络合可显著降低该脱水反应能垒,从而有利于脱水产物DOF的生成[50]。反应的完整机理路径如图6所示。
2.4 甲壳素及乙酰氨基葡萄糖转化制含氮呋喃衍生物
甲壳素及其单体化合物GlcNAc可制备含氮精细化学品3-乙酰氨基-5-乙酰呋喃(3A5AF,图5),3A5AF是抗生素proximicin A[51]、生物碱hyrtioseragamine A和B[52]等药物分子的前体。Kerton等[53]首次提出将甲壳素的单体GlcNAc,高效催化转化制3A5AF。相对惰性的乙酰氨基官能团不参与化学反应过程,因此会保留在产物结构中。实验发现,将硼酸分散在1-丁基-3-甲基-咪唑氯盐([BMIM]Cl)离子液体中,在微波照射条件下,GlcNAc可转化为3A5AF,收率高达60%。进一步研究发现,在微波加热条件下,反应温度为220℃,反应时间为15min,以硼酸和氯化钠为添加剂,在二甲基乙酰胺溶液中,可制备得到3A5AF,收率高达62%[54]。上述反应的可能路径为,吡喃糖环经开环得到开链醛糖,其经过闭环形成五元环呋喃结构;呋喃环结构氨糖脱除三分子水可得到目标产物3A5AF。此外,该研究工作还推断硼酸可能与反应底物上的活泼羟基发生相互作用,进而影响反应。
受Kerton工作的启发,Yan等[55]首次发现可将甲壳素直接转化为3A5AF。然而,由于甲壳素分子具有高结晶结构和大分子量,导致直接转化甲壳素制备含氮化学品过程挑战大。研究结果表明,反应温度为220℃时,甲壳素的转化率接近50%,3A5AF的收率仅为7.5%。此外,结合核磁共振的一维氢谱(1H NMR),11B NMR和13C NMR,证明硼酸与乙酰氨基葡萄糖之间的络合作用。13C NMR实验发现,在硼酸条件下,GlcNAc的α-构型向β-构型转化。因此,硼酸可以有效地促进糖开环,进而促进产物3A5AF的生成。
3 展 望
近年来以纤维素和甲壳素为原料,通过生物炼制获取液体燃料和精细化学品,取得了显著的进展,部分精细化学品的生产已实现工业化。生物质资源必将在未来能源化工领域中占据越来越重要的地位。针对目前该领域尚存的若干技术局限,构建新型高效的催化剂体系,如负载型功能化离子液体或双功能催化剂,实现生物质大分子一步法制备高附加值化学品,是今后研究的必然发展趋势。此外,开发绿色化、高效化以及价格低廉的新型溶剂体系,有利于促进生物质转化、便于后期产品分离,也是研究人员将长期关注的方向之一。
[1] RINAL DI R,SCHÜTH F. Design of solid catalysts for the conversion of biomass[J]. Energy & Environmental Science,2009,2(6):610-626.
[2] ZAKRZ EWSKA M E,BOGEL-LUKASIK E,BOGEL-LUKASIK R. Ionic liquid-mediated formation of 5-hydroxymethylfurfural-a promising biomass-derived building block[J]. Chemical Reviews,2011,111(2):397-417.
[3] CHHED A J N,HUBER G W,DUMESIC J A. Liquid-phase catalytic processing of biomass-derived oxygenated hydrocarbons to fuels and chemicals[J]. Angewandte Chemie International Edition,2007,46(38):7164-7183.
[4] ALONS O D M,WETTSTEIN S G,DUMESIC J A. Bimetallic catalysts for upgrading of biomass to fuels and chemicals[J]. Chemical Society Reviews,2012,41(24):8075-8098.
[5] CAES B R,TEIXEIRA R E,KNAPP K G,et al. Biomass to furanics:renewable routes to chemicals and fuels[J]. ACS Sustainable Chemistry & Engineering,2015,3(11):2591-2605.
[6] VAN P UTTEN R J,VAN DER WAAL J C,DE JONG E,et al. Hydroxymethylfurfural,a versatile platform chemical made from renewable resources[J]. Chemical Reviews,2013,113(3):1499-1597.
[7] WANG Y X,PEDERSEN C M,DENG T S,et al. Direct conversion of chitin biomass to 5-hydroxymethylfurfural in concentrated ZnCl2aqueous solution[J]. Bioresour Technol,2013,143:384-390.
[8] WANG H L,KONG Q Q,WANG Y X,et al. Graphene oxide catalyzed dehydration of fructose into 5-hydroxymethylfurfural with isopropanol as cosolvent[J]. ChemCatChem,2014,6(3):728-732.
[9] LV G Q,WANG H L,YANG Y X,et al. Graphene oxide:a convenient metal-free carbocatalyst for facilitating aerobic oxidation of 5-hydroxymethylfurfural into 2,5-diformylfuran[J]. ACS Catalysis,2015,5(9):5636-5646.
[10] WANG Y X,PEDERSEN C M,QIAO Y,et al. In situ NMR spectroscopy:inulin biomass conversion in ZnCl2molten salt hydrate medium-SnCl4addition controls product distribution[J]. Carbohydr Polym,2015,115:439-443.
[11] SEN S M,HENAO C A,BRADEN D J,et al. Catalytic conversion of lignocellulosic biomass to fuels:process development andtechnoeconomic evaluation[J]. Chemical Engineering Science,2012,67(1):57-67.
[12] KERT ON F M,LIU Y,OMARI K W,et al. Green chemistry and the ocean-based bioref nery[J]. Green Chemistry,2013,15(4):860-871.
[13] YAN N,CHEN X. Don’t waste seafood waste[J]. Nature,2015,524(7564):155-157.
[14] SHEL DON R A. Green and sustainable manufacture of chemicals from biomass:state of the art[J]. Green Chemistry,2014,16(3):950-963.
[15] ROMA N-LESHKOV Y,CHHEDA J N,DUMESIC J A. Phase modifiers promote efficient production of hydroxymethylfurfural from fructose[J]. Science,2006,312(5782):1933-1937.
[16] TAKA GAKI A,OHARA M,NISHIMURA S,et al. A one-pot reaction for bioref nery:combination of solid acid and base catalysts for direct production of 5-hydroxymethylfurfural from saccharides[J]. Chem Commun(Camb),2009,41:6276-6278.
[17] STAH LBERG T,RODRIGUEZ-RODRIGUEZ S,FRISTRUP P,et al. Metal-free dehydration of glucose to 5-(hydroxymethyl)furfural in ionic liquids with boric acid as a promoter[J]. Chemistry,2011,17(5):1456-1464.
[18] ZHAO H B,HOLLADAY J E,BROWN H,et al. Metal chlorides in ionic liquid solvents convert sugars to 5-hydroxymethylfurfural[J]. Science,2007,316(5831):1597-1600.
[19] HU S Q,ZHANG Z F,SONG J L,et al. Efficient conversion of glucose into 5-hydroxymethylfurfural catalyzed by a common Lewis acid SnCl4in an ionic liquid[J]. Green Chemistry,2009,11(11):1746-1749.
[20] HU S Q,ZHANG Z F,ZHOU Y X,et al. Conversion of fructose to 5-hydroxymethylfurfural using ionic liquids prepared from renewable materials[J]. Green Chemistry,2008,10(12):1280-1283.
[21] DENG T S,CUI X J,QI Y Q,et al. Conversion of carbohydrates into 5-hydroxymethylfurfural catalyzed by ZnCl2in water[J]. Chem Commun,2012,48(44):5494-5496.
[22] LEWK OWSKI J. Synthesis,chemistry and applications of 5-hydroxymethylfurfural and its derivatives[J]. Arkivoc,2001,1:17-54.
[23] KONG X,ZHU Y F,ZHENG H Y,et al. Switchable synthesis of 2,5-dimethylfuran and 2,5-dihydroxymethyltetrahydrofuran from 5-hydroxymethylfurfural over Raney Ni catalyst[J]. RSC Adv,2014,4(105):60467-60472.
[24] KONG X,ZHENG R X,ZHU Y F,et al. Rational design of Ni-based catalysts derived from hydrotalcite for selective hydrogenation of 5-hydroxymethylfurfural[J]. Green Chem,2015,17(4):2504-2514.
[25] KONG X,ZHU Y F,ZHENG H F,et al. Ni nanoparticles inlaid nickel phyllosilicate as a metal-acid bifunctional catalyst for lowtemperature hydrogenolysis reactions[J]. ACS Catalysis,2015,5(10):5914-5920.
[26] TAN J J,CUI J L,DENG T S,et al. Water-promoted hydrogenation of levulinic acid to γ-valerolactone on supported ruthenium catalyst[J]. ChemCatChem,2015,7(3):508-512.
[27] TAN J J,CUI J L,DING G,et al. Eff cient aqueous hydrogenation of levulinic acid to γ-valerolactone over a highly active and stable ruthenium catalyst[J]. Catal Sci Technol,2016,6(5):1469-1475.
[28] TAN J J,CUI J L,CUI X J,et al. Graphene-modif ed Ru nanocatalyst for low-temperature hydrogenation of carbonyl groups[J]. ACS Catalysis,2015,5(12):7379-7384.
[29] CUI J L,TAN J J,DENG T S,et al. Conversion of carbohydrates to furfural via selective cleavage of the carbon—carbon bond:the cooperative effects of zeolite and solvent[J]. Green Chem,2016,18(6):1619-1624.
[30] CUI J L,TAN J J,DENG T S,et al. Direct conversion of carbohydrates to γ-valerolactone facilitated by a solvent effect[J]. Green Chem,2015,17(5):3084-3089.
[31] OMAR I K W,BESAW J E,KERTON F M. Hydrolysis of chitosan to yield levulinic acid and 5-hydroxymethylfurfural in water under microwave irradiation[J]. Green Chemistry,2012,14(5):1480-1487.
[32] LI M G,ZANG H J,FENG J X,et al. Efficient conversion of chitosan into 5-hydroxymethylfurfural via hydrothermal synthesis in ionic liquids aqueous solution[J]. Polymer Degradation and Stability,2015,121:331-339.
[33] SZAB OLCS A,MOLNAR M,DIBO G,et al. Microwave-assisted conversion of carbohydrates to levulinic acid:an essential step in biomass conversion[J]. Green Chemistry,2013,15(2):439-445.
[34] GAO X Y,CHEN X,ZHANG J G,et al. Transformation of chitin and waste shrimp shells into acetic acid and pyrrole[J]. ACS Sustainable Chemistry & Engineering,2016,4(7):3912-3920.
[35] CHEN X,YANG H Y,YAN N. Shell biorefinery:dream or reality?[J]. Chemistry-A European Journal,2016,22(28):13402-13421.
[36] YOON J H. Enzymatic synthesis of chitooligosaccharides in organic cosolvents[J]. Enzyme and Microbial Technology,2005,37(6):663-668.
[37] AJAV AKOM A,SUPSVETSON S,SOMBOOT A,et al. Products from microwave and ultrasonic wave assisted acid hydrolysis of chitin[J]. Carbohydrate Polymers,2012,90(1):73-77.
[38] ZHAN G Z H,LI C Z,WANG Q,et al. Efficient hydrolysis of chitosan in ionic liquids[J]. Carbohydr Polym,2009,78(4):685-689.
[39] YABU SHITA M,KOBAYASHI H,KUROKI K,et al. Catalytic depolymerization of chitin with retention of N-acetyl group[J]. ChemSusChem,2015,8(22):3760-3763.
[40] PIER SON Y,CHEN X,BOBBINK F D,et al. Acid-catalyzed chitin liquefaction in ethylene glycol[J]. ACS Sustainable Chemistry &Engineering,2014,2(8):2081-2089.
[41] ZHAN G J G,YAN N. Formic acid-mediated liquefaction of chitin[J]. Green Chem,2016,18(18):5050-5058.
[42] AGYE I-AYE K,CHIAN M X,LAUTERBACH J H,et al. The role of the anion in the reaction of reducing sugars with ammonium salts[J]. Carbohydrate Research,2002,337(21-23):2273-2277.
[43] ZHU A,HUANG J B,CLARK A,et al. 2,5-deoxyfructosazine,a D-glucosamine derivative,inhibits T-cell interleukin-2 production better than D-glucosamine[J]. Carbohydrate Research,2007,342(18):2745-2749.
[44] ROHOVEC J,KOTEK J,PETERS J A,et al. A clean conversion of D-glucosamine hydrochloride to a pyrazine in the presence of phenylboronate or borate[J]. Eur J Org Chem,2001,2001(20):3899-3901.
[45] CANDIANO G,GHIGGERI G M,GUSMANO R,et al. Reaction of 2-amino-2-deoxy-d-glucose and lysine:isolation and characterization of 2,5-bis(tetrahydroxybutyl)pyrazine[J]. Carbohydrate Research,1988,184:67-75
[46] SUMO TO K,IRIE M,MIBU N,et al. Formation of pyrazine derivatives from D-glucosamine and their deoxyribonucleic-acid(DNA)strand breakage activity[J]. Chemical & Pharmaceutical Bulletin,1991,39(3):792-794.
[47] JIA L Y,WANG Y X,QIAO Y,et al. Efficient one-pot synthesis of deoxyfructosazine and fructosazine from D-glucosamine hydrochloride using a basic ionic liquid as a dual solvent-catalyst[J]. RSC Adv,2014,4(83):44253-44260.
[48] JIA L,PEDERSEN C M,QIAO Y,et al. Glucosamine condensation catalyzed by 1-ethyl-3-methylimidazolium acetate:mechanistic insight from NMR spectroscopy[J]. Phys Chem Chem Phys,2015,17(35):23173-23182.
[49] JIA L Y,LIU X C,QIAO Y,et al. Mechanism of the self-condensation of GlcNH2:insights from in situ NMR spectroscopy and DFT study[J]. Applied Catalysis B:Environmental,2017,202:420-429.
[50] JIA L Y,ZHANG Z Z,QIAO Y,et al. Product distribution control for glucosamine condensation:nuclear magnetic resonance(NMR)investigation substantiated by density functional calculations[J]. Industrial & Engineering Chemistry Research,2017,56(11):2925-2934.
[51] WOLT ER F E,MOLINARI L,SOCHER E R,et al. Synthesis and evaluation of a netropsin-proximicin-hybrid library for DNA binding and cytotoxicity[J]. Bioorganic and Medicinal Chemistry Letters,2009,19(14):3811-3815.
[52] TAKAHASHI Y,LINUMA Y,KUBOTA T,et al. Hyrtioseragamines A and B,new alkaloids from the spongehyrtiosspecies[J]. Organic Letters,2011,13(4):628-631.
[53] DROV ER M W,OMARI K W,MURPHY J N,et al. Formation of a renewable amide,3-acetamido-5-acetylfuran,via direct conversion of N-acetyl-D-glucosamine[J]. RSC Advances,2012,2(11):4642-4644.
[54] OMAR I K W,DODOT L,KERTON F M. A simple one-pot dehydration process to convert N-acetyl-D-glucosamine into a nitrogen-containing compound,3-acetamido-5-acetylfuran[J]. ChemSusChem,2012,5(9):1767-1772.
[55] CHEN X,CHEW S L,KERTON F M,et al. Direct conversion of chitin into a N-containing furan derivative[J]. Green Chemistry,2014,16(4):22 04-2212.
The catalytic conversion of sugar derivatives to oxygen containing liquid fuel and fine chemicals
WANG Yingxiong,HOU Xianglin,ZHU Yulei
Shanxi Engineering Research Center of Bioref nery, Institute of Coal Chemistry, Chinese Academy of Sciences, Taiyuan 030001, China
Biorefinery is an accessible way to get liquid fuel and chemicals, which could resolve the current energy crisis eff ciently. In this review, the progress in the utilization of lignocellulose and chitin biomass is summarized. Herein, hydrogenation of platform compounds to get liquid fuels, and the preparation of nitrogen containing heterocyclic fine chemicals from chitin biomass carried out by the author 's team are highlighted. At the same time, the future development direction of bioref nery f eld is also discussed.
bioref nery; lignocellulosic biomass; chitin biomass; platform molecular; f ne chemicals; liquid fuel
10.3969/j.issn.1674-0319.2017.03.007
王英雄,博士,副研究员。主要从事生物质资源,尤其是甲壳素类含氮生物质资源催化转化制燃料和精细化学品研究。E-mail:wangyx@sxicc.ac.cn
国家重点基础研究发展计划项目“糖类衍生物催化制含氧燃料的基础研究”(2012CB215305)

