来那度胺联合地塞米松治疗复发难治性轻链淀粉样变性的疗效及安全性
陈文萃 黄湘华 王庆文 任贵生 李 婷 赵 亮 任 强 刘志红
·论 著·
来那度胺联合地塞米松治疗复发难治性轻链淀粉样变性的疗效及安全性
陈文萃 黄湘华 王庆文 任贵生 李 婷 赵 亮 任 强 刘志红
目的:观察来那度胺联合地塞米松(LD)治疗复发难治性轻链淀粉样变性(AL型)的临床疗效及安全性。 方法:收集2012年12月至2015年11月在南京总医院国家肾脏疾病临床医学研究中心接受LD治疗的复发难治性AL淀粉样变性患者的临床资料。回顾性分析血液学、器官反应情况及不良反应。 结果:共10例患者纳入研究,其中男性7例、女性3例,中位年龄为64.5(56.8,68.8)岁。7例患者纳入疗效分析,3例患者获得血液学应,其中1例获得完全缓解。7例患者均未获得肾脏反应,2例获得心脏反应。所有患者均存活,无血液学进展,2例心脏进展,1例进入终末期肾病。无一例发生血液学进展。3/4级不良反应发生率30%。 结论:LD方案作为复发难治性AL淀粉样变性患者的挽救治疗有一定的疗效且安全性较高,严重不良反应发生率较低。
轻链淀粉样变性 来那度胺 疗效 不良反应
轻链淀粉样变性(AL型)是由于克隆性增生的浆细胞产生过多的轻链异常折叠形成淀粉样物质沉积在组织器官,导致结构破坏及功能障碍的疾病[1]。目前治疗的主要目的是抑制单克隆淀粉样蛋白轻链产生,从而改善脏器功能、延长生存期[2]。现国内外报道AL淀粉样变性的主要治疗方案包括自体外周血干细胞移植(ASCT)、硼替佐米、沙利度胺等[3-7]。这些治疗方案的应用,提高了AL淀粉样变性患者的血液学及器官反应率和总体生存率(OS),改善了生存质量,但仍有部分患者,经上述治疗无效或复发,或因各种原因不适合继续采用上述方案治疗,需要寻求新的治疗手段。来那度胺是第二代免疫调节剂,它同时作用于异常增生的骨髓细胞及骨髓间质微环境,触发自然杀伤细胞并抑制调节性T细胞,降低细胞的免疫耐受,刺激细胞免疫对异常增生骨髓细胞的杀伤作用而发挥效应,最初应用于多发性骨髓瘤的治疗,并证实安全有效。早在2007年开始,国外有研究报道来那度胺单用或联合地塞米松、马法兰等药物治疗初治或复发难治性AL淀粉样变性,安全有效[8-11],国内尚无相关报道。因此,本研究观察了10例接受来那度胺治疗的复发难治性AL淀粉样变性患者,以探讨来那度胺联合地塞米松(LD)治疗中国复发难治性AL淀粉样变性患者临床疗效及安全性。
对象和方法
研究对象 2012年12月至2015年11月在南京总医院国家肾脏疾病临床医学研究中心确诊并治疗的复发难治性AL淀粉样变性患者共10例。
治疗方案 LD方案28d为1个疗程,共治疗12个疗程。根据估算的肾小球滤过率(eGFR)调整来那度胺和地塞米松的剂量(表1)。前一方案治疗至少3个月观察疗效,血液学复发或进展患者,立即切换为LD方案治疗;血液学稳定者,停药3个月作为洗脱期,再切换为LD方案。治疗期间根据不良反应调整来那度胺和地塞米松剂量;出现肌酐倍增或其他患者不能耐受的不良反应经减量若仍不能好转则停药,出现4级及以上不良反应或血液学进展则停药。

表1 根据eGFR调整的治疗方案
eGFR:估算的肾小球滤过率
其他治疗 治疗期间患者均预防性应用阿司匹林100 mg/d,及泮托拉唑肠溶胶囊40 mg/d(与地塞米松同服),同时酌情可予利尿、营养心肌、营养神经等对症支持治疗。
观察指标 观察LD治疗前后临床及实验室指标:血轻链、血清免疫固定电泳、血常规、血生化、24h尿蛋白定量、N端前脑钠肽(NT-proBNP)、肌钙蛋白T(TnT)、超声测肝右肋下最大斜径、心脏室间隔厚度及左室射血分数等,并根据EPI公式计算eGFR值。评价血液学及器官反应情况,记录不良反应。
相关标准及定义 难治性AL淀粉变性定义为:初治患者经初始方案治疗3个月后血液学及器官均无反应;复发指经治疗取得缓解后维持3个月以上,出现血液学和/或器官进展[12]。AL淀粉样变性的诊断、器官受累评价参考相关文献[13],并按照Mayo 2012分级系统将患者分为Ⅰ、Ⅱ、Ⅲ、Ⅳ级[14]。主要疗效评价分为血液学反应和器官反应两方面,血液学反应分为完全缓解(CR):血清及尿免疫固定电泳转阴,κ/λ轻链比值正常;接近完全缓解(VGPR):差异轻链(受累轻链与未受累轻链的差值,dFLC)<40 mg/L;部分缓解(PR):dFLC降低>50%;无反应(NR):未达到PR者。进展:CR患者,受累轻链翻倍,并且比值异常或重新检测到M蛋白;PR患者血轻链水平升高>基线值50%且大于100 mg/L和(或)血清M蛋白升高>50%并大于0.5 g/dl,或尿液M蛋白升高50%并>200 mg/d。器官反应具体见表2,疗效评判标准参考相关文献[12,15]。不良反应评价依据不良反应常见术语标准( CTCAE v4. 0)。
统计学方法 统计学分析采用SPSS 17. 0 统计学软件,正态分布的计量资料采用均数±标准差描述,非正态分布的计量资料采用中位数(四分位间距)描述,计数资料采用百分数描述。
结 果
一般资料 2012年12月至2015年11月期间,共10例患者接受LD方案治疗。所有患者均有肾脏受累,8例有心脏受累,6例有胃肠道受累,7例受累脏器≥3个。10例患者初治方案均为硼替佐米联合地塞米松(BD)。4例为难治患者,6例为复发患者。患者一般情况见表3。
临床及实验室检查 根据Mayo 2012分级系统,Ⅰ级6例,Ⅱ级2例,Ⅲ级2例。中位尿蛋白定量为4.57(3.09,6.55)g/24h,血清白蛋白30.9(26.7,41.2) g/L,eGRF 71.9(49.6,95.0) ml/(min·1.73m2),dFLC 104.45(82.28,131.13) mg/L。所有患者血清白细胞及血小板均正常,1例患者血红蛋白为80 g/L,余9例患者血红蛋白正常。10例患者治疗前实验室检查见表4。

表2 器官反应及进展标准
NT-proBNP:N端前脑钠肽;NYHA:纽约心脏协会;eGFR:估算的肾小球滤过率;CCr:肌酐清除率

表3 10例患者的一般资料
BD:硼替佐米+地塞米松;ASCT:自体外周血干细胞移植;TD:沙利度胺+地塞米松;MP:马法兰+泼尼松;NR:无反应;CR:完全缓解;VGPR:接近完全缓解;PR:部分缓解;LD:来那度胺+地塞米松;*:病例3、5既往BD治疗有效,因经费问题,不能继续BD治疗;病例6、7、8既往BD治疗出现神经毒性;病例10既往BD治疗无效;病例3因估算的肾小球滤过率(eGFR)<30 ml/(min·1.73m2)不能接受ASCT;病例6、8、9因年龄>65岁不能接受ASCT;病例7拒绝接受ASCT

表4 10例患者治疗前实验室检查情况
RBC:红细胞计数;eGFR:估算的肾小球滤过率;dFLC:差异轻链(受累轻链与未受累轻链的差值)
疗效及预后 10例患者中7例治疗3个疗程以上(其中6例完成12疗程治疗),纳入疗效分析,此7例患者均有肾脏及心脏受累,中位随访29(17.5,35)月。3例患者获得血液学反应,其中1例在LD治疗4个月后获得血液学CR,2例分别在治疗6个月及9个月获得血液学PR,其余4例患者血液学稳定,无1例进展,所有患者均存活。
7例患者均未获得肾脏反应,1例患者血清肌酐持续升高,在治疗后26月进入终末期肾病,余6例患者肾脏均存活。2例患者分别在4及8个疗程后获得心脏反应,NT-proBNP下降>30%(1例降至正常)。2例分别在3及7个疗程后心脏进展,NT-proBNP升高>30%,3例患者心脏稳定。获得心脏反应的2例患者1例血液学为CR,1例PR。
不良反应 10例患者治疗过程中不良反应发生率为80%,不良反应发生情况见表5。3级及以上不良反应少见,无治疗相关死亡发生。2例患者分别在服用1个及2个疗程后出现肌酐倍增,eGRF降至30 ml/(min·1.73m2)以下而停药;1例首次服药后出现严重喉头水肿(4级)而停药。3例患者需要减量,减量后,2例患者不良反应(1例为皮疹伴瘙痒,1例为头晕)好转并完成12疗程治疗,另1例(反复皮疹伴瘙痒)无缓解,治疗6个疗程后停药。
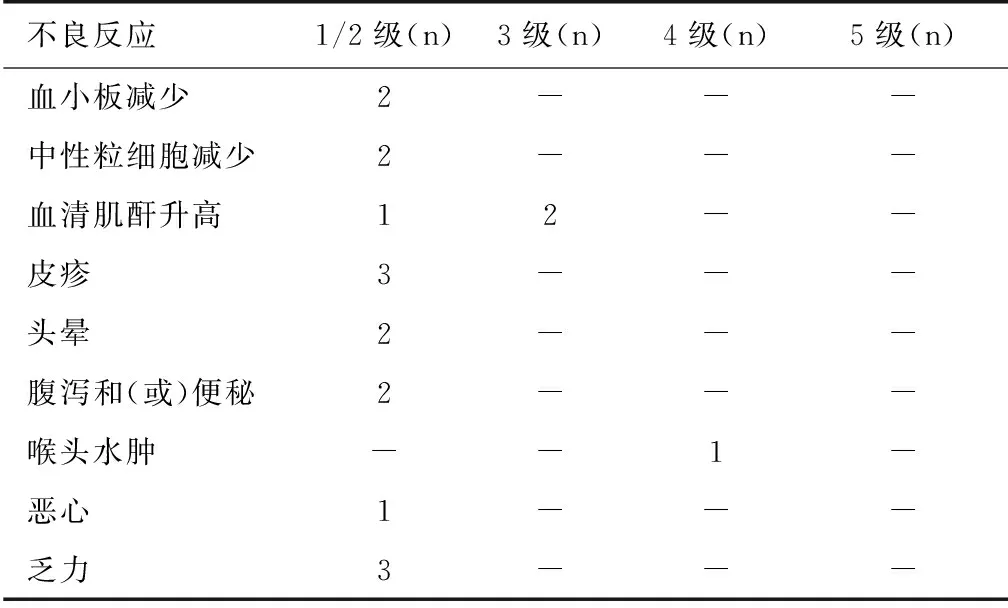
表5 治疗过程中不良反应发生情况
讨 论
随着AL淀粉样变性认识的深入,其诊断及治疗水平逐年提高,近年来硼替佐米、ASCT等治疗的应用,提高了患者的生存期及生活质量。但仍有部分患者经硼替佐米、ASCT、沙利度胺等治疗后复发,或对硼替佐米及ASCT等治疗无效,或因为体力状态、器官功能状态等原因不能接受上述方案治疗。该部分患者病情持续不缓解,器官功能下降明显,总体生存期缩短,需要寻求新的治疗方案。来那度胺在体外试验中其活性是沙利度胺的50~2 000倍,并且在多发性骨髓瘤的治疗中证实安全有效(包括部分对沙利度胺治疗无效的患者)。国外已有来那度胺单独或联合其他药物治疗AL淀粉样变性的相关研究[8-11,16-18],取得了一定的疗效,但国内尚无相关研究。
本研究为国内首次报道LD方案治疗复发难治性AL淀粉样变性的临床疗效及安全性。本研究中血液学ORR 42.9%,其中CR 1例,PR 2例,Palladini等[17]研究LD治疗复发难治的AL淀粉样变性患者,血液学ORR为41%,无CR患者,与本研究类似。而Dispenzieri等[8]采用LD治疗AL淀粉样变性(包括初治与复发难治患者),其ORR为39.1%,并且单用来那度胺的疗效低于LD。但Sanchorawala等[10]采用LD治疗AL淀粉样变性(包括初治与复发难治患者)其血液学ORR 67%(CR 29%)。Dispenzieri等[8]及Sanchorawala等[10]研究均示初治的患者反应率均高于非初治患者。器官反应率各个研究报道均不高,本研究中无1例获得肾脏反应,2/7例获得心脏反应,Palladini等[17]研究中1/16例获得心脏反应,Dispenzieri等[8]研究中5/22例获得器官反应。获得器官反应患者均获得了血液学反应。
本研究中不良反应发生率80%。3/4级不良反应类型与既往研究结果类似,但发生率(30%)低于既往研究[8,10,17]。可能与本研究在治疗前根据患者肾功能水平调整来那度胺和地塞米松剂量有关。本研究中性粒细胞、血小板减少及皮疹的发生率高于其他不良反应,但均为1/2级,且多在用药早期出现。这可能与我们在用药早期监测血常规及肝肾功能等指标频率较高有关,早期发现并处理,有效降低了严重不良反应发生率。但2例服药后短期内出现肌酐倍增患者,停药后虽然血清肌酐有所下降,但仍未能恢复至服药前水平,可能与患者基础肾功能差有关。在慢性肾功能不全基础上出现急性加重,因此虽发现后及时停药,但仍不能恢复至原有水平。
此外,既往国外有研究观察了来那度胺联合不同化疗药物治疗AL淀粉样变性的相关研究,如马法兰联合来那度胺及地塞米松(MLD)、环磷酰胺联合来那度胺及地塞米松(CLD)等,其血液学反应率均高于LD,但3/4级不良反应发生率明显升高,且骨髓抑制发生率及严重程度增加[9,11,16,18-19]。
本研究仍存在一些不足:(1)病例数比较少,随访时间不够长,未能得到总体生存期、疾病无进展生存期及相关危险因素等结果;同样,因病例数少,不能进行分组比较;(2)本研究为回顾性研究,结论存在一定局限性。
综上所述,本研究显示LD方案对复发难治性AL有一定的疗效,且安全性较高,3/4级反应发生率低,根据肾功能水平调整用药剂量及用药早期严密监测能降低严重不良反应发生率。LD方案可作为复发难治性AL淀粉样变性的挽救治疗。
1 Merlini G,Stone MJ.Dangerous small B-cell clones.Blood,2006,108(8): 2520-2530.
2 Palladini G,Lavatelli F,Russo P,et al.Circulating amyloidogenic free light chains and serum N-terminal natriuretic peptide type B decrease simultaneously in association with improvement of survival in AL.Blood,2006,107(10): 3854-3858.
3 Palladini G,Merlini G.Transplantation vs.conventional-dose therapy for amyloidosis.Curr Opin Oncol,2011,23(2): 214-220.
4 Jimenez-Zepeda VH,Franke N,Reece DE,et al.Autologous stem cell transplant is an effective therapy for carefully selected patients with AL amyloidosis: experience of a single institution.Br J Haematol,2014,164(5): 722-728.
5 Huang X,Wang Q,Chen W,et al.Induction therapy with bortezomib and dexamethasone followed by autologous stem cell transplantation versus autologous stem cell transplantation alone in the treatment of renal AL amyloidosis: a randomized controlled trial.BMC Med,2014.12: 2.
6 Palladini G,Perfetti V,Perlini S,et al.The combination of thalidomide and intermediate-dose dexamethasone is an effective but toxic treatment for patients with primary amyloidosis (AL).Blood,2005,105(7): 2949-2951.
7 陈文萃,黄湘华,张瑾等.自体外周血干细胞移植治疗原发性系统性淀粉样变性的中远期疗效观察.肾脏病与透析肾移植杂志,2016,25(4): 319-323.
8 Dispenzieri A,Lacy MQ,Zeldenrust SR,et al.The activity of lenalidomide with or without dexamethasone in patients with primary systemic amyloidosis.Blood,2007,109(2): 465-470.
9 Moreau P,Jaccard A,Benboubker L,et al.Lenalidomide in combination with melphalan and dexamethasone in patients with newly diagnosed AL amyloidosis: a multicenter phase 1/2 dose-escalation study.Blood,2010,116(23): 4777-4782.
10 Sanchorawala V,Wright DG,Rosenzweig M,et al.Lenalidomide and dexamethasone in the treatment of AL amyloidosis: results of a phase 2 trial.Blood,2007,109(2): 492-496.
11 Sanchorawala V,Patel JM,Sloan JM,et al.Melphalan,lenalidomide and dexamethasone for the treatment of immunoglobulin light chain amyloidosis: results of a phase II trial.Haematologica,2013,98(5): 789-792.
12 Comenzo RL,Reece D,Palladini G,et al.Consensus guidelines for the conduct and reporting of clinical trials in systemic light-chain amyloidosis.Leukemia,2012,26(11): 2317-2325.
13 Gertz MA,Comenzo R,Falk RH,et al.Definition of organ involvement and treatment response in immunoglobulin light chain amyloidosis (AL): a consensus opinion from the 10th International Symposium on Amyloid and Amyloidosis,Tours,France,18-22 April 2004.Am J Hematol,2005,79(4): 319-328.
14 Kumar S,Dispenzieri A,Lacy MQ,et al.Revised prognostic staging system for light chain amyloidosis incorporating cardiac biomarkers and serum free light chain measurements.J Clin Oncol,2012,30(9): 989-995.
15 Palladini G,Dispenzieri A,Gertz MA,et al.New criteria for response to treatment in immunoglobulin light chain amyloidosis based on free light chain measurement and cardiac biomarkers: impact on survival outcomes.J Clin Oncol,2012,30(36): 4541-4549.
16 Kumar SK,Hayman SR,Buadi FK,et al.Lenalidomide,cyclophosphamide,and dexamethasone (CRd) for light-chain amyloidosis: long-term results from a phase 2 trial.Blood,2012,119(21): 4860-4867.
17 Palladini G,Russo P,Foli A,et al.Salvage therapy with lenalidomide and dexamethasone in patients with advanced AL amyloidosis refractory to melphalan,bortezomib,and thalidomide.Ann Hematol,2012,91(1): 89-92.
18 Palladini G,Russo P,Milani P,et al.A phase II trial of cyclophosphamide,lenalidomide and dexamethasone in previously treated patients with AL amyloidosis.Haematologica,2013,98(3): 433-436.
19 Kastritis E,Terpos E,Roussou M,et al.A phase 1/2 study of lenalidomide with low-dose oral cyclophosphamide and low-dose dexamethasone (RdC) in AL amyloidosis.Blood,2012,119(23): 5384-5390.
(本文编辑 凡 心)
Efficacy and safety of lenalidomide with dexamethasone in relapse/refractory light-chain amyloidosis
CHENWencui,HUANGXianghua,WANGQingwen,RENGuisheng,LITing,ZHAOLiang,RENQiang,LIUZhihong
NationalClinicalResearchCenterofKidneyDiseases,JinlingHospital,NanjingUniversitySchoolofMedicine,Nanjing210016,China
Correspondingauthor:LIUZhihong(E-mail:liuzhihong@nju.edu.cn)
Objective:To observe the clinical efficacy and safety of lenalidomide with dexamethasone (LD) in the treatment of relapse/refractory light-chain amyloidosis. Methodology:Ten patients diagnosed relapse/refractory light-chain amyloidosis were enrolled in this retrospective study. Their clinical data were reviewed, the hematological and organ responses, treatment related adverse events were analyzed. Results:Seven males and three females were enrolled with a median age of 64.5(56.8,68.8)years old. Of seven evaluable patients, overall hematological response rate was 42.9%, including 14.3% with complete remission. Heart response was seen in two patients, none had renal response. All were alive and the overall survival and median progression free survival were not reached. Grade 3/4 adverse reaction rate was 30%. Conclusion:Lenalidomide with dexamethasone was effective and well-tolerated as a salvage treatment for relapse/refractory light-chain amyloidosis.
light-chain amyloidosis lenalidomide efficacy adverse event
10.3969/cndt.j.issn.1006-298X.2017.03.001
国家科技支撑计划项目课题(2015BAI09B05,2015BAI12B02),江苏省青年医学人才计划(QNRC2016895),国家“精准医学”重点研发计划项目(2016YFC0904100)
南京军区南京总医院肾脏科 国家肾脏疾病临床医学研究中心 全军肾脏病研究所(南京,210016)
刘志红(E-mail:liuzhihong@nju.edu.cn)
2016-11-29
ⓒ 2017年版权归《肾脏病与透析肾移植杂志》编辑部所有

