结肠息肉电切术后并发缺血性肠病1例
谈涛,李蜀豫
(湖北省第三人民医院 消化内科,湖北 武汉 430415)
病例报告
结肠息肉电切术后并发缺血性肠病1例
谈涛,李蜀豫
(湖北省第三人民医院 消化内科,湖北 武汉 430415)
结肠息肉;电切;缺血性肠病
出血和穿孔是结肠息肉电切术的最常见并发症,而并发缺血性肠病(ischemic colitis,IC)的则较为少见,如若误诊对患者的治疗和预后产生严重影响。本文回顾1例结肠息肉电切术后并发IC的诊治过程并结合文献进行分析讨论。
1 临床资料
患者 女,81岁,主因“间断腹痛、腹胀半个月,便血1 d”就诊于本院。患者半个月前无明显诱因出现腹痛、腹胀,以右下腹为主,疼痛不向腰背部放射,与进食无明显相关性,无腹泻、便血等相关伴随症状,自服抑酸、护胃等药物,症状稍有缓解。入院前1 d无明显诱因解红色血便2次,总量约50 ml,遂住院治疗。既往有高血压、冠心病等病史,曾行子宫肌瘤切除术。入院查体:神志清楚,痛苦面容,心肺未见明显异常,腹平软,右下腹压痛,无腹肌紧张及反跳痛,肠鸣音正常,移动性浊音阴性。入科后完善相关检查,血常规:白细胞13.30×109/L、中性粒细胞比率78.7%、血小板123.00×109/L、血红蛋白112 g/L;粪便潜血(++);肝肾功、电解质和凝血功能等指标均未见明显异常;腹部CT:肝脏体积缩小,左右叶比例失调,裂隙增宽,考虑肝硬化可能;心电图、胸片等未见明显异常。结肠镜检查提示结肠多发息肉(升结肠4枚、乙状结肠3枚),结肠黏膜光滑,血管纹理清晰,未见充血、水肿、糜烂及溃疡等病变。入院后第5天给予患者结肠多发息肉内镜下黏膜切除术,术中共切除0.7~1.2 cm息肉7枚,创面用氩气、金属钛夹等处理,操作时间约40 min。结肠息肉切除术后见图1,术后病理提示管状绒毛状腺瘤。术后给予抗感染(左氧氟沙星+奥硝唑)、止血(云南白药)、调节肠道菌群(培菲康)及补液等治疗,术后8 h左右患者突发腹痛、便血,共3次,每次50~100 ml不等,急查血常规:白细胞18.35×109/L、中性粒细胞比率89.7%、血小板156.00×109/L、血红蛋白97 g/L;粪便潜血(++++);术后12 h急诊肠镜检查提示:手术部位创面未见出血,而升结肠黏膜充血、水肿,溃疡形成,病变部位与正常黏膜有较清晰的分界线,考虑IC(图2)。随即行肠系膜CTA检查提示(图3):腹主动脉、腹腔干、肠系膜上、下动脉、双侧髂总、髂内及髂外动脉多发硬化伴狭窄,右半结肠及左半结肠肠壁增厚,腹腔及盆腔积液,考虑肠系膜动脉缺血性病变可能。此后给予患者改善微循环、抗感染、促进肠黏膜修复及补液等治疗,患者腹痛、便血症状逐渐好转,1周后腹痛、便血症状消失,大便转黄后出院。1个月后复查结肠镜未见明显异常(图4)。

图1 结肠息肉切除术后Fig.1 After resection of colonic polyps

图2 IC后急诊肠镜所示Fig.2 Emergency colonoscopy imaging after IC
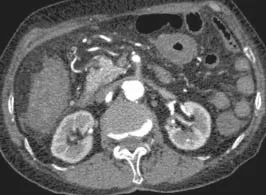
图3 肠系膜CTA所示Fig.3 Mesenteric CTA imaging

图4 1个月后复查肠镜所示Fig.4 Colonoscopy after 1 month
2 讨论
IC是由于闭塞性或非闭塞性动脉供血不足或静脉回流受阻所致的结肠缺血性损伤[1],临床主要表现为腹痛、便血和腹泻,严重者可出现肠梗阻、穿孔、坏死、腹膜炎和感染性休克等。其临床表现差异很大,疾病早期或轻症患者临床表现和体征无特异性,导致诊断困难,国内文献荟萃分析其误诊率高达63.40%[2];而小部分病例尤其是急性肠系膜动脉闭塞形成的患者,如不能早期发现及时给予有效的治疗,可很快发展为肠壁坏疽、腹膜炎、广泛的中毒性巨结肠甚至出现多器官功能衰竭,其病死率高达93.00%[3]。因此,对于有腹痛、便血等症状的患者,及时结肠镜或肠系膜CTA检查对于提高IC的检出率,减少病死率具有重要意义。
IC常见的致病因素包括全身循环动力异常、肠系膜血管病变、心血管疾病及全身性或局部疾病引起肠黏膜血流灌注减少。随着内镜技术的发展和内镜检查的逐渐普及,多种内镜诊治技术在临床中应用越来越广泛,而内镜诊治后并发的IC也越来越引起人们的重视。结肠息肉电凝电切术是最常见的结肠息肉内镜切除方法,其常见的并发症包括出血和穿孔等[4-5]。有研究报道[5],出血的发生率可能高达13.00%~18.00%,穿孔的发生率亦达到0.02%~2.14%,而并发IC的发生率低于0.10%,但仍缺乏大样本量、多中心的研究资料。
本例患者结肠息肉切除术后并发IC,分析原因可能和患者高血压、冠心病等基础疾病有关,但内镜操作及围手术期的管理也可能是其诱发因素[6-8]。经分析后总结如下:①肠道准备过程中肠液丢失过多,血容量不足导致肠壁缺血。该患者使用高渗溶液进行肠道准备,患者丢失大量肠液后并未进行相当程度的补充,导致血容量不足;术中见肠管干燥也证实了患者可能因肠液丢失过多而导致肠壁缺血;②操作不规范导致肠壁缺血。术中反复多次进退镜身,容易因镜身压迫肠管导致肠壁缺血;同时为了暴露视野而过度充气,致使肠腔管径增大,增加肠壁肌肉的张力,肠壁的外来压迫加大,使得肠壁血液供应缺少,容易导致肠缺血;③患者过度紧张导致肠道痉挛,肠壁血管收缩,使得肠壁缺血;同时由于手术时间过长,增加了肠道痉挛发生,易引起肠黏膜损伤,引起肠壁缺血缺氧。本例患者操作时间约40 min,增加了肠壁缺血的风险;④戊二醛消毒肠镜可能是诱发因素之一。有报道[6],使用戊二醛作为肠镜消毒剂时,由于清洗不彻底,残留的戊二醛直接接触肠黏膜,可损伤大肠隐窝上皮细胞,最终引起组织坏死,引起IC的出现。
本例中有两个问题值得深思:①患者因腹痛、便血入院,符合IC的临床表现,但第一次肠镜检查提示结肠黏膜正常,并没有IC的镜下表现,其腹痛、便血的原因是什么?是否存在隐匿性IC?笔者查阅了相关文献未见相关报道;②患者入院后腹部CT检查并未见腹腔积液,出现IC后腹部CTA检查可见明确的腹腔及盆腔积液,由此推想腹腔及盆腔积液的出现可能与并发IC有关。分析原因可能与IC患者的肠壁血循环障碍、淤血水肿和浆膜面液体外渗等有关,具体发生机制还有待进一步研究。
IC作为结肠镜诊治过程中少见并发症,往往容易被误诊或漏诊,从而危及患者生命[2]。在结肠镜诊治过程中做好围手术期的管理、规范操作流程、减少操作时间等可能对降低IC的发生率有一定帮助。尤其对于合并心脑血管疾病的老年患者,结肠镜诊治术后一旦出现腹痛、便血等症状时,要及时考虑到是否并发了IC,及时的结肠镜和肠系膜CTA检查可显著提高IC的诊断率[9]。
[1] LEE S O, KIM S H, JUNG S H, et al. Colonoscopy-induced ischemic colitis in patientswithout risk factors[J]. World J Gastroenterol, 2014, 20(13): 3698-3702.
[2] 孙丹莉, 张振玉, 张予蜀, 等. 近10年我国主要文献缺血性肠病误诊荟萃[J]. 临床误诊误治, 2009, 22(6): 68-70.
[2] SUN D L, ZHANG Z Y, ZHANG Y S, et al. Over the past 10 years,China’s major literature misdiagnosis meta of ischemic colitis[J].Clinical Misdiagnosis & Mistherapy, 2009, 22(6): 68-70. Chinese
[3] 范建高, 沈峰. 提高缺血性肠病的临床认识[J].胃肠病学和肝病学杂志, 2011, 20(6): 491-494.
[3] FAN J G, SHEN F. To strengthen the clinical recognition of ischemic bowel diseases[J]. Chin J Gastroenterol Hepatol, 2011,20(6): 491-494. Chinese
[4] 张凌云, 姜永梅, 纪风芝, 等. 大肠息肉结肠镜下高频电切除术后处理措施对术后并发症的影响[J]. 世界华人消化杂志, 2016,24(13): 2087-2092.
[4] ZHANG L Y, JIANG Y M, JI F Z, et al. Effect of high-frequency electroresection under colonoscopic for colorectal polyps on postoperative complications[J]. World Chinese Journal of Digestology, 2016, 24(13): 2087-2092. Chinese
[5] LOHSIRIWAT V. Colonoscopic perforation: incidence,risk factors,management and outcome[J]. World J Gastroenterol, 2010, 16(4):425-430.
[6] 王鸿, 张侠. 结肠镜检查后并发缺血性肠病2例报道[J]. 胃肠病学和肝病学杂志, 2015, 24(12): 1443-1444.
[6] WANG H, ZHANG X. Ischemic bowel disease induced by colonoscopy: 2 cases report[J]. Chin J Gastroenterol Hepatol,2015, 24(12): 1443-1444. Chinese
[7] 舒磊, 王华乔, 吴玉芳, 等. 内镜下结肠息肉治疗术后并发缺血性肠病16例临床分析[J]. 现代医学, 2014, 42(2): 192-193.
[7] SHU L, WANG H Q, WU Y F, et al. Clinical analysis of endoscopic colonic polyps in the treatment of 16 patients with ischemic bowel disease after operation[J]. Modern Medical Journal, 2014, 42(2):192-193. Chinese
[8] 周杰. 缺血性肠病30例临床特点分析[J]. 中国实用内科杂志,2015, 35(s1): 69-70.
[8] ZHOU J. Clinical characteristics of ischemic bowel disease: 30 cases[J]. Chinese Journal of Practical Internal Medicine, 2015,35(s1): 69-70. Chinese
[9] 袁媛, 于静, 兰玲, 等. 缺血性结肠炎的危险因素及肠镜表现37例[J]. 世界华人消化杂志, 2015, 23(17): 2830-2833.
[9] YUAN Y, YU J, LAN L, et al. Risk factors and endoscopic manifestations of ischemic colitis[J]. World Chinese Journal of Digestology, 2015, 23(17): 2830-2833. Chinese
(彭薇 编辑)
R656.9
D
2016-10-21
李蜀豫,E-mail:lsyzsyy@163.com;Tel:18963989603
10.3969/j.issn.1007-1989.2017.06.023
1007-1989(2017)06-0108-03

