Fe3O4@ILs-β -CDCP磁固相萃取-电感耦合等离子体发射 光谱法同时测定环境水样中铅和锑
俞梁敏, 顾唯希, 霍帅文, 朱霞石*
(1.扬州大学化学化工学院,江苏扬州 225002; 2.江苏省昆山市环境检测站,江苏昆山 215316)
水体重金属的污染从工业化开始一直是全世界共同面对的难题[1 - 2]。铅和锑是重金属制造的重要原材料,而在生产过程中会有部分无法被完全利用的铅和锑进入水体环境,将对水生生物造成潜在的威胁[3 - 4]。铅和锑在人体的积蓄会对人体造成极大的伤害[5-6]。锑属于第一类污染物,它的排放受到国家的严格控制,最高允许排放浓度为0.1 mg/L[7]。因此,对于环境水样中铅和锑的准确检测非常必要[8]。
铅和锑的主要测定方法有原子吸收光谱法(AAS)[9 - 10]、原子荧光光谱法(AFS)[11 - 12]、紫外-可见分光光度法(UV-Vis)[13]、电感耦合等离子体发射光谱/质谱法(ICP-OES/MS)[14 - 15]等。其中,ICP-OES具有灵敏度高、线性范围宽、分析速度快等优势[16]。但是,自然水体中重金属的浓度有时低于ICP-OES的仪器检测限,实际样品分析中的基体效应也不容忽视,因此在仪器分析前需要对水样进行分离和富集。目前,常见的分离和富集方法包括共沉淀[17]、液-液萃取[18 - 19]、固相萃取[20]、离子交换法[21]和浊点萃取法[22]等。磁固相萃取(MSPE)是一种以磁性或可磁化材料作为吸附剂的固相萃取技术。与传统固相萃取技术相比,MSPE具有操作简便、萃取时间短、易于分离等优点,显示出广阔的应用前景[23]。在磁核表面负载无机材料或有机材料后可提高它的选择性和吸附性能[24]。Fe3O4磁性纳米材料具有磁性材料和纳米材料的共同特性,可以在外加磁场的作用下实现快速分相,比表面积大,吸附容量高,分散性好。而且表面易于修饰,可以根据待测物的性质选择功能基团对其进行修饰,功能化环糊精聚合物(CD)是一种新型超分子材料,将其用于磁核表面修饰,可以改善其吸附性能[25]。
本文合成了吡啶类离子液体功能化环糊精聚合物(ILs-β-CDCP),并将其修饰于磁核表面。所得的磁性纳米复合材料(Fe3O4@ILs-β-CDCP)被用作固相萃取剂,基于此,建立了MSPE-ICP-OES联用技术同时测定Pb(Ⅱ)和Sb(Ⅲ)的方法,并将其成功用于环境水样中Pb(Ⅱ)和Sb(Ⅲ)的分析测定。
1 实验部分
1.1 主要仪器及试剂
Optima 8300型电感耦合等离子体发射光谱仪(美国,Perkin-Elmer公司);S-4800 Ⅱ型场发射扫描电镜(SEM)(日本,日立公司);马尔文Nano ES90粒度分析仪(英国,Malvern);pHS-25B型酸度计(上海精科雷磁仪器厂);TENSOR-27型傅里叶变换红外光谱仪(FT-IR)(德国,Bruker公司);BS224S型电子天平(北京赛多利斯科学仪器公司)。
Pb(Ⅱ)和Sb(Ⅲ)标准溶液(浓度均为1 000 μg/mL)。Pb(Ⅱ)和Sb(Ⅲ)混合标准溶液由各自标准贮备液中移取混合后用去离子水逐级稀释所得。N,N-二甲基甲酰胺、乙腈、丙酮、甲醇、HCl、KI、2-甲基吡啶、Fe3O4·7H2O、FeCl3·6H2O、氨水(分析纯,国药集团化学试剂(上海)有限公司);β-环糊精(分析纯,西安宏昌药业有限责任公司);六亚甲基二异氰酸酯(HDI,阿拉丁试剂有限公司)。实验用水为去离子水。
1.2 Fe3O4@ILs-β -CDCP的制备
β-CDOTs(a)、β-CDI(b)、ILs-β-CD(c)和ILs-β-CDCP(d) 的制备如图1所示,将得到的白色不溶固体产物研磨后,待用。将Fe3O4·7H2O、FeCl3·6H2O、ILs-β-CDCP按1∶1∶2摩尔配料比加入到200 mL去离子水中,在通氮气条件下,70 ℃水浴加热搅拌。加入25 mL氨水搅拌30 min,升温至90 ℃继续搅拌30 min,冷却后去离子水洗涤4次,无水乙醇清洗1次,60 ℃真空干燥过夜得黑色产物,研磨后,备用。

图1 ILs-β -CDCP的合成方法Fig.1 Synthesis scheme of ILs-β -CDCP
1.3 样品处理
实际水样分别为:(1)扬州淀粉厂附近水域水样:去除样品中悬浮颗粒杂质,然后过0.45 μm滤膜并收集于聚乙烯材质塑料容器中,4 ℃低温避光保存。(2)扬州冶金机械公司铸钢分厂附近水域水样:去除样品中悬浮颗粒杂质,用0.45 μm孔径微孔滤膜过滤水样,收集于聚乙烯材质塑料容器中,4 ℃低温避光保存。(3)瘦西湖湖水:去除湖水中悬浮颗粒杂质,过0.45 μm滤膜并收集于聚乙烯材质塑料容器中,4 ℃低温避光保存。
1.4 磁固相萃取(MSPE)过程
准确称取Fe3O4@ILs-β-CDCP 0.05 g,置于离心管中,加入处理后的样品溶液定容至10 mL,室温震荡10 min,磁分离后弃去上层清液,用5 mL洗脱液洗脱,磁分离后取上层清液用ICP-OES法测定。
2 结果与讨论
2.1 Fe3O4@ILs-β -CDCP的表征
图2曲线a为β-CDCP的红外谱图。图2曲线b为ILs-β-CDCP的红外谱图,2 928 cm-1处为亚甲基的特征峰,3 362 cm-1峰变宽且发生迁移是因为酰胺的N-H吸收影响,1 620、1 400、1 120 cm-1分别为酰胺Ⅰ、Ⅱ、Ⅲ吸收带。图2曲线c为Fe3O4@ILs-β-CDCP的,同时具有Fe3O4和ILs-β-CDCP的特征吸收峰,证明ILs-β-CDCP确实被Fe3O4修饰。

图2 β -CDCP(a)、ILs-β -CDCP(b)和Fe3O4@ILs-β -CDCP(c)的红外光谱图Fig.2 Infrared spectra of β -CDCP (a),ILs-β -CDCP (b) and Fe3O4@ILs-β -CDCP (c)
图3为β-CDCP、ILs-β-及Fe3O4@ILs-β-CDCP的扫描电镜(SEM)图。图3a中β-CDCP的表面呈层片状,较为光洁;图3b中ILs-β-CDCP表面呈海绵状,蓬松多孔,较为粗糙。由此可以认为离子液体的修饰使得聚合物表面发生了变化。比较图3b、3c可以发现,Fe3O4修饰ILs-β-CDCP后,他们呈现出由颗粒构成的球状结构,颗粒大小比较均一。
用磁强计测得Fe3O4纳米粒子、Fe3O4@ILs-β-CDCP的最大饱和磁化强度分别是121 emu/g和85.4 emu/g。Fe3O4@ILs-β-CDCP最大饱和磁化强度的减小是因为表面ILs-β-CDCP的影响。由磁性分析可知,它们都显示出超顺磁性。因此,制得的Fe3O4@ILs-β-CDCP因其超顺磁性和较大的磁化强度能够从溶液中被快速地分离。使用动态光散射以90度散射角在0.3 nm到5 μm(直径)的范围里测量颗粒粒度,得出纳米粒子的粒径大约为20 nm,与电镜图得到的结果吻合。

图3 β -CDCP(a)、ILs-β -CDCP(b)和Fe3O4@ILs-β -CDCP(c)的扫描电镜(SEM)图Fig.3 SEM images of β -CDCP(a),ILs-β -CDCP(b) and Fe3O4@ILs-β -CDCP(c)
2.2 萃取条件优化
2.2.1pH的选择溶液pH值对Pb(Ⅱ)和Sb(Ⅲ)的固相萃取效率有着重要影响。适当的pH值不仅可提高目标分析物的萃取效率,而且降低基体干扰。本文研究了溶液pH在4.0~12.0范围内对Pb(Ⅱ)和Sb(Ⅲ)萃取效率的影响(图4)。从结果可以看出,Pb(Ⅱ)在整个pH范围内吸附率都是100%;Sb(Ⅲ)在pH为5.0时吸附率最高,在pH值为中性或碱性条件时,Fe3O4@ILs-β-CDCP对Sb(Ⅲ)的吸附率较低,且随着pH值的增大其吸附率逐渐减小,在酸性条件下Sb(Ⅲ)的吸附率低可能是由于Sb(Ⅲ)在强酸环境下会与酸(HCl)反应,从而使Sb(Ⅲ)在酸性条件下吸附率低;而在中性及碱性条件下Sb(Ⅲ)以中性分子(Sb(OH)3)存在,而溶液中OH-会随着pH的增加而不断增多,与Sb(Ⅲ)的中性分子竞争吸附点位从而导致对Sb(Ⅲ)的吸附率下降。因此选择pH=5.0为萃取富集条件。
2.2.2温度的影响本文研究了不同温度(0~50 ℃)下Fe3O4@ILs-β-CDCP对Pb(Ⅱ)和Sb(Ⅲ)吸附率的影响。结果表明,温度对Pb(Ⅱ)的吸附率影响不大,而Sb(Ⅲ)的吸附率随着温度的升高而增大,在温度为40 ℃时吸附率达到90.2%。因此选择温度40 ℃为吸附的最佳条件。
2.2.3吸附时间在温度40 ℃下进行了Fe3O4@ILs-β-CDCP对Pb(Ⅱ)和Sb(Ⅲ)的吸附动力学研究。Pb(Ⅱ)的吸附率在2 min内即可达到100%,并且保持稳定,而Sb(Ⅲ)的吸附率在10 min时达到95%。所以本实验选择吸附时间为10 min。
2.2.4溶液体积研究了Pb(Ⅱ)和Sb(Ⅲ)含量均为1.0 μg时,溶液体积(5.0~80.0 mL)对萃取的影响。在5.0~30.0 mL内,Fe3O4@ILs-β-CDCP对Pb(Ⅱ)和Sb(Ⅲ)的吸附比较稳定,在30.0 mL处吸附率在85.0%左右,随着溶液体积的增加,吸附率持续下降。因此,选择最大吸附体积为30.0 mL。
2.3 吸附容量
图5所示为Fe3O4@ILs-β-CDCP对Pb(Ⅱ)和Sb(Ⅲ)的吸附容量。结果显示当两个体系中Pb(Ⅱ)和Sb(Ⅲ)浓度都达到250 μg/mL时(溶液体积为10.0 mL),Fe3O4@ILs-β-CDCP对Sb(Ⅲ)和Pb(Ⅱ)的吸附达到饱和,吸附容量分别为11.3 mg/g和9.14 mg/g。

图4 pH值对吸附率的影响Fig.4 Effect of pH on adsorption efficiency

图5 Fe3O4@ILs-β -CDCP对Pb(Ⅱ)和Sb(Ⅲ)吸附容量Fig.5 Adsorption capacities of Fe3O4@ILs-β -CDCP toward Pb(Ⅱ) and Sb(Ⅲ)
2.4 洗脱条件优化
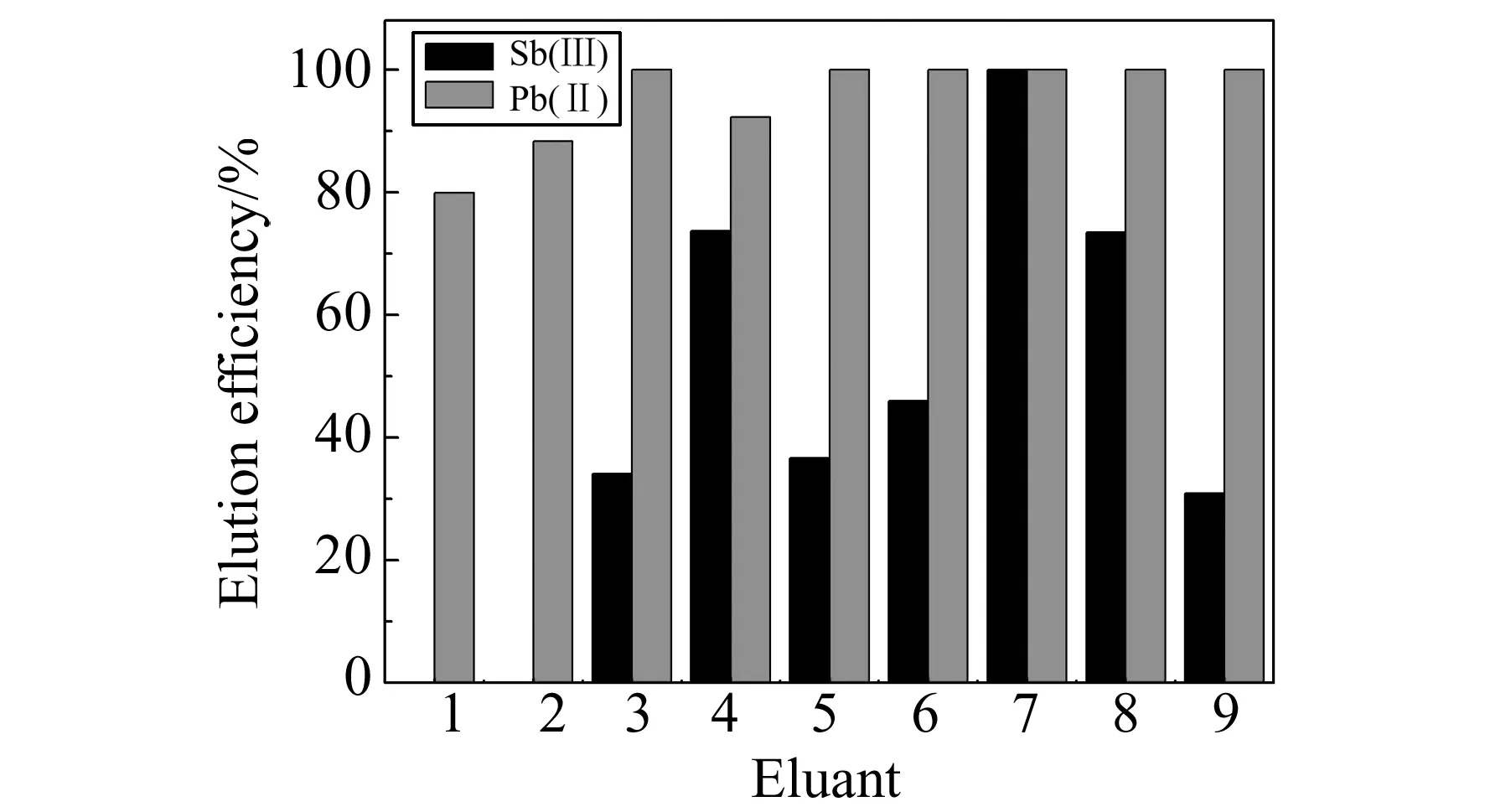
图6 不同洗脱剂对洗脱率的影响Fig.6 Effect of different eluent on elution efficiency 1:0.05 mol/L HNO3+0.1 mol/L HCl,2:0.05 mol/LHNO3+0.5 mol/L HCl,3:0.05 mol/L HNO3+1 mol/L HCl,4:0.1 mol/L HNO3+0.05 mol/L HCl,5:0.1 mol/L HNO3+0.5 mol/L HCl,6:0.1 mol/L HNO3+1 mol/L HCl,7:0.5 mol/L HNO3+0.05 mol/L HCl,8:0.5 mol/L HNO3+0.1 mol/L HCl,9:0.5 mol/L HNO3+1 mol/L HCl
2.4.1洗脱剂选择实验研究了不同浓度的HNO3和HCl组成的混酸的洗脱附效果(图6)。选择混酸作为洗脱剂是因为Fe3O4@ILs-β-CDCP在吸附Pb(Ⅱ)和Sb(Ⅲ)的过程中形成螯合物,加入混酸,其中的H+取代螯合物中Pb(Ⅱ)和Sb(Ⅲ),Pb(Ⅱ)和Sb(Ⅲ)重新被释放到溶液中。不同种类的混酸中,1 mol/L HNO3和0.05 mol/L HCl的混酸洗脱效果最好且稳定,因此选择其作为洗脱剂。
2.4.2洗脱剂体积洗脱剂体积从1.0~8.0 mL,洗脱率保持在90.0%以上,当洗脱剂体积为5.0 mL时,洗脱率可达100%。因此本实验选择最佳洗脱剂体积为5.0 mL。预富集倍数为8(吸附前溶液体积/洗脱体积)。
2.4.3洗脱温度本文研究了0~50 ℃下混酸对Pb(Ⅱ) 和Sb(Ⅲ)的洗脱效果的影响,发现温度对Pb(Ⅱ)的影响不大,洗脱率基本为100%。而Sb(Ⅲ)在温度较低时洗脱率低,随着温度的升高洗脱率逐渐增大。因此,本实验选择20 ℃作为洗脱的最佳温度。
2.4.4洗脱时间实验进行了室温下洗脱剂对Pb(Ⅱ)和Sb(Ⅲ)的脱附动力学研究 。在最佳洗脱体积下进行脱附,随着洗脱时间的增长,Pb(Ⅱ)的洗脱率为100%且基本保持不变。而Sb(Ⅲ)的洗脱率在0~20 min内随着时间的增大而增大,在20 min时达到100%。因此,本实验选择洗脱时间为20 min。
2.5 干扰实验
考察了溶液中常见共存金属离子对Pb(Ⅱ)和Sb(Ⅲ)萃取效果的影响(以Pb(Ⅱ)和Sb(Ⅲ)测定的吸光度相对误差≤±5%为计)。表1中结果表明,这些共存离子在一定浓度范围内均不影响Pb(Ⅱ)和Sb(Ⅲ)的测定。
2.6 分析性能
在优化条件下,考察了该方法的分析性能(表2),以及与其他测定方法分析性能的比较(表3)。本方法与其他方法比较,具有较低的检出限及较宽的线性范围。此外,本方法还可同时测定Pb(Ⅱ)、Sb(Ⅲ),结果稳定。

表1 干扰物质的影响Table 1 Effect of foreign substances on determination of Pb(Ⅱ) and Sb(Ⅲ)

表2 方法分析性能Table 2 Analytical performance of the proposed method

表3 本法与其他方法性能比较Table 3 Comparison with the results obtained by other methods
2.7 样品测定
分别取瘦西湖、淀粉厂与冶金厂附近水样,其编号依次为A、B、C,用该方法测定了三种实际水样中的Sb(Ⅲ)和Pb(Ⅱ)的含量,并进行加标回收实验,测定结果见表4。 为了验证方法的准确度,对标准水样(GSBG620439-90,GSB07-1183-2000)进行了分析,结果如表5所示,可见测定值与参考值吻合良好。

表4 样品中Pb(Ⅱ)和Sb(Ⅲ)的回收率(n=3)Table 4 Recoveries of Pb(Ⅱ) and Sb(Ⅲ) in samples(n=3)

表5 标准样品中Pb(Ⅱ),Sb(Ⅲ)的测定值(n=5)Table 5 Results of Pb(Ⅱ) and Sb(Ⅲ) in certified reference materials(n=5)
3 结论
本文合成了磁性固相萃取材料Fe3O4@ILs-β-CDCP,并与ICP-OES法联用用于分离分析水样中的Sb(Ⅲ)和Pb(Ⅱ)。所建立的MSPE-ICP-OES方法操作简单,萃取效率高,分离时间短,被成功应用于水样中Sb(Ⅲ)和Pb(Ⅱ)的分析检测。

