中药饮片生产企业实验室间比对研究
北京市通州区食品药品监督管理局(101101)吴东应 张鹂
1 背景
目前,通过实验室间检测结果的比对来确定或证明实验室的校准、检测能力的方式,在国内外越来越受到重视,实验室间比对是指按照预先规定的条件,由两个或多个实验室对相同或类似检测物品进行检测的组织、实施和评价[1]。参加实验室间比对,可为实验室提供评价其出具数据可靠性和有效性的客观依据,补充其内部质量控制技术,为自身的持续改进和质量管理提供信息,促进实验室管理能力和水平的进一步提高[2]。对近年来通州区中药饮片抽验不合格数据统计分析发现,同批次中药饮片法定检验机构检测结果与生产企业自检结果存在较大差异。因此希望通过实验室间比对查找问题、分析原因、提高检验能力。
2 实验室间比对方案
2.1 比对要求[3]为保证实验室间比对结果的真实可靠,在比对开展前,我们印发了《关于开展2016年度中药饮片企业检验比对研究的通知》(京通食药监〔2016〕22号),并通过专题会议方式要求各参比实验室:①高度重视此次比对工作,明确比对实验的各项要求;②独立完成比对实验项目,不得相互询问检测结果,不得以任何方式伪造检测数据;③按规定储存样品,在规定时间内提交检测结果和原始记录。
2.2 参加比对的实验室情况 由通州区10家中药饮片生产企业和通州区食品药品安全监控中心组成,其中通州区食品药品安全监控中心作为第三方检测实验室。
2.3 样品分发 本次实验室间比对所用样品为“白芷(饮片)”,由两家不同的中药饮片生产企业提供,称为A样、B样,各均分成11份,分发给参加比对实验室,样品分发遵循随机单盲的原则,见附表1。
2.4 样品检验方法 按照《中华人民共和国药典》(2015版)[4]进行白芷含量测定。
2.5 结果评价原则 本次实验室比对中白芷(饮片)由两家不同的中药饮片生产企业提供,称为A样、B样,因此,对A样和B样白芷含量测定结果分别进行统计计算。主要从以下三方面对各参比实验室的结果进行评价。
①为增加数据量,经讨论决定将仅有计算错误的结果予以矫正后纳入统计分析;②采用Grubbs检验法(α=0.05)分别对A样和B样白芷含量测定结果进行统计分析,剔除离群值;③剔除离群值后,分别计算A样和B样白芷含量测定结果平均值、标准偏差(SD)及平均值±3SD。
2.5.1 根据以下五项准则评价参与实验室的结果是否满意 ①含量测定结果存在明显错误数据的,为不满意结果;②含量测定结果经Grubbs检验法判定为离群值的,为不满意结果;③含量测定结果>平均值+3SD的,为不满意结果;④含量测定结果<平均值-3SD的,为不满意结果;⑤平均值-3SD≤含量测定结果≤平均值+3SD的,为满意结果。
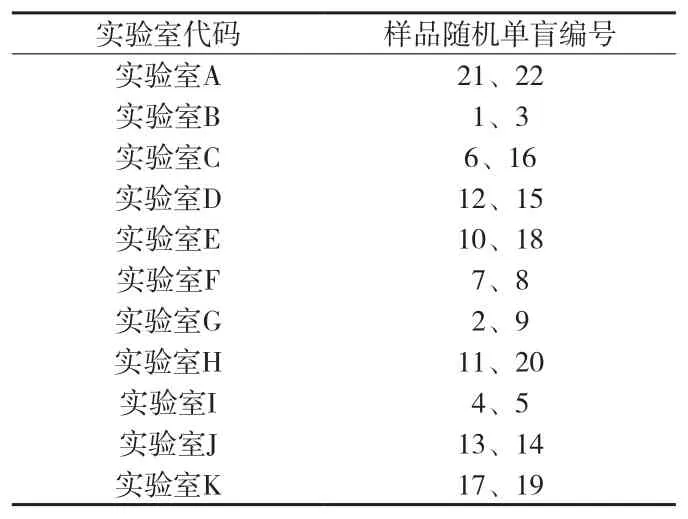
附表1 中药饮片白芷含量测定样品分发表
2.5.2 根据以下三项准则评价“满意”的实验室结果与平均值的偏离范围 ①︱含量测定结果Xi -平均值︱≤SD的,偏离度较小;②SD<︱含量测定结果Xi -平均值︱≤2SD的,偏离度中等;③2SD<︱含量测定结果Xi -平均值︱≤3SD的,偏离度较大。
3 实验室间比对结果
3.1 本次实验室比对共收到10家药品生产企业和1家食品药品安全监控中心的结果报告,其中实验室C的原始数据未折算成干燥品含量,对其数据进行矫正后参与统计分析,具体检验数据详见附表2。
3.2 采用Grubbs检验法(α=0.05)分别对A样和B样白芷含量测定结果进行统计分析,总计统计量结果见附表3。
3.3 经统计分析:离群值和不满意结果0个,满意结果11个,11家实验室比对测定结果情况见附表4。11家实验室的含量测定结果与平均值的差值结果情况见附表5。
3.4 综上,11家实验室的评价结果如下。
3.4.1 数据计算错误的实验室1家。
3.4.2 对数据矫正后经Grubbs检验法判定为离群值的0家,经统计分析为“满意结果”的11家。
具体评价结果见附表6。
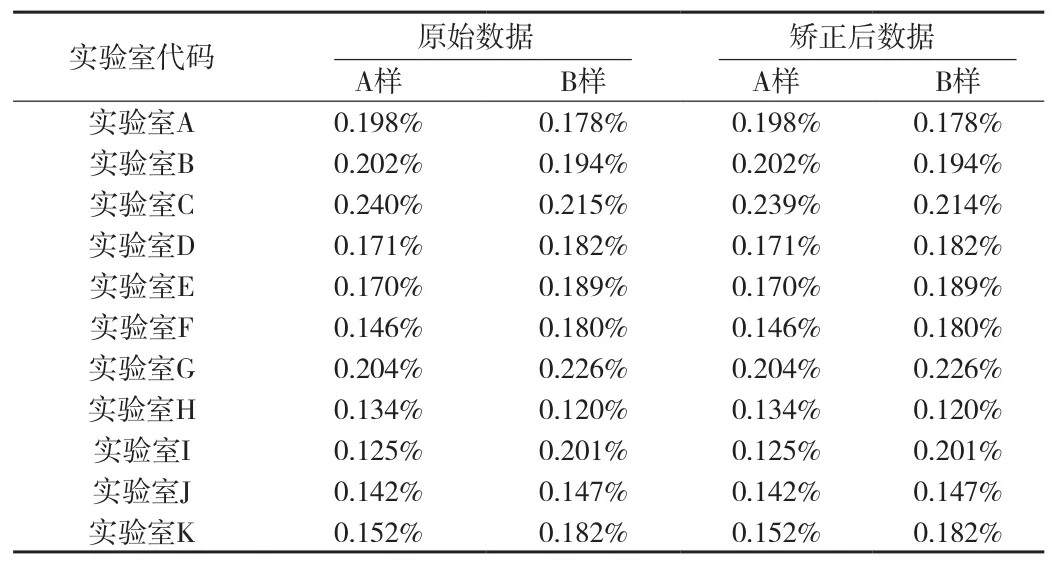
附表2 不同实验室中药饮片白芷含量测定结果

附表3 实验室比对含量测定结果的总计统计量

附表4 实验室比对判别结果统计
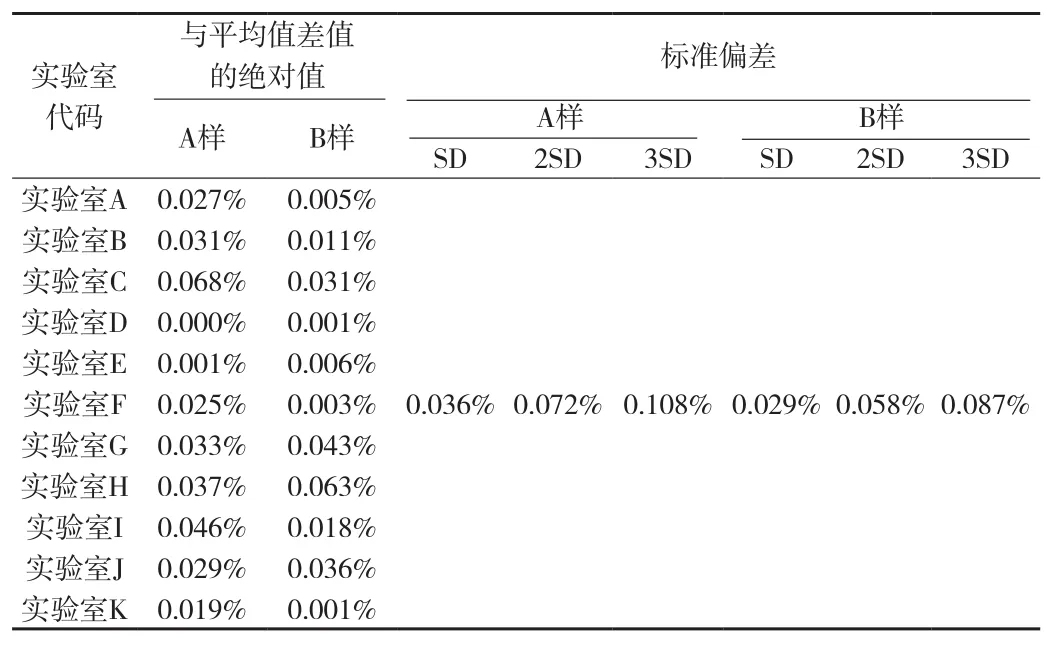
附表5 11家实验室的含量测定结果与平均值差值及标准偏差
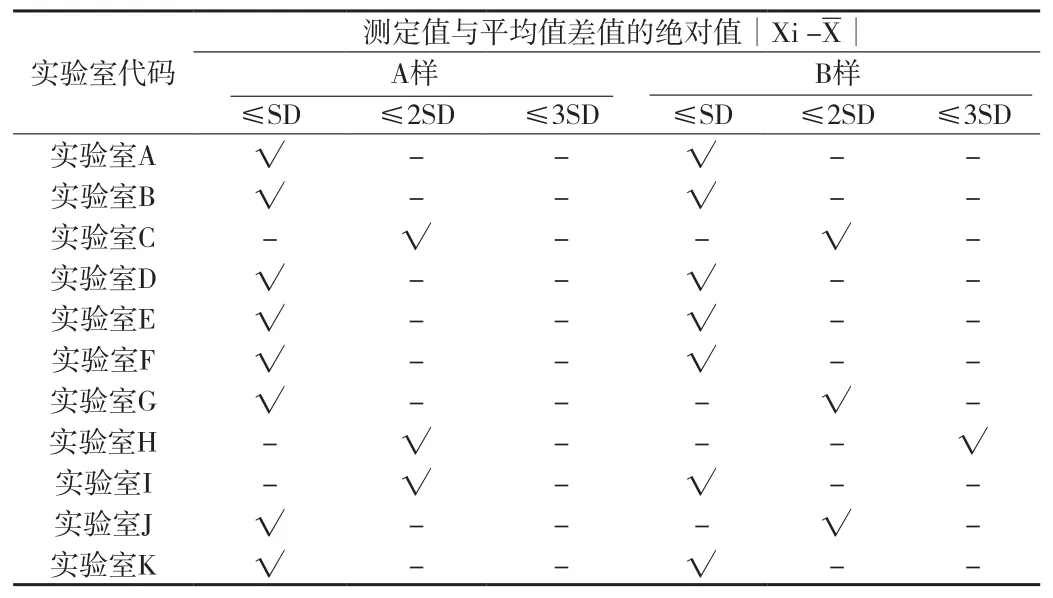
附表6 11家实验室的含量测定结果与平均值的偏离范围
4 发现问题
4.1 各实验室之间技术水平参差不齐。不同实验室在实验室管理水平、检验仪器和检验人员配备、色谱柱更换周期等方面均存在较大差距,部分实验室管理松散、检验仪器和检验人员配备不足、所用检验设备年限较长。
4.2 个别单位检验人员的专业技术水平不足。通过比对试验结果综合分析,发现检验人员专业技术水平能力不足导致检验结果不准确的现象较多。如①对照品溶液配制过程中未精密量取;②供试品含量测定时采用“双样单针”;③含量测定计算未扣除水分;④含量测定结果未按对照品含量进行折算。
4.3 未进行系统适用性试验。《中华人民共和国药典》(2015版)规定系统适用性试验包括理论板数、分离度、灵敏度、拖尾因子和重复性五个参数,至少需要进样5针,部分企业测试前未做系统适用性试验。
4.4 未使用最新批号的对照品。部分企业在中国食品药品检定研究院已出新批号对照品后仍长期使用旧批号对照品。
4.5 检验记录和对照品溶液配制记录书写错误,不能有效保证必要时进行溯源和调查分析。
5 改进建议
科学合理的硬件配制是必要的检测基础,专业人员的技术培训和科学合理的操作、完善的质量保证体系更是获得满意结果的关键。建议:①鼓励企业配备自动化的检验设备,提高检验效率,降低检验人员的工作量;完善质量管理体系和对照品更新制度。②要求企业结合实际完善人员学习培训和监督考核机制,加强新进人员的培训和技术能力确认。有条件的外派检验人员到专业检验检测机构接受专业知识和操作技能培训,切实提高检验人员专业技术水平和能力。③严格按照质量标准操作,记录填写真实完整、规范简洁,关键的实验细节不能遗漏,保证检测结果可以追溯、能够重现。
6 推进措施
6.1 建立全区中药饮片生产企业实验室间比对工作长效机制,使实验室比对工作按计划规范开展,促进辖区饮片生产企业检验整体能力水平的提高。
6.2 针对实验室比对结果,评估企业在质量控制方面的风险,开展针对性的监督检查,防控药品质量风险。

