杀菌剂/阻垢剂作用下硫酸盐还原菌对316L不锈钢电化学腐蚀行为的影响
, , ,,
(北京交通大学 土木建筑工程学院 水中典型污染物控制与水质保障北京市重点实验室,北京 100044)
再生水回用于工业循环冷却水系统是解决我国水资源危机的重要途径之一。同自然界淡水相比,再生水中的含盐量、有机物含量和氨氮含量高,极易导致微生物在冷却水系统中大量繁殖,造成输水水质恶化,形成生物黏泥,造成传热效率下降,管道腐蚀,输水管道能耗增加,堵塞冷却设备及输水管道等问题,使工业企业的正常运行受到威胁[1]。硫酸盐还原菌(SRB)是引起工业循环冷却水系统腐蚀的主要细菌之一,它在无氧或极少氧条件下,寄生附着在不锈钢表面并形成微生物膜[2],利用附着于金属表面的有机物作为碳源,并利用细菌生物膜内产生的氢,将硫酸盐还原成硫化氢,从氧化还原反应中获得生存的能量[3],进而引起微生物腐蚀和生物污损。
为解决循环冷却水系统中微生物的腐蚀和结垢问题:一方面,发电厂工业循环冷却水系统的凝汽器管材多采用具有良好的力学性能、耐蚀性、经济性和较好传热性的不锈钢[4];另一方面,通过添加杀菌剂和阻垢剂来解决腐蚀和结垢问题。目前大量研究主要针对杀菌剂的杀菌效果和阻垢剂的阻垢效果[5-8],而有关杀菌剂和阻垢剂同时使用时对材料耐蚀性影响的研究却不多见,因此研究杀菌剂和阻垢剂协同作用下SRB对不锈钢腐蚀行为的影响具有重要意义。本工作选取316L不锈钢,利用生物化学分析方法、电化学测试方法,对杀菌剂、阻垢剂及其配伍作用下SRB在316L不锈钢表面的电化学行为进行了研究。
1 试验
1.1 菌种活化与培养
试验菌种为硫酸盐还原菌,取自以再生水作为循环冷却系统补水的北京某热电厂冷却塔底黏泥,将5 g黏泥加入到45 mL无菌水中,充分振荡、静置,取上层清液,即黏泥浸出液,将浸出液接入分离富集培养基中进行厌氧培养。采用稀释涂布叠皿夹层培养法分离、纯化菌种,重复分离纯化2~3次,获得可以转接、保存的纯种SRB,4 ℃以下保存在冰箱中作为试验菌种。
菌种活化和试验培养基采用修正后的Postgate C培养基,其成分为:KH2PO40.5 g,NH4Cl 1.0 g,CaCl2·2H2O 0.06 g,Na2SO44.5 g,MgSO4·7H2O 0.06 g,乳酸钠(80%) 6 mL,酵母浸膏1.0 g,柠檬酸钠0.3 g,蒸馏水1 000 mL,用HCl和0.05 mol/L NaOH溶液调节pH为7.0~7.4,在0.15 MPa灭菌锅中灭菌20 min,快速冷却后加入经紫外线消毒30 min的半胱酸胺盐酸盐,在(37±1) ℃生化培养箱中恒温培养。
1.2 试样及溶液
试验材料为316L不锈钢管材,其主要化学成分为:wC0.08%,wSi1.00%,wMn2.00%,wP0.045%,wS0.03%,wNi10.00%~14.00%,wCr16.00%~18.00%,wMo2.00%~3.00%,余量为Fe。
将316L不锈钢管材加工成表面积为1 cm×1 cm的正方形试片,将不锈钢试片背后焊接导线,用环氧树脂密封在塑料圆环内,制成工作电极。用水洗砂纸(800~2 000号)逐级打磨工作电极,之后用金刚砂(0.5 μm)研磨膏抛光,用丙酮除去表面油污,再用无水乙醇清洁表面后干燥,置于干燥器内备用。
试验用杀菌剂为1227(分子式为C21H38NCl),加药量为45 mg·L-1;试验用阻垢剂有HEDP(分子式为C2H8O7P2)和PBTCA(分子式为C7H11O9P),加药量均为5 mg·L-1。试验用再生水的参数为:pH 8.2,TOC(总有机碳)质量浓度1.89 mg·L-1,氨氮质量浓度96.72 mg·L-1,Cl-质量浓度110.69 mg·L-1,SO42-质量浓度74.5 mg·L-1,TP(总磷)质量浓度0.01 mg·L-1,电导率890 μS·cm-1,总硬度8.36 mmol·L-1,碱度3.83 mg·L-1。
1.3 试验方法
1.3.1 电化学试验
电化学试验溶液如下:再生水+SRB(A溶液),再生水+SRB+1227(B溶液),再生水+SRB+HEDP(C溶液),再生水+SRB+PBTCA(D溶液),再生水+SRB+1227+HEDP(E溶液),再生水+SRB+1227+PBTCA(F溶液)。
电化学试验在Correst电化学工作上完成,采用三电极体系,参比电极为饱和甘汞电极(SCE),辅助电极为铂电极,工作电极为316L不锈钢试样。电化学阻抗谱的测定频率为0.05 Hz~100 kHz,正弦电压信号幅值为5 mV。极化曲线在开路电位下开始测量,扫描速率为0.5 mV/s,扫描范围为-0.30~1.5 V。
工作电极经30 min紫外灭菌后,浸泡在试验溶液中。并向试验溶液充氮气20 min以驱赶氧气,控制体系中菌液量为n×107个/mL数量级,在生化培养箱中(37±1) ℃的条件下恒温厌氧培养。分别在浸泡1,3,7 ,10 d后取出试样,并在6种溶液中进行电化学测试。试验均采用3个平行试样,测试体系使用的电极与电解池均经过灭菌处理,避免外界杂菌干扰。
1.3.2 脱氢酶测试
脱氢酶由活的微生物产生,因而脱氢酶的活性可以反映溶液中活性微生物量,脱氢酶含量高,生物活性强。将试样浸泡在几种试验溶液中,分别在浸泡1,3,7,10 d后提取试验溶液,用三苯基四氮唑氯化物(TTC)比色法检测试验溶液中的脱氢酶含量[9]。
2 结果与讨论
2.1 脱氢酶
由图1可见:在A溶液中,脱氢酶含量先迅速增加,3 d后达到峰值3.10 mg·L-1,而后逐渐减小。这是因为1~3 d是SRB的对数期,细菌数量迅速增加;3~7 d是稳定期,7~10 d时,由于营养物质不足细菌数量开始减少,脱氢酶含量也随之下降。在接种SRB的再生水中添加阻垢剂后,脱氢酶的变化趋势是相同的,HEDP和PBTCA会在一定程度上提高脱氢酶含量,这是由于HEDP和PBTCA含有机碳,分别为7.2%(质量分数,下同)和19.2%,可以为SRB的生长提供额外的有机碳,促进了SRB的增殖。1227杀菌剂显著降低了脱氢酶的含量,这是因为SRB细胞表面带有负电,1227杀菌剂是阳离子杀菌剂,在细菌表面有较强的吸附力,其疏水基与亲水基能深入菌体类脂层和蛋白层,导致SRB酶失活、蛋白质变性,进而将细菌杀死,有效抑制SRB的生长[10]。

图1 4种溶液中脱氢酶含量随时间的变化曲线Fig. 1 Change curves of dehydrogenase content with time in 4 kinds of solutions
2.2 电化学试验
2.2.1 1227杀菌剂的影响
由图2可见:在A溶液中,前3天,随着试样浸泡时间的延长,阻抗弧呈增大趋势,之后逐渐减小。

(a) A溶液

(b) B溶液图2 试样在A,B两种试验溶液中浸泡不同时间后的电化学阻抗谱Fig. 2 EIS of samples immersed in solutions A (a) and solution B (b) for different times
这是因为浸泡初期(1~3 d),细菌处于对数增长期,细菌数量逐渐达到最大值,在不锈钢表面形成生物膜,阻抗弧逐渐增大。之后,随着SRB进入衰亡期,代谢产物积累,短链脂肪酸和硫化物等含量增加,加速了不锈钢表面的腐蚀,阻抗弧逐渐减小。
在B溶液中,前7天,随着试样浸泡时间的延长,阻抗弧呈增大的趋势,之后逐渐减小。这是因为1227杀菌剂为典型的季铵盐类阳离子表面活性剂,季铵阳离子的极性基团与金属有较大亲和力而优先在金属表面吸附,形成疏水性表面,导致季铵阳离子不断在金属表面吸附成膜[11],浸泡后期(7~10 d),随着杀菌剂失效吸附成膜作用逐渐丧失,阻抗弧减小。总体来看,试样在B溶液中的阻抗弧大于在A溶液中的,这表明1227杀菌剂除了具有杀菌作用外,还具有一定的缓蚀作用。
由图3和表1可见:试样在B溶液中的腐蚀速率低于在A溶液中的。这是因为1227杀菌剂致使季铵阳离子不断在金属表面吸附成膜,从而阻碍了金属表面的析氢过程和金属离子向溶液扩散的过程,阻碍了微生物及代谢产物对不锈钢的腐蚀过程; 1227杀菌剂良好的杀菌效果很大程度上减少了SRB的数量,从而缓解了微生物对不锈钢的腐蚀。这与阻抗弧分析结果一致。

(a) A溶液

(b) B溶液图3 试样在A,B两种溶液中浸泡不同时间后的极化曲线Fig. 3 Polarization curves of samples immersed in solutions A (a) and solution B (b) for different times

试验溶液浸泡时间/dJ0/(μA·cm-2)E0/VVcorr/(mm·a-1)10.47850-0.38725.628×10-3A溶液30.32508-0.42633.842×10-370.44101-0.48495.187×10-3100.56368-0.44266.630×10-310.47725-0.43305.613×10-3B溶液30.36132-0.45224.233×10-370.25801-0.39003.035×10-3100.34783-0.44953.891×10-3
2.2.2 阻垢剂的影响
由图4可见:试样在C溶液中的阻抗弧更大,这表明PBTCA的缓蚀性更好。这是因为PBTCA中P原子的亲电活性程度更高[12],阻垢剂中的P原子与不锈钢表面Fe结合形成缓蚀膜的作用力更强,提高了不锈钢的耐蚀性。因此,PBTCA的缓蚀效果要优于HEDP的。
由图5和表2可见:浸泡初期,试样在C,D两种溶液中的腐蚀速率均逐渐上升;浸泡后期,试样在这两种溶液中的腐蚀速率明显小于在A溶液中的。这是因为HEDP/PBTCA分子中的磷酸根可与介质溶液中的Ca2+和Fe2+经过一系列反应,生成具有保护性的膜[13]。浸泡初期SRB数量大,阻垢剂形成缓蚀膜的作用不明显;浸泡后期为SRB的衰亡期,细菌数量逐渐减少,在HEDP/PBTCA作用下缓蚀膜不断修复,因而阻抗弧增大,腐蚀速率减小,这对不锈钢起到了一定的保护作用。由表2还可见:试样在D溶液中的腐蚀速率小于在C溶液中的,进一步说明PBTCA的缓蚀效果更好,这与阻抗谱的分析结果一致。

(a) 溶液C

(b) 溶液D图4 试样在C,D两种试验溶液中浸泡不同时间后的电化学阻抗谱Fig. 4 EIS of samples immersed in solutions C (a) and solution D (b) for different times

(a) C溶液

(b) D溶液图5 试样在C,D两种溶液中浸泡不同时间后的极化曲线Fig. 5 Polarization curves of samples immersed in solutions C (a) and solution D (b) for different times

试验溶液浸泡时间/dJ0/(μA·cm-2)E0/VVcorr/(mm·a-1)10.35881-0.41144.220×10-3C溶液30.48157-0.44485.664×10-370.33014-0.44783.883×10-3100.45738-0.39905.380×10-310.34311-0.43374.036×10-3D溶液30.47406-0.38045.576×10-370.33443-0.32893.934×10-3100.17686-0.24761.242×10-3
2.2.3 杀菌剂和阻垢剂的协同影响
以上的试验结果表明,7 d后杀菌剂/阻垢剂的作用比较稳定,测试了浸泡7 d后试样在A溶液、E溶液及F溶液中的腐蚀行为,以便分析杀菌剂、阻垢剂共同作用下316L不锈钢表面生物膜的电化学腐蚀行为。
由图6可见:溶液中加入1227+HEDP(E溶液)后,试样在此溶液中的阻抗半径明显小于在A溶液中的,且也小于在仅含有PBTCA溶液中的。这是因为1227是阳离子表面活性剂,显示一定正电性,而HEDP和PBTCA是阴离子表面活性剂,显示一定的负电性,因此两者在溶液中混合使用后,可以某种键的形式结合,降低了有机膦酸作为阻垢剂的活性,抵消了阻垢剂对不锈钢的缓蚀作用[14]。对比试样在溶液F与溶液E中的阻抗弧,可以发现PBTCA和1227同时使用时阻抗弧更大一些,这是因为PBTCA中P原子亲电活性程度更高,因而P原子与不锈钢表面Fe结合形成缓蚀膜的作用力更强,1227对PBTCA阻垢剂的抵消程度小。所以PBTCA+1227共同使用的效果优于HEDP+1227的。
由表3可见:试样在不同溶液中的腐蚀速率由小到大依次为:溶液D<溶液C<溶液A<溶液F<溶液E。这表明两种药剂同时使用,会相互抵消一部分功效。此外,对比腐蚀速率可看出,1227和PBTCA同时使用时比1227和HEDP同时使用的效果更好,单独作用时的效果均优于协同作用时的,这与电化学阻抗谱的分析结果一致。

(a) A,C,E溶液

(b) A,D,F溶液图6 试样在不同溶液中浸泡7 d后的电化学阻抗谱Fig. 6 EIS of samples immersed in different solutions for 7 d
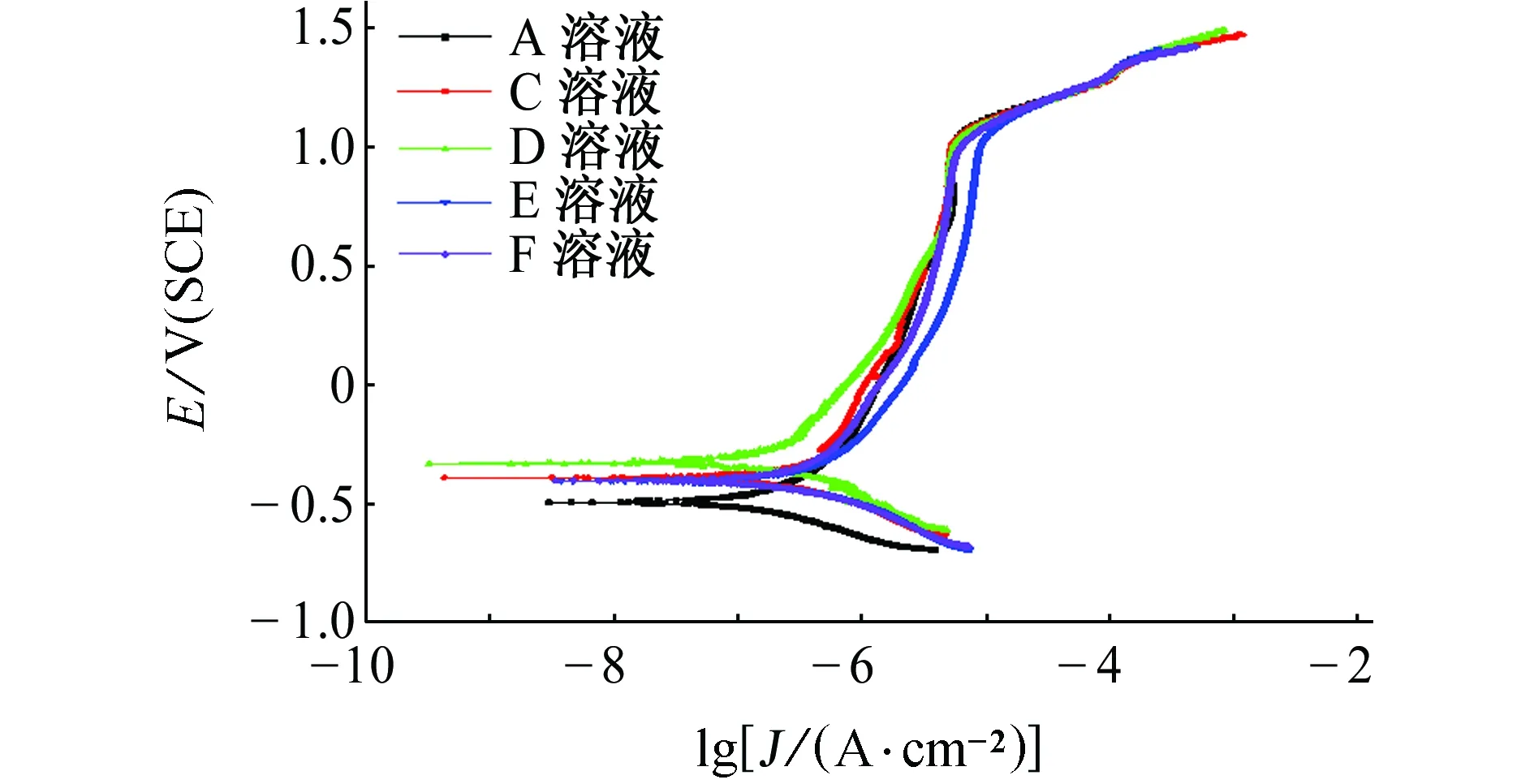
图7 试样在不同溶液中浸泡7 d后的极化曲线Fig. 7 Polarization curves of samples immersed in different solutions for 7 d

表3 在不同溶液中浸泡7 d后316L不锈钢的极化曲线的拟合结果Tab. 3 Fitting results of polarization curves of 316L stainless steel immersed in different solutions for 7 day
3 结论
(1) 从脱氢酶含量变化可知:添加HEDP和PBTCA,脱氢酶含量有所增加,微生物的生长得到促进;添加1227脱氢酶显著减少,微生物生长得到抑制。
(2) 由电化学分析结果可知:添加1227杀菌剂可以缓解微生物对不锈钢的腐蚀;添加HEDP、PBTCA阻垢剂会显著缓解微生物对不锈钢的腐蚀,而且PBTCA的缓蚀效果要优于HEDP的;联合使用1227+HEDP或1227+PBTCA时,会相互抵消一部分各自的功效。两者比较,1227+PBTCA的使用效果优于1227+HEDP的。
[1] 应一梅,周瑞云,杨崇豪,等. 循环冷却水输水管壁生物膜生长发育及微生物腐蚀问题研究[J]. 给水排水,2008,28(3):117-121.
[2] 张静,李进,王开强,等. 再生水中弗氏柠檬酸杆菌生物膜特性研究[J]. 环境化学,2011(10):1688-1694.
[3] 陈野,刘贵昌. 硫酸盐还原菌腐蚀的防治方法及其研究进展[J]. 腐蚀与防护,2004,25(3):102-108.
[4] 吕楠楠,梁磊,林建珍,等. 凝汽器不锈钢管锰致腐蚀初探[J]. 腐蚀与防护,2013,34(1):56-59.
[5] 孙彩霞,徐会武,陈燕敏,等. 异色唑啉酮和NaClO复合杀菌剂性能研究[J]. 清洗世界,2013,29(10):14-46.
[6] 朱雄伟,苏腾甲,李卫鹏,等. 三种杀菌剂杀灭硫酸盐还原菌的研究[J]. 广州化工,2012(11):65-67.
[7] 覃海华,李彩亭,刘海,等. PASP、PAA与PBTCA阻垢性能的对比试验研究[J]. 中国环境科学,2010,30(11):1466-1472.
[8] 曹英霞,杨坚,李杰. 阻垢剂PBTCA和HEDP阻垢机理探讨[J]. 同济大学学报,2004(4):556-560.
[9] 李今,吴振斌,贺锋. 生物膜活性测定中TTC-脱氢酶活性测定法的改进[J]. 吉首大学学报,2005,26(1):37.
[10] 孟琳,周丽萍,葛双启,等. 双季铵盐杀菌剂的合成及其杀菌性能研究[J]. 化学工程师,2005(4):59-60.
[11] 王旭珍,焦庆祝,郭相坤. 盐酸介质中苯扎氯胺在纯铝上的吸附、缓蚀作用[J]. 材料保护,2001(6):16-17.
[12] 崔崇威,李邵峰,杨红,等. PBTCA、HEDP、ATMP缓蚀性能的理论研究[J]. 材料科学与工艺,2006,14(6):608-611.
[13] 王霞,思玉琥,白媛丽. 缓蚀阻垢剂HEDP的制备及性能分析[J]. 应用化工,2012,41(1):33-36.
[14] 韩霞. 胜利油田采出水处理系统药剂配伍性研究[J]. 工业水处理,2010,30(1):32-34.

