环磷酰胺治疗特发性膜性肾病的疗效
刘玲玲 徐维玮 综述 刘志红 审校
膜性肾病(MN)是引起成人肾病综合征(NS)最常见的原因[1],中老年男性多发,病理表现为肾小球毛细血管袢上皮侧免疫复合物沉积,通常不伴有肾小管固有细胞增殖和局部炎症。特发性膜性肾病(IMN)是指排除了感染、肿瘤、系统性红斑狼疮等原发性疾病的MN。据南京总医院国家肾脏疾病临床医学研究中心40 759例肾活检病理资料显示,其发病率占原发性肾小球疾病的18.42%,仅次于IgA肾病[2]。磷脂酶A2受体(PLA2R)抗体是IMN的特异性抗体,研究显示IMN患者中,高达90.7%的患者血清PLA2R抗体或肾小球PLA2R抗原染色呈阳性。其中,血清PLA2R抗体阳性率为68.5%,肾小球PLA2R抗原阳性率为89.9%[3]。文献报道未经治疗的IMN患者31.7%可自发缓解,部分患者肾功能长期保持稳定,部分患者会进入终末期肾病或死亡[4]。而肾活检时血清肌酐升高及肾活检病理示肾小管间质慢性化病变重是影响IMN患者预后的独立危险因素,高龄和高血压亦与IMN患者的预后密切相关[5]。
目前文献报道用于治疗IMN的药物包括血管紧张素转化酶抑制剂(ACEI)/血管紧张素Ⅱ受体拮抗剂(ARB)、环磷酰胺(CTX)、他克莫司(FK506)、雷公藤多苷(TW)、环孢素A(CsA)、吗替麦考酚酯(MMF)、抗CD20单克隆抗体、促肾上腺皮质激素(ACTH)等。而CTX是2012年KDIGO指南推荐治疗成人IMN的首选药物[6]。本文就CTX治疗IMN的疗效机制、安全性及与其他药物的对比作一综述。
作用机制
CTX是一种无活性前体细胞毒类药物,须在肝脏中经微粒体功能氧化酶转化为4-羟基环磷酰胺,后者开环生成醛磷酰胺,两者为同分异构体,处于动态平衡。4-羟基环磷酰胺与醛磷酰胺经β消除可产生丙烯醛、磷酰胺氮芥(图1),后者为烷化剂,通过与DNA形成交叉联结结构,能抑制免疫细胞及肿瘤细胞的增殖,非特异地杀伤抗原敏感性小淋巴细胞,限制其转化为免疫母细胞,对体液免疫和细胞免疫均有抑制作用,因此常用于自身免疫性疾病及肿瘤的治疗。而丙烯醛则可产生膀胱炎、血尿等尿毒性症状[7-8]。

图1 环磷酰胺作用机制[7-8]
临床疗效
1958年,CTX作为抗肿瘤药物应用于临床[9],后逐渐应用于治疗类风湿性关节炎、系统性红斑狼疮、器官移植后排异反应、肾病综合征等疾病。1974年,文献报道了CTX治疗IMN患者随机对照试验(RCT),该研究纳入CTX治疗组11例,对照组11例,随访时间1年,最终结果为两组患者肾功能均保持稳定,CTX组蛋白尿平均下降4.7 g/24h,对照组下降2.6 g/24h,无统计学差异,这一结果可能与随访时间较短及研究对象较少有关[10]。1984年,意大利学者Ponticelli等[11]首次在《新英格兰医学杂志》上报道甲泼尼龙(MP)联合苯丁酸氮芥用于治疗IMN的RCT临床研究,实验组使用激素联合苯丁酸氮芥,对照组未使用免疫抑制剂治疗,分别通过31.4±18.2、37.0±20个月的随访,得出激素联合苯丁酸氮芥交替使用6个月有助于IMN患者蛋白尿缓解以及肾功能维持的结论,证实了细胞毒类药物对于IMN的治疗具有明显疗效,奠定了细胞毒类药物治疗IMN的重要临床地位。1998年,Ponticelli等[12]比较了CTX和苯丁酸氮芥治疗IMN的疗效,基于MP联合苯丁酸氮芥6月交替方案用药,第1、3、5个月静脉滴注MP 1 g/d连续3d,后口服MP 0.4 mg/(kg·d)或泼尼松0.5 mg/(kg·d)连续27d,第2、4、6个月停用,改口服CTX 2.5 mg/(kg·d)或氮芥0.2 mg/(kg·d)连续30d,总疗程6个月。随访1年时,CTX组蛋白尿的缓解率为93%,复发率25%,苯丁酸氮芥组缓解率和复发率分别为82%、30.5%,两者差异无统计学意义。随访3年时两组肾功能均稳定。该研究证明激素联合CTX或苯丁酸氮芥对于IMN蛋白尿的缓解及肾功能的维持均具有明显疗效。另一项随访长达10年的研究发现CTX较对症治疗可明显增加蛋白尿缓解率及肾脏存活率[13]。这些研究为CTX缓解IMN患者蛋白尿及维持长期肾功能稳定的疗效提供了确实的证据,但多局限于欧美人群。考虑到人种差异性,南京总医院国家肾脏疾病临床医学研究中心提出改良Ponticelli方案,即MP从1 g/d减量至0.5 g/d连续冲击3d,后口服泼尼松0.5 mg/(kg·d)连续27d,CTX仍为每2、4、6个月使用,但将口服CTX 2.5 mg/(kg·d)连续30天改为0.75 g/m2冲击治疗1次/月,总疗程6个月。此研究发现,随访6个月时,CTX治疗组完全缓解率31%,部分缓解率27.6%,总有效率为58.6%。而缬沙坦治疗组分别为0、9.7%、9.7%,差异具有统计学意义[14]。虽然本文仅纳入59例患者,随访6个月,其长期疗效仍有待进一步观察,但是对于说明CTX在亚洲人种的疗效具有一定的意义。1项纳入21个临床研究(19个来自中国,1个来自印度,1个来自希腊)的Meta分析得出激素联合CTX治疗组6个月总缓解率为64.7% ,12个月为77.4%的结论[15]。因此,激素联合CTX治疗亚洲人群IMN有显著疗效。但是CTX起效缓慢,文献报道CTX达到最佳临床疗效时间为1年左右[15-16]。
激素联合烷化剂治疗方案不仅对肾功能正常的IMN患者的长期肾功能具有保护作用,对已有肌酐升高的患者长期肾功能的维持也有帮助。1987年,West等[17]通过对照实验表明CTX对于肾功能不全的IMN患者肾功能的维持及蛋白尿的缓解具有明显的疗效。本实验入组患者血清肌酐均高于135 μmol/L,蛋白尿在肾病范围且经肾活检证实为IMN。研究共纳入26例,CTX治疗组9例(CTX平均100 mg/d,治疗23±4个月),对照组17例,分别经过49±10个月、50±6个月的随访,治疗组血清肌酐明显下降,而对照组血清肌酐明显上升,同时治疗组蛋白尿显著减少[17]。另一项入组患者血清肌酐均高于135 μmol/L的研究显示CTX治疗组5年肾存活率为86%,而对照组仅为32%[18]。也有研究发现与CTX同属于细胞毒类药物的苯丁酸氮芥较CsA或对症治疗对肾功能的维持有明显优势[19]。以上研究均表明,已有肾功能不全的患者使用CTX治疗仍可有效保护远期肾功能。
对于难治性或复发性IMN,CTX对蛋白尿的缓解以及长期肾功能的维持也有一定的疗效。CTX或氮芥治疗无效或复发的IMN患者,临床表现为肾病综合征且伴有肾功能不全(血清肌酐117~567 μmol/L,平均265 μmol/L),经再次激素联合CTX 1.5~2.0 mg/(kg·d)治疗12个月,10年肾脏存活率为86%。但由于该研究仅纳入15例患者且未设置对照组,所得结论尚需进一步研究证实[20]。
用药途径
CTX有口服和静脉冲击两种使用方法。有研究认为口服或静脉冲击治疗对维持肾功能及减少尿蛋白排泄率的效果并无明显差异,但静脉冲击治疗更有利于提高血清白蛋白水平[21]。另一研究认为,口服与静脉治疗起效时间有所不同,治疗3个月时口服有效率(48%)明显高于静脉冲击(18%),可能与口服治疗导致药物累积速度较快有关,两者缓解高峰无明显差异,均出现在治疗后12个月。而治疗后18个月时,静脉冲击完全缓解率(50%)明显高于口服治疗(24%),且复发率(3%)低于口服组(28%)[22]。总体而言,用药方式的优劣尚需进一步研究比较。
安全性
使用CTX常见的不良反应有出血性膀胱炎、骨髓抑制、恶心、呕吐、性腺功能障碍、肝功能损害、感染、心脏毒性、脱发、药物性皮炎、电解质紊乱等,而肿瘤则是远期不良反应。大约67%的患者会出现至少1种不良反应,其发生率及严重程度个体差异较大,大部分患者不良反应程度较轻,暂停用药或对症治疗后能迅速缓解,约10%需中断治疗[18,23]。一项纳入21个临床研究的Meta分析显示CTX相关不良反应发生率如下:感染(22.2%),粒细胞减少症(16.7%),肝功能损害(15.4%),脱发(10.9%),胃肠道不耐受(8.6%),葡萄糖不耐受(7.5%)[15]。CTX引起的肿瘤主要是膀胱癌、淋巴网状细胞瘤,并且肿瘤的发生率与CTX使用疗程和累积剂量呈正相关[24-25]。平均累积剂量20g的IMN患者相对于未用CTX治疗者6年癌症风险增加了3倍[26]。欧美患者采用6月交替方案时CTX累积剂量多不超过15g,少数患者采用连续口服CTX 1年治疗方案,累积剂量高达40g左右时,临床缓解率无明显差异,相应不良反应明显增加[12,14,27-29]。在本研究所使用的改良Ponticelli治疗方案中,CTX累积剂量多不超过8g,仅1例因肺部感染退出研究,余未见严重不良反应[14]。综上,使用CTX确实存在多种副作用,远期可增加肿瘤患病率,因此,出于安全性考虑,以下情况不建议使用CTX治疗:未控制的感染、肿瘤、尿潴留、无法随访监测的患者、血白细胞<4×109/L、血清肌酐>309 μmol/L。由于CTX副作用的发生率及严重程度与治疗疗程和累积剂量相关,KDIGO指南推荐激素联合CTX 6月交替方案最多使用2个疗程即CTX累积剂量不超过360 mg/kg[6]。根据南京总医院国家肾脏疾病临床医学研究中心提出的改良Ponticelli方案,CTX累积剂量8g既能产生明显疗效,副作用发生率也较低,可作为用药参考。
CTX与其他药物治疗IMN的疗效对比
在烷化剂之后,又出现了多种新型免疫抑制剂用于治疗IMN,CTX与这些免疫抑制剂相比较各有优缺点,其中代表性研究见表1。与苯丁酸氮芥相比,CTX对于IMN患者蛋白尿的缓解及肾功能的维持有类似的效果,但是副作用发生率更低[12,27]。钙神经蛋白抑制剂(CNIs)包括FK506、CsA等,是目前治疗IMN使用率较高的一类药物。与FK506相比,6个月时CTX组缓解率低于FK506组,12个月时两组缓解率相当,但复发率低于FK506组,两者不良反应发生率相当,但不良反应类型有所区别(表1)[16,28]。相关Meta分析也表明,通过6个月的随访,CTX组完全缓解率低于FK506组,但总缓解率、不良事件发生率无明显差异,且两组肌酐均保持稳定[30]。与CsA相比,9个月时CTX组缓解率明显高于CsA组,此外,CTX组肾功能明显改善,而CsA组肾功能显著下降[31]。相关Meta分析显示CTX起效时间晚于CsA,但两组最大缓解率无明显差异,且CTX组复发率低于CsA组,两组安全性各有优劣,CTX组白细胞减少症、脱发、肝功能异常发生率较高,而CsA组多毛症、牙龈增生、高血压、高尿酸血症的发生率较高[15]。总体来说,与CNIs相比,CTX虽起效缓慢,但1年疗效相当,且复发率更低。与TW相比,CTX起效时间晚,但是最大缓解率两者并无统计学差异,且复发率较低[32]。Meta分析显示两组胃肠道不适、肝酶升高、经期紊乱、白细胞减少等不良反应无统计学差异,而TW组脱发风险明显低于CTX组[33]。多个临床实验及meta分析均证实CTX在有效性、安全性、复发率方面均优于MMF[34-35]。CD20单抗等生物制剂正越来越多的用于治疗IMN,研究表明CTX较利妥昔单抗部分缓解率高,但是完全缓解率无明显差异,而CTX治疗组不良反应发生率明显高于利妥昔单抗组[36]。近年促肾上腺皮质激素(ACTH)也开始用于治疗肾病综合征,有研究表明CTX与ACTH治疗总缓解率无明显差异,但CTX组副作用发生率明显低于ACTH组[29]。根据以上研究结果,CTX对IMN的治疗效果及副作用的发生率并不劣于其他免疫抑制剂,且复发率较低。
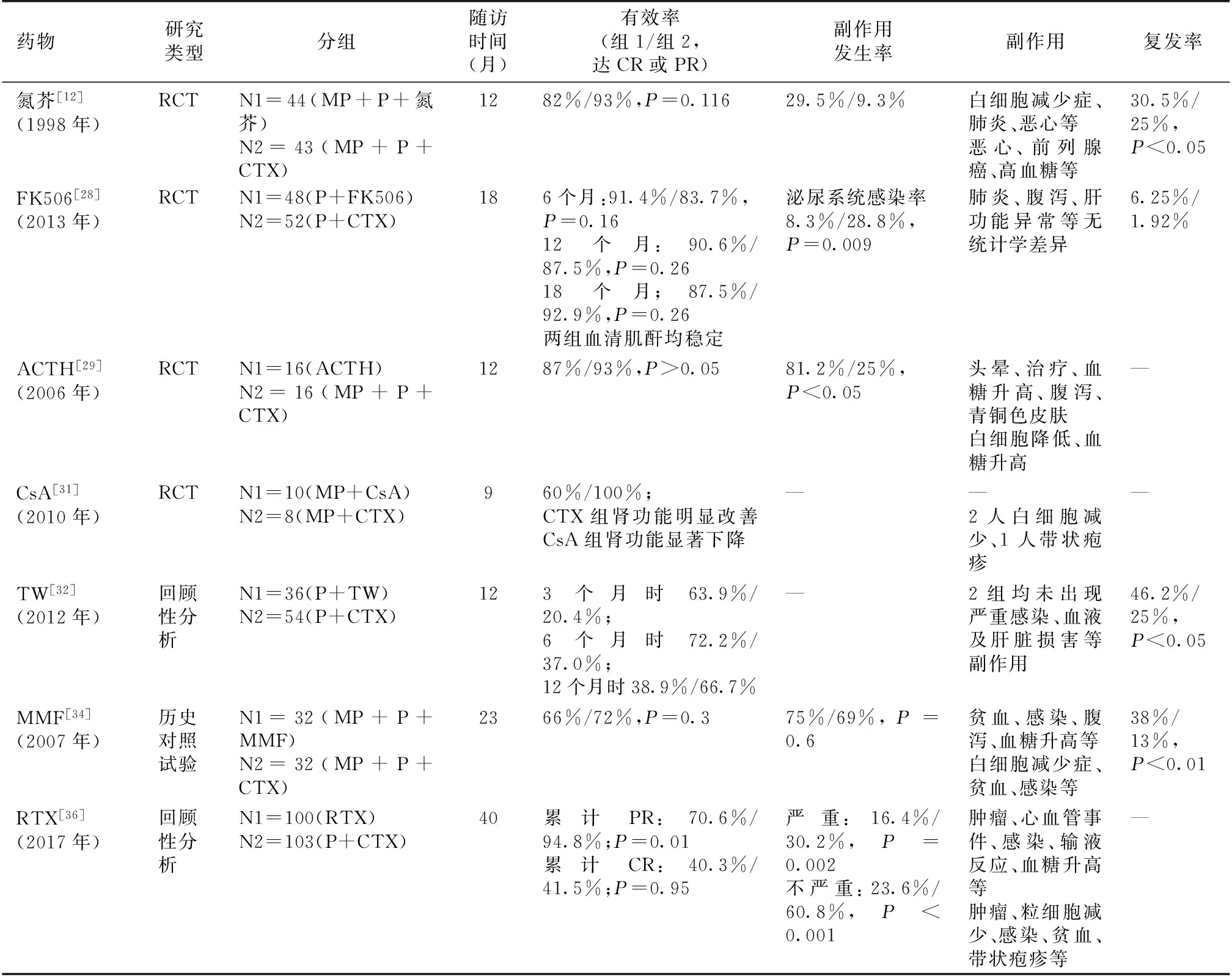
表1 CTX与其他药物治疗IMN的疗效对比
IMN:特发性膜性肾病;CTX:环磷酰胺;FK506:他克莫司;CsA:环孢素A;TW:雷公藤多苷;MMF:吗替麦考酚酯;RTX:利妥昔单抗;ACTH:促肾上腺皮质激素;MP:甲泼尼龙;P:泼尼松;RCT:随机对照试验;CR:完全缓解;PR:部分缓解
综上所述,CTX作为一种使用史长达半世纪的细胞毒类药物,因其疗效确切、价格低廉,临床应用广泛,在肿瘤、自身免疫性疾病的治疗中发挥着重要的作用。虽然CTX在治疗IMN中存在一定的不足,如起效缓慢、增加肿瘤患病率等,但是大量临床试验证实CTX对蛋白尿的缓解及肾功能的维持并不劣于其他免疫抑制剂,因此CTX仍是治疗IMN的良好选择。因CTX治疗副作用的发生率和严重程度与治疗疗程和累积剂量相关,所以临床应用需把握适应症及用量,且在用药过程中严密监测白细胞、尿蛋白定量等指标。
1 Hofstra JM,Wetzels JF.Management of patients with membranous nephropathy.Nephrol Dial Transplant,2012,27(1):6-9.
2 Hou JH,Zhu HX,Zhou ML,et al.Changes in the spectrum of kidney diasease:an analysis of 40759 biopsy-proven cases from 2003 to 2014 in China.Kidney Disease,2017.
3 Qin HZ,Zhang MC,Le WB,et al.Combined Assessment of Phospholipase A2 Receptor Autoantibodies and Glomerular Deposits in Membranous Nephropathy.J Am Soc Nephrol,2016,27(10):3195-3203.
4 Polanco N,Gutiérrez E,Covarsí A,et al.Spontaneous remission of nephrotic syndrome in idiopathic membranous nephropathy.J Am Soc Nephrol,2010,21(4):697-704.
5 Zuo K,Wu Y,Li SJ,et al.Long-term outcome and prognostic factors of idiopathic membranous nephropathy in the Chinese population.Clin Nephrol,2013,79(6):445-453.
6 Drüeke TB,Parfrey PS.Summary of the KDIGO guideline on anemia and comment:reading between the (guide)line(s).Kidney Int,2012,82(9):952-960.
7 de Jonge ME,Huitema AD,Rodenhuis S,et al.Clinical pharmacokinetics of cyclophosphamide.Clin Pharmacokinet,2005,44(11):1135-1164.
8 Batista CK,Brito GA,Souza ML,et al.A model of hemorrhagic cystitis induced with acrolein in mice.Braz J Med Biol Res,2006,39(11):1475-1481.
9 Brock N,Wilmanns H.Effect of a cyclic nitrogen mustard-phosphamidester on experimentally induced tumors in rats; chemotherapeutic effect and pharmacological properties of B 518 ASTA.Dtsch Med Wochenschr,1958,83(12):453-458.
10 Donadio JV,Holley KE,Anderson CF,et al.Controlled trial of cyclophosphamide in idiopathic membranous nephropathy.Kidney Int,1974,6(6):431-439.
11 Ponticelli C,Zucchelli P,Imbasciati E,et al.Controlled trial of methylprednisolone and chlorambucil in idiopathic membranous nephropathy.N Engl J Med,1984,310(15):946-950.
12 Ponticelli C,Altieri P,Scolari F,et al.A randomized study comparing methylprednisolone plus chlorambucil versus methylprednisolone plus cyclophosphamide in idiopathic membranous nephropathy.J Am Soc Nephrol,1998,9(3):444-450.
13 Jha V,Ganguli A,Saha TK,et al.A randomized,controlled trial of steroids and cyclophosphamide in adults with nephrotic syndrome caused by idiopathic membranous nephropathy.J Am Soc Nephrol,2007,18(6):1899-1904.
14 吴燕,左科,王波,等.激素联合环磷酰胺治疗特发性膜性肾病前瞻性对照性临床观察.肾脏病与透析肾移植杂志,2012,21(2):109-114.
15 Qiu TT,Zhang C,Zhao HW,et al.Calcineurin inhibitors versus cyclophosphamide for idiopathic membranous nephropathy:A systematic review and meta-analysis of 21 clinical trials.Autoimmun Rev,2017,16(2):136-145.
16 Li ZQ,Hu ML,Zhang C,et al.Efficacy and safety of tacrolimus vs.cyclophosphamide for idiopathic membranous nephropathy:A meta-analysis of Chinese adults.J Huazhong Univ Sci Technolog Med Sci,2015,35(5):623-628.
17 West ML,Jindal KK,Bear RA,et al.A controlled trial of cyclophosphamide in patients with membranous glomerulonephritis.Kidney Int,1987,32(4):579-584.
18 du BPW,Branten AJ,Wetzels JF.Cytotoxic therapy for membranous nephropathy and renal insufficiency:improved renal survival but high relapse rate.Nephrol Dial Transplant,2004,19(5):1142-1148.
19 Howman A,Chapman TL,Langdon MM,et al.Immunosuppression for progressive membranous nephropathy:a UK randomised controlled trial.Lancet,2013,381(9868):744-751.
20 du BPW,Wetzels JF.Efficacy of a second course of immunosuppressive therapy in patients with membranous nephropathy and persistent or relapsing disease activity.Nephrol Dial Transplant,2004,19(8):2036-2043.
21 Dede F,Ayili D,Sahiner S.Effective treatment administration of cyclophosphamide in membranous nephropathy.J Nephrol,2008,21(4):560-565.
22 孙燕,高妍婷,王晓明.环磷酰胺口服及冲击治疗特发性膜性肾病的疗效比较.临床肾脏病杂志,2015,15(10):626-628.
23 Hofstra JM,Wetzels JF.Alkylating agents in membranous nephropathy:efficacy proven beyond doubt.Nephrol Dial Transplant,2010,25(6):1760-1766.
24 Wall RL,Clausen KP.Carcinoma of the urinary bladder in patients receiving cyclophosphamide.N Engl J Med,1975,293(6):271-273.
25 Baltus JA,Boersma JW,Hartman AP,et al.The occurrence of malignancies in patients with rheumatoid arthritis treated with cyclophosphamide:a controlled retrospective follow-up.Ann Rheum Dis,1983,42(4):368-373.
26 van den Brand JA,van Dijk PR,Hofstra JM,et al.Cancer risk after cyclophosphamide treatment in idiopathic membranous nephropathy.Clin J Am Soc Nephrol,2014,9(6):1066-1073.
27 Branten AJ,Reichert LJ,Koene RA,et al.Oral cyclophosphamide versus chlorambucil in the treatment of patients with membranous nephropathy and renal insufficiency.QJM,1998,91(5):359-366.
28 Xu J,Zhang W,Xu Y,et al.Tacrolimus combined with corticosteroids in idiopathic membranous nephropathy:a randomized,prospective,controlled trial.Contrib Nephrol,2013,181:152-162.
29 Ponticelli C,Passerini P,Salvadori M,et al.A randomized pilot trial comparing methylprednisolone plus a cytotoxic agent versus synthetic adrenocorticotropic hormone in idiopathic membranous nephropathy.Am J Kidney Dis,2006,47(2):233-240.
30 Santosh T,Liu H,Liu B.Effect of tacrolimus in idiopathic membranous nephropathy:a meta-analysis.Chin Med J (Engl),2014,127(14):2693-2699.
31 Kosmadakis G,Filiopoulos V,Smirloglou D,et al.Comparison of immunosuppressive therapeutic regimens in patients with nephrotic syndrome due to idiopathic membranous nephropathy.Ren Fail,2010,32(5):566-571.
32 孙铁忠,何晓芳.雷公藤多甙与环磷酰胺分别联合泼尼松治疗特发性膜性肾病疗效比较.武警后勤学院学报(医学版),2012,21(9):678-681,封3.
33 Chen YZ,Gong ZX,Cai GY,et al.Efficacy and safety of Flos Abelmoschus manihot (Malvaceae) on type 2 diabetic nephropathy:A systematic review.Chin J Integr Med,2015,21(6):464-472.
34 Branten AJ,du BPW,Vervloet M,et al.Mycophenolate mofetil in idiopathic membranous nephropathy:a clinical trial with comparison to a historic control group treated with cyclophosphamide.Am J Kidney Dis,2007,50(2):248-256.
35 Xie G,Xu J,Ye C,et al.Immunosuppressive treatment for nephrotic idiopathic membranous nephropathy:a meta-analysis based on Chinese adults.PLoS One,2012,7(9):e44330.
36 van den Brand JAJG,Ruggenenti P,Chianca A,et al.Safety of Rituximab Compared with Steroids and Cyclophosphamide for Idiopathic MembranousNephropathy.J Am Soc Nephrol,2017,28(9):2729-2737.

