蒽酮-硫酸显色法测定栽培白及的白及多糖含量*
李德旺,邓 芳,汪 胜
(湖南省衡阳市食品药品检验检测中心,湖南 衡阳 421001)
白及具有收敛、止血、清热利湿、消肿生肌之功效,用于治疗咳血、吐血、外伤出血、疮疡肿毒、皮肤皲裂、溃疡出血等症,富含白及胶[1]。现代药理研究表明,白及胶能抑制肿瘤血管生成,兼有抗感染、抗肿瘤和促进凝血的功能[2-3],其主要成分为大分子多糖[4]。2015年版《中国药典(一部)》对白及的质量控制仅见性状、显微鉴别和薄层色谱鉴别,未对白及中具有药理活性的白及多糖进行质量控制。为评价栽培白及内在质量,本研究中采用蒽酮-硫酸显色法测定其多糖含量,并与野生白及进行比较,探讨其变异性。
1 仪器与试药
1.1 仪器
Agilent Cary60型紫外可见分光光度计(美国安捷伦公司);Mettler Ae 240型电子天平(瑞士梅特勒公司);GZX-9146MBE型电热鼓风干燥箱(上海博讯实业有限公司);TG16-Ⅱ型医用离心机(湖南平凡科技有限公司)。
1.2 试药
D-无水葡萄糖(中国食品药品检定研究院,批号为110833-201506,浓度为100%);蒽酮(分析纯,国药集团化学试剂有限公司,批号为20170706);硫酸(优级纯,国药集团化学试剂有限公司,批号为20170108);试验用水为试验室自制纯化水。野生白及(湖南衡岳中药饮片有限公司,采于湖南南岳后山区,批号为171003,171004);栽培白及(湖南衡岳中药饮片有限公司中药材种植基地,批号为 160901,160902,171001,171002);市售白及(市场购入,产地云南,批号为 20161201,170511),以上药材均经本中心副主任中药师王先教鉴定为兰科白及属植物白及 Bletilla striata(Thunb.ex A.Murray)Rchb.f.的干燥块茎,且符合药典标准[5]。
2 方法与结果
2.1 溶液制备
试液:0.2%蒽酮-硫酸溶液的配制,取蒽酮,精密称定0.301 2 g,加80%硫酸溶液100 mL使溶解,摇匀即得(棕色瓶保存或临用时配制)。
对照品溶液:取 D-无水葡萄糖对照品,精密称定0.032 38 g,置100 mL容量瓶中,加水溶解并稀释至刻度,摇匀,即得对照品溶液(D-无水葡萄糖对照品使用以100%计,即每1mL中含 D-无水葡萄糖0.3238mg)。
供试品溶液:取经60℃干燥12 h的白及供试品粉末0.3 g,精密称定,置圆底烧瓶中,加入60 mL水,加热回流提取1 h,趁热用布氏漏斗滤过,残渣及烧瓶用热水洗涤3次,每次10 mL,合并滤液和洗液,放冷,转移至100 mL容量瓶中,加水至刻度,摇匀,溶液滤过,精密量取续滤液0.5 mL,加入4 mL丙酮,摇匀,静置10 min,离心,倾去上清液,沉淀加水溶解,转移至10 mL容量瓶中,加水至刻度,摇匀,精密量取2 mL,照标准曲线制备项下方法,自“在冰水浴中缓缓加0.2%蒽酮-硫酸溶液至刻度”起,依法测定吸光度,计算百分含量。
2.2 检测波长选择
取对照品溶液,稀释成0.009 7 g/L,按标准曲线制备项下方法显色后,在200~800 nm波长范围内扫描,色谱图见图1。选取最大吸收波长582 nm作为检测波长。

图1 D-无水葡萄糖紫外吸收光谱图
2.3 方法学考察
标准曲线制备:精密量取对照品溶液 0.1,0.2,0.3,0.4,0.5,0.6 mL,分别置 10 mL 具塞试管中,各加水至2.0 mL,混匀,在冰水浴中缓缓加0.2%蒽酮-硫酸溶液至刻度,混匀,放冷后置水浴中保温10 min,取出,立即置冰水浴中冷却10 min,取出,以相应试剂为空白。照紫外-可见分光光度法,在582 nm波长处测定吸光度。以吸光度(Y)为纵坐标、质量浓度为横坐标(X),绘制标准曲线,得回归方程 Y=24.11X-0.001,R2=0.996(n=6)。结果表明,D-无水葡萄糖质量浓度在3.238~19.428 μg/mL范围内与吸光度线性关系良好。
精密度试验:精密吸取对照品溶液(0.097 1 g/L),按拟订色谱条件,重复进样6次,测定。结果吸光度平均值为 0.252 9,RSD 为 0.12%(n=6),表明仪器精密度良好。
重复性试验:称取样品(批号为171001)6份,依法测定,计算含量。结果平均含量为34.44%,RSD为0.32%(n=6),表明方法重复性良好。
稳定性试验:取白及(批号为171001),依法制备供试品溶液,分别于放置 20,40,60,90,120,150 min 后上样测定。结果的 RSD为1.27%(n=6),供试品溶液在90 min内 D-无水葡萄糖吸光度基本稳定。
加样回收试验:取样品(批号为171001)精密称定0.3 g 6份,分别精密加入0.032 4 mg的 D-无水葡萄糖,依法测定。结果见表1。
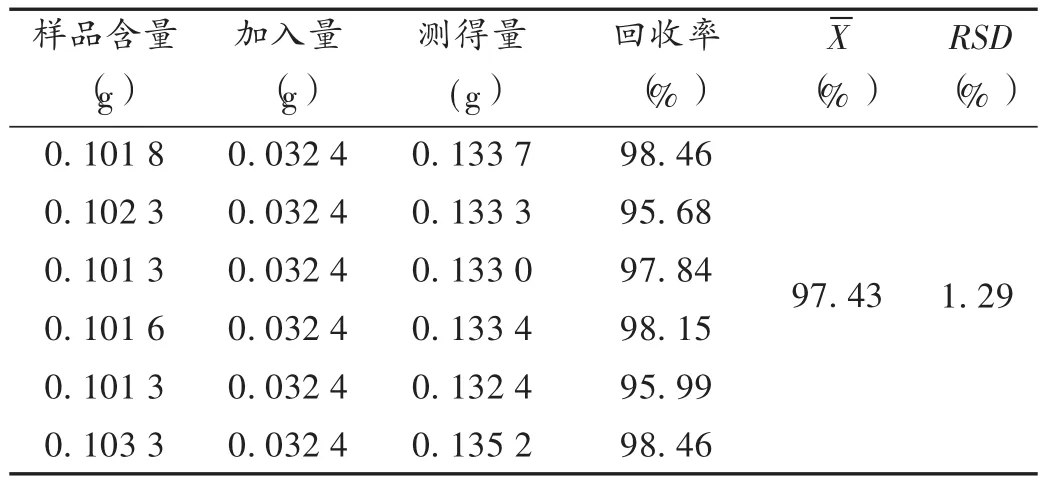
表1 D-无水葡萄糖加样回收试验结果(n=6)
2.4 样品含量测定
结果见表2。

表2 不同批次白及多糖含量测定结果(以 D-无水葡萄糖计,n=6)
3 讨论
3.1 显色法选择
考察了苯酚-浓硫酸显色法,其样品测定结果重复性较差,且苯酚毒性较大,易氧化,试验前需进行纯化处理[6-7],操作烦琐;而蒽酮-硫酸显色法测定结果较稳定,操作简便,故采用蒽酮-硫酸显色法进行测定。
3.2 样品提取方法选择
比较了以稀乙醇去杂质再水提的方法与水提醇沉法测定白及多糖含量,2种方法测定结果较接近,但前者过滤时间太长,后者操作简便,故选择水提醇沉法。
3.3 方法优势
紫外分光光度法是一种常用的分析方法,应用范围广,成本较低,操作快速、简便,同时具有良好的稳定性和重复性[8];2015年版《中国药典(一部)》白及项下的相关检测项不能对其具有药理活性的相关成分进行相应评价,方法精密度、重复性和准确度良好,可作为评价其内在质量的参考方法。
3.4 样品测定情况分析
结果显示,栽培白及2年生样品与3年生样品相比,白及多糖含量差异显著,栽培白及3年生样品白及多糖含量与野生白及、市售白及相近,表明栽培白及采挖时限至少3年;结合其外在形态特征符合药典标准,表明该种植基地从野外引种的白及栽培变异不明显,植物形态稳定,野生引种块茎繁殖的技术方法可行,可加大规模种植和推广力度。同时,将继续跟进该种植基地,研究4年生、5年生白及的白及多糖含量,筛选效益最高、质量最优的种植方案。
[1]肖培根.新编中药志(第一卷)[M].北京:化学工业出版社,2001:320.
[2]冯敢生,李 欣,郑传胜,等.中药白芨提取物抑制肿瘤血管生成机制的试验研究[J].中华医学杂志,2003,83(5):412.
[3]徐小炉,尹 刘,程元芝,等.白芨栓塞治疗中晚期肝癌的临床观察[J].实用癌症杂志,2000,15(6):640-641.
[4]罗新根,刘文庸,张卫东.中药白及的化学成分及临床研究进展[J].药学实践杂志,1999,17(6):359.
[5]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:103.
[6]丁 玲,王 东,张中林,等.不同商品地山药多糖含量的分析[J].辽宁中医药大学学报,2009,11(4):187-188.
[7]杨 春,杨金笛,林 帅.菊花、野菊花中的总糖含量测定[J].山西中医,2009,24(6):40-41.
[8]王 雷,杨新建,寇 欣.紫外分光光度法在中药分析中的应用进展[J].天津药学,2003,15(5):62-64.

