老年高剂量四价流感病毒裂解疫苗的研究
余军 杨文彬 杨宪普 帅旗 赵越 张赟 朱实惠 蒋正东 吴建华 赵静付建林
225300泰州,江苏金迪克生物技术有限公司
中国是流感高发地区[1-2],自1957年以来中国大陆和香港发生了几次流感大流行,其病毒株也源于两地[3-6]。流感和并发性肺炎在成人(≥40岁)死亡的主要原因中排名第四[7]。流感在老年人群中可引起高致病率和高病死率,随着年龄增长,尤其70岁以上,除了由急性流感和继发性细菌性肺炎造成的死亡外,流感还可增加缺血性心脏病、脑血管疾病、糖尿病人群的住院率和死亡率[8]。由于老年人免疫力低下,现有的流感疫苗对老年人的保护不力,疫苗效力低于青壮年(分别为68.6%和74%)[9]。疫苗免疫效力可能只有健康成人的60%并且效力随着年龄增加及免疫力衰退的加剧而下降[8]。由于目前中国拥有世界上最大的老年人口(>8 000万),今后随老年人口继续增加,流感流行将造成更大的健康危害和社会经济负担[10]。
目前世界上只有高剂量的三价疫苗和加佐剂标准剂量疫苗应用于≥65岁老年人群[11],它们缺乏对另一谱系的B型流感病毒的预防,需要提供新型高剂量流感疫苗和新的接种方式以增加免疫原性并提供更多保护。国外迄今还没有四价老年流感疫苗,国内尚无任何老年流感疫苗。本研究的目的是在本公司研发的四价流感病毒裂解疫苗的基础上研制适用于老年高危群体的安全有效的流感疫苗。
1 材料与方法
1.1 材料
1.1.1 流感疫苗:采用2016—2017年流感季WHO推荐疫苗株:A1(A/California/7/2009,H1N1)、A3(A/Hong Kong/4801/2014)、B1(B/Brisbane/60/2008,B/Victoria)和 B2(B/Phuket/3073/2013,B/Yamagata),从英国国家生物标准与控制研究所(NIBSC)引进。采用本公司研制并经检定合格的流感病毒疫苗单价原液分别配制成标准剂量和高剂量试验动物用疫苗(具体免疫剂量的计算参见2.2)。第一、二批试验所用四型单价原液批号分别为:YA120161001(HA 含量 190 μg/ml)、YA320161001(HA 含量 286 μg/ml)、YB120161001(HA 含量 129 μg/ml)和 YB220161001(HA 含量 112 μg/ml);第三批试验所用四型单价原液批号分别为:YA120161003(HA 含量 231 μg/ml)、YA320161003(HA 含量 445 μg/ml)、YB120161003(HA 含量 251 μg/ml)和 YB220161003(HA 含量 286 μg/ml);标准剂量两针试验所用四型单价原液批号分别为:YA120170601(HA 含量 199 μg/ml)、YA320170601(HA 含量 273 μg/ml)、YB120170601(HA 含量 106 μg/ml)、YB220170601(HA 含量 277 μg/ml)。
1.1.2 主要试剂及仪器:A1(H1N1)、A3(H3N2)、B1(B/Victoria)和 B2(B/Yamagata)流感病毒标准抗原参考品、标准抗体参考品均来源于NIBSC;霍乱滤液购自美国SIGMA公司;氯化钠等常规试剂均为国产或进口分析纯产品;三用电热恒温水箱购自天津市泰斯特仪器有限公司,型号为SHHW21-420;纯水仪Milli-Q低热原型购自法国Millipore公司,型号为A10;漩涡震荡仪购自IKA公司,型号为V2S025;台式低速离心机购自湖南湘仪实验室仪器开发有限公司,型号为L500;数控超声波清洗器购自昆山市超声仪器有限公司,型号为KQ5200DE。
1.2 免疫原性试验
1.2.1 实验动物:SPF级KM小鼠,18~22 g,购自北京维通利华实验动物技术有限公司。随机分组,每笼5~6只。
1.2.2 免疫剂量:近年来新药药效研究中多以以下公式计算实验动物给药剂量:
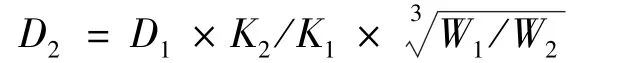
其中D为药物剂量,K为常数,W为动物体重(Kg),人及不同种类动物的K值不同,如人10.6、小鼠9.1[12]。根据以上给药公式及现在市场上常规注射流感疫苗的血凝素含量15μg/株/剂。计算小鼠标准剂量肌肉注射流感疫苗血凝素含量应为4.5μg/株/剂[13]。
本试验使用的高剂量流感疫苗每株血凝素的浓度为18μg/株/剂是标准剂量的4倍[14]。将单价原液分别配制为高剂量、标准剂量四价流感病毒裂解疫苗和高剂量、标准剂量A+B套苗,其中A苗含A1和A3型血凝素高剂量为各18μg/株/剂,标准剂量为各4.5μg/株/剂,B苗含B1和B2型血凝素高剂量为各18μg/株/剂,标准剂量为各4.5μg/株/剂,并分两次接种小鼠,下文中均根据A+B套苗接种先后顺序称为先A苗后B苗或先B苗后A苗。
1.2.3 试验设计
1.2.3.1 免疫剂量及次数试验分组:将小鼠随机分为7组,试验组每组12只以上,分别为:高剂量单次免疫组、高剂量先A苗后B苗组、高剂量先B苗组后A苗组、标准剂量单次免疫组、标准剂量先A苗后B苗组、标准剂量先B苗后A苗组及PBS对照组。重复3次。
1.2.3.2 高剂量二针间隔时间选择试验分组:将小鼠随机分为9组,分别为:先A苗后B苗间隔3 d组、7 d组和10 d组;先B苗后A苗间隔3 d组、7 d组和10 d组。其中试验组每组15只,对照组每组5只。
1.2.3.3 免疫方法和采血时间:每只小鼠经后腿肌肉注射,注射量控制在0.25 ml以内。两次免疫的小鼠,免疫间隔均为7 d。单次免疫和第二次免疫后21 d,小鼠眼眶采血,分离血清,置-20℃保存待测。1.2.4 血凝抑制试验:每份血清经霍乱滤液处理,进行血凝抑制试验,测定其抗体滴度。血凝抑制试验使用来自NIBSC的标准抗原及标准血清以确定和配制血凝抑制试验中所使用的四个血凝单位的抗原浓度。采用微量半加敏法测定每份小鼠血清的抗血凝素抗体滴度。
1.2.5 免疫原性的判定:抗体滴度为采用血凝抑制法(HI)测定血清中对所有的原型病毒株的抗血凝素抗体,以达到完全抑制凝集最高稀释度的倒数表示。同时设有阳性和阴性血清的参考标准。血凝抑制效价≥40,判为阳性血清;效价 <40,为阴性血清[13]。

表1 不同免疫剂量及次数试验阳转率Tab.1 Seroconversion rate of the assay of immunization dose and frequency
1.3 统计学方法 统计各组小鼠血清阳转率及血凝抑制抗体几何平均滴度(HI GMT)[3]。血凝抑制试验实验结果以平均几何滴度±标准差表示。为便于计算,任何 HI<10表示为5[13]。 运用 SPSS16.0统计软件对各组试验数据进行Mann Whitney test检验对抗体水平进行显著性检验分析,以P<0.05为显著性差异。“∗”表示P<0.05,“∗∗”表示P<0.01,“∗∗∗”表示 P <0.001。
2 结果
本实验测定动物免疫后血清中抗血凝素抗体滴度,并计算血清阳转率和抗血凝素抗体几何平均滴度。
2.1 比较动物接种不同剂量次数、阳转率和抗血凝素抗体 测定7组共261份小鼠血清的抗血凝素抗体滴度。
2.1.1 计算各组阳转率:除高剂量组、标准剂量组和PBS组的单次注射组外,其余先A苗后B苗组、先B苗后 A苗组均为两针注射,间隔7 d,重复3次。
表1结果显示,高剂量单次免疫组和高剂量A+B套苗组免疫动物血清中抗各种血凝素抗体均呈现高的阳转率。高剂量单次免疫组血清中抗各种血凝素抗体的阳转率远高于标准剂量的单次免疫组,A3型除外。高剂量A+B套苗组血清中抗各种血凝素抗体的阳转率与标准剂量A+B套苗组阳转率相近似,高剂量A+B套苗组血清中抗B1型血凝素抗体阳转率远高于标准剂量A+B套苗组。无论是高剂量还是标准剂量,两次免疫组阳转率均高于单次免疫组。整体表明,高剂量组血清阳转率优于标准剂量组,两次免疫组优于单次免疫组。
2.1.2 高剂量和标准剂量单次免疫动物后抗血凝素抗体反应:对单次免疫时高剂量与标准剂量组抗血凝素抗体滴度比较显示(表2),高剂量单次免疫组抗各种血凝素抗体滴度均高于标准剂量单次免疫组,特别是 A1、B1和 B2(P <0.001),PBS组无抗血凝素抗体产生。
2.1.3 比较A+B套苗免疫后动物抗体反应
2.1.3.1 比较标准剂量A+B套苗免疫后动物抗体反应:先A苗后B苗组或先B苗A苗组,进行两次免疫,间隔7 d。
表3结果显示标准剂量A+B套苗无论是先A苗后B苗组,还是先B苗后A苗组,各中抗血凝素抗体滴度均高于表2中标准剂量单次免疫组。
2.1.3.2 比较高剂量A+B套苗免疫动物后抗体反应:无论是高剂量组中(表2和表4)还是在标准剂量组中(表2和表3),在免疫总剂量相同时,A+B套苗两次免疫的效果优于单次免疫。

表2 单次免疫高剂量组与标准剂量组免疫后抗血凝素抗体滴度比较Tab.2 Comparison of the HI titers of one high and standard dose groups

表3 标准剂量A+B套苗两次免疫组抗血凝素抗体滴度比较Tab.3 Comparison of the HI titers of standard dose A+B serial vaccine groups
表3和表4中有更令人注意的一致性结果:高剂量A+B套苗和标准剂量A+B套苗如采取先A苗后B苗的免疫方式,其抗B1和B2的血凝素抗体滴度高于先B苗后A苗组中的抗B1和B2的血凝素抗体滴度;反之,如采取先B苗后A苗的免疫方式,其抗A1和A3型血凝素抗体滴度高于先A苗后B苗组的抗A1和A3型血凝素抗体滴度。除高剂量先A苗后B苗组抗B1型血凝素抗体滴度与先B苗后A苗组抗B1型血凝素抗体滴度差异无统计学意义外,其余各组相应型别的抗血凝素抗体滴度差异均有统计学意义(P<0.001)。
2.2 高剂量A+B套苗免疫两次的时间选择 为了进一步探究A+B套苗两次免疫的间隔时间对抗体产生的影响,设高剂量单次免疫组、先A苗后B苗组、先B苗A苗组为实验组,PBS对照组,试验组动物总数为15只,对照组为5只,测其单次免疫和间隔3 d、7d和10 d两次免疫的小鼠血清中的抗血凝素抗体滴度和阳转率。

表4 高剂量A+B套苗两次免疫组抗血凝素抗体滴度比较Tab.4 Comparison of the HI titers of HD A+B serial vaccine groups
本次试验高剂量单次免疫组和先A苗后B苗组、先B苗后A苗组免疫最终血凝素总含量都为72μg。
学科核心素养是学科育人的集中体现,是学生通过学科学习而逐步形成的正确价值观念、必备品格和关键能力。语文学科核心素养是学生在积极的语言实践活动中积累与构建起来,并在真实的语言运用情境中表现出来的语言能力及其品质;是学生在语文学习中获得的语言知识与语言能力,思维方法与思维品质,情感、态度与价值观的综合体现。主要包括“语言建构与运用”“思维发展与提升”“审美鉴赏与创造”“文化传承与理解”四个方面。那么,如何通过语文教学提升学生的语文学科素养呢?笔者认为,阅读和表达能力的培养是提升学生语文学科素养的根本途径和基本手段。
从表5可见,当先接种B苗,隔7 d再接种A苗时,除对A3和B1型抗原的血清阳转率为93.33%外,其他各组对四型抗原的血清阳转率均为100%。该结果表明,两次免疫的间隔时间及免疫先后顺序对A+B套苗血清阳转率的影响没有显著差异。
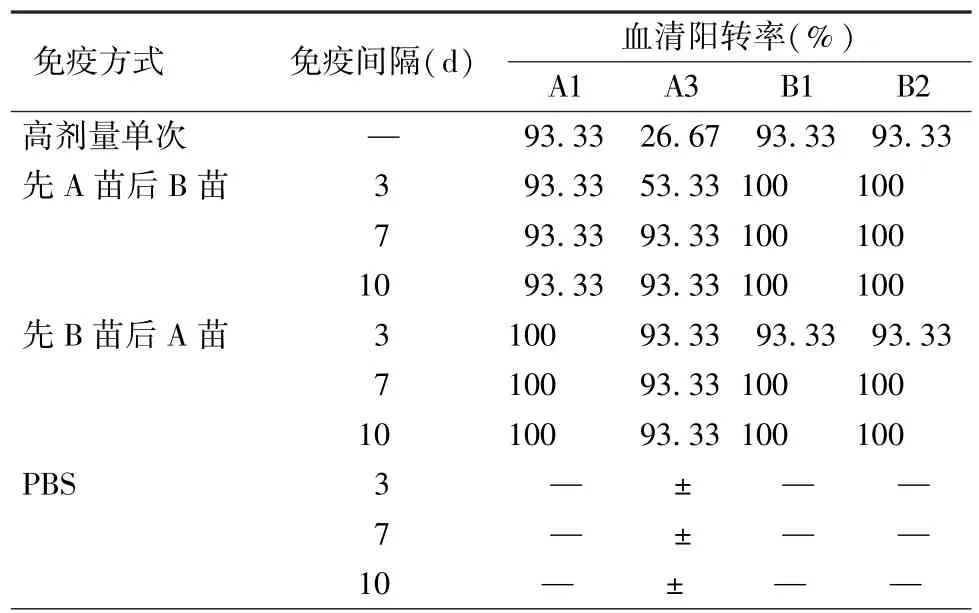
表5 高剂量A+B套苗两次免疫间隔时间和阳转率Tab.5 Seroconversion rate of the immunization intervals of HD A+B serial vaccine
两次免疫时间间隔的选择是以抗血凝素抗体滴度的高低来确定最优免疫时间间隔。测定一次高剂量和两次高剂量A+B套苗分别间隔3、7、10 d的抗血凝素抗体滴度,见表6。
从表6可见,高剂量A+B套苗组和高剂量的单次免疫组所使用的血凝素总剂量相同,在高剂量A+B套苗组,两次免疫间隔3、7、10 d的动物血清抗血凝素抗体滴度高于高剂量单次免疫。高剂量A+B套苗7 d和10 d组的各项抗血凝素抗体滴度均高于3 d组。同时再次证实,与表2和表3中的结果一致。先A苗后B苗组中,抗B型血凝素抗体滴度增加显著;先B苗后A苗组中,抗A型血凝素抗体滴度明显增加,P<0.001。
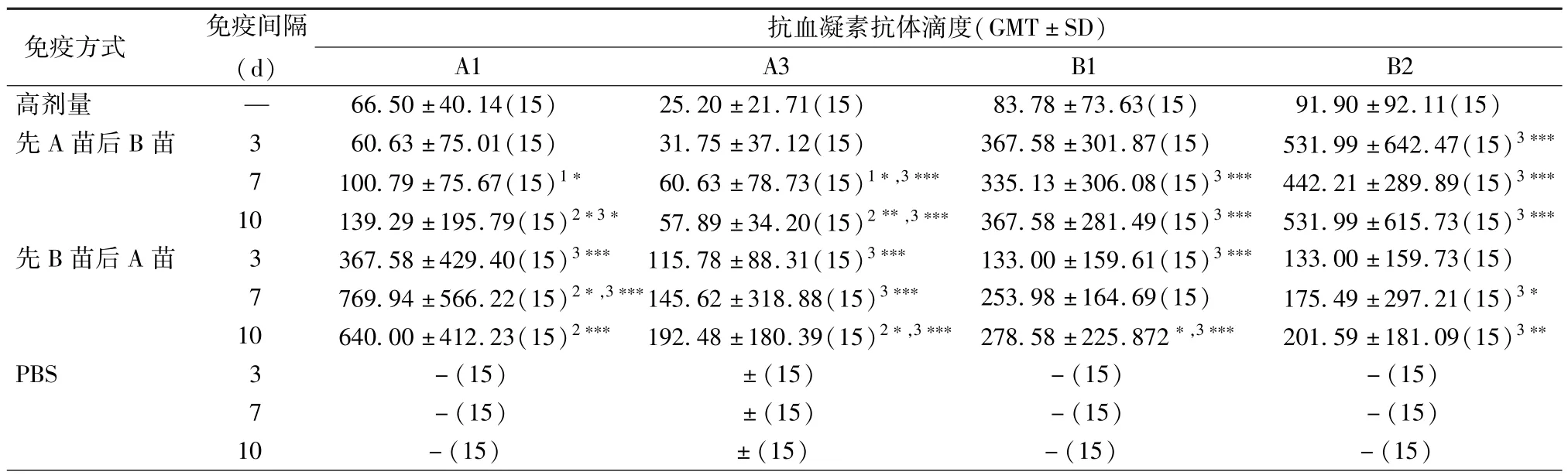
表6 高剂量A+B套苗免疫间隔时间对动物产生抗血凝素抗体滴度的比较Tab.6 The effect of immunization intervals on the immunogenicity of different antigens
3 讨论
每年都有A型和B型流感病毒引起的季节性流感,特别是老年人群易受流感病毒感染,造成高发病率和病死率。流感疫苗是预防季节性流感的最佳手段,但是我国老年人群接种疫苗的比例不足仅5%。因为老年人免疫力低下、免疫反应较差[15],传统的标准流感疫苗对老年人群的保护力不够,并随着年龄增加而下降。因此需要研制更有效的疫苗。有临床研究证明,提高疫苗中流感血凝素含量的高剂量疫苗可在老年人群中诱导比标准剂量疫苗更高的免疫反应[8]。目前国外没有四价高剂量老年流感疫苗,国内尚无任何老年流感疫苗。
赛诺菲公司进行的高剂量三价流感疫苗Fluzone 的研究表明[11,16],高剂量 Fluzone 在65 岁以上老年群体中预防流感时,比标准剂量Fluzone更有效,产生的血清抗体滴度显著高于标准剂量Fluzone,是安全性的。高剂量的三价Fluzone疫苗每针剂中每株血凝素含量为60μg,总血凝素含量为180μg;标准剂量的三价Fluzone疫苗每针剂中每株血凝素含量为15μg,总血凝素含量为45μg。赛诺菲高剂量三价Fluzone疫苗是2009年12月获得FDA批准上市,由Glaxo Smith Kline公司生产四价流感疫苗Fluarix于2012年7月20日经FDA批准上市[17]。历经多年,并无高剂量四价流感疫苗出现,其原因可能是,若按高剂量三价流感疫苗的配方,每剂四价高剂量的流感疫苗,每株病毒血凝素含量为60μg,其总血凝素含量高达240μg。随着血凝素含量的增加可以推测其注射后副反应相应增加。因此,本研究设计老年高剂量四价流感疫苗A+B套苗,将疫苗分为A苗和B苗,分两次免疫,如用于人群免疫,每次总血凝素含量不超过120μg,低于高剂量三价疫苗血凝素总量,其注射后免疫反应应随之减少而更安全。当然,对于已有高剂量三价流感疫苗,是否可以通过增加注射一次高剂量另一B型血凝素达到加强免疫反应还有待验证,也不失为一种研制老年流感疫苗的新途径。
高剂量A+B套苗中高血凝素含量可增加疫苗免疫原性,诱生更高水平的抗血凝素抗体。高剂量的A+B套苗如果采用先A苗后B苗的免疫方式,其抗B1和B2型的血凝素抗体滴度高于先B苗后A苗组;反之,如先B苗后A苗的免疫方式,其抗A1和A3型的血凝素抗体滴度高于先A苗后B苗组。同样的结果在标准剂量的A+B套苗组等试验中证实。因此,可根据当年对A型和B型流感病毒流行病学监测,选择或改变使用先A苗后B苗或者是先B苗后A苗的免疫顺序,增加疫苗的保护效果。
免疫间隔时间试验结果则再次证明了高剂量A+B套苗相对于高剂量单次免疫疫苗在免疫原性方面的显著优越性,间隔7 d和10 d的免疫反应优于间隔3 d,原因是流感病毒A型和B型抗原间存在共同抗原[18],在第2次免疫对共同抗原产生更高的免疫应答,提供第2次免疫时间可灵活选择7~10 d。
本研究研发高剂量四价流感A+B套苗,为免疫力低下、对高剂量疫苗的副反应耐受性差的高危老年人群提供一种安全有效、新型老年流感疫苗和免疫模式。
利益冲突 无

