术前超选择栓塞富血运脑膜瘤的临床疗效分析
李捷 龙霄翱 莫伟 梁远生 尹延庆 黄拔齐
脑膜瘤是仅次于星形细胞瘤的发生率第二高的颅内原发性肿瘤,多数生长慢、病程长,患者的颅内压增高不明显,在肿瘤被发现时往往生长体积巨大,且由于多数脑膜瘤都接受颅内、外动脉的双重供血,因此常规开颅手术切除时出血量较多[1],特别是对富血运的巨大脑膜瘤及一些无法在切除肿瘤早期对肿瘤基底供血动脉进行电烧或结扎等止血处理的,对脑膜瘤进行术前供血动脉的栓塞能减少开颅手术的出血量[2-3],促使肿瘤软化坏死[4],降低手术切除的难度。本研究现对2013年1月-2017年6月本院收治的34例采用术前介入栓塞方法治疗的富血运脑膜瘤,回顾性分析其栓塞程度、开颅切除肿瘤的出血量及肿瘤切除程度,为临床治疗提供更多的依据及参考。
1 资料与方法
1.1 一般资料 回顾性分析本院2013年1月-2017年6月收治的34例脑膜瘤患者,术前均行全脑血管造影(DSA)造影,证实为富血运脑膜瘤,术后均经病例证实为脑膜瘤;其中男15例,女19例,根据使用的栓塞材料分为2组,PVA组15例,采用PVA颗粒栓塞;明胶海绵组12例,采用明胶海绵进行栓塞。另有7例在行DSA后未进行栓塞直接手术,为未栓塞组,共3组。未栓塞组在行DSA后未予进一步栓塞的有以下几个原因:(1)肿瘤供血动脉同时对正常功能区的脑组织进行供血;(2)肿瘤的供血分支过细或迂曲,微导管未能到达治疗栓塞位置;(3)患者及其家属不能接受术前栓塞可能发生的风险或费用,仅同意行全脑血管造影术。
1.2 纳入及排除标准
纳入标准:(1)DSA显示肿瘤染色明显;(2)术后病理确诊为脑膜瘤。
排除标准:(1)术前影像学检查显示肿瘤体积较小、部位表浅、强化及水肿不明显等提示直接开颅手术难度不大,直接进行手术切除者;(2)因肿瘤卒中或术前脑疝而直接行急诊手术切除,而术前未予行全脑血管造影术评估者;(3)患者因全身状况不佳或凝血功能障碍,有严重肝脏或肾脏功能不全者,仅予行肿瘤供血动脉栓塞者而未予手术切除肿瘤;(4)已对肿瘤进行过放射治疗者。
1.3 治疗
患者采用局部浸润麻醉,采用Seldinger技术,经皮穿刺右侧股动脉置管,用5F椎动脉造影导管对双侧颈内、颈外和椎动脉进行造影,确定肿瘤供血动脉及染色情况。如果肿瘤染色明显,供血动脉无过分迂曲及细小,则改上6F指引导管,全身静脉肝素化,根据目标血管情况将微导丝微导管头端塑性好,多数采用大C型塑型或单弯塑型,在路图下通过微导丝(TraxcesS-10)将微导管(Marathon漂浮导管)超选进入肿瘤供血动脉分支,可以让飘浮导管随着动脉血流的流动自由飘浮前进,缓慢到供血动脉远端,在靠近目标血管或者飘浮导管无法顺利通过迂曲或者分叉血管时将导丝头端伸出微导管,依靠反复旋转微导丝,将微导丝超选进入目标血管,到达一定深度,支撑力足够以后固定微导丝,推送微导管,在微导管即将到达目标血管时一边推送微导管一边回撤微导丝,利用相反作用力将微导管轻柔的送入目标血管,最后撤出微导丝;由于肿瘤供血血管因为通常为病理血管,血管壁常比正常血管脆弱,使用微导丝时应避免盲目推送,动作一定要轻柔,防止刺破血管壁导致肿瘤卒中;超选进入目标血管后应尽量多角度观察供血动脉,选取尽可能将供血血管全程显露的位置,这不仅有利于超选进入目标血管,还能保证在栓塞时及时判断造影剂有无返流;在排除供血动脉没有对正常脑组织或脑神经进行供血,再次明确肿瘤的供血动脉没有危险吻合后注入固体栓塞剂(PVA颗粒或明胶海绵颗粒),对病灶血管床及供血动脉进行栓塞;注射时注意观察血管显影情况及肿瘤染色情况变化,掌握好注射力度,缓慢注射,要均匀用力,力量柔和,避免PVA颗粒或明胶海绵颗粒反流甚至误栓,直至造影见肿瘤供血动脉血流明显减慢、造影剂滞留及染色明显变淡后再次造影,直至肿瘤染色完全消失或大部分消失(图1),最后拔出微导管,重新造影确认栓塞效果,如果肿瘤是由多支颈内外动脉的分支进行供血,需分次上微导管超选择性栓塞;术毕,拔出导管鞘,穿刺点压迫止血;栓塞术后3~5 d予行开颅肿瘤切除术。

图1 后颅窝脑膜瘤术前血供丰富,肿瘤染色明显,经介入栓塞后肿瘤血供明显减少,染色消失
1.4 疗效评价和不良反应观察 栓塞效果采用栓塞术后栓塞的肿瘤染色完全消失和大部分消失的例数来评价;手术效果采用术中出血量、肿瘤全切和肿瘤次全切的例数来判定;术后记录与介入栓塞相关的并发症发生情况。
1.5 统计学处理
2 结 果
2.1 栓塞效果 34例患者术前DSA检查可见脑膜瘤供血动脉主要为颈外动脉系统供血的占8例,由颈内动脉及颈外动脉双重供血的占20例,单纯颈内动脉供血的4例,椎动脉系统供血的2例,其中脑膜中动脉分支参与供血的最多,达26例,其次为大脑前动脉分支8例。栓塞后均无严重并发症出现,栓塞术后到手术切除的平均时间为(4.35±2.2)d。其中12例使用明胶海绵栓塞;15例使用PVA颗粒栓塞;明胶海绵组栓塞的肿瘤染色完全消失3例,大部分消失9例;PVA颗粒组栓塞的肿瘤染色完全消失9例;大部分消失6例(表1)。经χ2检验,υ= 1,理论频数> 5,PVA组与明胶海绵组的栓塞程度有明显差异(χ2=6.32,0.025 表1 栓塞程度比较(例) 注:与PVA组比较,*P<0.05 2.2 手术效果 PVA栓塞组手术切除术中出血量为(350±135)mL,明胶海绵栓塞组手术切除术中出血量为(475±265)mL,未予栓塞组手术切除术中出血量为(660±350)mL,经多样本的秩和检验比较3组之间有明显差异(P=0.015)。术中出血量两两比较中PVA组与未栓塞组比较有明显差异(P=0.012),明胶海绵组与PVA组比较有明显差异(P=0.032),明胶海绵组与未栓塞组比较有明显差异(P=0.014)。所有病例在栓塞后3~5 d手术,PVA组肿瘤全切14例,次全切除1例;明胶海绵组全切11例,次全切1例,未栓塞组全切7例,次全切0例(表2),其中栓塞的病例手术时因为出血更少,所以术野更清晰,术中均可见肿瘤瘤体较为苍白、部分的肿瘤瘤体中央有不同程度的坏死,坏死部分质地软,容易吸除。未栓塞组7例患者有5例需要输血,而PVA颗粒组只有2例在术中进行了输血,明胶海绵组有3例患者在术中进行了输血。 表2 手术效果比较 注:这里的肿瘤全切指肿瘤全部切除并切除肿瘤累及的硬膜和颅骨,或电灼肿瘤附着硬膜;次全切除指肿瘤全切除,肿瘤附着的硬膜没有任何处理;或肿瘤大部分切除,只剩少量包绕终于血管神经的肿瘤残余;与未栓塞组比较,*P<0.05;与明胶海绵组比较,△P<0.05 脑膜瘤是颅内发生率第二高的肿瘤,发病率仅次于星形细胞瘤,它们多数可能来自蛛网膜细胞。大部分的脑膜瘤属于良性肿瘤,最直接有效的治疗方法是开颅手术切除肿瘤,大多数脑膜瘤都能直接开颅全切,预后良好,但部分脑膜瘤发现时已经体积巨大,血供丰富,又或者与周围重要的血管、神经以及脑组织的关系密切,或者肿瘤位置较深,手术视野深且狭小,肿瘤基底在手术时难以早期阻断,术中早期难以止血容易导致术野不清,误伤神经、血管或脑功能区,从而产生严重的并发症[5],肿瘤组织也不易完全剔除,进而导致术后复发[6]。大量的术中出血也使手术输血量大大增加,增加了血库的压力,术后贫血也延长了恢复及住院时间,给患者及社保等带来沉重的经济负担。因此,研究表明如果能对这部分富血运脑膜瘤在开颅手术前进行介入栓塞,阻断或者减少肿瘤的血供[7],能减少手术切除时的术中出血量,而且栓塞后血供明显减少,能使脑膜瘤坏死、软化,这样肿瘤与周围正常组织分界会变清,术中出血变少也能使术野更加清晰,从而使手术操作更加简单,能有效缩短手术时间、降低手术并发症及复发率[1]。 随着介入材料的发展,已有越来越多的栓塞材料适合进行脑膜瘤的术前栓塞。这些栓塞材料包括固体的栓塞材料如PVA颗粒、明胶海绵、液体的栓塞材料如NBCA、Gubran、Onyx等[5]。本研究采用了PVA颗粒及明胶海绵颗粒作为栓塞材料,PVA颗粒是应用最为广泛的脑肿瘤栓塞材料[8],它是不可溶于水的惰性物质,虽然PVA颗粒之间的血栓被溶血酶降解后肿瘤血管会发生再通,被组织吸收缓慢,但一般在数周到数个月后才会开始降解[1],所以栓塞后早期手术基本不会出现血管再通的情况。从技术上说,PVA易于通过微导管注射。使用大颗粒的PVA可减少误栓正常血管的风险,需要注意的是PVA的高摩擦系数会引起导管的堵塞;PVA颗粒不可透射线,需要与显影剂混合,以观察造影剂的弥散及回流情况及栓塞程度。但PVA颗粒的价格较贵,作为辅助治疗,较为稍微加重了患者的经济负担。明胶海绵颗粒虽然摩擦系数更大,导致比PVA颗粒更容易堵管[9],但作为廉价的栓塞材料在经济上有明显优势,也较常被使用。 在选择颗粒大小的问题上越小的栓塞颗粒越容易到达瘤内的微小血管,也越容易完全栓塞肿瘤血供,但小的颗粒也更容易误栓危险吻合及正常血管[10],大的颗粒虽然不容易到达更细小的供血动脉,且比小颗粒更容易堵管[11],但却不容易发生误栓,术前的栓塞作为治疗富血运脑膜瘤辅助方案,本研究更看重的是要将并发症发生率控制在比单纯手术切除更低的范围内,因此为了防止误栓事件的发生,本研究都选用了300 μm以上的颗粒进行栓塞,所有病例均没有发生部分文献报道的误栓事件、肿瘤卒中、颅神经麻痹、头皮坏死等严重并发症[12]。 从研究结果来看,PVA颗粒比明胶海绵颗粒更容易完全栓塞肿瘤的供血血管,这与明胶海绵颗粒的大小不如PVA颗粒均匀,且摩擦系数更高,更容易堵管有关。由于PVA颗粒组完全栓塞的病例更多,所以手术切除时发现PVA颗粒组的肿瘤中心坏死程度比明胶海绵组更高,肿瘤分离更容易。在出血量上PVA颗粒组的平均出血量为(350±135)mL,明胶海绵组的出血量为(475±265)mL,两者差异有统计学意义,PVA颗粒组术中出血明显较明胶海绵组少,而明胶海绵组的出血量也明显较未栓塞组少,术后也发现未栓塞组需要输血的病例更多。 但在最终全切的病例上,3组间却无明显差别,明胶海绵组及PVA颗粒组均有1例次全切除,其余患者均达到完全切除。2例未全切病例,1例是前颅窝底巨大脑膜瘤,肿瘤包绕眼动脉分支,为保护眼动脉,残留少量包绕血管的肿瘤;另1例是岩斜区巨大脑膜瘤,与脑干黏连紧密,压迫脑干,在与脑干紧密黏连部分残余少量肿瘤包膜;同时这还说明了脑膜瘤的全切程度更多的是与生长部位,有无累及重要的神经及血管有关。 综上所述,术前介入栓塞富血运脑膜瘤的供血动脉,能能明显减少术中出血,更少的出血可以帮助患者术后更快的康复,也能减少输血的情况,从而降低输血的相关并发症,也能减轻血库的压力。但显微外科的进步,使脑膜瘤的全切率大大提高,术中出血的减少并没有提高肿瘤的全切率,介入栓塞供血动脉是富血运脑膜瘤手术切除术前的一项安全、有效及有益的辅助手段,采用PVA颗粒能更好地栓塞供血动脉,更好地减少出血,而对于患者远期的预后而言,仍需进一步追踪观察。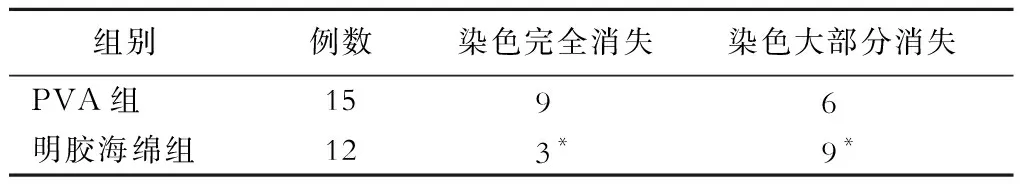
3 讨 论

