高碱煤含钠矿物沉积层的高温熔融及多相反应过程分析
靳 虎,王泽安,阳 维,宁 坚,谢逸豪,刘 豪
(华中科技大学 煤燃烧国家重点实验室,湖北 武汉 430074)
新疆煤炭资源储量丰富,其中准东煤田预测储量达3.9×1011t[1]。但由于新疆煤富含碱金属Na,导致燃用过程中极易出现沾污、结渣,给锅炉的高效运行造成安全隐患[2]。准东煤中Na主要以原子、氧化物、氯化物形式释放,有机硫和黄铁矿则氧化为SO2[3],Na原子、气态的NaCl易与烟气中的SO2反应,生成大量的Na2SO4,气态的Na2SO4随后冷凝在受热面形成积灰内层[4-9],随着内层变厚,表面迎烟侧形成黏性的熔融或半熔融基体。此外,一部分Na、Ca硫酸盐附着于飞灰颗粒表面,使得灰颗粒的黏性增加[10],不同粒径的灰颗粒通过布朗运动、热泳、惯性运动、冷凝以及化学反应等方式被黏性的硫酸盐初始积灰层捕获[11],形成烧结层。沉积层厚度增加使得表面温度随之升高,新捕获的灰颗粒在表面熔化、团聚,并与煤灰矿物质之间发生复杂的反应,生成新的低温共熔物,形成致密渣层[3,12]。
矿物组分决定沉积层的熔融特征,含Na物质能够降低灰熔点,陈晓东等[13]研究了气化条件下Na2O对灰熔融的影响,韩克鑫等[14]研究了Na基矿物与煤灰的作用机制,Qi等[15]研究了Na基矿物对煤的结渣特性影响。Wei等[11]在350 MW锅炉渣层中发现,渣层出现分层现象,内层硫含量较高,外层Na含量高且都含有硬石膏。此外,无水芒硝、钠长石、钠钙硫酸盐、钠铁硫酸盐、钠钙硅铝酸盐是灰沉积中重要矿物[3,16,17]。
如前所述,碱金属硫酸盐的沉积是沾污结渣的重要原因[3-12,16,17],已有研究主要集中在:对沉积层取样分析推测沾污结渣的形成和发展过程;将Na盐添加到煤或煤灰中,研究其熔融和结渣特性[13-15];但由于沉积层与煤灰的元素含量有较大差异[3],因此,它的熔融过程及沉积过程中Na2SO4和其他矿物的反应过程也不相同,目前,对富硫酸盐沉积层的熔融特性和不同硫酸盐含量与矿物反应过程研究报道较少。因此,本研究采用热机械分析(TMA)、高温煅烧实验研究了不同Na2SO4含量、不同温度下沉积灰的熔融和多相反应过程,有助于深入理解Na2SO4在沾污、结渣过程中与沉积矿物的作用机理。
1 实验部分
1.1 实验原料
沉积层是易挥发碱金属与部分煤灰矿物经过凝结、黏附以及长时间的高温多相反应(包括熔融)形成,因此,沉积层中矿物相成分非常复杂;已有的研究者主要从化学组成、断面元素含量等方面对沉积层中易结渣矿物的富集行为进行分析[18,19],进而推测灰沉积的形成和发展过程。本研究在前人对沉积层化学组成分析的基础上[8,11],采用CaO、SiO2、Al2O3、Fe2O3、 MgO、Na2SO4的混合物模拟典型沉积层中各元素的含量,较为直观地考察Na的掺量对沉积层矿物熔融和反应过程的影响。
研究表明,灰沉积中的硅铝比(S/A)一般在3左右,Ca含量也较高[3,8,11]。Wei等[11]发现屏式过热器沉积层内层和外层元素含量有明显差异,Na含量在2%-10%,S含量在8%-15%,以Na2SO4来模拟沉积层中的Na和S,因此,掺混比(以Na2SO4/沉积矿物的质量分数计)选择10%-60%。
实验采用化学纯(CP)矿物按质量比来配制,保持CaO、SiO2、Al2O3、Fe2O3、MgO的矿物相对比例不变,将掺混比分别为0、10%、20%、40%、60%的Na2SO4与上述矿物混合制成样品S1-S5,各实验样品的组成见表1。由于燃烧产生的飞灰颗粒细小[20],实验时将各矿物粉碎和研磨后筛到平均粒度小于74 μm,通过机械振荡30 min使其充分混合。
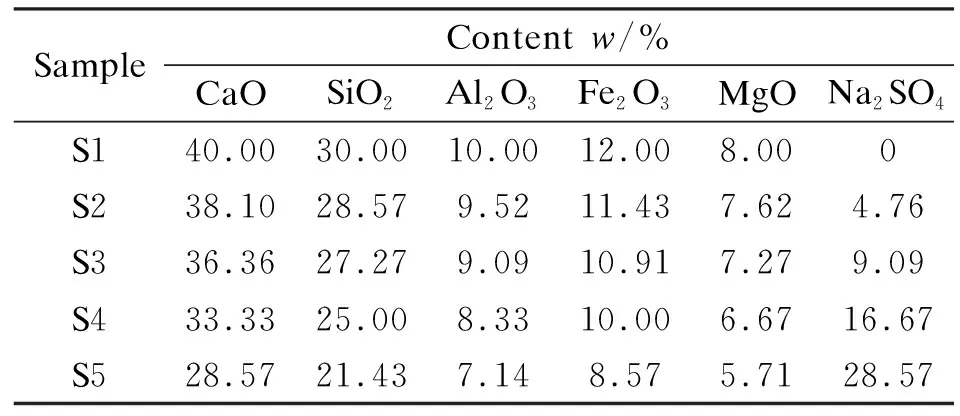
表 1 样品的化学组成
1.2 热机械分析(TMA)和综合热分析(TG-DSC)
TMA可以反映煤灰在升温过程中是否发生了膨胀、收缩、熔化等现象及煤灰熔融的快慢[21]。此外,它还可以预测煤粉锅炉的灰沉积行为,基于TMA判别煤灰结渣指标与实际具有较好的一致性[21-23]。通常研究者主要采用传统灰熔点测试(AFT)煤灰熔融和结渣特性[13,15],但TMA比AFT具有更高精度和更好的重复性,通常的角锥法测得的灰熔点误差为±40 ℃,TMA只有±10 ℃[23]。本研究采用法国SETARAM公司的热机械分析仪(Setsys Evo)来研究样品的熔融过程。将大约20 mg样品置于钼制坩埚,以1 MPa的压力压紧,将探头插入坩埚,随后一起放置到TMA仪器中,探头连杆施加2 g负载。以高纯N2净化15 min,样品以15 ℃/min的速率从室温加热至900 ℃,随后以5 ℃/min加热到1500 ℃。加热过程记录探头的位移并计算出样品收缩比例。TG-DSC分析采用耐驰STA449F3,在20%O2/80%N2气氛下,以10 ℃/min由室温升至1300 ℃。
1.3 高温煅烧实验
将所有样品用高温电阻炉(SX4-5-17Q,中国武汉亚华炉业有限公司)在空气气氛下以10 ℃/min的恒定加热速率从室温加热至四个目标温度:800、1000、1100和1200 ℃,然后再保温1 h。在空气中快速冷却后,采用X射线衍射仪来分析样品中的矿物相组成。实验采用德国Bruker公司生产的D8 Advance X射线衍射仪,CuKα辐射(波长λ= 0.15406 nm),石墨单色器。扫描以5(°)/ min的恒定扫描速率从5°至90°(2θ角),加速电压为40 kV,相应的电流为40 mA。同时采用带有能谱仪的扫描电子显微镜(SEM-EDS)对不同温度下制备的渣样的微观结构进行表征。实验采用德国蔡司的Ultra Plus扫描电镜,放大倍数为12-1×106倍。此外,能谱仪还能半定量的分析样品的特定区域的元素组成。
2 结果与讨论
2.1 Na盐沉积层熔融过程分析
图1为不同Na2SO4掺混比样品的TMA收缩曲线。由图1可知,含有Na2SO4的沉积灰与沉积矿物具有完全不同的收缩曲线,而不同Na2SO4的含量的收缩曲线具有相似性,尤其是当掺混比为10%、20%、40%时,这表明此掺混比条件下具有相似的熔融过程。
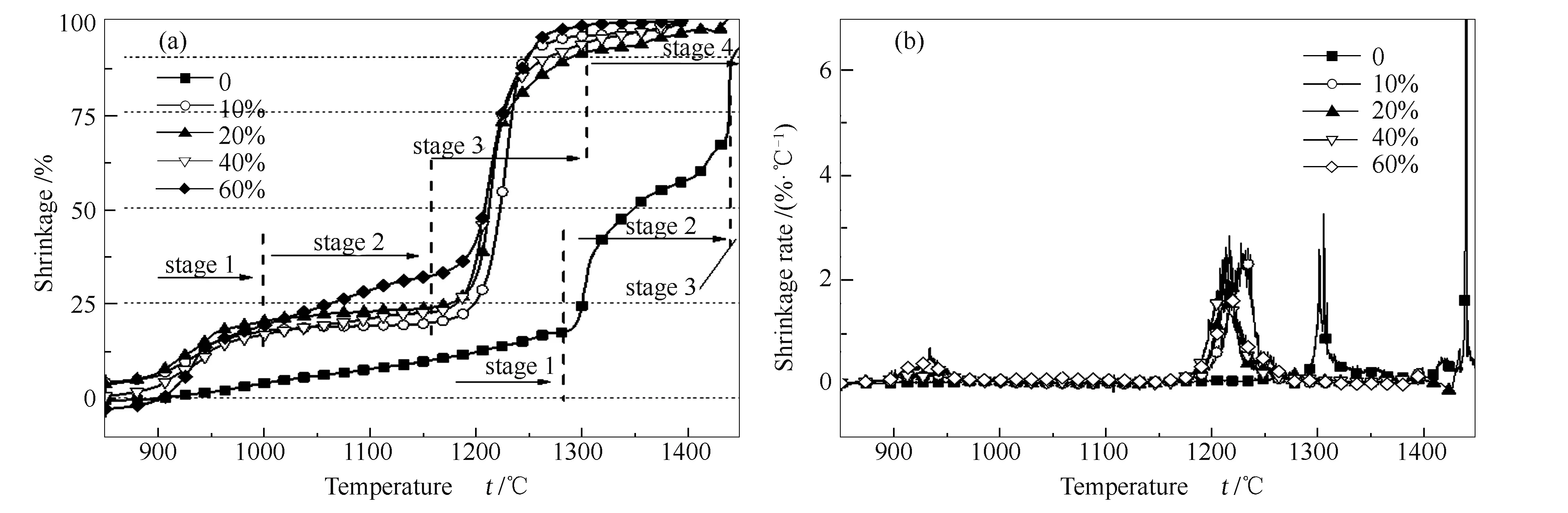
图 1 不同Na2SO4含量样品的TMA收缩曲线(a)和收缩速率曲线(b)
根据收缩的比例和收缩速率,可以将样品S1的熔化过程分为缓慢烧结、大量熔化、自由液相三个阶段[23]:第一阶段为900-1280 ℃,缓慢的收缩了20%,没有出现收缩速率峰值,这个阶段主要发生的是颗粒的烧结,使得气孔减少,颗粒重排,体积收缩;第二阶段为1280-1440 ℃,这时大量的矿物开始熔化,液固比急速增加,在1300和1430 ℃出现两个收缩速率峰值,说明在这两个阶段有不同的共熔物形成;第三阶段开始于1440 ℃,此阶段样品只有轻微的收缩,主要发生的是少量难熔的物质溶解在液相渣中,并且影响渣的流动性能。S2-S5的熔化过程有所不同,可以分为液相形成、液相烧结、大量熔化、自由液相四个阶段。第一阶段为900-1000 ℃,样品快速收缩约20%,在940 ℃出现收缩速率峰值,Na2SO4熔点是884 ℃,此时的快速收缩是因为液相的Na2SO4与矿物反应生成霞石(NaAlSiO4)、钠长石(NaAlSi3O8)、CaSO4等(图3、图5),霞石和钠长石、三斜霞石形成的共熔物以及Na2SO4和CaSO4形成的复合硫酸盐在900-950 ℃熔融,因此,Na2SO4促进了初始共熔物的形成。第二阶段为液相烧结,发生在1000-1150 ℃,液相的形成加速了烧结,使得沉积灰快速团聚形成致密结构。掺混比增加时收缩速率有增加趋势,60%的掺混比液相烧结显著快于其他样品。相比于S1的缓慢烧结,S2-S5先快速形成部分液相,随后发生液相烧结,并且烧结结束阶段提前了130 ℃。第三阶段为1150-1300 ℃,这时大量的液相开始形成,1220 ℃达到峰值,表明此温度下矿物发生共熔。第四阶段开始于1300 ℃左右,此时认为样品基本处于液相。
TMA的熔化特征温度t25、t50、t75、t90被广泛用来表征煤灰熔化特征,分别定义为收缩比例为25%、50%、75%、90%时的温度[22]。不同样品的TMA熔化特征温度见图 2。

图 2 不同Na2SO4含量样品的特征温度
t25被认为是灰的软化和烧结阶段,t50代表了大量熔化阶段,此时60%的灰开始熔化,类似于初始变形温度IDT,t75则表示80%的灰已经熔化,与半球温度HT具有相同趋势,可以被认为是物质的熔化温度,而t90被认为基本完全为液相时的温度[24]。TMA收缩比取决于液固比L/S,与AFT并不是完全对应。由图2可知,Na2SO4的存在使得四个特征温度都显著降低,10%掺混比使得t25和t50降低100 ℃,t75和t90降低200 ℃。这表明Na2SO4与矿物的反应加速液相的形成,促进低熔点物质的生成,揭示其强结渣性。t25在掺混比为10%-40%基本不变,到60%时明显下降,结合图3三元相图[25]可知,掺混比为20%、40%时位于霞石区,而掺混比为60%时位于Na2SiO3(熔点为1088 ℃)区,因此,推测Na2SiO3的熔融导致t25降低,这与S5的TMA曲线在此时的收缩相一致。对比Na2SO4掺混比从10%-60%发现,t50、t75变化较小,这是因为快速收缩阶段主要是Ca-Si-Mg-Al等元素生成的物质在1200-1250 ℃共熔,增加Na含量对其影响较小。陈晓东等[13]也发现对于低硅铝高钙准东煤灰,增加Na2O含量对煤灰特征温度的降低作用不明显。而t90在10%-60%则呈现先升高后降低的趋势,这可能是因为20%掺混比在高温下生成了CaO等部分高熔点的物质(图6)。TG-DSC曲线可以反映硫酸盐的分解和样品的吸放热特性,结果见图4。
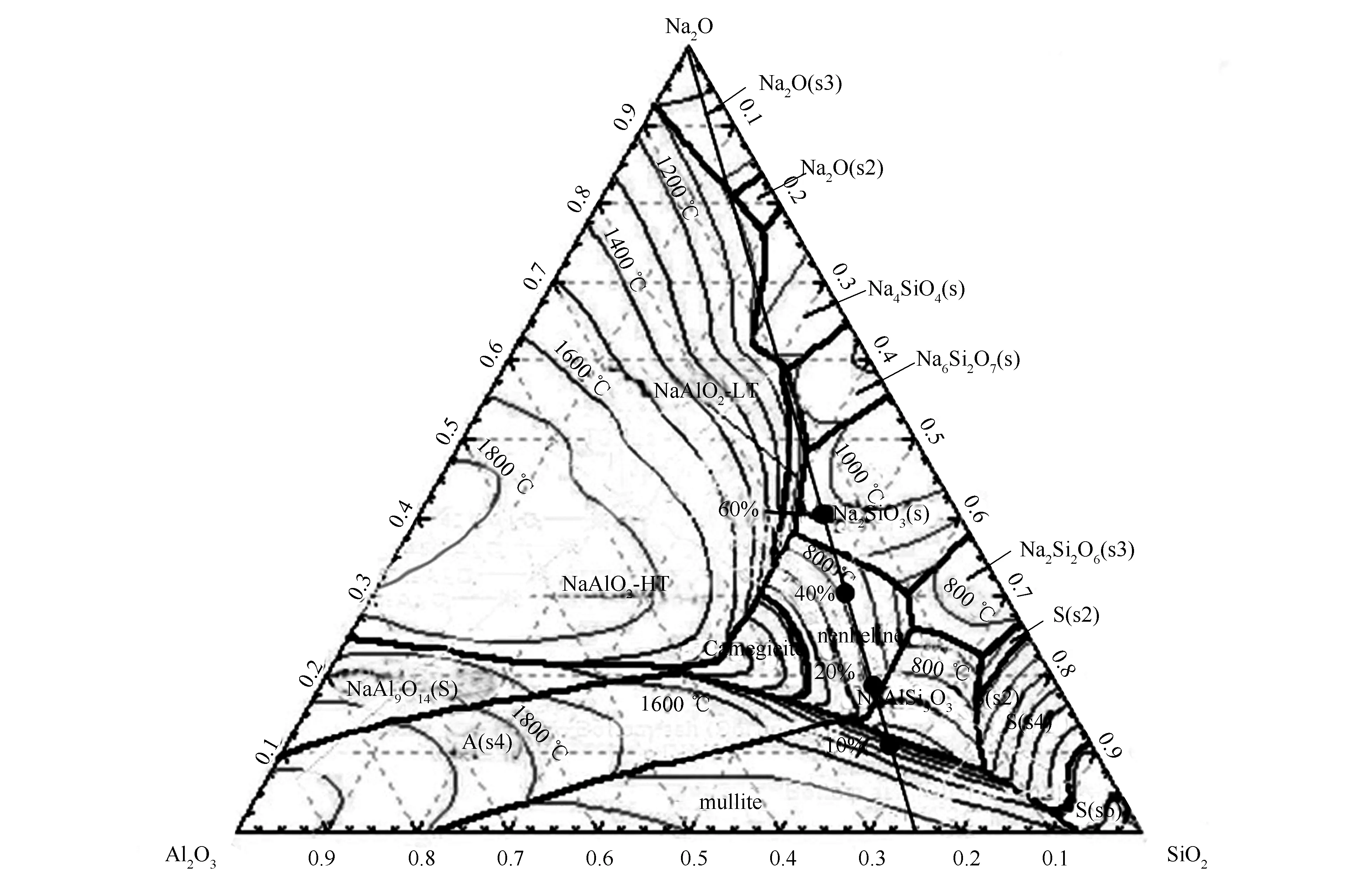
图 3 Na2O-SiO2-Al2O3三元相图[25]
由于样品中CaO在混合过程中易潮解为Ca(OH)2,升温过程中又分解,因此,将TG曲线在700 ℃归一化处理。TG在700-1200 ℃基本不变,1200-1300 ℃样品S2-S5急速失重,这主要是因为超过1200 ℃硫酸盐开始分解,因此,当沉积层外侧温度超过1200 ℃,硫酸盐很难沉积。到1300 ℃失重比分别为5.2%、7.9%、8.3%、10.5%,而理论上硫酸盐全部分解失重比为5.1%、9.3%、16.0%、21.2%,因此,掺混比为10%时,硫酸盐在超过1300 ℃几乎全部分解为SO2,由于Si、Al矿物能促进其分解,因此,Na2SO4掺混比越高,残留在渣中的越多,掺混比超过20%时,在1300 ℃仍有较多残留。因此,Na2SO4与煤灰作用过程与Na2CO3或Na2O有所不同,因为高温下高含量的Na2SO4不能完全分解。此外,DSC曲线表明,在700-1200 ℃样品不断吸热,S4和S5在940 ℃出现吸热峰,表明高含量的Na2SO4生成的低温共熔物在此时熔融,结合XRD分析推测是硫酸复盐的熔融引起的。在1300 ℃附近的吸热峰表明,部分高熔点的物质此时熔融或反应。
2.2 矿物多相反应过程分析
为进一步确定不同温度下矿物之间的反应过程,对掺混比为0和20%的样品S1、S3在不同温度煅烧后的渣样进行XRD分析,结果见图5。S1在800-1200 ℃矿物间较难反应,在1000 ℃生成黑钙铁石,1100 ℃生成硅灰石,在1200 ℃依然有石英、生石灰等初始矿物。
S3在800 ℃时出现大量初始矿物的衍射峰,表明低于800 ℃沉积矿物间难以发生反应,因此,800 ℃以下的积灰主要通过物理作用进一步生长。1000 ℃时出现CaSO4峰,CaSO4是结渣层中的主要物质,具有较高的黏结性[3,11,16]。同时,1000 ℃时石英的衍射强度减弱,且没有其他Si、Al矿物,说明Na2SO4可能与Si、Al矿物反应生成低熔点的物质。Kyi等[26]认为,Na2SO4可以直接和SiO2生成硅酸盐和SO2,且温度升高促进反应的进行,而TG曲线此时没有失重,由此推测,在900 ℃左右,CaO和SiO2、Al2O3的协同作用使得液相Na2SO4转变为CaSO4和Na的硅酸盐或硅铝酸盐(反应(2)或(3)),结合相图可知,S3位于霞石(NaAlSiO4)相区,S2位于钠长石(NaAiSi3O8)相区,而霞石可以和周围相区钠长石、三斜霞石等发生共熔,最低共熔温度915 ℃。这与TMA曲线在900-950 ℃收缩相一致。此外,MgO、CaO分别与Fe2O3反应生成镁铁尖晶石和黑钙铁石。

图 4 不同Na2SO4含量样品的TG(a)和DSC(b)曲线

图 5 S1(a)和S3(b)在不同温度下煅烧的XRD谱图
800-1000 ℃可能发生的反应如下:
Na2SO4(s)→Na2SO4(l)
(1)
Na2SO4(l)+CaO+nSiO2→Na2O·nSiO2+CaSO4
(2)
Na2SO4(l)+ CaO+nSiO2+mAl2O3→Na2O·mAl2O3·nSiO2+CaSO4
(3)
MgO+ Fe2O3→MgFe2O4(镁铁尖晶石)
(4)
2CaO+ Fe2O3→Ca2Fe2O5(黑钙铁石)
(5)
1100 ℃时,石英衍射峰进一步降低,这是由于SiO2和CaO反应生成硅灰石和斜硅钙石,此外CaO、SiO2、MgO反应生成镁黄长石、镁硅钙石和白硅钙石,这些物质具有较高熔点,因此,S3在1000-1100 ℃没有低熔点物质生成,在TMA曲线上表现为水平过渡阶段。1000-1100 ℃主要反应如下:
CaO+SiO2→CaSiO3(硅灰石)
(6)
2CaO+SiO2→Ca2SiO4(斜硅钙石)
(7)
CaO+2SiO2+MgO→Ca2MgSi2O7(镁黄长石)
(8)
3CaO+MgO+2SiO2→Ca3Mg(SiO4)2(镁硅钙石)
(9)
7CaO+MgO+4SiO2→Ca7Mg(SiO4)4(白硅钙石)
(10)
S3在1200 ℃时CaSO4衍射峰减弱,硅灰石、斜硅钙石消失,含量最多的物相为镁黄长石Ca2MgSi2O7,此外,还有尖晶石、镁硅钙石、白硅钙石相,这是由于CaSO4高温分解,这与TG结果一致,而硅灰石、斜硅钙石则在高温下转变为镁黄长石。虽然镁黄长石的熔点在1300 ℃以上,但Na的存在可以促进其与含钙矿物发生共熔[27]。尖晶石虽然熔点较高,但在高Fe煤沉积中起重要作用[28],含Fe矿物有助熔作用,可以在积灰外层形成共熔体[3]。因此,1200-1250 ℃的大量熔融主要是由镁黄长石的共熔引起的。主要反应如下:
CaSO4→CaO+SO2(g)+0.5O2(g)
(11)
2CaSiO3+MgO→Ca2MgSi2O7
(12)
Ca2SiO4+SiO2+MgO→Ca2MgSi2O7
(13)
为了对比Na2SO4含量对矿物反应的影响,对样品S1-S5在1100 ℃煅烧后的产物进行了XRD分析,结果见图6。由图6可知,S1在1100 ℃存在大量初始矿物,结合TMA知此时处于缓慢烧结阶段。S2-S5具有相似的矿物组成,且都没有发现Na的硅铝酸盐衍射峰,表明Na的硅铝酸盐在1100 ℃以下都已熔融。S2-S5都存在的矿物有尖晶石、硅灰石、镁硅钙石和白硅钙石,这些物质具有较高的熔点,高温下依然存在,Li等[12]发现,燃烧器入口结渣为硅灰石和钙长石。S2和S3含硫物相为CaSO4,而S4和S5为复合硫酸盐(Na0.8Ca0.1)2SO4和未反应的Na2SO4。这表明,Na2SO4在掺混比低于20%时与高含量的CaO、SiO2、Al2O3反应全部转变为CaSO4,继续增加掺混比,Na2SO4与CaSO4生成复合硫酸盐(反应(14)),当超过40%时出现残留的Na2SO4。Wang等[3]发现积灰内层中没有Na2SO4,可能是因为Na2SO4转化为CaSO4。
0.8Na2SO4+0.2CaSO4→(Na0.8Ca0.1)2SO4
(14)
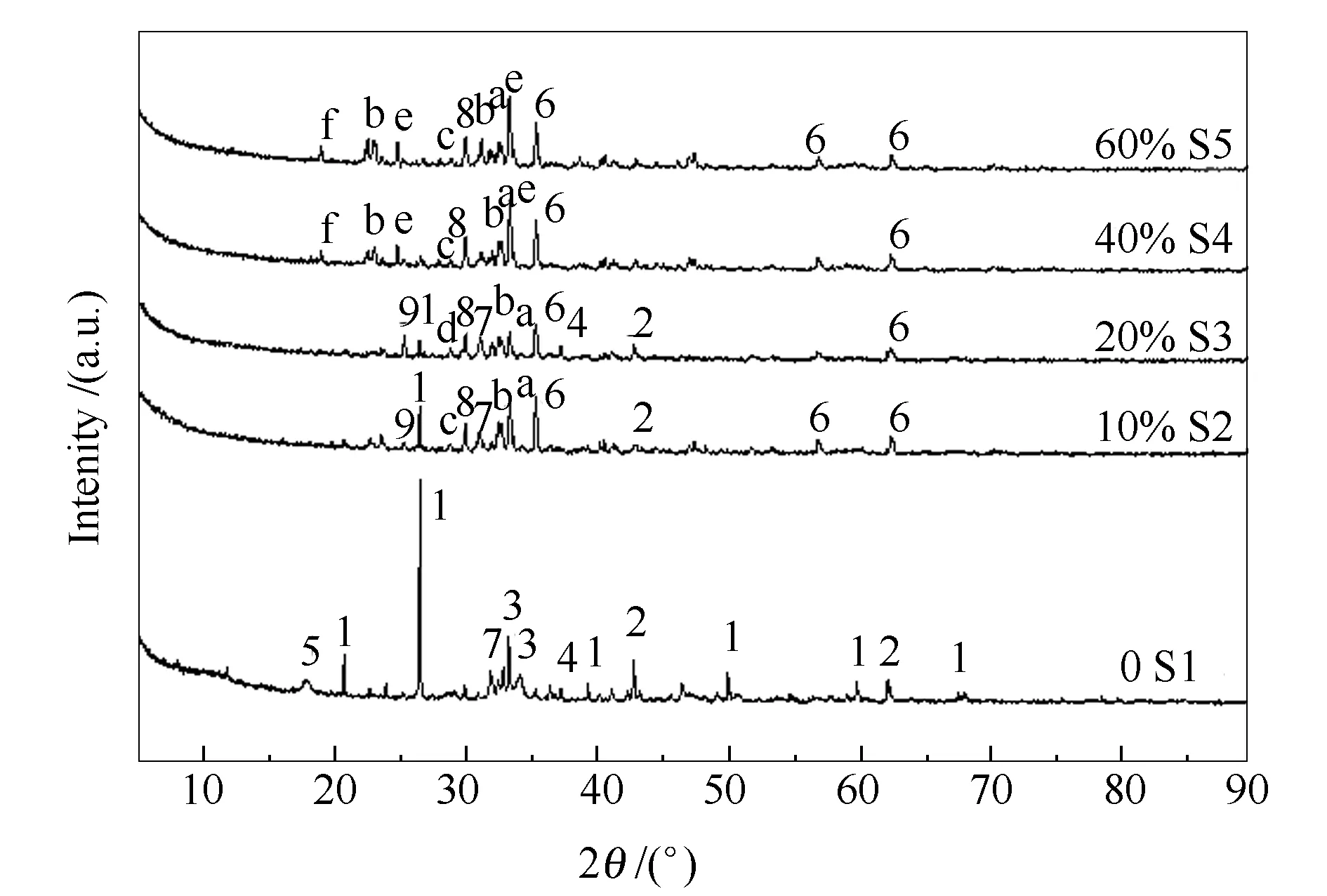
图 6 不同Na2SO4掺混比1100 ℃下煅烧的XRD谱图
Na2SO4-CaSO4的复合硫酸盐最低共熔点为916 ℃,(Na0.8Ca0.1)2SO4熔点只有950 ℃左右[29],是硫酸盐共熔物冷却过程中易形成的相,复合硫酸盐的共熔也是TMA曲线在900-950收缩的一个原因,DSC曲线中940 ℃的吸热峰推测是由复合硫酸盐熔融吸热引起的。(Na0.8Ca0.1)2SO4复合盐在长时间的高温作用下也可以转化为Na4Ca(SO4)3等稳定相,事实上Wei等[11]在过热器渣层内层发现有Na2Ca2(SO4)3存在,这说明复合盐的形成在灰沉积过程中具有重要作用[30]。图6中,S2、S4、S5中都出现了S3中没有的钙黄长石Ca2Al2SiO7,而钙黄长石易与镁黄长石发生共熔,降低熔点,S3还有游离的CaO,这可能是导致S3的t90较高的原因。S5中Na的硅酸盐熔融可能导致其t25明显下降。综合上述实验结果可以推测,在灰沉积过程中,熔融或半熔融的Na2SO4首先黏附在管壁上形成白内层,随后含Ca、Si、Al的颗粒碰撞并黏附,反应生成黏性的CaSO4以及Na硅铝酸盐,进一步生成复合硫酸盐,此外低熔点的Na硅酸盐和复合硫酸盐也可以直接在气相中生成并沉积[11]。随着温度升高进一步熔融并捕获含Ca、Si、Mg的灰颗粒,形成积灰生长层,矿物之间发生反应形成硅灰石、钙黄长石、镁黄长石随后形成低熔点的共熔物,热阻增大使得表面温度进一步升高,最后富含Si、Fe的灰颗粒黏附,在高温下熔融烧结形成致密渣层。
2.3 灰渣的微观形貌分析
不同掺混比在不同温度下煅烧后所得渣样的微观形貌及元素分析见图7。对比图7(a)、(b)、(c)可知,温度对矿物的烧结和反应过程有重要影响。800 ℃时大量的小颗粒开始黏结,形成蜂窝状多孔结构,颗粒间孔隙小于1 μm,可见富Na2SO4的渣样低温时具有较高黏性,能够黏附在受热面上,并捕获飞灰。Wang等[3]认为,850 ℃是硫酸盐沉积的临界温度,较低的沉积表面温度促进硫酸盐的形成[7]。1000 ℃时,黏结的小颗粒间孔隙消失,开始熔融,呈棱角模糊的流态状。1200 ℃时,发生严重的熔融烧结,表面形成致密的平面,玻璃化程度高。结合元素分析可知,A处主要元素为Ca、Si、Mg,结合XRD分析推测A处为镁黄长石,B处主要元素为Fe、Mg,推测为尖晶石。对比图7(d)、(e)、(f)可以看出,S1颗粒间没有明显烧结,S3和S5的渣样都出现严重的熔融烧结,且S5致密程度更高,D处Na、Ca、S含量最高,推测形成了Na、Ca复合硫酸盐,C处则主要为Ca、Mg、Fe、 Si,推测是含Ca矿物发生共熔。
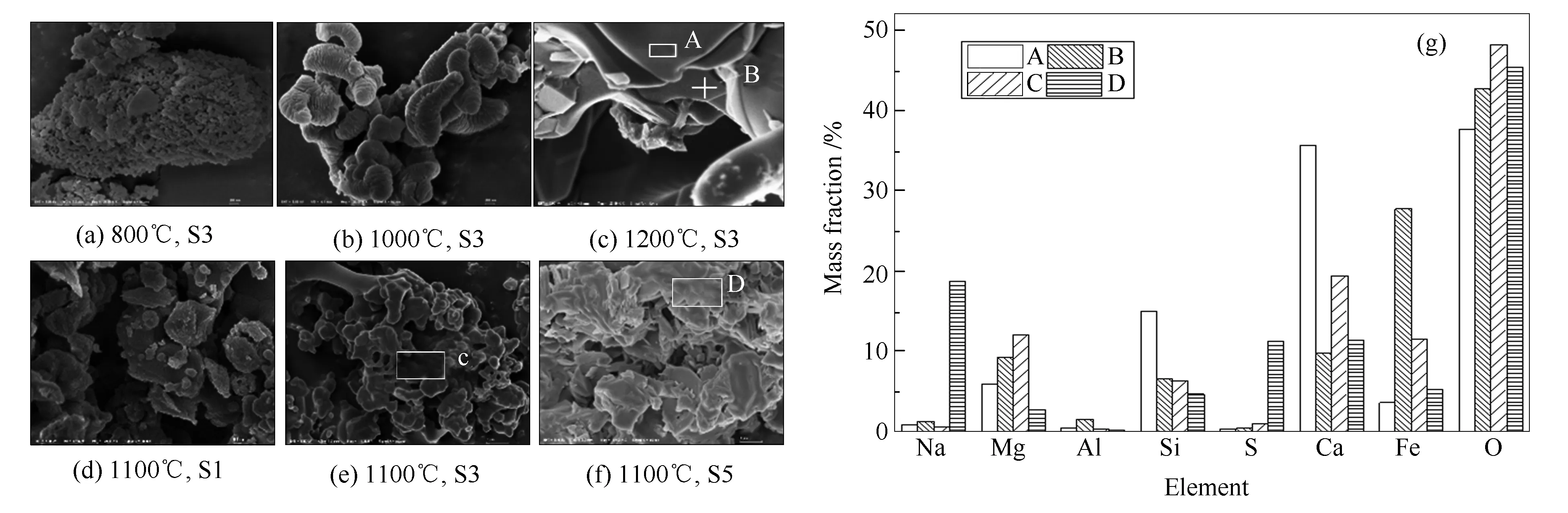
图 7 渣样的微观形貌和元素分析
3 结 论
富Na沉积层熔融过程分为液相形成、液相烧结、大量熔化、自由液相四个阶段。800 ℃时颗粒开始黏结,在900-950 ℃ 熔融的Na2SO4与SiO2、CaO和Al2O3反应生成CaSO4和霞石、钠长石等Na的硅铝酸盐,Na2SO4和CaSO4进一步生成复合硫酸盐,硅铝酸盐的共熔和复合硫酸盐的熔融使沉积层在900-950 ℃形成部分液相;在1000-1150 ℃发生液相烧结,颗粒间孔隙消失;在1200 ℃时生成大量的镁黄长石,镁黄长石与含Ca矿物共熔使矿物大量熔化;超过1300 ℃难熔的矿物溶解形成自由液相。
Na2SO4掺混比低于20%时,与高含量的CaO、SiO2和Al2O3反应全部转变为CaSO4和Na的硅酸盐或硅铝酸盐,继续增加掺混比,Na2SO4与CaSO4生成复合硫酸盐,当超过40%时出现残留的Na2SO4。Na2SO4向CaSO4的转化是一些积灰内层中没有Na2SO4的原因。
Na2SO4的存在使沉积层TMA特征温度显著降低,10%掺混比使得t25和t50降低100 ℃,t75和t90降低200 ℃。增加掺混比对t50、t75影响较小,而Na硅酸盐的熔融使得60%掺混比时t25显著降低。

