新诊断超重/肥胖2型糖尿病在短期胰岛素强化治疗后转换不同降糖方案的临床疗效和安全性研究
徐礼五,钟 兴,齐晓玲,李晓蕾,陈 斌
我国糖尿病患病率正在快速增长[1],超重/肥胖是中国2型糖尿病(type 2 diabetes mellitus,T2DM)人群一个显著的特征[2]。对于血糖较高新诊断的T2DM患者多采取短期胰岛素强化治疗以提高胰岛β细胞功能并能较长时间维持血糖达标[3],且临床报道较多。针对新诊断超重/肥胖2型糖尿病短期胰岛素强化治疗后,转换为不同的序贯治疗模式的比较性研究报道较少。该研究拟以严重高血糖的新诊断超重/肥胖T2DM患者为研究对象,进行短期胰岛素强化治疗后,转换为不同的序贯降糖治疗模式,探讨其临床有效性和安全性。
1 材料与方法
1.1病例资料98例新诊断T2DM患者系本院住院的患者,均符合1999年WHO诊断标准。其中男56例,女42例,年龄21~70(47±11)岁,均排除急性并发症、感染、肿瘤、妊娠、昏迷、外伤及脏器功能衰竭等严重应激状态。所有患者符合体质量指数(body mass index,BMI)≥25 kg/m2和(或)腰围≥90 cm(男性)、85 cm(女性),糖化血红蛋白(glycosylated hemoglobin A1C,HbA1C)≥9.0 %和(或)空腹血糖(fasting plasma glucose,FPG)≥11.1 mmol/L。
1.2研究方法符合入组条件的住院患者进行1周短期胰岛素强化治疗后,采用数字表法随机纳入甘精胰岛素治疗组(A组)36例,采用甘精胰岛素(赛诺菲-安万特公司,批号:J20140053)联合二甲双胍(口服剂量为0.5 g、tid,上海信谊,批号:H31020246)+/-阿卡波糖(口服剂量为50 mg、tid,拜耳公司,批号:H19990205)治疗;单纯口服降糖药物(除外DPP-4抑制剂)治疗组(B组)32例,采用二甲双胍+阿卡波糖,剂量同前,根据血糖情况酌情联合格列美脲(口服剂量2 mg、qd,重庆康刻尔公司,批号:H20030800);利拉鲁肽联合口服降糖药治疗组(C组)30例,采用利拉鲁肽(丹麦诺和诺德公司,批号S20160004)0.6 mg、qd,皮下注射,1周后改为1.2 mg、qd,联合二甲双胍+/-阿卡波糖,剂量同前。各组均根据血糖监测调整药物剂量直至血糖达标。观察期12周,观察各组血糖达标率、低血糖等不良反应发生率、治疗前后BMI、腰围、血脂及其它生化、稳态模型胰岛β细胞功能指数(homeostasis model assessment for islet β-cell function,HOMA-β)及胰岛素抵抗指数(homeostasis model assessment for insulin resistance,HOMA-IR)等指标变化。入组患者均进行糖尿病健康宣教,告知饮食和运动治疗益处和必要性并督促其落实。研究方案以及知情同意书均通过安徽理工大学第一附属医院伦理委员会批准,所有患者签署书面知情同意书。
受试者禁食12 h,晨起空腹采静脉血分离血清检测。HbA1C采用西门子医学诊断产品公司提供的HbA1C测定试剂盒(免疫比浊法)测定。FPG、餐后2 h血糖(2hPG)、总胆固醇(total cholesterol,TC)、三酰甘油(trilaurate glycerin,TG)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、血肌酐(serum creatinine,Scr)、谷丙转氨酶(alanine transaminase,ALT)用美国德灵公司产RxL2Max全自动生化分析仪测定。空腹胰岛素(fasting insulin,FIns)采用电化学发光法(罗氏化学发光分析仪)测定, HOMA-β=20×FIns/(FPG-3.5), HOMA-IR=FPG×FIns/22.5。血糖达标率以治疗后HbA1C≤7.0 %为标准,FPG达标标准是≤6.0 mmol/L、2hPG达标标准是≤8.0 mmol/L。血糖达标时间以FPG、2hPG皆达标的时间为准。低血糖发生率计算以发生1次及以上低血糖人数占总人数比率,严重低血糖事件另行记录。

2 结果
2.1各组间基线资料和HbA1C达标率比较① 治疗前3组患者年龄、BMI、腰围、FPG、2hPG、HbA1C比较差异无统计学意义(P>0.05),具有可比性,见表1~2;② 3组HbA1C达标率分别为69%、68%、90%,差异无统计学意义(P>0.05),见表1。
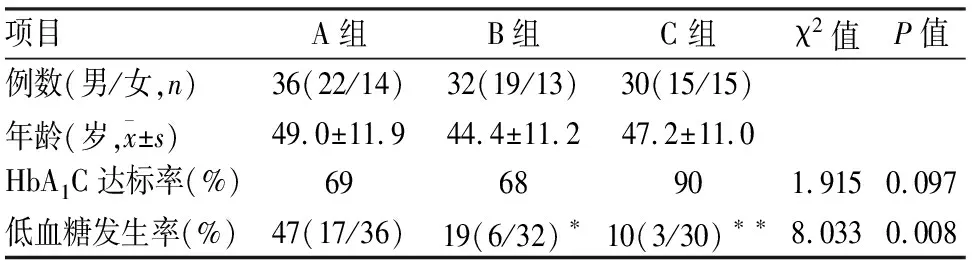
表1 各组间不同指标的比较
与A组比较:*P<0.05,**P<0.01
2.2各组治疗前后各项指标比较① 3组患者治疗后HbA1C、FPG、2hPG较治疗前均显著减少(P<0.01);治疗后,3组HbA1C降低幅度相似,但是A组FPG下降幅度优于B和C组,C组2hPG下降优于A和B组;② 3组患者HOMA-β指数治疗后均较治疗前明显升高(P<0.05),HOMA-IR治疗后均较治疗前显著减少(P<0.01),与A组治疗后比较,B组、C组治疗后HOMA-IR明显减少(P<0.05);③ A组BMI(P<0.01)和腰围(P<0.05)较治疗前均增加;C组BMI(P<0.01)、腰围(P<0.05)较治疗前均减少。治疗后,C组BMI和腰围较B和A组明显下降(P<0.05);④ 各组血清TC均显著下降(P<0.01),B组血清TG(P<0.01)、HDL-C(P<0.05)均有不同程度下降;⑤ B组和C组ALT较治疗前均显著下降(P<0.05)。见表2。
2.3各组治疗前后安全性评价3组患者低血糖发生率分别为47%、19%、10%,差异有统计学意义(P<0.01);与A组比较,B组(P<0.05)及C组(P<0.01)低血糖发生率明显减少,见表1。各组均未发生严重低血糖事件。3组均出现了不同程度恶心、腹泻、腹胀等胃肠道反应病例,其中A组3例、B组2例、C组4例,差异无统计学意义(P>0.05),且症状均在1周内缓解。

表2 各组治疗前后临床和实验室检查指标的比较中位数(四分位数间距)]
与同组治疗前比较:*P<0.05,**P<0.01;与A组比较:△P<0.05;与B组比较:▲P<0.05
3 讨论
多个国家流行病学调查显示T2DM以超重肥胖者居多[1,4-5]。糖尿病是动脉粥样硬化性脑心血管病(ASCCVD)独立危险因素之一,而一定幅度的体质量下降且长时间维持对超重肥胖T2DM患者ASCCVD预防很重要[6]。为此针对超重肥胖T2DM患者选择合适的降糖方案时需考虑体质量影响因素[7]。
对于严重高血糖(HbA1C>9.0%)的新诊断T2DM患者,应启用短期胰岛素强化治疗[8]。T2DM早期启用胰岛素治疗不仅能带来血糖良好控制,改善胰岛β细胞功能,而且会改善脂质代谢紊乱并阻止或延缓糖尿病相关的并发症发展[9]。而由于大部分T2DM患者存在超重或肥胖,T2DM的BMI与胰岛素抵抗呈正相关性[10]。胰岛素治疗带来的体质量增加及由此带来的胰岛素抵抗加剧使临床医师不愿选择胰岛素起始治疗及强化治疗[9]。因此新诊断超重或肥胖T2DM患者,在良好的血糖控制与体质量增加和胰岛素抵抗之间存在矛盾,促使本课题组探讨短期胰岛素强化治疗后,转换为不同治疗方案的临床疗效和安全性比较。
本研究显示,严重血糖升高的新诊断的超重/肥胖T2DM存在明显的胰岛素抵抗,采用胰岛素短期强化治疗后,转换为3种不同降糖方案治疗进行比较,3个月后3组HbA1C达标率无显著差别。本研究显示在改善胰岛素抵抗和胰岛功能方面,3个月后均较治疗前明显改善,但是利拉鲁肽组优于甘精胰岛素和口服药物组。LEAD系列研究[11]显示,利拉鲁肽无论是单药还是与其他口服药物联合治疗,其降糖效果更优,可改善胰岛功能和胰岛素抵抗。
有效的体质量管理有助于血糖控制,降低心血管事件的发生风险。本研究显示在随访3个月后,甘精胰岛素组BMI和腰围较治疗前增加,口服药物组无明显变化,而利拉鲁肽组较治疗前明显下降。本研究结果与一项针对亚洲人群的随机对照研究[12]类似,比较在二甲双胍基础上加用利拉鲁肽或格列美脲,显示利拉鲁肽组16周治疗体质量下降1.8~2.4 kg,而格列美脲组体质量增加0.1 kg。本课题组既往研究[13]显示在新诊断T2DM患者中使用利拉鲁肽联合胰岛素治疗,显著减少胰岛素用量和降低体质量。GLP-1受体激动剂降低体质量的作用机制主要包括抑制中枢神经系统食欲及摄食,抑制胃肠蠕动和胃液分泌从而延缓胃排空。
在安全性方面,利拉鲁肽组低血糖发生率明显低于其它两组,可能与利拉鲁肽是葡萄糖浓度依赖性的降低血糖有关。另外口服药治疗组和利拉鲁肽治疗组治疗后ALT均较治疗前明显下降,可能与超重肥胖T2DM体质量腰围的改善带来不同程度脂肪肝改善有关。有报道[14]显示GLP-1受体激动剂能显示改善T2DM合并非酒精性脂肪肝。

